医薬品情報
| 総称名 | レペタン |
|---|---|
| 一般名 | ブプレノルフィン塩酸塩 |
| 欧文一般名 | Buprenorphine Hydrochloride |
| 製剤名 | ブプレノルフィン塩酸塩坐剤 |
| 薬効分類名 | 鎮痛剤 |
| 薬効分類番号 | 1149 |
| ATCコード | N02AE01 |
| KEGG DRUG |
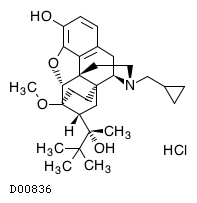
D00836
ブプレノルフィン塩酸塩
|
| KEGG DGROUP |
DG00820
ブプレノルフィン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年2月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 25.保険給付上の注意 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| レペタン坐剤0.2mg | Lepetan suppositories 0.2mg | 大塚製薬 | 1149703J1020 | 100.2円/個 | 劇薬, 向精神薬(第二種), 習慣性医薬品注1), 処方箋医薬品注2) |
| レペタン坐剤0.4mg | Lepetan suppositories 0.4mg | 大塚製薬 | 1149703J2027 | 130.1円/個 | 劇薬, 向精神薬(第二種), 習慣性医薬品注1), 処方箋医薬品注2) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
下記疾患並びに状態における鎮痛
術後、各種癌
6. 用法及び用量
<術後>
通常、成人にはブプレノルフィンとして1回0.4mgを直腸内に投与する。その後、必要に応じて約8〜12時間毎に反復投与する。
ただし、術直後の激しい疼痛にはブプレノルフィンの注射剤を投与し、その後、必要に応じて坐剤を投与する。
ただし、術直後の激しい疼痛にはブプレノルフィンの注射剤を投与し、その後、必要に応じて坐剤を投与する。
<各種癌>
通常、成人にはブプレノルフィンとして1回0.2mg又は0.4mgを直腸内に投与する。その後、必要に応じて約8〜12時間毎に反復投与する。なお、低用量より投与を開始することが望ましい。
8. 重要な基本的注意
8.1 本剤を投与後、特に起立、歩行時に悪心、嘔吐、めまい、ふらつきなどの症状があらわれやすいので、投与後はできる限り安静にするように注意すること。特に、外来患者に投与した場合には十分に安静にした後、安全を確認して帰宅させること。
8.2 眠気、めまい、ふらつき、注意力・集中力・反射運動能力等の低下が起こることがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械の操作に従事させないように注意すること。
8.3 薬物依存を生じることがあるので、観察を十分に行い、用量を超えないように慎重に投与すること。
8.4 用法及び用量の範囲で効果のない場合は、他の治療方法に切り替えること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 呼吸機能の低下している患者
呼吸抑制があらわれることがある。
9.1.2 胆道疾患のある患者
動物実験(イヌ)において高用量(0.1mg/kg i.v.以上)でOddi筋の収縮がみられる。
9.1.3 麻薬依存患者
麻薬拮抗作用を有するため禁断症状を誘発するおそれがある。
9.1.4 薬物依存の既往歴のある患者
薬物依存を生じることがある。
9.2 腎機能障害患者
9.2.1 腎機能の低下している患者
作用が増強されるおそれがある。
9.3 肝機能障害患者
9.3.1 重篤な肝機能障害のある患者
投与しないこと。代謝が遅延し、作用が増強されるおそれがある。[2.3参照]
9.3.2 肝機能の低下している患者(重篤な肝機能障害のある患者を除く)
作用が増強されるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。外国において、妊娠中に本剤を大量に投与した患者から出生した新生児に禁断症状がみられたとの報告がある。また、動物実験(ラット)で難産、拙劣な哺育行動、出生児の生存率の低下及び体重増加の抑制が報告されている。[2.6参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中への移行が報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
用量に留意して慎重に投与すること。一般に生理機能が低下している。
10. 相互作用
相互作用序文
本剤は、CYP3A4により代謝される。[16.4参照]
薬物代謝酵素用語
CYP3A4
10.1 併用禁忌
| ナルメフェン塩酸塩水和物(セリンクロ) [2.8参照] | ナルメフェン塩酸塩水和物はオピオイド受容体作動薬の鎮痛作用を減弱させるため、効果を得るために必要な本剤の用量が通常用量より多くなるおそれがある。 | μオピオイド受容体拮抗作用により、μオピオイド受容体作動薬に対して競合的に阻害する。 |
10.2 併用注意
| 中枢性鎮痛剤 ペンタゾシン エプタゾシン臭化水素酸塩等 | 本剤の作用が増強することがあるので、併用が必要な場合は一方又は両方の投与量を減らすなど慎重に投与すること。 | 本剤は中枢性鎮痛剤と同じオピオイドレセプターに作用するため。 |
| ベンゾジアゼピン誘導体・その他の鎮静剤 ジアゼパム ニトラゼパム メダゼパム等 中枢抑制剤(催眠剤等) バルビツール酸誘導体(フェノバルビタール等) アルコール等 | 本剤の作用が増強することがあるので、併用が必要な場合は一方又は両方の投与量を減らすなど慎重に投与すること。 | ともに中枢神経抑制作用を有するため。 |
| モルヒネ | 本剤の作用が増強するおそれがあるので、併用が必要な場合は一方又は両方の投与量を減らすなど慎重に投与すること。また、本剤は高用量(8mg連続皮下投与)においてモルヒネの作用に拮抗するとの報告がある。 | 本剤はモルヒネと同じオピオイドレセプターに作用するため、本剤の作用は、脳内オピオイドレセプターの飽和濃度に左右される。 |
| MAO阻害剤 | 本剤の作用が増強するおそれがある。 | 機序は不明であるが、本剤の代謝速度や生体アミンの変化が関係していると考えられている。 |
| CYP3A4阻害作用を有する薬剤 イトラコナゾール エリスロマイシン リトナビル アタザナビル硫酸塩等 | 本剤の作用が増強するおそれがあるので、本剤を減量するなど考慮すること。 | 本剤の主要代謝酵素であるCYP3A4を阻害するため本剤の血中濃度が上昇するおそれがある。 |
| CYP3A4誘導作用を有する薬剤 フェノバルビタール リファンピシン カルバマゼピン フェニトイン等 | 本剤の作用が減弱するおそれがある。 | 本剤の主要代謝酵素であるCYP3A4の誘導により本剤の血中濃度が低下するおそれがある。 |
| セロトニン作動薬 | セロトニン症候群の徴候及び症状(錯乱、せん妄、情緒不安、振戦、潮紅、発汗、高熱)があらわれるおそれがあるので、十分に注意すること。これらの徴候や症状が認められた場合には、本剤と併用薬の両方あるいはいずれか一方の投与を中止するなど適切な処置を行うこと。なお、セロトニン作動薬の急激な減量又は投与中止により離脱症状があらわれることがあるので注意すること。 | 中枢のセロトニン作動活性を増強すると考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 呼吸抑制(1%未満)、呼吸困難(1〜5%未満)
呼吸抑制から呼吸不全、呼吸停止に至った症例が報告されている。呼吸抑制があらわれた場合、人工呼吸又は呼吸促進剤のドキサプラム塩酸塩水和物が有効である。ナロキソン塩酸塩、レバロルファン酒石酸塩などの麻薬拮抗薬の効果は確実ではない。
11.1.2 舌根沈下(頻度不明)
手術後早期に舌根沈下による気道閉塞があらわれることがある。このような場合には気道確保等の適切な処置を行い、投与を中止すること。
11.1.3 ショック(頻度不明)
顔面蒼白、呼吸困難、チアノーゼ、血圧降下、頻脈、全身発赤等の症状があらわれた場合には投与を中止し、適切な処置を行うこと。
11.1.4 せん妄(頻度不明)、妄想(1%未満)
11.1.5 依存性(頻度不明)
長期の使用により薬物依存を生じることがあるので観察を十分に行い、慎重に投与すること。長期使用後、急に投与を中止すると、不安、不眠、興奮、胸内苦悶、嘔気、振戦、発汗等の禁断症状があらわれることがあるので、投与を中止する場合は徐々に減量することが望ましい。
11.1.6 急性肺水腫(頻度不明)
11.1.7 失神(頻度不明)
血圧低下から失神に至った症例が報告されている。
11.2 その他の副作用
| 5%以上 | 1〜5%未満 | 1%未満 | 頻度不明 | |
| 精神神経系 | めまい・ふらつき、眠気、頭痛・頭重感、発汗 | 幻覚、不安感、意識障害、しびれ、健忘、悪夢 | 抑うつ、顔面蒼白、見当識障害、痙攣、鎮静、軽度の多幸感、興奮 | |
| 循環器 | 血圧低下、血圧上昇、動悸、徐脈、皮膚潮紅 | 不整脈、胸内苦悶、熱感 | ||
| 消化器 | 嘔気、嘔吐 | 口渇 | 食欲不振、便秘、下痢、腹痛、肛門部痛 | 腸管運動障害 |
| 過敏症 | そう痒感、発疹 | |||
| 肝臓 | 総ビリルビン、AST、ALT、Al-Pの上昇 | |||
| 眼 | 羞明感 | 縮瞳、視力異常 | ||
| その他 | 倦怠感 | 不快感、尿閉、尿失禁、発熱 | 脱力感、悪寒、耳鳴 |
13. 過量投与
13.1 症状
悪心、嘔吐、縮瞳、鎮静、低血圧、呼吸抑制及び死亡に至るおそれがある。
13.2 処置
呼吸抑制があらわれた場合、人工呼吸又は呼吸促進剤のドキサプラム塩酸塩水和物が有効である。ナロキソン塩酸塩、レバロルファン酒石酸塩などの麻薬拮抗薬の効果は確実ではない。
14. 適用上の注意
14.1 薬剤投与時の注意
できるだけ排便後に投与すること。
16. 薬物動態
16.1 血中濃度
術後患者にブプレノルフィン坐剤0.2mg(10例)、0.4mg(8例)を直腸内投与した時、血漿中濃度を測定した結果、tmaxはいずれも約2時間で注射剤の筋肉内投与に比べ遅かった。本剤投与後の血漿中濃度には用量反応性がみられた1)。
16.3 分布
ヒト血漿蛋白結合率は、約96%であった(in vitro、平衡透析法)。
16.4 代謝
16.5 排泄
主排泄経路は胆汁を介した糞中排泄であり、糞中への排泄率は約70%で、残りは尿中へ排泄された2)(外国人データ)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床試験
<術後>
<各種癌>
18. 薬効薬理
18.1 作用機序
ブプレノルフィンは、オピオイド受容体に部分作動薬として作用し、中枢神経系の痛覚伝導系を抑制することにより鎮痛効果を発揮する。
18.2 鎮痛作用
ブプレノルフィンは、化学刺激、熱刺激及び圧刺激(マウス、ラット)、及び電気刺激(ウサギ)を侵害刺激として用いたいずれの試験においてもモルヒネ、ペンタゾシンより強く、かつ長い鎮痛効果を示した9)。
18.3 麻酔拮抗作用
マウスを用いた試験において、ブプレノルフィンのモルヒネに対する拮抗作用はナロキソン塩酸塩とほぼ同程度かやや弱かった9)。
19. 有効成分に関する理化学的知見
19.1. ブプレノルフィン塩酸塩
20. 取扱い上の注意
医療外使用を防止するため、本品の保管管理には十分注意すること。
22. 包装
<レペタン坐剤0.2mg>
アルミ製コンテナ:50個(5個×10)
<レペタン坐剤0.4mg>
アルミ製コンテナ:50個(5個×10)
23. 主要文献
- 太城力良 ほか, 麻酔, 38 (2), 182-189, (1989) »PubMed
- Heel,R.C.et al., Drugs., 17, 81-110, (1979) »PubMed
- 田口鐵男 ほか, 薬理と治療, 16 (11), 4577-4594, (1988)
- 佐藤寿雄 ほか, 医学のあゆみ, 148 (4), 285-294, (1989)
- 檀 健二郎 ほか, 医学のあゆみ, 148 (6), 435-446, (1989)
- 田口鐵男 ほか, 医学のあゆみ, 148 (8), 553-564, (1989)
- ブプレノルフィン坐剤研究会, 薬理と治療, 16 (11), 4623-4638, (1988)
- 檀 健二郎 ほか, 薬理と治療, 16 (11), 4639-4650, (1988)
- 桧山隆司 ほか, 日薬理誌, 79 (3), 147-162, (1982) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
大塚製薬株式会社
医薬情報センター
〒108-8242
東京都港区港南2-16-4 品川グランドセントラルタワー
電話:0120-189-840
FAX:03-6717-1414
製品情報問い合わせ先
大塚製薬株式会社
医薬情報センター
〒108-8242
東京都港区港南2-16-4 品川グランドセントラルタワー
電話:0120-189-840
FAX:03-6717-1414
25. 保険給付上の注意
本剤は厚生労働省告示第107号(平成18年3月6日付)に基づき、1回14日分を限度として投薬する。
26. 製造販売業者等
26.1 製造販売元
大塚製薬株式会社
東京都千代田区神田司町2-9