医薬品情報
| 総称名 | コニール |
|---|---|
| 一般名 | ベニジピン塩酸塩 |
| 欧文一般名 | Benidipine Hydrochloride |
| 薬効分類名 | 高血圧症・狭心症治療剤(持続性Ca拮抗薬) |
| 薬効分類番号 | 2179 |
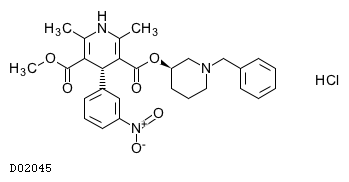
| KEGG DRUG |
D02045
ベニジピン塩酸塩
|
| KEGG DGROUP |
DG01928
ジヒドロピリジン系カルシウム拮抗薬
DG03231
血圧降下薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2021年4月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| コニール錠2 | Coniel Tablets | 協和キリン | 2171021F1024 | 10.8円/錠 | 劇薬, 処方箋医薬品注) |
| コニール錠4 | Coniel Tablets | 協和キリン | 2171021F2020 | 14.5円/錠 | 劇薬, 処方箋医薬品注) |
| コニール錠8 | Coniel Tablets | 協和キリン | 2171021F3027 | 29.8円/錠 | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 心原性ショックの患者[症状が悪化するおそれがある。]
2.2 妊婦又は妊娠している可能性のある女性[9.5参照]
4. 効能または効果
6. 用法及び用量
<高血圧症、腎実質性高血圧症>
通常、成人にはベニジピン塩酸塩として1日1回2〜4mgを朝食後経口投与する。なお、年齢、症状により適宜増減するが、効果不十分な場合には、1日1回8mgまで増量することができる。
ただし、重症高血圧症には1日1回4〜8mgを朝食後経口投与する。
ただし、重症高血圧症には1日1回4〜8mgを朝食後経口投与する。
<狭心症>
通常、成人にはベニジピン塩酸塩として1回4mgを1日2回朝・夕食後経口投与する。
なお、年齢、症状により適宜増減する。
なお、年齢、症状により適宜増減する。
8. 重要な基本的注意
8.1 カルシウム拮抗剤の投与を急に中止したとき、症状が悪化した症例が報告されているので、本剤の休薬を要する場合は徐々に減量し、観察を十分に行うこと。また、患者に医師の指示なしに服薬を中止しないように注意すること。
8.2 本剤の投与により、過度の血圧低下を起こし、一過性の意識消失等があらわれるおそれがあるので、そのような場合には減量又は休薬するなど適切な処置を行うこと。
8.3 降圧作用に基づくめまい等があらわれることがあるので高所作業、自動車の運転等危険を伴う機械を操作する際には注意させること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 過度に血圧の低い患者
本剤の降圧作用により血圧低下が悪化するおそれがある。
9.3 肝機能障害患者
9.3.1 重篤な肝機能障害のある患者
肝機能障害が悪化するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。動物実験(ラット、ウサギ)で胎児毒性が、また妊娠末期に投与すると妊娠期間及び分娩時間が延長することが報告されている。[2.2参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で母乳中へ移行することが報告されている。
9.7 小児等
小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
9.8 高齢者
一般に過度の降圧は好ましくないとされていることから、高血圧症に使用する場合は、低用量(2mg/日)から投与を開始するなど経過を十分に観察しながら慎重に投与することが望ましい。
10. 相互作用
相互作用序文
本剤は主としてCYP3A4で代謝される。
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| 降圧作用を有する薬剤 | 血圧が過度に低下することがある。 | 降圧作用が増強される。 |
| ジゴキシン | ジギタリス中毒があらわれるおそれがある。 ジゴキシンの血中濃度と心臓の状態をモニターし、異常が認められた場合には、ジゴキシンの用量の調節又は本剤の投与を中止する。 | カルシウム拮抗剤が、ジゴキシンの尿細管分泌を阻害し、血中ジゴキシン濃度を上昇させるとの報告がある。 |
| シメチジン | 血圧が過度に低下するおそれがある。 | シメチジンが肝ミクロソームにおけるカルシウム拮抗剤の代謝酵素を阻害する一方で胃酸を低下させ、薬物の吸収を増加させるとの報告がある。 |
| リファンピシン | 降圧作用が減弱されるおそれがある。 | リファンピシンが肝の薬物代謝酵素を誘導し、カルシウム拮抗剤の代謝を促進し、血中濃度を低下させるとの報告がある。 |
| イトラコナゾール | 血圧が過度に低下することがある。 | イトラコナゾールが、肝臓における本剤の代謝を阻害し、本剤の血中濃度が上昇するおそれがある。 |
| グレープフルーツジュース | 血圧が過度に低下することがある。 | グレープフルーツジュースが、肝臓における本剤の代謝を阻害し、本剤の血中濃度が上昇する。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 肝機能障害(0.1%未満)、黄疸(頻度不明)
AST、ALT、γ-GTPの上昇等を伴う肝機能障害や黄疸があらわれることがある。
注)発現頻度は、1997年10月までの使用成績調査を含む。
11.2 その他の副作用
| 0.1〜5%未満 | 0.1%未満 | 頻度不明 | |
| 肝臓 | 肝機能異常(AST,ALT,γ-GTP,ビリルビン,Al-P,LDH上昇等) | ||
| 腎臓 | BUN上昇、クレアチニン上昇 | ||
| 血液 | 白血球減少、好酸球増加 | 血小板減少 | |
| 循環器 | 動悸、顔面紅潮、ほてり、血圧低下 | 胸部重圧感、徐脈、頻脈 | 期外収縮 |
| 精神神経系 | 頭痛、頭重、めまい、ふらつき、立ちくらみ | 眠気、しびれ感 | |
| 消化器 | 便秘 | 腹部不快感、嘔気、胸やけ、口渇 | 下痢、嘔吐 |
| 過敏症 | 発疹 | そう痒感 | 光線過敏症 |
| 口腔 | 歯肉肥厚 | ||
| その他 | 浮腫(顔・下腿・手)、CK上昇 | 耳鳴、手指の発赤・熱感、肩こり、咳嗽、頻尿、倦怠感、カリウム上昇 | 女性化乳房、結膜充血、霧視、発汗 |
13. 過量投与
13.1 症状
過度の血圧低下を起こすおそれがある。
13.2 処置
本剤は蛋白結合率が高いため、透析による除去は有用ではない。
14. 適用上の注意
14.1 薬剤調製時の注意
<錠4mg、錠8mg>
14.1.1 錠剤半切機には適用できないことがある。均等に二分割できない場合がある。
14.1.2 分割後は遮光のうえ、早めに使用すること。
14.2 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
CAPD(持続的外来腹膜透析)施行中の患者の透析排液が白濁することが報告されているので、腹膜炎等との鑑別に留意すること。
16. 薬物動態
16.1 血中濃度
健康成人男性6例にベニジピン塩酸塩2mg、4mg及び8mgをそれぞれ空腹時に単回経口投与したときの血漿中未変化体濃度推移及び薬物動態パラメータは以下のとおりであった1)。
単回経口投与したときの血漿中濃度推移(mean+S.D.,n=6)
| 投与量 | tmax(h) | Cmax(ng/mL) | AUC0-∞(ng・h/mL) | t1/2(h) |
| 2mg | 1.1±0.5 | 0.55±0.41 | 1.04±1.26 | − |
| 4mg | 0.8±0.3 | 2.25±0.84 | 3.94±0.96 | 1.70±0.70 |
| 8mg | 0.8±0.3 | 3.89±1.65 | 6.70±2.73 | 0.97±0.34 |
16.2 吸収
16.2.1 食事の影響
健康成人男性8例にベニジピン塩酸塩8mgを空腹時及び食後30分に経口投与したとき、摂食によりtmaxの遅延、AUCの増加及び見かけのクリアランスの減少が認められた。食後投与によりベニジピン塩酸塩の吸収速度の低下及び生物学的利用率の上昇が認められたことから、投与方法として食後投与が好ましいと考えられた2)。
16.3 分布
16.3.1 体組織への分布
14C-ベニジピン塩酸塩1mg/kgをラットに経口投与したとき、肝臓、腎臓、副腎、顎下腺、肺、下垂体、膵臓の順に移行が認められ、脳、脊髄、精巣への移行は少なかった3)。
16.3.2 胎児移行性
14C-ベニジピン塩酸塩1mg/kgを妊娠ラットに経口投与したとき、胎児への移行性が認められ、その総量は母体血漿中の1/3以下であった4)。
16.3.3 母乳移行性
14C-ベニジピン塩酸塩1mg/kgを授乳ラットに経口投与したとき、乳汁中濃度は血漿中濃度と同様の推移を示した4)。
16.3.4 蛋白結合率
ヒト血清蛋白結合率は3H-ベニジピン塩酸塩1〜100,000ng/mLの濃度で98.46〜98.93%であった5)(in vitro、平衡透析法)。
16.4 代謝
16.5 排泄
外国人健康成人男性5例に14C-ベニジピン塩酸塩8mgを単回経口投与したとき、累積放射能排泄率は投与後48時間までに尿中に投与量の約35%、糞中には約36%が排泄され、投与後120時間では尿中で約36%、糞中で約59%が排泄された8)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床試験
<高血圧症>
本態性高血圧患者(軽症〜中等症)549例を対象に、本剤1〜8mgを経口投与したとき、有効率は84.2%(443/526例注))であった。
副作用発現頻度は、7.8%(43/549例)であった。主な副作用は、動悸12件、顔面紅潮7件、ふらつき及び頭重・頭重感 各6件、めまい、立ちくらみ及び顔面のむくみ 各3件、便秘、手のむくみ、浮腫(下腿)及び耳鳴 各2件であった。
副作用発現頻度は、7.8%(43/549例)であった。主な副作用は、動悸12件、顔面紅潮7件、ふらつき及び頭重・頭重感 各6件、めまい、立ちくらみ及び顔面のむくみ 各3件、便秘、手のむくみ、浮腫(下腿)及び耳鳴 各2件であった。
重症高血圧患者37例を対象に、本剤2〜8mgを経口投与したとき、有効率は94.4%(34/36例注))であった9)。
副作用発現頻度は、5.4%(2/37例)であった。認められた副作用は、全身倦怠感及び頭痛 各1件であった。
副作用発現頻度は、5.4%(2/37例)であった。認められた副作用は、全身倦怠感及び頭痛 各1件であった。
腎実質性高血圧患者39例を対象に、本剤2〜8mgを経口投与したとき、有効率は82.4%(28/34例注))であった10)11)。
副作用発現頻度は、5.1%(2/39例)であった。認められた副作用は、頭痛、顔面紅潮及び倦怠感 各1件であった。
副作用発現頻度は、5.1%(2/39例)であった。認められた副作用は、頭痛、顔面紅潮及び倦怠感 各1件であった。
注)有効率は降圧効果判定の「下降」以上で集計した。
<狭心症>
狭心症患者216例を対象に、本剤2〜12mgを経口投与したとき、狭心症に対しては60.8%(110/181例)の改善率(改善以上)を示した。その内訳は労作狭心症59.2%(71/120例)、労作・安静狭心症63.9%(39/61例)の改善率であった。
副作用発現頻度は、3.7%(8/216例)であった。認められた副作用は、頭痛3件、嘔気2件、ふらつき、眠気、顔面紅潮、顔のほてり、かゆみ・そう痒及び発疹 各1件であった。
副作用発現頻度は、3.7%(8/216例)であった。認められた副作用は、頭痛3件、嘔気2件、ふらつき、眠気、顔面紅潮、顔のほてり、かゆみ・そう痒及び発疹 各1件であった。
18. 薬効薬理
18.1 作用機序
18.2 降圧作用
18.3 抗狭心症作用
18.4 腎機能保持作用
19. 有効成分に関する理化学的知見
19.1. ベニジピン塩酸塩
22. 包装
<コニール錠2>
[PTP]100錠(10錠×10)
<コニール錠4>
[PTP]100錠(10錠×10)、500錠(10錠×50)
<コニール錠8>
[PTP]100錠(10錠×10)
23. 主要文献
- 宇治康明ほか, 薬理と治療, 18, S689-S702, (1990)
- 社内資料:食事の影響試験(臨床第I相試験)(1991年10月4日承認、資料概要ヘ.I.2.3))
- 小林弘幸ほか, 薬物動態, 5, 71-86, (1990) »DOI
- 小林弘幸ほか, 薬物動態, 5, 103-109, (1990) »DOI
- 社内資料:In vitro血清蛋白結合の測定(その1)(1991年10月4日承認、資料概要ヘ.II.5)
- 社内資料:ヒトにおける単回経口投与時の血漿中濃度、尿中排泄及び尿中代謝物(臨床第I相試験)(1991年10月4日承認、資料概要ト.I)
- Kobayashi H,et al., Arzneim-Forsch/Drug Res., 38, 1753-1756, (1988)
- Kobayashi H,et al., Xenobiotica., 27, 597-608, (1997) »PubMed
- 吉永馨ほか, 薬理と治療, 18, S785-S799, (1990)
- 吉永馨ほか, 薬理と治療, 18, S801-S822, (1990)
- 吉永馨ほか, 薬理と治療, 20, S3647-S3664, (1992)
- Karasawa A,et al., Jan J Pharmacol., 47, 35-44, (1988) »PubMed
- Ishii A,et al., J Cardiovasc Pharmacol., 21, 191-196, (1993) »PubMed
- Karasawa A,et al., Arzneim-Forsch/Drug Res., 38, 1684-1690, (1988)
- Karasawa A,et al., Arzneim-Forsch/Drug Res., 38, 1695-1697, (1988)
- 吉永馨ほか, 薬理と治療, 18, S721-S729, (1990)
- Karasawa A,et al., Arzneim-Forsch/Drug Res., 38, 1702-1707, (1988)
- Karasawa A,et al., Arzneim-Forsch/Drug Res., 38, 1717-1721, (1988)
- 野田汎史ほか, 薬理と治療, 18, S843-S850, (1990)
- 金澤雅之ほか, 日腎誌, 32, 33-44, (1990) »DOI
- Fuji Y,et al., J Cardiovasc Pharmacol., 11, 438-443, (1988) »PubMed
- 築山久一郎ほか, 薬理と治療, 18, S713-S719, (1990)
- Fukuda S,et al., J Cardiovasc Pharmacol., 12, S155-S156, (1988)
24. 文献請求先及び問い合わせ先
文献請求先
協和キリン株式会社
くすり相談窓口
〒100-0004
東京都千代田区大手町1-9-2
電話:0120-850-150 受付時間 9:00〜17:30(土・日・祝日及び弊社休日を除く)
製品情報問い合わせ先
協和キリン株式会社
くすり相談窓口
〒100-0004
東京都千代田区大手町1-9-2
電話:0120-850-150 受付時間 9:00〜17:30(土・日・祝日及び弊社休日を除く)
26. 製造販売業者等
26.1 製造販売元
協和キリン株式会社
東京都千代田区大手町1-9-2