医薬品情報
| 総称名 | ジプレキサ |
|---|---|
| 一般名 | オランザピン |
| 欧文一般名 | Olanzapine |
| 製剤名 | オランザピン錠 |
| 薬効分類名 | 抗精神病薬 双極性障害治療薬 制吐剤 |
| 薬効分類番号 | 1179 2391 |
| ATCコード | N05AH03 |
| KEGG DRUG |
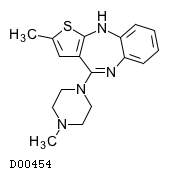
D00454
オランザピン
|
| KEGG DGROUP |
DG01482
ヒスタミンH1受容体拮抗薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年11月 改訂(第3版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ジプレキサ錠2.5mg | Zyprexa tablets | チェプラファーム | 1179044F1029 | 27.9円/錠 | 劇薬, 処方箋医薬品注) |
| ジプレキサ錠5mg | Zyprexa tablets | チェプラファーム | 1179044F2025 | 52.1円/錠 | 劇薬, 処方箋医薬品注) |
| ジプレキサ錠10mg | Zyprexa tablets | チェプラファーム | 1179044F3021 | 104.5円/錠 | 劇薬, 処方箋医薬品注) |
1. 警告
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
5. 効能または効果に関連する注意
<抗悪性腫瘍剤(シスプラチン等)投与に伴う消化器症状(悪心、嘔吐)>
本剤は強い悪心、嘔吐が生じる抗悪性腫瘍剤(シスプラチン等)の投与の場合に限り使用すること1)。
6. 用法及び用量
<統合失調症>
通常、成人にはオランザピンとして5〜10mgを1日1回経口投与により開始する。維持量として1日1回10mg経口投与する。なお、年齢、症状により適宜増減する。ただし、1日量は20mgを超えないこと。
<双極性障害における躁症状の改善>
通常、成人にはオランザピンとして10mgを1日1回経口投与により開始する。なお、年齢、症状により適宜増減するが、1日量は20mgを超えないこと。
<双極性障害におけるうつ症状の改善>
通常、成人にはオランザピンとして5mgを1日1回経口投与により開始し、その後1日1回10mgに増量する。なお、いずれも就寝前に投与することとし、年齢、症状に応じ適宜増減するが、1日量は20mgを超えないこと。
<抗悪性腫瘍剤(シスプラチン等)投与に伴う消化器症状(悪心、嘔吐)>
他の制吐剤との併用において、通常、成人にはオランザピンとして5mgを1日1回経口投与する。なお、患者の状態により適宜増量するが、1日量は10mgを超えないこと。
7. 用法及び用量に関連する注意
<抗悪性腫瘍剤(シスプラチン等)投与に伴う消化器症状(悪心、嘔吐)>
8. 重要な基本的注意
<効能共通>
8.1 本剤の投与により、著しい血糖値の上昇から、糖尿病性ケトアシドーシス、糖尿病性昏睡等の致命的な経過をたどることがあるので、本剤投与中は、血糖値の測定や口渇、多飲、多尿、頻尿等の観察を十分に行うこと。特に、高血糖、肥満等の糖尿病の危険因子を有する患者では、血糖値が上昇し、代謝状態を急激に悪化させるおそれがある。[1.2、8.3、9.1.1、11.1.1参照]
8.3 本剤の投与に際し、あらかじめ上記8.1及び8.2の副作用が発現する場合があることを、患者及びその家族に十分に説明し、高血糖症状(口渇、多飲、多尿、頻尿等)、低血糖症状(脱力感、倦怠感、冷汗、振戦、傾眠、意識障害等)に注意し、このような症状があらわれた場合には、直ちに投与を中断し、医師の診察を受けるよう、指導すること。[1.2、8.1、8.2、9.1.1、11.1.1、11.1.2参照]
8.4 本剤の投与により体重増加を来すことがあるので、肥満に注意し、肥満の徴候があらわれた場合は、食事療法、運動療法等の適切な処置を行うこと。
8.5 本剤は制吐作用を有するため、他の薬剤に基づく中毒、腸閉塞、脳腫瘍等による嘔吐症状を不顕在化することがあるので注意すること。
8.6 傾眠、注意力・集中力・反射運動能力等の低下が起こることがあるので、本剤投与中の患者には高所での作業あるいは自動車の運転等危険を伴う機械の操作に従事させないよう注意すること。
<双極性障害における躁症状及びうつ症状の改善>
8.7 躁症状及びうつ症状が改善した場合には、本剤の投与継続の要否について検討し、本剤を漫然と投与しないよう注意すること。双極性障害の維持療法における日本人での本剤の有効性及び安全性は確立していない。
<双極性障害におけるうつ症状の改善>
8.8 双極性障害におけるうつ症状を有する患者に本剤を投与する場合、以下の点に注意すること。[9.1.7、15.1.3参照]
8.8.1 大うつ病性障害等の精神疾患(双極性障害におけるうつ症状を含む)を有する患者への抗うつ剤の投与により、24歳以下の患者で、自殺念慮、自殺企図の発現のリスクが増加するとの報告があるため、本剤の投与にあたっては、リスクとベネフィットを考慮すること。
8.8.2 うつ症状を有する患者は希死念慮があり、自殺企図のおそれがあるので、このような患者は投与開始早期並びに投与量を変更する際には患者の状態及び病態の変化を注意深く観察すること。
8.8.3 不安、焦燥、興奮、パニック発作、不眠、易刺激性、敵意、攻撃性、衝動性、アカシジア/精神運動不穏等があらわれることが報告されている。また、因果関係は明らかではないが、これらの症状・行動を来した症例において、基礎疾患の悪化又は自殺念慮、自殺企図、他害行為が報告されている。患者の状態及び病態の変化を注意深く観察するとともに、これらの症状の増悪が観察された場合には、服薬量を増量せず、徐々に減量し、投与を中止するなど適切な処置を行うこと。[8.8.5、9.1.8、9.1.9参照]
8.8.4 自殺目的での過量服用を防ぐため、自殺傾向が認められる患者に処方する場合には、1回分の処方日数を最小限にとどめること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
<効能共通>
9.1.2 尿閉、麻痺性イレウス、閉塞隅角緑内障のある患者
抗コリン作用により症状を悪化させることがある。
9.1.3 てんかん等の痙攣性疾患又はこれらの既往歴のある患者
痙攣閾値を低下させることがある。
9.1.4 本剤のクリアランスを低下させる要因(非喫煙者、女性、高齢者)を併せ持つ患者
本剤の血漿中濃度が増加することがある。[9.8参照]
9.1.5 心・血管疾患(心筋梗塞あるいは心筋虚血の既往、心不全、伝導異常等)、脳血管疾患及び低血圧が起こりやすい状態(脱水、血液量減少、血圧降下剤投与による治療等)を有する患者
治療初期に、めまい、頻脈、起立性低血圧等があらわれることがある。
9.1.6 不動状態、長期臥床、肥満、脱水状態等の危険因子を有する患者[11.1.10参照]
<双極性障害におけるうつ症状の改善>
9.3 肝機能障害患者
9.3.1 肝障害のある患者又は肝毒性のある薬剤による治療を受けている患者
肝障害を悪化させることがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。妊娠後期に抗精神病薬が投与されている場合、新生児に哺乳障害、傾眠、呼吸障害、振戦、筋緊張低下、易刺激性等の離脱症状や錐体外路症状があらわれたとの報告がある。
9.6 授乳婦
授乳しないことが望ましい。ヒト母乳中への移行が報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
本剤のクリアランスを低下させる要因(非喫煙者、女性等)を併せ持つ高齢者では、2.5〜5mgの少量から投与を開始するなど、患者の状態を観察しながら慎重に投与すること。高齢者は一般的に生理機能が低下しており、本剤のクリアランスが低下していることがある。[9.1.4参照]
10. 相互作用
相互作用序文
本剤の代謝には肝薬物代謝酵素CYP1A2が関与している。また、CYP2D6も関与していると考えられている。[16.4.1参照]
薬物代謝酵素用語
CYP1A2
薬物代謝酵素用語
CYP2D6
10.1 併用禁忌
10.2 併用注意
| 中枢神経抑制剤 バルビツール酸誘導体等 | 減量するなど注意すること。 | 本剤及びこれらの薬剤は中枢神経抑制作用を有する。 |
| アルコール | 相互に作用を増強することがある。 | アルコールは中枢神経抑制作用を有する。 |
| 抗コリン作用を有する薬剤 抗コリン性抗パーキンソン剤 フェノチアジン系化合物 三環系抗うつ剤等 | 腸管麻痺等の重篤な抗コリン性の毒性が強くあらわれることがある。 | 本剤及びこれらの薬剤は抗コリン作用を有する。 |
| ドパミン作動薬 レボドパ製剤 | これらの薬剤のドパミン作動性の作用が減弱することがある。 | ドパミン作動性神経において、本剤がこれらの薬剤の作用に拮抗することによる。 |
| フルボキサミン [16.7.1参照] | 本剤の血漿中濃度を増加させるので、本剤を減量するなど注意すること。 | これらの薬剤は肝薬物代謝酵素(CYP1A2)阻害作用を有するため本剤のクリアランスを低下させる。 |
| シプロフロキサシン | 本剤の血漿中濃度を増加させる可能性がある。 | これらの薬剤は肝薬物代謝酵素(CYP1A2)阻害作用を有するため本剤のクリアランスを低下させる。 |
| カルバマゼピン [16.7.2参照] | 本剤の血漿中濃度を低下させる。 | これらの薬剤は肝薬物代謝酵素(CYP1A2)を誘導するため本剤のクリアランスを増加させる。 |
| オメプラゾール リファンピシン | 本剤の血漿中濃度を低下させる可能性がある。 | これらの薬剤は肝薬物代謝酵素(CYP1A2)を誘導するため本剤のクリアランスを増加させる。 |
| 喫煙 | 本剤の血漿中濃度を低下させる。 | 喫煙は肝薬物代謝酵素(CYP1A2)を誘導するため本剤のクリアランスを増加させる。 |
| アドレナリン含有歯科麻酔剤 リドカイン・アドレナリン | 重篤な血圧降下を起こすことがある。 | アドレナリンはアドレナリン作動性α、β-受容体の刺激剤であり、本剤のα-受容体遮断作用によりβ-受容体刺激作用が優位となり、血圧降下作用が増強されるおそれがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 高血糖(0.9%)、糖尿病性ケトアシドーシス(頻度不明)、糖尿病性昏睡(頻度不明)
11.1.2 低血糖(頻度不明)
11.1.3 悪性症候群(Syndrome malin)(0.1%未満)
無動緘黙、強度の筋強剛、脈拍及び血圧の変動、発汗等が発現し、それに引き続き発熱がみられる場合は、投与を中止し、水分補給、体冷却等の全身管理とともに、適切な処置を行うこと。本症発症時には、血清CKの上昇や白血球の増加がみられることが多い。また、ミオグロビン尿を伴う腎機能の低下に注意すること。なお、高熱が持続し、意識障害、呼吸困難、循環虚脱、脱水症状、急性腎障害へと移行し、死亡した例が報告されている。
11.1.4 肝機能障害、黄疸
AST(1.5%)、ALT(2.5%)、γ-GTP(0.7%)、Al-P(頻度不明)の上昇等を伴う肝機能障害、黄疸(頻度不明)があらわれることがある。
11.1.5 痙攣(0.3%)
痙攣(強直間代性、部分発作、ミオクロヌス発作等)があらわれることがある。
11.1.6 遅発性ジスキネジア(0.6%)
長期投与により、不随意運動(特に口周部)があらわれ、投与中止後も持続することがある。
11.1.7 横紋筋融解症(頻度不明)
筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇等が認められた場合には投与を中止し、適切な処置を行うこと。また、横紋筋融解症による急性腎障害の発症に注意すること。
11.1.8 麻痺性イレウス(頻度不明)
腸管麻痺(食欲不振、悪心・嘔吐、著しい便秘、腹部の膨満あるいは弛緩及び腸内容物のうっ滞等の症状)を来し、麻痺性イレウスに移行することがあるので、腸管麻痺があらわれた場合には、投与を中止するなど適切な処置を行うこと。
11.1.9 無顆粒球症(頻度不明)、白血球減少(0.6%)
11.1.10 肺塞栓症(頻度不明)、深部静脈血栓症(頻度不明)
肺塞栓症、静脈血栓症等の血栓塞栓症が報告されているので、観察を十分に行い、息切れ、胸痛、四肢の疼痛、浮腫等が認められた場合には、投与を中止するなど適切な処置を行うこと。[9.1.6参照]
11.1.11 薬剤性過敏症症候群(頻度不明)
初期症状として発疹、発熱がみられ、更に肝機能障害、リンパ節腫脹、白血球増加、好酸球増多、異型リンパ球出現等を伴う遅発性の重篤な過敏症状があらわれることがあるので、観察を十分に行い、このような症状があらわれた場合には投与を中止し、適切な処置を行うこと。なお、ヒトヘルペスウイルス6(HHV-6)等のウイルスの再活性化を伴うことが多く、投与中止後も発疹、発熱、肝機能障害等の症状が再燃あるいは遷延化することがあるので注意すること3)。
11.2 その他の副作用
| 1%以上 | 0.1〜1%未満 | 0.1%未満 | 頻度不明 | |
| 精神神経系 | 興奮、傾眠(22.3%)、不眠(10.3%)、不安、めまい・ふらつき、頭痛・頭重、抑うつ状態、構音障害、立ちくらみ | 易刺激性、自殺企図、幻覚、妄想、脱抑制、性欲亢進、躁状態、感覚鈍麻、下肢静止不能症候群、記憶障害、知覚過敏、違和感、意識喪失、焦燥 | 独語、空笑、会話障害、もうろう状態 | しびれ感、吃音、健忘 |
| 錐体外路症状 | アカシジア(静坐不能)、振戦、筋強剛、ジストニア、ジスキネジア、歩行異常、ブラジキネジア(動作緩慢) | 嚥下障害、眼球挙上 | 舌の運動障害、運動減少、パーキンソン病徴候 | |
| 循環器 | 血圧低下、動悸、頻脈 | 起立性低血圧、血圧上昇、徐脈、心室性期外収縮、心電図QT延長 | 心房細動 | 血栓 |
| 消化器 | 便秘、食欲亢進、口渇、嘔気、胃不快感、食欲不振、嘔吐、流涎過多 | 下痢、腹痛、口角炎 | 胃潰瘍、黒色便、痔出血、腹部膨満、胃炎 | 膵炎 |
| 血液 | 白血球減少、貧血、好中球減少 | リンパ球減少 | 白血球増多、好酸球増多、赤血球減少、好中球増多、血小板減少、ヘモグロビン減少、血小板増多、好酸球減少、赤血球増多、単球減少、単球増多、ヘマトクリット値減少 | |
| 内分泌 | 月経異常 | プロラクチン上昇 | 乳汁分泌、乳房肥大、甲状腺機能亢進症 | プロラクチン低下 |
| 肝臓 | ALT上昇、AST上昇 | γ-GTP上昇 | LDH上昇 | Al-P上昇、総ビリルビン上昇、ウロビリノーゲン陽性、総ビリルビン低下、肝炎 |
| 腎臓 | 蛋白尿 | 腎盂炎 | BUN低下、尿沈渣異常、クレアチニン低下、BUN上昇 | |
| 泌尿器 | 排尿障害 | 尿失禁 | 頻尿、尿閉 | |
| 過敏症 | 発疹、顔面浮腫 | 蕁麻疹、小丘疹 | 光線過敏症、血管浮腫、そう痒症 | |
| 代謝異常 | トリグリセリド上昇、コレステロール上昇、糖尿病 | 尿糖、高尿酸血症、水中毒、高脂血症 | トリグリセリド低下、脱水症、カリウム低下、カリウム上昇、ナトリウム低下 | 総蛋白低下、ナトリウム上昇、クロール上昇、クロール低下 |
| 呼吸器 | 鼻閉 | 鼻出血、嚥下性肺炎 | ||
| その他 | 体重増加(20.1%)、倦怠感、脱力感、体重減少、発熱、浮腫 | 発汗、CK上昇、転倒、胸痛、骨折、低体温、肩こり、脱毛症 | 腰痛、死亡、眼のチカチカ、霧視感、ほてり | 持続勃起、離脱反応(発汗、嘔気、嘔吐)、アルブミン低下、A/G比異常、グロブリン上昇、関節痛 |
13. 過量投与
13.1 症状
本剤の過量投与時に、頻脈、激越/攻撃性、構語障害、種々の錐体外路症状、及び鎮静から昏睡に至る意識障害が一般的な症状(頻度10%以上)としてあらわれることが報告されている。また他の重大な症状として、譫妄、痙攣、悪性症候群様症状、呼吸抑制、誤嚥、高血圧あるいは低血圧、不整脈(頻度2%以下)及び心肺停止があらわれることがある。450mg程度の急性過量投与による死亡例の報告があるが、2gの急性過量投与での生存例も報告されている。
13.2 処置
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
<効能共通>
15.1.1 本剤による治療中、原因不明の突然死が報告されている。
15.1.2 外国で実施された高齢認知症患者を対象とした17の臨床試験において、本剤を含む非定型抗精神病薬投与群はプラセボ投与群と比較して死亡率が1.6〜1.7倍高かったとの報告がある。
なお、本剤の5試験では、死亡及び脳血管障害(脳卒中、一過性脳虚血発作等)の発現頻度がプラセボと比較して高く、その死亡の危険因子として、年齢(80歳以上)、鎮静状態、ベンゾジアゼピン系薬物の併用、呼吸器疾患が報告されている。脳血管障害を発現した患者においては、脳血管障害・一過性脳虚血発作・高血圧の既往又は合併、喫煙等の危険因子を有していたことが報告されている。また、外国での疫学調査において、定型抗精神病薬も非定型抗精神病薬と同様に死亡率の上昇に関与するとの報告がある。
なお、本剤の5試験では、死亡及び脳血管障害(脳卒中、一過性脳虚血発作等)の発現頻度がプラセボと比較して高く、その死亡の危険因子として、年齢(80歳以上)、鎮静状態、ベンゾジアゼピン系薬物の併用、呼吸器疾患が報告されている。脳血管障害を発現した患者においては、脳血管障害・一過性脳虚血発作・高血圧の既往又は合併、喫煙等の危険因子を有していたことが報告されている。また、外国での疫学調査において、定型抗精神病薬も非定型抗精神病薬と同様に死亡率の上昇に関与するとの報告がある。
<双極性障害におけるうつ症状の改善>
15.2 非臨床試験に基づく情報
がん原性試験において、雌マウス(8mg/kg/日以上、21ヵ月)及び雌ラット(2.5/4mg/kg/日以上、21ヵ月、投与211日に増量)で乳腺腫瘍の発生頻度の上昇が報告されている。これらの所見は、プロラクチンに関連した変化として、げっ歯類ではよく知られている。臨床試験及び疫学的調査において、ヒトにおける本剤あるいは類薬の長期投与と腫瘍発生との間に明確な関係は示唆されていない。
16. 薬物動態
16.1 血中濃度
16.1.1 血漿中濃度
健康成人男子に本剤5mgを空腹時単回経口投与した5)。
| 投与量 | Tmax(hr) | Cmax(ng/mL) | t1/2(hr) | AUC0-96(ng・hr/mL) |
| 5mg錠×1錠 | 4.8±1.2 | 10.5±2.2 | 28.5±6.1 | 279±86.6 |
オランザピンカプセル注)を投与したとき、患者の血漿中濃度は、2.5〜20mgの範囲において投与量比例的であり、薬物動態の線形性が確認された。健康成人では、平均消失半減期は33時間(20.7〜54.1時間:5〜95パーセンタイル)であり、見かけのクリアランスは平均26.1L/hr(12〜47L/hr:5〜95パーセンタイル)である。1週間以内に定常状態に達する(外国人データ)。
16.2 吸収
16.2.1 食事の影響
食事による吸収への影響は認められなかった。
16.3 分布
16.3.1 蛋白結合
約93%(in vitro、超遠心法)。特にアルブミンとα1-酸性糖蛋白質に結合する。
16.4 代謝
16.4.1 主な代謝産物及び代謝経路
オランザピンの代謝に関与する酵素はグルクロン酸転移酵素、フラビン含有モノオキシゲナーゼ、チトクロームP450(CYP)である。オランザピンの代謝物10-N-グルクロン酸抱合体及び4'-N-グルクロン酸抱合体は、直接グルクロン酸抱合される6)。10-N-グルクロン酸抱合体が血漿中及び尿中における主要代謝物である。4'-N-オキシド体代謝物の生成はフラビン含有モノオキシゲナーゼが関与している。主な酸化代謝物である4'-N-デスメチル体はCYP1A2を介して生成される。比較的少ない代謝物である2-ヒドロキシメチル体はCYP2D6を介して生成されるが、オランザピンの全般的なクリアランスに大きく影響することはない。in vivoの動物試験において、4'-N-デスメチル体及び2-ヒドロキシメチル体の薬理活性はないか、又はオランザピンと比較して極めて低く、薬理活性の本体はオランザピンであることが確認されている。定常状態における未変化体、10-N-グルクロン酸抱合体及び4'-N-デスメチル体の血漿中濃度比は100:44:31であった。[10.参照]
16.5 排泄
16.5.1 排泄経路及び排泄率
健康成人に14Cオランザピンを経口投与したとき、21日間で全放射活性の約57%及び30%がそれぞれ尿中及び糞便中に排泄された(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
腎機能低下被験者10例にオランザピンカプセル注)を投与した検討によると、腎機能の低下はオランザピンの薬物動態に影響を与えなかった(外国人データ)。
16.6.2 肝機能障害患者
肝機能障害はオランザピンのクリアランスを低下させることが予想されたが、肝機能低下患者8例に本剤又はオランザピンカプセル注)を投与した検討によると、肝機能低下はオランザピンの薬物動態に影響を与えなかった(外国人データ)。
16.6.3 高齢者
オランザピンカプセル注)の単回投与では65歳以上の被験者16例の消失半減期は非高齢者に比し53%延長した(高齢者:52時間、非高齢者:34時間)。14日間連続投与では、65歳以上の被験者8例の消失半減期は59時間であった(外国人データ)。
16.6.4 性別・喫煙
本剤又はオランザピンカプセル注)を投与した検討によると、女性におけるオランザピンのクリアランスは男性よりも約30%低く、また喫煙者におけるオランザピンのクリアランスは非喫煙者よりも約40%高かったが、これらの要因のどれかひとつが存在することにより一般的に投与量を調節する必要はない。性別と喫煙を組み合わせた場合の平均クリアランス値は男性喫煙者で最も高く、次いで女性喫煙者、男性非喫煙者の順で、女性非喫煙者が最も低かった(外国人データ)。
16.7 薬物相互作用
16.7.1 フルボキサミン
本剤とフルボキサミンとの併用により、オランザピンの血漿中濃度は高値を示した。相互作用は男性(すべて喫煙者)で大きく、Cmaxの増加率は男性(喫煙)で75%、女性(すべて非喫煙者)で52%であった。AUC0-24の増加率は男性(喫煙)で108%、女性(非喫煙)で52%であった。また、クリアランス(CLp/F)は男性(喫煙)で52%、女性(非喫煙)で37%低下した。これはフルボキサミンがCYP1A2の阻害作用を有するためと推定された(外国人データ)。[10.2参照]
16.7.2 カルバマゼピン
オランザピンカプセル注)とカルバマゼピンとの併用により、オランザピンの血漿中濃度は低値を示した。併用によりCmaxは24%、AUC0-∞は34%低下した。これはカルバマゼピンがCYP1A2の誘導作用を有するためと推定された(外国人データ)。[10.2参照]
16.7.3 フルオキセチン
本剤とフルオキセチン(国内未承認)との併用により、オランザピンの血漿中濃度はわずかに増加した。併用によりCmaxは16%増加、クリアランス(CLp/F)は16%低下した。これはフルオキセチンがCYP2D6の阻害作用を有するためと推定された(外国人データ)。
16.7.4 その他
(1)喫煙者におけるオランザピンのクリアランス値は非喫煙者より約35%高かった。これは喫煙がCYP1A2の誘導作用を有するためと推定された。
注)オランザピンカプセルは開発途中に用いた製剤で、オランザピンカプセル5mgと本剤5mgは生物学的に同等であることが確認されている。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<統合失調症>
17.1.1 国内第II相試験
(1)初期第II相試験
最初に実施された8週間投与試験でオランザピンカプセル注1)1〜12.5mgが投与され、統合失調症患者計81例における中等度改善以上の改善率は59.3%(48/81例)であった9)。
主な副作用は不眠(症)17.3%(14/81例)及び眠気16.0%(13/81例)であった。
主な副作用は不眠(症)17.3%(14/81例)及び眠気16.0%(13/81例)であった。
(2)後期第II相試験
引き続き実施された8週間投与試験では2.5〜15mgが投与され、統合失調症患者計156例における中等度改善以上の改善率は58.3%(91/156例)であった10)。
主な副作用は不眠(症)19.9%(31/156例)、眠気13.5%(21/156例)、無月経11.3%(女性のみ6/53例)、倦怠(感)10.9%(17/156例)、振戦10.9%(17/156例)及び口渇10.9%(17/156例)であった。
主な副作用は不眠(症)19.9%(31/156例)、眠気13.5%(21/156例)、無月経11.3%(女性のみ6/53例)、倦怠(感)10.9%(17/156例)、振戦10.9%(17/156例)及び口渇10.9%(17/156例)であった。
17.1.2 国内第III相試験
8週間の二重盲検比較試験で本剤5〜15mgが投与され、本剤投与群の44.4%(40/90例)が中等度改善以上を示し、本剤の統合失調症に対する有用性が認められた11)。
主な副作用は倦怠(感)、アカシジア、眠気、興奮、不安及び不眠(症)各11.1%(10/90例)であった。
主な副作用は倦怠(感)、アカシジア、眠気、興奮、不安及び不眠(症)各11.1%(10/90例)であった。
17.1.3 外国第III相試験
(1)オランザピンカプセル注1)の固定用量範囲(低用量:5±2.5mg/日、中用量:10±2.5mg/日、高用量:15±2.5mg/日)とプラセボ及びハロペリドール(15±5mg/日)注2)を比較した6週間の二重盲検比較試験において、オランザピンの中・高用量群はプラセボと比較して陽性・陰性症状を含む精神症状全般に有意な改善を示し、高用量群はハロペリドール投与群と比較し、陰性症状を有意に改善した。錐体外路症状(EPS)はすべてのオランザピン投与群では改善を示したが、ハロペリドール投与群では悪化した。パーキンソニズム、アカシジアの発現率はすべてのオランザピン投与群で有意に低かった12)。
注1)オランザピンカプセルは開発途中に用いた製剤で、オランザピンカプセル5mgと本剤5mgは生物学的に同等であることが確認されている。
注2)ハロペリドール(経口剤)の国内承認用量(維持量)は1日3〜6mgである。
<双極性障害における躁症状の改善>
17.1.4 国内第III相試験
躁病エピソード又は混合性エピソードを呈した双極I型障害患者を対象に実施したプラセボ対照二重盲検比較試験において、本剤5〜20mgを1日1回3週間投与したとき、最終評価時におけるヤング躁病評価尺度(Young-Mania Rating Scale、YMRS)合計点のベースラインからの変化量(平均値±標準偏差)は本剤群−12.6±10.0、プラセボ群−6.8±14.0で、群間差とその95%信頼区間は−5.8[−9.1,−2.4]であり、統計学的な有意差が認められた(p<0.001、t検定)15)。
| 投与群 | 例数 | YMRS合計点 | 群間差 [95%信頼区間] | p値注3) | ||
| ベースライン | 最終評価時 | ベースラインからの変化量 | ||||
| 本剤群 | 104 | 27.7±5.9 | 15.1±10.4 | −12.6±10.0 | −5.8 [−9.1,−2.4] | <0.001 |
| プラセボ群 | 97 | 26.9±5.6 | 20.1±15.0 | −6.8±14.0 | ||
6週間の評価期間における主な副作用は、傾眠23.8%(25/105例)及び口渇15.2%(16/105例)であった。
17.1.5 国内第III相試験
二重盲検試験に継続して実施した18週間の非盲検長期継続投与試験において、二重盲検試験を完了した被験者にはオランザピンの単剤投与を、効果不十分を理由に二重盲検試験を中止した被験者にはオランザピン単剤と気分安定薬1剤との併用投与を行った16)。
(1)オランザピン単剤での検討
本剤5〜20mgを1日1回経口投与したときのYMRS合計点のベースラインからの変化量(平均値±標準偏差)は、投与6週後で−3.3±5.3、18週後で−4.2±5.3であった。
| ベースライン | 1週 | 2週 | 4週 | 6週 | 10週 | 14週 | 18週 | |
| 例数 | 100 | 100 | 96 | 91 | 81 | 76 | 65 | 61 |
| YMRS合計点 | 5.7±6.4 | 4.9±6.0 | 4.0±5.8 | 3.0±4.3 | 2.1±3.4 | 2.6±5.8 | 1.9±3.3 | 1.6±2.9 |
| 変化量 | − | −0.8±3.6 | −1.5±5.3 | −2.4±4.9 | −3.3±5.3 | −2.8±5.7 | −3.7±5.7 | −4.2±5.3 |
副作用発現頻度は41.0%(41/100例)であった。主な副作用は、傾眠13.0%(13/100例)であった。
(2)オランザピン+気分安定薬での検討
本剤5〜20mgを1日1回経口投与、気分安定薬として炭酸リチウム、バルプロ酸ナトリウム、カルバマゼピンのいずれか1剤を承認用法及び用量で併用投与したときのYMRS合計点のベースラインからの変化量(平均値±標準偏差)は、投与6週後で−25.9±9.3、投与18週後で−29.6±5.7であった。
| ベースライン | 1週 | 2週 | 4週 | 6週 | 10週 | 14週 | 18週 | |
| 例数 | 39 | 39 | 34 | 31 | 22 | 18 | 14 | 12 |
| YMRS合計点 | 33.2±6.6 | 25.1±9.6 | 17.9±10.3 | 12.5±12.8 | 7.1±8.7 | 2.9±4.4 | 3.1±4.1 | 1.7±3.2 |
| 変化量 | − | −8.1±8.6 | −15.4±11.1 | −21.0±12.6 | −25.9±9.3 | −30.3±8.7 | −30.0±9.4 | −29.6±5.7 |
副作用発現頻度は59.0%(23/39例)であった。主な副作用は、血中トリグリセリド増加15.4%(6/39例)、傾眠12.8%(5/39例)及び体重増加10.3%(4/39例)であった。
<双極性障害におけるうつ症状の改善>
17.1.6 国際共同第III相試験
(1)二重盲検期
うつ病エピソードを呈した双極I型障害患者(514例、日本人患者156例を含む)を対象に実施したプラセボ対照二重盲検比較試験において、本剤5〜20mgを就寝時に1日1回6週間投与したとき、最終評価時におけるMontgomery-Asberg Depression Rating Scale(MADRS)合計点のベースラインからの変化量(平均値±標準偏差)は本剤群−14.26±9.73、プラセボ群−11.71±11.09で、群間差とその95%信頼区間は−2.15[−3.93,−0.36]であり、統計学的な有意差が認められた(p=0.018、共分散分析)17)。
| 投与群 | 例数 | MADRS合計点 | 群間差 [95%信頼区間]注4) | p値注4) | |
| ベースライン | ベースラインからの変化量 | ||||
| 本剤群 | 339 | 29.36±5.71 | −14.26±9.73 | −2.15 [-3.93,−0.36] | 0.018 |
| プラセボ群 | 169 | 28.69±6.33 | −11.71±11.09 | ||
副作用発現頻度は本剤群で55.7%(191/343例)、プラセボ群で36.8%(63/171例)であった。本剤群の主な副作用は、体重増加15.7%(54/343例)、傾眠15.2%(52/343例)及び食欲亢進12.0%(41/343例)であった。
(2)非盲検継続投与期
国際共同試験(二重盲検期)に継続して実施した18週間の非盲検継続投与期において、本剤5〜20mgを就寝時に1日1回経口投与したときのMADRS合計点は下表のとおりであった。MADRS合計点のベースライン(二重盲検期終了時)からの変化量(平均値±標準偏差)は、投与6週後で−3.76±8.50、投与18週後で−6.34±9.43であった18)。なお、本試験においては気分安定薬、抗うつ薬及び抗精神病薬の併用を可として実施した。
| ベースライン | 6週 | 18週 | |
| 例数 | 385 | 349 | 295 |
| MADRS合計点 | 14.00±9.05 | 10.10±8.37 | 7.61±7.20 |
| 変化量 | − | −3.76±8.50 | −6.34±9.43 |
副作用発現頻度は38.3%(149/389例)であった。主な副作用は体重増加15.9%(62/389例)であった。
17.1.7 国内第III相試験
国際共同試験(非盲検継続投与期)を完了した日本人患者又は新規患者を対象に実施した24又は48週間の国内非盲検長期投与試験において、本剤5〜20mgを就寝時に1日1回経口投与したときのMADRS合計点は下表のとおりであった。国際共同試験を完了した日本人患者におけるMADRS合計点のベースライン(国際共同試験終了時)からの変化量(平均値±標準偏差)は、投与24週後で−1.0±6.7であった。新規患者では、MADRS合計点のベースライン(国内非盲検長期投与試験開始時)からの変化量(平均値±標準偏差)は、投与24週後で−5.2±13.2、投与48週後で−3.8±7.4であった18)。なお、本試験においては気分安定薬、抗うつ薬及び抗精神病薬の併用を可として実施した。
| ベースライン | 12週 | 24週 | 36週 | 48週 | ||
| 国際共同試験の完了例 | 例数 | 81 | 73 | 65 | − | |
| MADRS合計点 | 8.6±7.2 | 8.7±8.1 | 6.9±6.8 | |||
| 変化量 | − | 0.4±6.0 | −1.0±6.7 | |||
| 新規症例 | 例数 | 20 | 14 | 11 | 7 | 6 |
| MADRS合計点 | 16.5±9.0 | 9.9±8.7 | 10.6±9.6 | 8.3±8.1 | 7.3±9.5 | |
| 変化量 | − | −6.9±10.8 | −5.2±13.2 | −5.3±8.6 | −3.8±7.4 | |
副作用発現頻度は40.6%(41/101例)であった。全体の主な副作用は体重増加17.8%(18/101例)であった。
18. 薬効薬理
18.1 作用機序
オランザピンはチエノベンゾジアゼピン骨格を有する非定型抗精神病薬である。非臨床薬理試験において定型抗精神病薬とは異なる薬理学的特徴が明らかにされている。
オランザピンは多数の神経物質受容体に対する作用を介して統合失調症の陽性症状のみならず、陰性症状、認知障害、不安症状、うつ症状等に対する効果や錐体外路症状の軽減をもたらし(多元作用型:multi-acting)、また、多くの受容体に対する作用が脳内作用部位への選択性につながる(受容体標的化:receptor-targeting)と考えられる19)20)21)。オランザピンは、ドパミンD2タイプ(D2、D3、D4)、セロトニン5-HT2A,2B,2C、5-HT6、α1-アドレナリン及びヒスタミンH1受容体へほぼ同じ濃度範囲で高い親和性を示すが、ドパミンD1タイプ(D1、D5)やセロトニン5-HT3受容体へはやや低い親和性で結合する22)23)。また、ムスカリン(M1、M2、M3、M4、M5)受容体への親和性はin vitroと比較してin vivoでは弱い24)。オランザピンはこれらの受容体に対し拮抗薬として働く25)。更にオランザピンによる大脳皮質前頭前野でのドパミンとノルアドレナリンの遊離増加26)や、グルタミン酸神経系の伝達障害の回復27)28)も、オランザピンと複数の受容体との相互作用より引き起こされている可能性がある20)。
オランザピンは多数の神経物質受容体に対する作用を介して統合失調症の陽性症状のみならず、陰性症状、認知障害、不安症状、うつ症状等に対する効果や錐体外路症状の軽減をもたらし(多元作用型:multi-acting)、また、多くの受容体に対する作用が脳内作用部位への選択性につながる(受容体標的化:receptor-targeting)と考えられる19)20)21)。オランザピンは、ドパミンD2タイプ(D2、D3、D4)、セロトニン5-HT2A,2B,2C、5-HT6、α1-アドレナリン及びヒスタミンH1受容体へほぼ同じ濃度範囲で高い親和性を示すが、ドパミンD1タイプ(D1、D5)やセロトニン5-HT3受容体へはやや低い親和性で結合する22)23)。また、ムスカリン(M1、M2、M3、M4、M5)受容体への親和性はin vitroと比較してin vivoでは弱い24)。オランザピンはこれらの受容体に対し拮抗薬として働く25)。更にオランザピンによる大脳皮質前頭前野でのドパミンとノルアドレナリンの遊離増加26)や、グルタミン酸神経系の伝達障害の回復27)28)も、オランザピンと複数の受容体との相互作用より引き起こされている可能性がある20)。
18.2 統合失調症諸症状の動物モデルでの選択的作用
18.3 中脳辺縁系及び大脳皮質前頭前野への選択性
18.4 統合失調症に関わる不均衡な神経系との特異的相互作用
19. 有効成分に関する理化学的知見
19.1. オランザピン
22. 包装
<錠2.5mg>
100錠[10錠(PTP)×10]
100錠[瓶、バラ、乾燥剤入り]
1000錠[瓶、バラ、乾燥剤入り]
<錠5mg>
100錠[10錠(PTP)×10]
100錠[瓶、バラ、乾燥剤入り]
1000錠[瓶、バラ、乾燥剤入り]
<錠10mg>
100錠[10錠(PTP)×10]
100錠[瓶、バラ、乾燥剤入り]
1000錠[瓶、バラ、乾燥剤入り]
23. 主要文献
- 医療上の必要性の高い未承認薬・適応外薬検討会議 公知申請への該当性に係る報告書:オランザピン 抗悪性腫瘍剤投与に伴う消化器症状(悪心・嘔吐)
- 厚生労働省医薬食品局:医薬品・医療機器等安全性情報, (258), (2009)
- 厚生労働省:重篤副作用疾患別対応マニュアル 薬剤性過敏症症候群
- Stone M,et al., BMJ., 339, b2880, (2009) »PubMed »DOI
- 天本敏昭他, 臨床医薬, 14 (15), 2717-2735, (1998)
- Kassahun K,et al., Drug.Metab.Dispos., 25 (1), 81-93, (1997) »PubMed
- Callaghan JT,et al., Clin.Pharmacokinet., 37 (3), 177-193, (1999) »PubMed »DOI
- 社内資料:双極I型障害又は統合失調感情障害患者を対象としたオランザピンとバルプロ酸の薬物相互作用試験(2010年10月27日承認、CTD2.7.6.2.1)
- Ishigooka J,et al., Psychiatry.Clin.Neurosci., 55 (4), 353-363, (2001) »PubMed »DOI
- Ishigooka J,et al., Psychiatry.Clin.Neurosci., 54 (4), 467-478, (2000) »PubMed »DOI
- Ishigooka J,et al., Psychiatry.Clin.Neurosci., 55 (4), 403-414, (2001) »PubMed »DOI
- Beasley CM Jr,et al., Neuropsychopharmacology., 14 (2), 111-123, (1996) »PubMed »DOI
- Tran PV,et al., Br.J.Psychiatry., 172, 499-505, (1998) »PubMed »DOI
- Beasley CM,et al., Br.J.Psychiatry., 174, 23-30, (1999) »PubMed »DOI
- 社内資料:躁病又は混合性エピソードを呈した双極I型障害と診断された急性期の患者を対象に実施した二重盲検比較試験(2010年10月27日承認、CTD2.7.6.3.1)
- 社内資料:躁病又は混合性エピソードを呈した双極I型障害と診断された急性期の患者を対象に実施した長期継続投与試験(2010年10月27日承認、CTD2.7.6.3.2)
- 社内資料:うつ病エピソードを呈した双極I型障害と診断された患者を対象に実施した二重盲検比較試験(2012年2月22日承認、CTD2.7.6.2.1)
- 社内資料:うつ病エピソードを呈した双極I型障害と診断された患者を対象に実施した長期継続投与試験(2012年2月22日承認、CTD2.7.6.2.2)
- Bymaster FP,, J.Clin.Psychiatry.Monograph., 15 (2), 10-12, (1997)
- Bymaster FP他, 臨床精神薬理, 2 (8), 885-911, (1999)
- 村崎光邦, 臨床精神医学講座, 14, 96-108, (1999), (中山書店)
- Bymaster FP,et al., Neuropsychopharmacology., 14 (2), 87-96, (1996) »PubMed »DOI
- Schotte A,et al., Psychopharmacology(Berl)., 124 (1-2), 57-73, (1996) »PubMed »DOI
- Bymaster FP,et al., Eur.J.Pharmacol., 390 (3), 245-248, (2000) »PubMed »DOI
- Bymaster FP,et al., Schizophr.Res., 37 (1), 107-122, (1999) »PubMed »DOI
- Li XM,et al., Psychopharmacology(Berl)., 136 (2), 153-161, (1998) »PubMed »DOI
- Bakshi VP,et al., Psychopharmacology(Berl)., 122 (2), 198-201, (1995) »PubMed »DOI
- Corbett R,et al., Psychopharmacology(Berl)., 120 (1), 67-74, (1995) »PubMed »DOI
- Moore NA,et al., J.Pharmacol.Exp.Ther., 262 (2), 545-551, (1992) »PubMed
- Moore NA,et al., Behav.Pharmacol., 5 (2), 196-202, (1994) »PubMed »DOI
- Stockton ME,et al., Neuropsychopharmacology., 14 (2), 97-105, (1996) »PubMed »DOI
- Robertson GS,et al., Neuropsychopharmacology., 14 (2), 105-110, (1996) »PubMed »DOI
24. 文献請求先及び問い合わせ先
文献請求先
チェプラファーム株式会社
メディカルインフォメーションセンター
〒101-0021
東京都千代田区外神田4丁目14-1
電話:0120-772-073
製品情報問い合わせ先
チェプラファーム株式会社
メディカルインフォメーションセンター
〒101-0021
東京都千代田区外神田4丁目14-1
電話:0120-772-073
26. 製造販売業者等
26.1 製造販売元
チェプラファーム株式会社
東京都千代田区外神田4丁目14-1