医薬品情報
| 総称名 | アムビゾーム |
|---|---|
| 一般名 | アムホテリシンB |
| 欧文一般名 | Amphotericin B |
| 製剤名 | 注射用アムホテリシンBリポソーム製剤 |
| 薬効分類名 | ポリエンマクロライド系抗真菌性抗生物質製剤 |
| 薬効分類番号 | 6173 |
| ATCコード | A07AA07 G01AA03 J02AA01 |
| KEGG DRUG |
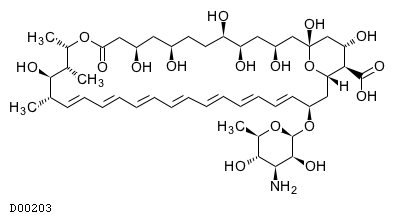
D00203
アムホテリシンB
|
| JAPIC | 添付文書(PDF) |
添付文書情報2022年10月 改訂(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アムビゾーム点滴静注用50mg | AmBisome For I.V.Infusion | 住友ファーマ | 6173400D2023 | 15239円/瓶 | 毒薬, 処方箋医薬品注) |
2. 禁忌
4. 効能または効果
○真菌感染症
アスペルギルス属、カンジダ属、クリプトコッカス属、ムーコル属、アブシジア属、リゾプス属、リゾムーコル属、クラドスポリウム属、クラドヒアロホーラ属、ホンセカエア属、ヒアロホーラ属、エクソフィアラ属、コクシジオイデス属、ヒストプラズマ属及びブラストミセス属による下記感染症
真菌血症、呼吸器真菌症、真菌髄膜炎、播種性真菌症
○真菌感染が疑われる発熱性好中球減少症
5. 効能または効果に関連する注意
<真菌感染症>
5.1 アゾール系抗真菌薬等が十分奏効するような軽症のカンジダ感染症に対しては、他剤を第一選択薬として使用することを考慮すること。
5.2 クロモブラストミコーシス(黒色分芽菌症)に対する本剤の有効性は確立されていない。
5.3 アスペルギルス属の呼吸器真菌症のうちアスペルギローマ(慢性壊死性肺アスペルギルス症を含む)においては、発熱等の臨床症状及び炎症反応が強く、胸部X線等で空洞周囲に浸潤影を認め、注射用抗真菌薬投与の必要性を認めた場合に、本剤投与の必要性を十分検討した上で投与すること。
<真菌感染が疑われる発熱性好中球減少症>
5.4 本剤は以下の3条件を満たす症例に投与すること。
・1回の検温で38℃以上の発熱、又は1時間以上持続する37.5℃以上の発熱
・好中球数が500/mm3未満の場合、又は1,000/mm3未満で500/mm3未満に減少することが予測される場合
・適切な抗菌薬投与を行っても解熱せず、抗真菌薬の投与が必要と考えられる場合
5.5 発熱性好中球減少症の治療に十分な経験を持つ医師のもとで、本剤の投与が適切と判断される症例についてのみ実施すること。
5.6 投与前に適切な培養検査等を行い、起炎菌を明らかにする努力を行うこと。起炎菌が判明した際には、本剤投与継続の必要性を検討すること。
6. 用法及び用量
<真菌感染症>
体重1kg当たりアムホテリシンBとして2.5mg(力価)を1日1回、1〜2時間以上かけて点滴静注する。
患者の症状に応じて適宜増減できるが、1日総投与量は体重1kg当たり5mg(力価)までとする。但し、クリプトコッカス髄膜炎では、1日総投与量は体重1kg当たり6mg(力価)まで投与できる。
患者の症状に応じて適宜増減できるが、1日総投与量は体重1kg当たり5mg(力価)までとする。但し、クリプトコッカス髄膜炎では、1日総投与量は体重1kg当たり6mg(力価)まで投与できる。
<真菌感染が疑われる発熱性好中球減少症>
体重1kg当たりアムホテリシンBとして2.5mg(力価)を1日1回、1〜2時間以上かけて点滴静注する。
<リーシュマニア症>
免疫能の正常な患者には、投与1〜5日目の連日、14日目及び21日目にそれぞれ体重1kg当たりアムホテリシンBとして2.5mg(力価)を1日1回、1〜2時間以上かけて点滴静注する。
免疫不全状態の患者には、投与1〜5日目の連日、10日目、17日目、24日目、31日目及び38日目にそれぞれ体重1kg当たりアムホテリシンBとして4.0mg(力価)を1日1回、1〜2時間以上かけて点滴静注する。
8. 重要な基本的注意
<効能共通>
8.1 腎機能障害があらわれることがあるので、定期的に腎機能、血清電解質(特にカリウム、マグネシウム)の検査を行うなど、観察を十分に行うこと。[9.2、9.2.1、9.8.1、11.1.3、11.1.5参照]
8.2 肝不全、黄疸、高ビリルビン血症等の重篤な肝機能障害、低カリウム血症、無顆粒球症、白血球減少、血小板減少があらわれることがあるため、また本剤の毒性に対する感受性は、患者によって個体差があるため、定期的に腎機能、肝機能、血清電解質(特にカリウム、マグネシウム)、血球数等の検査を行うなど、観察を十分に行うこと。[11.1.3-11.1.5、11.1.7参照]
8.4 投与終了時期あるいは本剤無効による投与中止時期を判断する場合は、国内外の学会ガイドライン等の情報を参考にすること。
8.5 投与時関連反応の予防には、点滴速度を遅らせるか、ジフェンヒドラミン、アセトアミノフェン及びヒドロコルチゾン等の投与が有効であるとの報告がある。[11.1.2参照]
8.6 本剤の投与量に相関して副作用の発現頻度が上昇するため、高用量を投与する場合には十分注意すること。
<真菌感染症>
8.7 本剤投与開始後において、原因菌が本剤の適応菌種でないことが明確になった場合、又は本剤投与で効果が認められない場合は、他の薬剤に変更するなど適切な処置を行うこと。
<真菌感染が疑われる発熱性好中球減少症>
8.8 本剤投与開始後に、腫瘍熱・薬剤熱等の非感染性の発熱であることが確認された場合には、速やかに投与を中止すること。
8.9 本剤投与開始後は随時治療効果を評価し、効果が認められない場合は、本剤の中止、他の薬剤に変更するなど適切な処置を行うこと。
<リーシュマニア症>
8.10 治療後に再発することがあり、特に免疫不全状態の患者では再発率が高いので、治療後も定期的に観察を行うなど注意すること。[17.1.5参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.2 大豆アレルギーのある患者
本剤の添加剤に大豆由来の成分が含まれる。[8.3参照]
9.2 腎機能障害患者
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。ラットの周産期の投与により母動物の状態悪化に起因する死産率の高値が認められている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁移行が認められている。
9.7 小児等
低出生体重児又は新生児を対象とした臨床試験は実施していない。
9.8 高齢者
10. 相互作用
10.1 併用禁忌
| 白血球輸注 [2.2参照] | 白血球輸注中又は直後にアムホテリシンBを投与した患者に、急性肺機能障害がみられたとの報告がある。 | 機序は不明である。 |
10.2 併用注意
| シスプラチン ペンタミジン アミノグリコシド系抗生物質 バンコマイシン シクロスポリン ガンシクロビル タクロリムス ホスカルネットナトリウム | 腎障害が発現、悪化するおそれがあるので、頻回に腎機能検査(クレアチニン、BUN等)を行うなど、患者の状態を十分に観察すること。 | 両薬剤とも腎毒性をもつ。 |
| 副腎皮質ホルモン剤 ヒドロコルチゾン プレドニゾロン ベタメタゾン 等 ACTH | 低カリウム血症を増悪させるおそれがあるので、血清中の電解質及び心機能を観察すること。 | 副腎皮質ホルモンは血清カリウムを排泄する作用がある。 |
| 三酸化ヒ素 | 血清電解質の異常をきたし、左記の薬剤によるQT延長が発現するおそれがあるので、血清中の電解質及び心機能を観察すること。 | 両薬剤とも血清電解質の異常を引き起こすことがある。 |
| 強心配糖体 ジギトキシン ジゴキシン 等 | ジギタリスの毒性(不整脈等)を増強するおそれがあるので、血清電解質及び心機能を観察すること。 | 本剤による低カリウム血症により、多量のジギタリスが心筋Na-K ATPaseに結合し、心筋収縮力増強と不整脈が起こる可能性がある。 |
| 抗不整脈剤 アミオダロン キニジン プロカインアミド 等 | 抗不整脈剤の催不整脈作用を増強するおそれがあるので、血清電解質及び心機能を観察すること。 | 本剤による低カリウム血症のため、抗不整脈剤の毒性が増強される可能性がある。 |
| 非脱分極性筋弛緩剤 ツボクラリン パンクロニウム 等 | クラーレ様薬剤の麻痺作用を増強し、呼吸抑制が起こるおそれがある。 | 本剤による低カリウム血症により、これらの薬剤の神経・筋遮断作用を増強させる可能性がある。 |
| フルシトシン | フルシトシンの毒性(骨髄抑制作用)を増強させるおそれがある。 | アムホテリシンBによるフルシトシンの細胞内取り込み促進や腎排泄障害作用により、フルシトシンの毒性が増強される可能性がある。 |
| 利尿剤 フロセミド トリクロルメチアジド ヒドロクロロチアジド 等 | 腎障害を発現、悪化するおそれがあるので、併用する場合は十分に塩類を補給し、腎毒性の軽減をはかることが望ましい。 | 利尿剤によるナトリウム欠乏により、本剤による腎血流量の減少を助長する可能性がある。 |
| 頭部放射線療法 | 併用により白質脳症があらわれるおそれがある。 | 頭部放射線照射により血液脳関門に変化が生じ、アムホテリシンBの神経毒性が発症する。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも1%未満)
ショック、アナフィラキシー(呼吸困難、チアノーゼ、血圧低下、じん麻疹等)があらわれた場合には投与を中止し、適切な処置を行うこと。
11.1.2 投与時関連反応(1%未満)
本剤注入に伴う重篤な症状として咽頭炎、嚥下障害、呼吸困難、チアノーゼ、心房粗動、胸痛等があらわれることがある。投与時関連反応(発熱、悪寒、悪心、嘔吐、頭痛、背部痛、骨痛等)が発現した場合は、点滴を一時中断し、患者の様子をみながら点滴速度を遅らせて投与を再開するなどの措置をとること。投与時関連反応の治療法には、点滴速度を遅らせるか、ジフェンヒドラミン、アセトアミノフェン及びヒドロコルチゾン等の投与が有効であるとの報告がある。[8.5参照]
11.1.3 腎不全、中毒性ネフロパシー等の重篤な腎障害(1〜5%未満)
11.1.4 肝不全、黄疸、高ビリルビン血症等の重篤な肝機能障害(1〜5%未満)
重篤な肝機能検査値異常等の異常が認められた場合には投与を中止し、適切な処置を行うこと。[8.2参照]
11.1.5 低カリウム血症(1%未満)
11.1.6 横紋筋融解症(頻度不明)
低カリウム血症を伴う横紋筋融解症があらわれることがあるので、筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇等があらわれた場合には投与を中止し、適切な処置を行うこと。
11.1.7 無顆粒球症、白血球減少(いずれも頻度不明)、血小板減少(1%未満)[8.2参照]
11.1.8 心停止、心不全、不整脈(心室頻拍、心室細動、心房細動等)(いずれも1%未満)
11.1.9 敗血症、肺炎等の重篤な感染症(1〜5%未満)
11.1.10 痙攣、意識障害等の中枢神経症状(1%未満)
11.1.11 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(いずれも頻度不明)
11.1.12 肺水腫(頻度不明)
11.2 その他の副作用
| 5%以上 | 1〜5%未満 | 1%未満 | 頻度不明 | |
| 過敏症 | アレルギー反応、血管神経性浮腫 | |||
| 皮膚・皮下障害 | 発疹 | そう痒、多汗 | 紅斑、じん麻疹、顔面浮腫、皮膚障害 | |
| 眼障害 | 結膜炎、網膜炎 | |||
| 呼吸器 | 呼吸困難、咳嗽、低酸素症、頻呼吸 | 鼻炎(鼻漏、鼻閉)、胸水、鼻出血、肺水腫注)、気管支痙攣 | ||
| 循環器 | 頻脈 | 血圧上昇、徐脈、血圧低下 | ||
| 血管障害 | 熱感・潮紅、高血圧、低血圧、静脈炎 | 点状出血 | ||
| 消化器 | 悪心(17.7%)、嘔吐(12.7%)、下痢・軟便 | 腹痛、食欲不振、便秘 | 便失禁、消化管出血、口内炎、舌苔、大腸炎、リパーゼ増加、口内乾燥、消化不良、吐血、膵炎 | |
| 肝臓 | ALT増加、AST増加、ALP増加 | γ-GTP増加、LDH増加、血中ビリルビン増加 | 胆汁うっ滞、胆嚢炎、肝腫大 | |
| 腎臓 | 血中クレアチニン増加(18.2%)、BUN増加(11.4%) | β2ミクログロブリン増加、尿潜血、尿円柱 | 尿蛋白、尿中赤血球陽性、尿失禁、尿中白血球陽性、尿量減少、乏尿、血尿 | |
| 精神神経系 | うつ病、幻覚(幻視、幻聴)、不眠症、錯乱状態、不安 | |||
| 神経系 | 頭痛 | めまい | 異常感覚、痙攣、傾眠、味覚異常、脳症 | |
| 筋骨格系 | 背部痛、筋痛 | 関節痛 | 骨痛 | |
| 全身・投与局所 | 発熱(40.0%)、悪寒(19.3%) | 胸痛、浮腫、疼痛 | 無力症、注射部位反応(紅斑、腫脹、知覚異常等)、倦怠感 | |
| 血液 | 貧血、血小板減少注)、白血球減少注)、単球増加 | 好中球減少、リンパ球減少、好塩基球増加、好酸球増加、白血球増加 | ||
| 代謝・栄養 | 低カリウム血症(25.4%)注)、低マグネシウム血症(14.8%) | 低カルシウム血症、低ナトリウム血症、リン脂質増加、コレステロール増加、高血糖、高カリウム血症、血中尿酸増加、トリグリセリド増加、高クロール血症、高リン酸塩血症、低リン酸血症 | 高マグネシウム血症、高ナトリウム血症、血中尿酸減少、低蛋白血症、高カルシウム血症、血中アミラーゼ増加、コレステロール減少、脱水、低クロール血症、アシドーシス、血液量増加症 | |
| 傷害、中毒・処置合併症 | 処置合併症、輸血反応 | |||
| 感染症 | 膿瘍 | |||
| その他 | CRP増加 |
12. 臨床検査結果に及ぼす影響
シンクロンLXシステム無機リン試薬(PHOSm試薬)による無機リン検査で偽高値を呈するとの報告がある1)。
13. 過量投与
13.1 処置
血液透析や腹膜透析では、本剤は体内から除去されないと思われる。
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.1 本品1バイアル(50mg(力価))中に注射用水12mLを加えて、直ちに振とうし、均一な黄色の半透明な液になるまで激しく振り混ぜる。溶解にあたっては注射用水のみを使用すること。
このアムホテリシンB4mg(力価)/mLの薬液を必要量シリンジに採取し、添付のフィルター(孔径5μm)を取り付け、フィルターろ過しながら薬液を5%ブドウ糖注射液(2.5mg/kg/日未満投与の場合100mL、2.5mg/kg/日以上投与の場合250mLが望ましい)で希釈して使用する。希釈にあたっては、必ず5%ブドウ糖注射液を使用すること。[14.1.2参照]
このアムホテリシンB4mg(力価)/mLの薬液を必要量シリンジに採取し、添付のフィルター(孔径5μm)を取り付け、フィルターろ過しながら薬液を5%ブドウ糖注射液(2.5mg/kg/日未満投与の場合100mL、2.5mg/kg/日以上投与の場合250mLが望ましい)で希釈して使用する。希釈にあたっては、必ず5%ブドウ糖注射液を使用すること。[14.1.2参照]
14.1.2 溶解液又は希釈液として、生理食塩液等の電解質溶液を使用しないこと。濁りを生じることがある。[14.1.1参照]
14.1.3 添付フィルター
(1)アムビゾーム注射液の調製以外に使用しないこと。
(2)1回限りの使用のみで再使用・再滅菌できない。
(3)包装が開いていたり、汚損したりしている場合、又はひび割れが確認された場合は、使用しないこと。
(4)アルコールを含む消毒剤で拭かないこと。接続部分にひび割れが生じる可能性がある。
(5)10mL以下の注射筒を使用しないこと。フィルターに過剰に圧力がかかり、最大使用圧力を超えることがある。
(6)過剰に圧がかかっている場合は、使用しないこと。フィルターに異物が捕捉されると、注射筒を押しにくくなることがある。
14.1.4 注射用水で溶解後、薬液は2〜8℃で最長24時間まで保存できる(禁凍結)。薬液を5%ブドウ糖注射液で希釈した後、6時間以内に投与開始すること。なお、希釈後の薬液は0.2〜2mg(力価)/mLの濃度において安定性が確認されている。
14.1.5 沈殿、異物が確認された場合は使用しないこと。
14.2 薬剤投与時の注意
14.2.1 本剤を投与する場合は1〜2時間以上かけて点滴静注すること。
14.2.2 本剤の点滴投与時にインラインフィルターを使用しないこと。目詰まりを生じることがある。
14.2.3 他の薬物とは混合しないこと。また、既に留置されている静注ラインは5%ブドウ糖注射液であらかじめ置き換えること。これができない場合には、別のラインを使って投与すること。
14.2.4 可塑剤としてDEHP(di-(2-ethylhexyl)phthalate;フタル酸ジ-2-エチルヘキシル)を含むポリ塩化ビニル製の輸液セット等を使用した場合、DEHPが製剤中に溶出するので、DEHPを含まない輸液セット等を使用することが望ましい。
15. その他の注意
15.1 臨床使用に基づく情報
国内臨床試験において、総投与日数303日を超える使用経験はない。
15.2 非臨床試験に基づく情報
ラットの1ヵ月間静脈内投与及び6ヵ月間静脈内投与では3mg/kg/日においてコレステロールやリン脂質の上昇が認められた。また、イヌの1ヵ月間静脈内投与では4mg/kg/日、3ヵ月間静脈内投与では2.5mg/kg/日、9ヵ月間静脈内投与では1.5mg/kg/日においてコレステロールやリン脂質の上昇が認められた。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
(1)成人の深在性真菌症患者31例に、本剤1mg/kg/日注)、2.5mg/kg/日及び5mg/kg/日を1時間かけて静脈内投与したときのCmax及びAUC0〜24は用量が増すにつれ増加し、特に5mg/kg/日投与群で一段と増加する傾向であった。半減期(T1/2)は用量による一定の変化は見られなかった。
| 投与量(mg/kg) | 例数 | Cmax(μg/mL) | T1/2(h) | AUC0〜24(μg・h/mL) | MRT※1)(h) | Cl※2)(mL/h/kg) | Vd※3)(L/kg) |
| 1.0 | 13 | 5.96±3.02 | 8.3±2.0 | 55.5±39.0 | 11.3±3.2 | 26±18 | 0.30±0.25 |
| 2.5 | 9 | 16.19±7.41 | 9.8±8.0 | 138.5±56.5 | 13.7±12.4 | 19±13 | 0.21±0.13 |
| 5.0 | 9 | 45.71±20.14 | 7.0±1.4 | 390.3±223.2 | 9.9±1.9 | 18±17 | 0.18±0.16 |
血清中薬物濃度
1mg/kg投与
2.5mg/kg投与
5mg/kg投与
(2)米国において、成人の発熱性好中球減少症患者33例を対象に、本剤1mg/kg/日、2.5mg/kg/日、5mg/kg/日及び7.5mg/kg/日注)を1時間かけて静脈内投与したときのCmax及びAUC0〜24は用量が増すにつれ増加する傾向であった。半減期(T1/2)には用量による一定の変化は見られなかった2)(外国人データ)。
| 投与量(mg/kg) | 例数 | Cmax(μg/mL) | T1/2(h) | AUC0〜24(μg・h/mL) | MRT※1)(h) | Cl※2)(mL/h/kg) | Vd※3)(L/kg) |
| 1.0 | 8 | 7.3±3.8 | 10.7±6.4 | 27±14 | 12.2±6.8 | 39±22 | 0.44±0.27 |
| 2.5 | 7 | 17.2±7.1 | 8.1±2.3 | 65±33 | 8.0±1.0 | 51±44 | 0.40±0.37 |
| 5.0 | 12 | 57.6±21.0 | 6.4±2.1 | 269±96 | 8.2±2.0 | 21±14 | 0.16±0.10 |
| 7.5 | 6 | 83.7±43.0 | 8.5±3.9 | 476±371 | 9.5±3.2 | 25±22 | 0.18±0.10 |
16.1.2 成人の深在性真菌症患者8例において、限外ろ過によりアムホテリシンBの血漿中での存在形態を検討した。リポソーム型、蛋白結合型及びフリー体としての存在比率はそれぞれ89.1±15.1、10.1±13.9及び0.8±1.1%(平均±標準偏差)であり、ほとんどがリポソーム型として血漿中に存在していた。
16.3 分布
本剤をラット(1及び9mg/kg)及びイヌ(1mg/kg)に単回静脈内投与した時の臓器中アムホテリシンB濃度は、細網内皮系臓器である肝臓、脾臓で高く、消失は緩やかであった。
16.4 代謝
16.4.1 健康成人に本剤2mg/kg注)を1回静脈内投与し、代謝物の存在を調査したが、アムホテリシンBの代謝物の存在は確認できなかった(外国人データ)。
16.4.2 ラット及びイヌの肝S9では、種々の補酵素添加系においても明確な代謝反応は認められず、本剤を静脈内投与した時の各種臓器、排泄物及び屍体ホモジネートを分析した時のHPLCクロマトグラムには代謝物と考えられるピークは検出されなかった。
16.5 排泄
16.5.1 健康成人に本剤の14C-コレステロール脂質標識体2mg/kgを1回静脈内投与した結果、投与後1週間までにアムホテリシンBの約10%が尿中及び糞便中に排泄され、血漿中のアムホテリシンBと併せて24.0%が確認された(外国人データ)。
16.5.2 胆汁導出ラットに本剤3mg/kgを単回静脈内投与した時、投与後72時間までのアムホテリシンBの累積排泄率は、尿中に4.3%、胆汁中に5.9%であり、肝臓中のアムホテリシンBの残存率は投与量の60.1%であった。
16.5.3 肝機能障害モデルラットでのアムホテリシンBの血漿クリアランスは、対照動物に比べて約4分の1に低下したが、腎機能障害モデルラットでは対照動物と差がなかったことから、本剤のクリアランスには主に肝臓が関与し、腎臓の関与は小さいと考えられた。[9.8.1参照]
16.6 特定の背景を有する患者
16.6.1 小児等
米国において、免疫不全状態にある小児の発熱性好中球減少症あるいは侵襲性真菌感染症の患者に対し、本剤2.5mg/kg/日及び5mg/kg/日注)を1時間かけて静脈内投与したときの薬物動態は、成人と大きな差はなかった(外国人データ)。
| 投与量(mg/kg) | 例数 | Cmax(μg/mL) | T1/2(h) | AUC0〜24(μg・h/mL) | Cl※1)(mL/h/kg) | Vd※2)(L/kg) |
| 2.5 | 10 | 15.1±9.0 | 8.8±2.1 (n=8) | 54.7±32.9 | 38±13 (n=8) | 0.47±0.18 (n=8) |
| 5.0 | 13 | 46.2±46.7 | 12.6±8.4 | 351±445 | 45±38 | 0.86±0.86 |
注)本剤の承認された1日用量は、アムホテリシンBとして2.5mg(力価)/kg(但し、免疫不全状態のリーシュマニア症患者においては4mg(力価)/kg)である。なお、真菌感染症においては、患者の症状に応じて5mg(力価)/kgまで投与できる(但し、クリプトコッカス髄膜炎においては6mg(力価)/kgまで)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<真菌感染症>
17.1.1 国内臨床試験
成人患者(年齢:16〜79歳)を対象に実施された臨床試験(投与量1.0〜5.0mg/kg/日注)、投与期間原則7日間、最長21日間又は原則3週間、最長12週間)のうち真菌感染症を対象とした臨床試験成績の概要は下記のとおりで、総有効率は、47.3%(35/74)であった。
| 真菌感染症疾患名 | 有効例数/症例数(有効率) | |
| アスペルギルス症 | 侵襲性肺アスペルギルス症 | 8/15(53.3%) |
| 慢性壊死性肺アスペルギルス症 | 6/9(66.7%) | |
| 肺アスペルギルス症※ | 3/5 | |
| アスペルギローマ | 4/19(21.1%) | |
| その他のアスペルギルス感染症 | 3/7(42.9%) | |
| 合計 | 24/55(43.6%) | |
| カンジダ症 | カンジダ血症 | 6/12(50.0%) |
| 播種型カンジダ症 | 3/4 | |
| 合計 | 9/16(56.3%) | |
| クリプトコッカス症 | 肺クリプトコッカス症 | 2/2 |
| クリプトコッカス髄膜(脳)炎 | 0/1 | |
| 合計 | 2/3 | |
| 合計 | 35/74(47.3%) | |
<クリプトコッカス髄膜炎>
17.1.2 海外第III相試験
HIV陽性のクリプトコッカス髄膜炎患者を対象とした臨床試験成績(投与期間11〜21日間)は下記のとおりであった(外国人データ)。
| 評価項目\投与量 | 3mg/kg/日 | 6mg/kg/日 |
| 2週後の有効率※1) | 35/60(58.3%) | 36/75(48.0%) |
| 10週後の有効率※2) | 27/40(67.5%) | 42/57(73.7%) |
1〜4週目において有害事象は93.3%(168/180例)に認められ、主な有害事象(発現頻度が20.0%以上)は低カリウム血症41.7%(75例)、低マグネシウム血症39.4%(71例)、貧血37.8%(68例)、血中クレアチニン増加29.4%(53例)、悪心28.9%(52例)、嘔吐28.9%(52例)であった。
<発熱性好中球減少症>
17.1.3 海外第III相試験
発熱性好中球減少症患者を対象とした臨床試験成績は下記のとおりで、主要評価項目である総合臨床効果は49.9%(171/343)であった(外国人データ)。
| 評価項目\投与量 | 1.5〜6.0mg/kg/日注) |
| 総合臨床効果 | 171/343(49.9%) |
| 治験薬投与終了後7日間の生存 | 318/343(92.7%) |
| 好中球減少期間中の解熱 | 199/343(58.0%) |
| 新たな真菌感染症の発症なし※1) | 294/343(85.7%) |
| 毒性又は無効で早期の投与中止なし | 294/343(85.7%) |
有害事象は99.7%(342/343例)に認められ、主な有害事象(発現頻度が30.0%以上)は発熱89.5%(307例)、悪寒47.5%(163例)、低カリウム血症42.9%(147例)、悪心39.7%(136例)、嘔吐31.8%(109例)、下痢30.3%(104例)であった。
<ヒストプラズマ症>
17.1.4 海外臨床試験
AIDS患者に併発した中等度から重度の播種性ヒストプラズマ症を対象とした臨床試験成績(投与量3.0mg/kg/日、投与期間2週間)における有効率は88.2%(45/51)であった3)(外国人データ)。
<リーシュマニア症>
17.2 製造販売後調査等
<真菌感染症、真菌感染が疑われる発熱性好中球減少症>
17.2.1 製造販売後臨床試験
小児患者39例(年齢:0〜15歳)を対象として実施された製造販売後臨床試験(投与量1.0〜5.0mg/kg/日注))のうち真菌感染症を対象とした臨床試験成績の概要は下記のとおりで、試験実施計画書に適合した対象集団(PPS)のうち総合効果が評価可能であった17例(年齢:1〜14歳)の総有効率は52.9%(9/17)であった。
| 真菌感染症疾患名 | 有効例数/症例数(有効率) | |
| アスペルギルス症 | 侵襲性肺アスペルギルス症 | 2/3 |
| 慢性壊死性肺アスペルギルス症 | 0/1 | |
| その他のアスペルギルス症 | 1/1 | |
| 合計 | 3/5 | |
| カンジダ症 | カンジダ血症 | 1/5 |
| 肝・脾カンジダ | 0/1 | |
| 合計 | 1/6(16.7%) | |
| クリプトコッカス症 | 肺クリプトコッカス症 | 1/1 |
| その他の真菌感染症 | 4/5 | |
| 合計 | 9/17(52.9%) | |
なお、真菌感染が疑われる発熱性好中球減少症では、PPSの5例(年齢:7〜15歳)において臨床的な改善は認められなかった。
副作用(臨床検査値の異常変動を含む)は92.3%(36/39例)に認められ、主な副作用は低カリウム血症・血中カリウム減少51.3%(20例)、β2ミクログロブリン増加28.2%(11例)、ALT増加23.1%(9例)、AST増加23.1%(9例)、BUN増加23.1%(9例)、嘔吐20.5%(8例)、血中クレアチニン増加20.5%(8例)等であった。
副作用(臨床検査値の異常変動を含む)は92.3%(36/39例)に認められ、主な副作用は低カリウム血症・血中カリウム減少51.3%(20例)、β2ミクログロブリン増加28.2%(11例)、ALT増加23.1%(9例)、AST増加23.1%(9例)、BUN増加23.1%(9例)、嘔吐20.5%(8例)、血中クレアチニン増加20.5%(8例)等であった。
注)本剤の承認された1日用量は、アムホテリシンBとして2.5mg(力価)/kg(但し、免疫不全状態のリーシュマニア症患者においては4mg(力価)/kg)である。なお、真菌感染症においては、患者の症状に応じて5mg(力価)/kgまで投与できる(但し、クリプトコッカス髄膜炎においては6mg(力価)/kgまで)。
18. 薬効薬理
18.1 作用機序
本剤の有効成分であるアムホテリシンBは、真菌及びリーシュマニア原虫のそれぞれの細胞膜成分であるエルゴステロール及びエピステロールに高い親和性を持ち、これらのステロールと結合することにより、細胞膜の透過性を高め、細胞質成分を漏出させることで真菌及びリーシュマニア原虫を死滅させる。一方、アムホテリシンBは動物細胞の細胞膜成分であるコレステロールに対しても、親和性は低いものの結合し、細胞傷害性を示す。
本剤は、リポソームのコレステロールを含む脂質二重膜中にアムホテリシンBを保持することにより、真菌及びリーシュマニア原虫に対する膜傷害活性を維持しつつ、動物細胞に対する膜傷害活性が低減されている。
本剤は、リポソームのコレステロールを含む脂質二重膜中にアムホテリシンBを保持することにより、真菌及びリーシュマニア原虫に対する膜傷害活性を維持しつつ、動物細胞に対する膜傷害活性が低減されている。
18.2 抗真菌作用
18.3 リーシュマニア原虫に対する作用
本剤はアムホテリシンBと同様にリーシュマニア原虫に対してin vitro抗原虫活性を示し、マウスのリーシュマニア症に対して治療効果を示す。
19. 有効成分に関する理化学的知見
19.1. アムホテリシンB
22. 包装
50mg[1バイアル(フィルター1個添付)]
23. 主要文献
- Jensen G.M.,et al., Clinica Chimica Acta., 411, 1900-1905, (2010)
- Walsh T.J.,et al., Antimicrob.Agents and Chemother., 42, 2391-2398, (1998) »PubMed
- Johnson P.C.,et al., Annals of Internal Medicine., 137, E-105-E-110, (2002)
- 社内資料:内臓型リーシュマニア症における有効性
- 馬庭貴司ほか, 日薬理誌, 129, 129-134, (2007) »PubMed
- 竹本浩司ほか, 臨床と微生物, 34, 759-766, (2007)
- Takemoto K.,et al., Microbiol.Immunol., 50, 579-586, (2006) »PubMed
- Takemoto K.,et al., J.Antimicrob.Chemother., 53, 311-317, (2004) »PubMed
- Takemoto K.,et al., J.Antimicrob.Chemother., 57, 724-731, (2006) »PubMed
- Takemoto K.,et al., Chemotherapy., 52, 271-278, (2006) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
住友ファーマ株式会社
くすり情報センター
〒541-0045
大阪市中央区道修町2-6-8
電話:0120-034-389
製品情報問い合わせ先
住友ファーマ株式会社
くすり情報センター
〒541-0045
大阪市中央区道修町2-6-8
電話:0120-034-389
26. 製造販売業者等
26.1 製造販売元
住友ファーマ株式会社
大阪市中央区道修町2-6-8
その他の説明
(補足情報)注射液の調製法
1 患者さんの体重にあわせ必要なバイアルを準備し、1バイアルにつき注射用水12mLを加える。
注意
●コアリング※防止のため、針刺し時はゴム栓の中心部に針を垂直に挿入すること。
●溶解には必ず注射用水を用い、それ以外のもの(生理食塩液等の電解質溶液等)は使用しないこと。
※コアリング:バイアルのゴム栓に注射針を穿刺するときに、ゴムの削片が生じ注射液に異物混入をおこす現象。
2 本剤は溶けにくいので、注射用水注入後、直ちに振とうし、均一な黄色の半透明な液になるまで激しく振り混ぜる。
注意
●溶解状態を目視にて確認し、溶け残りの小さな塊を認めた場合には、完全に溶解するまでさらに振とうを続けること。
3 完全に溶解した本剤は、黄色く半透明な液[4mg(力価)/mL]で泡立ちやすい。
4 溶解した本剤をシリンジに採取する。
注意
●針刺し時はゴム栓の中心部に針を垂直に挿入すること。
5 シリンジに添付のフィルター(孔径5μm)を取り付ける。
注意
●本フィルターは除菌フィルターではない。
●フィルターは汚染を避けるため、使用直前に開封し、速やかに使用すること。また、フィルターあるいはシリンジの接合部分(先端部分)は直接触らないこと。
●添付のフィルター(孔径5μm)以外のものを用いないこと。また、各々のバイアルについて新たなフィルターを使用すること。
6 採取した溶解薬液をフィルターろ過しながら5%ブドウ糖注射液に加え、静注用希釈液とする。
<参考>
・2.5mg/kg/日未満投与の場合、100mLの5%ブドウ糖注射液に希釈する。
・2.5mg/kg/日以上投与の場合、250mLの5%ブドウ糖注射液に希釈する。
注意
●希釈には必ず5%ブドウ糖注射液を用い、それ以外のものは用いないこと。
添付のフィルターについては「14.1薬剤調製時の注意」の項を参照すること。