医薬品情報
| 総称名 | キシロカイン |
|---|---|
| 一般名 | リドカイン |
| 欧文一般名 | Lidocaine |
| 製剤名 | リドカイン塩酸塩ゼリー |
| 薬効分類名 | 粘滑・表面麻酔剤 |
| 薬効分類番号 | 1214 |
| ATCコード | C01BB01 C05AD01 D04AB01 N01BB02 R02AD02 S01HA07 S02DA01 |
| KEGG DRUG |
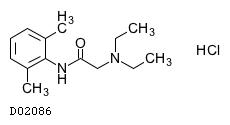
D02086
リドカイン塩酸塩
|
| KEGG DGROUP |
DG00196
リドカイン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年9月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 14.適用上の注意 15.その他の注意 16.薬物動態 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| キシロカインゼリー2% | Xylocaine Jelly 2% | サンドファーマ | 1214700P1054 | 6.3円/mL |
2. 禁忌
次の患者には投与しないこと
本剤の成分又はアミド型局所麻酔薬に対し過敏症の既往歴のある患者
4. 効能または効果
表面麻酔
6. 用法及び用量
リドカイン塩酸塩として、尿道麻酔には通常成人では男子は200〜300mg、女子は60〜100mgを使用する。気管内挿管には適当量を使用する。
なお、年齢、麻酔領域、部位、組織、体質により適宜増減する。
なお、年齢、麻酔領域、部位、組織、体質により適宜増減する。
8. 重要な基本的注意
8.1 まれにショックあるいは中毒症状を起こすことがあるので、本剤の投与に際しては、十分な問診により患者の全身状態を把握するとともに、異常が認められた場合に直ちに救急処置のとれるよう、常時準備をしておくこと。
8.2 本剤の投与に際し、その副作用を完全に防止する方法はないが、ショックあるいは中毒症状をできるだけ避けるために、以下の点に留意すること。
8.2.1 患者の全身状態の観察を十分に行うこと。
8.2.2 麻酔部位に応じ、できるだけ必要最少量とすること。特に他のリドカイン製剤と併用する場合には、総リドカイン量を考慮し過量投与とならないよう注意すること。
8.2.3 気道内表面麻酔の場合には、吸収が速いので、できるだけ少量を使用すること。
8.2.4 外傷、びらん、潰瘍又は炎症部位への投与は吸収が速いので注意すること。[13.参照]
8.3 本剤の投与により、誤嚥・口腔内咬傷の危険性を増加させるおそれがあるので注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.2 腎機能障害患者
9.2.1 重篤な腎機能障害のある患者
中毒症状が発現しやすくなる。
9.3 肝機能障害患者
9.3.1 重篤な肝機能障害のある患者
中毒症状が発現しやすくなる。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
幼児(特に3歳以下)には、低用量から投与を開始する等、患者の状態を観察しながら慎重に投与すること。麻酔効果の把握が困難なため高用量又は頻回投与されやすく、中毒を起こすことがある。[8.2.5参照]
9.8 高齢者
患者の全身状態の観察を十分に行う等、慎重に投与すること。一般に生理機能の低下により麻酔に対する忍容性が低下している。[8.2.5参照]
10. 相互作用
相互作用序文
本剤は、主として肝代謝酵素CYP1A2及びCYP3A4で代謝される。
薬物代謝酵素用語
CYP1A2
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| クラスIII抗不整脈剤 アミオダロン等 | 心機能抑制作用が増強するおそれがあるので、心電図検査等によるモニタリングを行うこと。 | 作用が増強することが考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック(頻度不明)
徐脈、不整脈、血圧低下、呼吸抑制、チアノーゼ、意識障害等を生じ、まれに心停止を来すことがある。また、まれにアナフィラキシーショックを起こしたとの報告がある。
11.1.2 意識障害、振戦、痙攣(いずれも頻度不明)
意識障害、振戦、痙攣等の中毒症状があらわれることがあるので、このような症状があらわれた場合には、直ちに投与を中止し、適切な処置を行うこと。[13.参照]
11.2 その他の副作用
| 頻度不明 | |
| 中枢神経注1) | 眠気、不安、興奮、霧視、眩暈等 |
| 消化器注1) | 悪心・嘔吐等 |
| 過敏症 | 蕁麻疹等の皮膚症状、浮腫等 |
13. 過量投与
局所麻酔剤の血中濃度の上昇に伴い、中毒が発現する。その症状は、主に中枢神経系及び心血管系の症状としてあらわれる。[8.2.4、11.1.2参照]
13.1 症状
13.1.1 中枢神経系の症状
初期症状として不安、興奮、多弁、口周囲の知覚麻痺、舌のしびれ、ふらつき、聴覚過敏、耳鳴、視覚障害、振戦等があらわれる。症状が進行すると意識消失、全身痙攣があらわれ、これらの症状に伴い低酸素血症、高炭酸ガス血症が生じるおそれがある。より重篤な場合には呼吸停止を来すこともある。
13.1.2 心血管系の症状
血圧低下、徐脈、心筋収縮力低下、心拍出量低下、刺激伝導系の抑制、心室性頻脈及び心室細動等の心室性不整脈、循環虚脱、心停止等があらわれる。
13.2 処置
振戦や痙攣が著明であれば、ジアゼパム又は超短時間作用型バルビツール酸製剤(チオペンタールナトリウム等)を投与する。
14. 適用上の注意
14.1 薬剤投与後の注意
本剤は金属を侵す性質があるので、長時間金属器具(匙等)に接触させないことが望ましい。なお、金属器具を使用した場合は、使用後十分に水洗すること。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 本剤の投与により、気管内挿管後の咽頭痛、嗄声等の発現を増加させたとの報告がある。
15.1.2 ポルフィリン症の患者に投与した場合、急性腹症、四肢麻痺、意識障害等の急性症状を誘発するおそれがある。
16. 薬物動態
16.1 血中濃度
患者に2%リドカイン液(リドカイン塩酸塩約25mg)を気管内挿管時に使用したとき、吸収は速く、血中濃度は15分後に0.1〜0.2μg/mLの最高濃度に達した1)(外国人データ)。
16.2 吸収
消化管からの吸収率は高いが、吸収後に肝臓で代謝されるために血中濃度の上昇への寄与は少ない。
16.3 分布
リドカイン2μg/mLの血漿蛋白結合率は約65%で、α1−酸性糖蛋白及びアルブミンと結合する。血液/血漿中濃度比は約0.8であることから、血球への分布は少ないと考えられる。妊婦にリドカイン塩酸塩を硬膜外投与注1)したとき、臍帯静脈血液中濃度と母体血漿中濃度の比は0.5〜0.7で、胎盤を通過する2)。
16.4 代謝
リドカインは、主として肝臓でN-脱エチル体monoethyl glycinexylidide(MEGX)に代謝された後、glycinexylidide(GX),2,6-xylidineに代謝され、投与量の約70%が4-hydroxy-2,6-xylidineとして尿中に排泄される2)。
16.5 排泄
リドカイン塩酸塩250mgを健康人に経口投与したとき、24時間後までの尿中放射能排泄率は投与量の83.8%、未変化体は投与量の2.8%であった3)(外国人データ)。
16.6 特定の背景を有する患者
18. 薬効薬理
18.1 作用機序
リドカイン塩酸塩は、神経膜のナトリウムチャネルをブロックし、神経における活動電位の伝導を可逆的に抑制し、知覚神経及び運動神経を遮断する局所麻酔薬である。
19. 有効成分に関する理化学的知見
19.1. リドカイン
22. 包装
[チューブ]
30mL×5本
23. 主要文献
- Ouellette,R.et al., Regional Anesthesia., 9, 200-202, (1984)
- Burm,A.G.L., Clin. Pharmacokinet., 16, 283-311, (1989) »PubMed
- Keenaghan,J.B.et al., J.Pharmacol.Exp.Ther., 180, 454-463, (1972) »PubMed
- Nation,R.L.et al., Br.J.Clin.Pharmacol., 4, 439-448, (1977) »PubMed
- Thomson,P.D.et al., Ann.Intern.Med., 78, 499-508, (1973) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
サンド株式会社
カスタマーケアグループ
〒105-6333
東京都港区虎ノ門1-23-1
電話:0120-982-001
FAX:03-6257-3633
製品情報問い合わせ先
サンド株式会社
カスタマーケアグループ
〒105-6333
東京都港区虎ノ門1-23-1
電話:0120-982-001
FAX:03-6257-3633