医薬品情報
| 総称名 | ル・エストロジェル |
|---|---|
| 一般名 | エストラジオール |
| 欧文一般名 | Estradiol |
| 製剤名 | エストラジオール外用ゲル剤 |
| 薬効分類名 | 経皮吸収エストラジオール製剤 |
| 薬効分類番号 | 2473 |
| ATCコード | G03CA03 |
| KEGG DRUG |
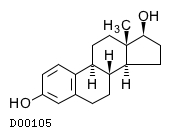
D00105
エストラジオール
|
| KEGG DGROUP |
DG00462
エストラジオール
DG01986
卵胞ホルモン
DG01584
エストロゲン受容体作動薬
DG03232
骨粗鬆症治療薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年10月 改訂(第5版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ル・エストロジェル0.06% | l'estrogel 0.06% | 富士製薬工業 | 2473700M2026 | 19.1円/g | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
<効能共通>
2.1 エストロゲン依存性悪性腫瘍(例えば、乳癌、子宮内膜癌)及びその疑いのある患者[腫瘍の悪化あるいは顕性化を促すことがある。][8.5参照]
2.2 乳癌の既往歴のある患者[乳癌が再発するおそれがある。][8.5参照]
2.3 未治療の子宮内膜増殖症のある患者[子宮内膜増殖症は細胞異型を伴う場合がある。][8.5参照]
2.4 血栓性静脈炎や肺塞栓症のある患者、又はその既往歴のある患者[卵胞ホルモン剤は凝固因子を増加させ、血栓形成傾向を促進するとの報告がある。][11.1.2参照]
2.6 本剤の成分に対し過敏症の既往歴のある患者
2.7 授乳婦[9.6参照]
2.8 重篤な肝障害のある患者[9.3.1参照]
2.9 診断の確定していない異常性器出血のある患者[出血が子宮内膜癌による場合は、癌の悪化あるいは顕性化を促すことがある。][8.5参照]
2.10 ポルフィリン症で急性発作の既往歴のある患者[症状を悪化させるおそれがある。]
<更年期障害及び卵巣欠落症状に伴う血管運動神経症状(Hot flush及び発汗)、生殖補助医療における調節卵巣刺激の開始時期の調整>
2.11 妊婦又は妊娠している可能性のある女性[9.5.1参照]
4. 効能または効果
○更年期障害及び卵巣欠落症状に伴う血管運動神経症状(Hot flush及び発汗)
○生殖補助医療における調節卵巣刺激の開始時期の調整
○凍結融解胚移植におけるホルモン補充周期
5. 効能または効果に関連する注意
<生殖補助医療における調節卵巣刺激の開始時期の調整、凍結融解胚移植におけるホルモン補充周期>
6. 用法及び用量
<更年期障害及び卵巣欠落症状に伴う血管運動神経症状(Hot flush及び発汗)>
通常、成人に対しル・エストロジェル2プッシュ(1.8g、エストラジオールとして1.08mg含有)を1日1回、両腕の手首から肩までの広い範囲に塗擦する。なお、症状に応じて、適宜減量する。減量する場合は、ル・エストロジェル1プッシュ(0.9g、エストラジオールとして0.54mg含有)を1日1回、両腕の手首から肩までの広い範囲に塗擦する。
<生殖補助医療における調節卵巣刺激の開始時期の調整>
通常、ル・エストロジェル1又は2プッシュ(0.9又は1.8g、エストラジオールとして0.54又は1.08mg含有)を1日1回、21〜28日間、両腕の手首から肩までの広い範囲に塗擦し、投与期間の後半に黄体ホルモン剤を併用する。
<凍結融解胚移植におけるホルモン補充周期>
通常、ル・エストロジェル2〜10プッシュ(1.8〜9.0g、エストラジオールとして1.08〜5.40mg含有)を1日1回、両腕の手首から肩、腹部、大腿部及び腰部の広い範囲に塗擦し、子宮内膜の十分な肥厚が得られた時点で、黄体ホルモン剤の併用を開始して、妊娠8週まで本剤の投与を継続する。
7. 用法及び用量に関連する注意
<凍結融解胚移植におけるホルモン補充周期>
本剤の妊娠成立後の投与期間は、本剤投与より予想されるリスクと患者の状態を考慮して慎重に判断し、漫然と投与を継続せず、最長妊娠10週を超えないこと。
8. 重要な基本的注意
<効能共通>
8.2 本剤投与後の血清中エストラジオール濃度の個人間及び個人内変動は大きく、過度に上昇する場合があり、定期的に血清中エストラジオール及びFSHを測定すること。
8.3 血清中エストラジオール濃度が過度に上昇していると判断された場合、副作用の発現に留意し、本剤の投与中止等の適切な対応をとること。
<更年期障害及び卵巣欠落症状に伴う血管運動神経症状(Hot flush及び発汗)>
8.4 外国において、卵胞ホルモン剤と黄体ホルモン剤を長期併用した女性では、乳癌になる危険性が対照群の女性と比較して高くなり、その危険性は併用期間が長期になるに従って高くなるとの報告があるので、本剤の使用にあたっては、患者に対し本剤のリスクとベネフィットについて十分な説明を行うとともに必要最小限の使用にとどめ、漫然と長期投与を行わないこと。[15.1.3参照]
<生殖補助医療における調節卵巣刺激の開始時期の調整、凍結融解胚移植におけるホルモン補充周期>
8.6 本剤は、不妊治療に十分な知識と経験のある医師のもとで使用すること。本剤投与により予想されるリスク及び注意すべき症状について、あらかじめ患者に説明を行うこと。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 子宮筋腫のある患者
子宮筋腫の発育を促進するおそれがある。[8.5参照]
9.1.2 子宮内膜症のある患者
症状が増悪するおそれがある。[8.5参照]
9.1.3 乳癌家族素因が強い患者、又は乳房結節、乳腺症を有する患者、乳房レントゲン像に異常がみられた患者
定期的に乳房検診を行うなど慎重に使用すること。卵胞ホルモン剤投与と乳癌発生との因果関係については未だ明らかではないが、使用期間と相関性があることを示唆する疫学調査の結果が報告されている。また、動物実験において乳腺腺腫が認められている。[8.5参照]
9.1.4 高血圧、心疾患、又はその既往歴のある患者
卵胞ホルモン剤の過量投与では体液貯留をきたし、これらの疾患を悪化させるおそれがある。
9.1.5 糖尿病患者
十分管理を行いながら使用すること。耐糖能を低下させるおそれがある。
9.1.6 片頭痛、てんかんのある患者
観察を十分に行うこと。症状を悪化させることがある。
9.1.7 術前又は長期臥床状態の患者
9.1.8 全身性エリテマトーデスの患者
症状を悪化させるおそれがある。
9.2 腎機能障害患者
9.2.1 腎疾患のある患者又はその既往歴のある患者
卵胞ホルモン剤の過量投与では体液貯留をきたし、これらの疾患を悪化させるおそれがある。
9.3 肝機能障害患者
9.3.1 重篤な肝障害のある患者
使用しないこと。代謝能が低下しており肝臓への負担が増加するため、症状が増悪することがある。[2.8参照]
9.3.2 肝障害のある患者(重篤な肝障害のある患者を除く)
定期的に肝機能検査を実施するなど観察を十分に行うこと。肝障害を悪化させるおそれがある。
9.5 妊婦
<更年期障害及び卵巣欠落症状に伴う血管運動神経症状(Hot flush及び発汗)、生殖補助医療における調節卵巣刺激の開始時期の調整>
9.5.1 妊婦又は妊娠している可能性のある女性には使用しないこと。[2.11参照]
<効能共通>
9.5.2 卵胞ホルモン剤であるジエチルスチルベストロールを妊娠動物(マウス)又は妊婦に投与したとき、出生児に生殖器系臓器の異常が報告されている。エストラジオールのヒトにおける催奇形性の報告はないが、妊娠動物(ラット)への投与によって児の生殖器系臓器に異常が起こることが報告されている。ヒトにおいて、妊娠中の女性ホルモン剤(経口避妊薬等)投与によって児の先天性異常(先天性心臓奇形及び四肢欠損症)のリスク増加の報告がある。
9.5.3 卵胞ホルモン剤を妊娠動物(マウス)に投与した場合、児の成長後、腟上皮及び子宮内膜の癌性変化を示唆する結果が報告されている。また、新生児(マウス)に投与した場合、児の成長後腟上皮の癌性変化を認めたとの報告がある。
9.6 授乳婦
使用しないこと。
ヒトにおいて、母乳中への移行が報告されている。また、動物実験(マウス)で新生児に卵胞ホルモン剤を投与した場合、児の成長後腟上皮の癌性変化を認めたとの報告がある。[2.7参照]
ヒトにおいて、母乳中への移行が報告されている。また、動物実験(マウス)で新生児に卵胞ホルモン剤を投与した場合、児の成長後腟上皮の癌性変化を認めたとの報告がある。[2.7参照]
9.8 高齢者
患者の状態を観察しながら慎重に使用すること。一般に生理機能が低下している。
10. 相互作用
相互作用序文
本剤は主に薬物代謝酵素チトクロームP450(CYP3A4)で代謝されるので、本酵素の活性に影響を及ぼす薬剤と併用する場合には、注意して使用すること。
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| リファンピシン 抗てんかん剤 フェノバルビタール フェニトイン カルバマゼピン HIV逆転写酵素阻害剤 エファビレンツ セイヨウオトギリソウ(St.John's Wort、セント・ジョーンズ・ワート)含有食品 ステロイドホルモン | 本剤の代謝が促進され、血中濃度が低下するおそれがある。 | これらの薬剤等は薬物代謝酵素チトクロームP450(CYP3A4)を誘導することにより、本剤の代謝を促進し、血中濃度を低下させる可能性がある。 |
| プロテアーゼ阻害剤 リトナビル ネルフィナビル等 | 本剤の血中濃度が変化するおそれがある。 | これらの薬剤は薬物代謝酵素チトクロームP450(CYP3A4)を誘導又は阻害する可能性がある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 アナフィラキシー(頻度不明)
11.1.2 静脈血栓塞栓症、血栓性静脈炎(いずれも頻度不明)
11.2 その他の副作用
| 1%以上 | 1%未満 | 頻度不明 | |
| 生殖器 | 腟分泌物(18.3%)、性器出血、陰部そう痒症、骨盤痛 | 消退出血、不正子宮出血、外性器痛、外陰部炎、外陰腟不快感、子宮内膜生検異常、子宮筋腫、子宮頚管ポリープ | 腟乾燥、陰部そう痒症、子宮内膜症(再燃) |
| 乳房 | 乳房不快感(13.2%)、乳房痛、乳頭痛 | 乳房嚢胞 | |
| 皮膚 投与部位 | そう痒感、紅斑、湿疹 | 色素沈着変化、乾燥、刺激感 | |
| 皮膚 全身 | 湿疹、紅斑、色素沈着障害、そう痒症、ざ瘡 | じん麻疹 | |
| 精神神経系 | めまい、頭痛 | しびれ感、抑うつ気分、睡眠障害、傾眠 | 易刺激性、片頭痛 |
| 循環器 | 動悸、高血圧 | ||
| 消化器 | 膨満感 | 食欲不振、悪心、下痢、腹痛、逆流性食道炎 | 嘔吐、排便痛 |
| 肝臓 | 肝機能異常(AST増加、ALT増加、ALP増加) | ||
| 血液 | 白血球数減少、貧血(赤血球数減少、ヘモグロビン量減少、ヘマトクリット値低下) | ||
| 骨・筋肉 | 背部痛、四肢痛、筋骨格硬直、関節炎 | 四肢重感 | |
| その他 | 血中トリグリセリド増加、浮腫 | 疲労、潮紅、血中Ca減少、アンチトロンビンIII減少、耳鳴、耳不快感、鼻出血、血中フィブリノゲン増加 | コンタクトレンズ不耐性、鼻咽頭炎、過換気 |
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 塗布部位
(1)顔面、乳房、外陰部及び粘膜には塗布しないこと。
(2)創傷面又は湿疹、皮膚炎等(重度の乾燥や日焼けなどによる皮膚炎も含む)がみられる部位は避けて塗布すること。
(3)投与後1時間以内の投与部位の洗浄は十分な血中濃度が得られない可能性がある。また、投与直後にアルコールを多量に含む化粧品等の使用は避けること。
(4)投与後は手を洗うこと。また、投与直後は投与部位を他人に触れさせないこと。
14.1.2 塗布時
(1)初めて使用するときには、本剤が出るまでポンプを数回押してから使用すること。
(2)本剤はアルコールを含有するため、投与後は十分換気を行い、ゲルが乾燥するまでは火気及び喫煙を避けること。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 ホルモン補充療法(HRT)と子宮内膜癌の危険性
卵胞ホルモン剤を長期間(約1年以上)使用した閉経期以降の女性では、子宮内膜癌になる危険性が対照群の女性と比較して高く、この危険性は、使用期間に相関して上昇し(1〜5年間で2.8倍、10年以上で9.5倍)、黄体ホルモン剤の併用により抑えられる(対照群の女性と比較して0.8倍)との疫学調査の結果が報告されている1)。
15.1.2 更年期障害及び卵巣欠落症状に伴う血管運動神経症状に対する黄体ホルモン剤の併用投与については、以下のいずれかの方法で行うことが望ましい。
(1)持続的投与方式
| 本剤 | 持続投与 |
| 黄体ホルモン剤 | 持続投与 |
本剤の投与期間中、黄体ホルモン剤を1日1回連日併用投与する。
(2)周期的投与方式
| 本剤 | 持続投与28日 | |
| 黄体ホルモン剤 | 投与なし | 12〜14日間 |
黄体ホルモン剤を併用して毎月12〜14日間投与する。
15.1.3 HRTと乳癌の危険性
HRTと乳癌発生との因果関係については明らかではないが、次のような報告がある。
(1)米国における閉経後女性を対象とした無作為化臨床試験(Women's Health Initiative(WHI)試験)の結果、結合型エストロゲン・黄体ホルモン配合剤投与群では、乳癌になる危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.24)との報告がある2)。並行して行われた子宮摘出者に対する試験の結果、結合型エストロゲン単独投与群では、乳癌になる危険性がプラセボ投与群と比較して有意差はない(ハザード比:0.80)との報告がある3)4)。[8.4参照]
(2)英国における疫学調査(Million Women Study(MWS))の結果、卵胞ホルモン剤と黄体ホルモン剤を併用している女性では、乳癌になる危険性が対照群と比較して有意に高くなり(2.00倍)、この危険性は、併用期間が長期になるに従って高くなる(1年未満:1.45倍、1〜4年:1.74倍、5〜9年:2.17倍、10年以上:2.31倍)との報告がある5)。[8.4参照]
(3)閉経後女性を対象とした大規模な疫学調査のメタアナリシスの結果、閉経期ホルモン補充療法(MHT)として卵胞ホルモン剤を単独投与又は卵胞ホルモン剤と黄体ホルモン剤を併用した女性は、乳癌になる危険性がMHTの期間とともに高くなり(調整リスク比[95%信頼区間]は1〜4年間の卵胞ホルモン剤と黄体ホルモン剤併用:1.60[1.52-1.69]、卵胞ホルモン剤単独:1.17[1.10-1.26]、5〜14年間の卵胞ホルモン剤と黄体ホルモン剤併用:2.08[2.02-2.15]、卵胞ホルモン剤単独:1.33[1.28-1.37])、MHT非使用者に対する調整リスク比はMHT過去使用者よりMHT現使用者の方が高かった。また、MHT過去使用者において、投与中止後も過去の投与期間に依存して乳癌になる危険性が10年以上持続する場合があるとの報告がある6)。[8.4参照]
15.1.4 HRTと冠動脈性心疾患の危険性
15.1.5 HRTと脳卒中の危険性
15.1.6 HRTと認知症の危険性
15.1.7 HRTと卵巣癌の危険性
(2)米国におけるWHI試験の結果、結合型エストロゲン・黄体ホルモン配合剤投与群において、卵巣癌になる危険性がプラセボ投与群と比較して有意ではないが、高い傾向がみられた(ハザード比:1.58)との報告がある15)。
15.1.8 HRTと胆のう疾患の危険性
米国におけるWHI試験の結果、結合型エストロゲン・黄体ホルモン配合剤投与群において、胆のう疾患になる危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.59)との報告がある。並行して行われた子宮摘出者に対する試験の結果、結合型エストロゲン単独投与群では、胆のう疾患になる危険性がプラセボ投与群と比較して有意に高くなる(ハザード比:1.67)との報告がある16)。
15.1.9 卵胞ホルモン剤の長期投与により、ヒトで肝腫瘍が発生したとの報告がある。
15.1.10 調節卵巣刺激の前周期に低用量卵胞ホルモン・黄体ホルモン配合剤を投与した場合の生産率及び継続妊娠率は、投与しなかった場合と比較して低かったとの報告がある17)。[5.参照]
15.1.11 ホルモン補充周期での凍結融解胚移植は自然排卵周期での凍結融解胚移植と比較して妊娠率及び生産率が低く、流産率が高かったとの報告がある18)。[5.参照]
15.2 非臨床試験に基づく情報
実験動物に卵胞ホルモン剤を皮下投与(埋め込み投与を含む)したとき、マウスにおけるリンパ系腫瘍、ラットの下垂体腺腫及びハムスターにおいては腎腫瘍の発生が報告されている。
16. 薬物動態
16.1 血中濃度
健康閉経後女性に本剤1.25及び1.8gを反復投与(1日1回、14日間)したときの血清中エストラジオール(E2)濃度は、いずれの投与群においても初回投与72時間後(3回目投与24時間後)に定常状態に達した。
定常状態(初回投与72〜336時間後)の平均血清中E2濃度は、1.25及び1.8g群でそれぞれ、26.3及び60.8pg/mLであった。
いずれの投与群においても概ね最終投与120時間後(初回投与432時間後)には、ほぼ投与前値まで回復しており蓄積性は認められなかった19)。
定常状態(初回投与72〜336時間後)の平均血清中E2濃度は、1.25及び1.8g群でそれぞれ、26.3及び60.8pg/mLであった。
いずれの投与群においても概ね最終投与120時間後(初回投与432時間後)には、ほぼ投与前値まで回復しており蓄積性は認められなかった19)。
反復投与時の血清中エストラジオール(E2)濃度推移(平均値、標準誤差)
| パラメータ | 投与量 | |
| 1.25g注) (n=5〜6) | 1.8g (n=6) | |
| Css(pg/mL) | 26.3±4.8 | 60.8±22.6 |
| AUC312-336(pg・hr/mL) | 756.2±233.0 | 1269.4±371.1 |
| Cmax(pg/mL) | 46.58±25.67 | 59.53±11.02 |
| Tmax(hr) | 19.2±6.6 | 20.0±6.2 |
| T1/2(hr) | 87.6±27.9 | 94.9±16.8 |
更年期障害及び卵巣欠落症状を有する患者に本剤1.8gを1日1回、8週間投与したときの8週後の血清中エストラジオール(E2)濃度の平均値±標準偏差は112.1±68.8pg/mL、中央値は91.4pg/mLであった。
注)本剤の更年期障害及び卵巣欠落症状に伴う血管運動神経症状に対する承認用量は、1日1回1.8gである。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<更年期障害及び卵巣欠落症状に伴う血管運動神経症状(Hot flush及び発汗)>
国内で実施した更年期障害及び卵巣欠落症状を有する患者を対象とした用量設定試験及び長期投与試験において、本剤の有効性が認められている。また、国内で実施した低用量維持療法試験において、本剤1.8g/日で改善効果を示した患者では、0.9g/日に減量し継続投与することで、治療効果を維持することが認められている。
17.1.1 国内用量設定試験
更年期障害及び卵巣欠落症状を有する患者(平均年齢±標準偏差50.2±5.6)にプラセボ、本剤1.8gを1日1回、8週間投与した。その結果、Hot flush回数の最終改善度は、プラセボ群と比較して1.8g群において有意差が認められ(Steel検定:p=0.0072)、最終改善率(中等度改善以上)は、プラセボ群70.8%(34/48)に対し、1.8g群は94.3%(50/53)であった20)。
また、血管運動神経症状の最終改善度(Hot flush回数の改善度、Hot flush程度の改善度及び発汗の改善度の総合評価)はプラセボ群と比較して1.8g群において有意差が認められ(Steel検定:p=0.0026)、最終改善率(中等度改善以上)は、プラセボ群62.5%(30/48)に対し、1.8g群は90.6%(48/53)であった20)。
また、血管運動神経症状の最終改善度(Hot flush回数の改善度、Hot flush程度の改善度及び発汗の改善度の総合評価)はプラセボ群と比較して1.8g群において有意差が認められ(Steel検定:p=0.0026)、最終改善率(中等度改善以上)は、プラセボ群62.5%(30/48)に対し、1.8g群は90.6%(48/53)であった20)。
| 投与群 | 著明改善a)(%) | 中等度改善a)(%) | 軽度改善a)(%) | 不変a)(%) | 悪化a)(%) | 計 | 平均値b)±標準偏差 | Steel検定c) | 最終改善率(中等度改善以上)(%) |
| プラセボ群 | 27(56.3) | 7(14.6) | 10(20.8) | 3(6.3) | 1(2.1) | 48 | 2.2±1.10 | − | 34/48(70.8) |
| 1.8g群 | 43(81.1) | 7(13.2) | 3(5.7) | 0(0.0) | 0(0.0) | 53 | 2.8±0.55 | p=0.0072 | 50/53(94.3) |
| 時期 | 投与群 | Hot flush回数 |
| 観察期 | プラセボ群 n=48 | 5.3±2.25 5(3〜14) |
| 1.8g投与群 n=53 | 5.3±1.87 5(3〜11) | |
| 8週後 (中止時) | プラセボ群 n=48 | 1.9±2.12 1(0〜7) |
| 1.8g投与群 n=53 | 0.8±1.32 0(0〜8) |
安全性評価対象例161例中108例(67.1%)に副作用が認められた。主な副作用は、腟分泌物46.0%(74/161)、乳房不快感31.7%(51/161)、性器出血NOS8.1%(13/161)、投与部位そう痒感6.8%(11/161)、乳頭痛5.0%(8/161)、乳房痛4.3%(7/161)、投与部位紅斑4.3%(7/161)等であった20)。
17.1.2 国内長期投与試験
更年期障害及び卵巣欠落症状を有する患者(平均年齢±標準偏差51.5±3.7)に本剤1.8gを1日1回、24週間投与した。その結果、Hot flush回数の改善度における時期別の改善率(中等度改善以上)は、投与4、8、12、16、20及び24週後でそれぞれ64.2%(43/67)、86.2%(56/65)、88.5%(54/61)、95.2%(59/62)、95.2%(59/62)及び96.7%(59/61)であった21)。
また、血管運動神経症状の改善度における24週後の改善率(中等度改善以上)は、95.1%(58/61)であった21)。
また、血管運動神経症状の改善度における24週後の改善率(中等度改善以上)は、95.1%(58/61)であった21)。
| 時期 | 投与群 | Hot flush回数 |
| 観察期 | 1.8g投与群 n=68 | 3.9±1.9 4(1〜11) |
| 24週後 (中止時) | 1.8g投与群 n=61 | 0.3±0.6 0(0〜2) |
安全性評価対象例68例中28例(41.2%)に副作用が認められた。主な副作用は、骨盤痛NOS11.8%(8/68)、性器出血NOS8.8%(6/68)、腟分泌物7.4%(5/68)、腟カンジダ症2.9%(2/68)、乳頭痛2.9%(2/68)、乳房不快感2.9%(2/68)、投与部位そう痒感2.9%(2/68)、投与部位湿疹1.5%(1/68)、投与部位発疹1.5%(1/68)等であった21)。
17.1.3 国内低用量維持療法試験
更年期障害及び卵巣欠落症状を有する患者(平均年齢±標準偏差51.7±4.0)に本剤1.8gを1日1回、8週間投与した後、著明改善(Hot flush回数が投与前の1/3未満に減少)を示した患者をプラセボ群又は本剤の低用量(0.9g)群に無作為に割り付け、1日1回、16週間投与した。その結果、Hot flush回数の最終改善度は、プラセボ群と比較して0.9g群において有意差が認められ(2標本Wilcoxon検定:p=0.0097)、最終改善率(中等度改善以上)は、プラセボ群87.4%(76/87)に対し、0.9g群は97.7%(85/87)であった22)。
また、血管運動神経症状の最終改善度(Hot flush回数の改善度、Hot flush程度の改善度及び発汗の改善度の総合評価)は、プラセボ群と比較して0.9g群において有意差が認められ(2標本Wilcoxon検定:p=0.0031)、最終改善率(中等度改善以上)は、プラセボ群74.7%(65/87)に対し、0.9g群は95.4%(83/87)であった22)。
また、血管運動神経症状の最終改善度(Hot flush回数の改善度、Hot flush程度の改善度及び発汗の改善度の総合評価)は、プラセボ群と比較して0.9g群において有意差が認められ(2標本Wilcoxon検定:p=0.0031)、最終改善率(中等度改善以上)は、プラセボ群74.7%(65/87)に対し、0.9g群は95.4%(83/87)であった22)。
| 投与群 | 著明改善a)(%) | 中等度改善a)(%) | 軽度改善a)(%) | 不変a)(%) | 悪化a)(%) | 判定不能 | 計 | 2標本Wilcoxon検定b) | 最終改善率(中等度改善以上)(%) |
| プラセボ群 | 67(77.0) | 9(10.3) | 4(4.6) | 2(2.3) | 5(5.7) | 2 | 89 | − | 76/87(87.4) |
| 0.9g群 | 79(90.8) | 6(6.9) | 1(1.1) | 1(1.1) | 0(0.0) | 1 | 88 | p=0.0097 | 85/87(97.7) |
| 時期 | 投与群 | Hot flush回数 |
| 観察期 | プラセボ群a) n=89 | 6.4±5.0 5(3〜35) |
| 0.9g投与群a) n=88 | 5.8±3.5 4(3〜23) | |
| 8週後 | プラセボ群a) n=89 | 0.4±1.1 0(0〜8) |
| 0.9g投与群a) n=88 | 0.3±0.7 0(0〜4) | |
| 24週後 (中止時) | プラセボ群 n=87 | 1.7±3.8 0(0〜24) |
| 0.9g投与群 n=87 | 0.4±1.1 0(0〜6) |
また、安全性評価対象例209例中74例(35.4%)に副作用(臨床検査値の異常を含む)が認められた。主な副作用は、骨盤痛13.4%(28/209)、性器出血7.2%(15/209)等であった。
18. 薬効薬理
18.1 作用機序
<更年期障害及び卵巣欠落症状に伴う血管運動神経症状(Hot flush及び発汗)>
卵巣からのエストロゲン分泌が急激に減少又は消失することにより、Hot flush、発汗等の血管運動神経症状及び泌尿生殖器の萎縮症状等が発現する。本剤は、17β-エストラジオールを経皮より直接全身循環へ供給し、エストラジオールの血中濃度を閉経前女性の卵胞期前期に認められる生理的血中濃度と同レベルに維持することにより、これらの症状を改善する。
<生殖補助医療における調節卵巣刺激の開始時期の調整>
E2による子宮内膜の増殖は、黄体ホルモンにより抑制され、子宮内膜が分泌期像へと変化する。その後、E2及び黄体ホルモンの血中濃度を急激に低下させることにより子宮内膜がはく落し、生殖補助医療における調節卵巣刺激の開始時期を規定する消退出血が生じる。
<凍結融解胚移植におけるホルモン補充周期>
ホルモン補充周期において、E2により子宮内膜を肥厚させた後、黄体ホルモンにより子宮内膜を分泌期像へと変化させることで、妊娠の成立及び維持が可能な子宮内膜が形成される。
18.2 女性ホルモン作用
卵巣摘出ラットに本剤(エストラジオールとして0.3、1、3、10、30μg/kg)を1日1回、2週間連続経皮投与した。その結果、卵巣摘出による体重増加及び子宮萎縮を用量依存的に抑制し、また発情期様状態を呈する動物の増加が認められた23)。
19. 有効成分に関する理化学的知見
19.1. エストラジオール
20. 取扱い上の注意
20.1 火気を避けて保管すること。
20.2 小児の手の届かないところに保管すること。
22. 包装
ボトル 80g×1
23. 主要文献
- Grady,D.,et al., Obstet.Gynecol., 85 (2), 304, (1995) »PubMed »DOI
- Chlebowski,R.T.,et al., JAMA., 289 (24), 3243, (2003) »PubMed »DOI
- Anderson,G.L.,et al., JAMA., 291 (14), 1701, (2004) »PubMed »DOI
- Stefanick,M.L.,et al., JAMA., 295 (14), 1647, (2006) »PubMed »DOI
- Beral,V.,et al., Lancet., 362 (9382), 419, (2003) »PubMed »DOI
- Collaborative Group on Hormonal Factors in Breast Cancer, Lancet., 394, 1159-1168, (2019)
- Manson,J.E.,et al., New Engl.J.Med., 349 (6), 523, (2003) »PubMed
- Wassertheil-Smoller,S.,et al., JAMA., 289 (20), 2673, (2003) »PubMed
- Hendrix,S.L.,et al., Circulation., 113 (20), 2425, (2006) »PubMed
- Shumaker,S.A.,et al., JAMA., 289 (20), 2651, (2003) »PubMed
- Shumaker,S.A.,et al., JAMA., 291 (24), 2947, (2004) »PubMed
- Rodriguez,C.,et al., JAMA., 285 (11), 1460, (2001) »PubMed
- Lacey,J.V.Jr.,et al., JAMA., 288 (3), 334, (2002) »PubMed
- Beral,V.,et al., Lancet., 369 (9574), 1703, (2007) »PubMed
- Anderson,G.L.,et al., JAMA., 290 (13), 1739, (2003) »PubMed
- Cirillo,D.J.,et al., JAMA., 293 (3), 330, (2005) »PubMed
- Cochrane Database Syst Rev, 5, (2017), (CD006109)
- Human Reprod, 34, 1567-75, (2019)
- 社内資料:国内反復投与試験/国内反復投与試験II(薬物動態)(2006年10月20日承認、CTD2.7.6.5)
- 社内資料:国内用量設定試験(2006年10月20日承認、CTD2.7.6.9)
- 社内資料:国内長期投与試験(2006年10月20日承認、CTD2.7.6.13)
- Mizunuma,H., Climacteric., 14 (5), 581, (2011) »PubMed
- 社内資料:効力を裏付ける試験(薬理作用)(2006年10月20日承認、CTD2.6.2.2)
24. 文献請求先及び問い合わせ先
文献請求先
富士製薬工業株式会社
くすり相談室
〒939-3515
富山県富山市水橋辻ヶ堂1515番地
電話:0120-956-792
FAX:076-478-0336
製品情報問い合わせ先
富士製薬工業株式会社
くすり相談室
〒939-3515
富山県富山市水橋辻ヶ堂1515番地
電話:0120-956-792
FAX:076-478-0336
26. 製造販売業者等
26.1 製造販売元
富士製薬工業株式会社
富山県富山市水橋辻ヶ堂1515番地