医薬品情報
| 総称名 | アルダクトン |
|---|---|
| 一般名 | スピロノラクトン |
| 欧文一般名 | Spironolactone |
| 製剤名 | スピロノラクトン細粒・スピロノラクトン錠 |
| 薬効分類名 | 抗アルドステロン性利尿・降圧剤 |
| 薬効分類番号 | 2133 |
| ATCコード | C03DA01 |
| KEGG DRUG |
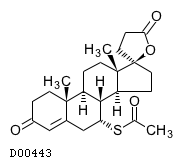
D00443
スピロノラクトン
|
| KEGG DGROUP |
DG01676
アルドステロン拮抗薬
DG03231
血圧降下薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年3月 改訂(第4版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アルダクトンA細粒10% | Aldactone-A Fine Granules 10% | ファイザー | 2133001C1097 | 40.8円/g | 処方箋医薬品注) |
| アルダクトンA錠25mg | Aldactone-A Tablets 25mg | ファイザー | 2133001F1522 | 11.5円/錠 | 処方箋医薬品注) |
| アルダクトンA錠50mg | Aldactone-A Tablets 50mg | ファイザー | 2133001F2057 | 22.9円/錠 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
6. 用法及び用量
スピロノラクトンとして、通常成人1日50〜100mgを分割経口投与する。
なお、年齢、症状により適宜増減する。
ただし、「原発性アルドステロン症の診断および症状の改善」のほかは他剤と併用することが多い。
なお、年齢、症状により適宜増減する。
ただし、「原発性アルドステロン症の診断および症状の改善」のほかは他剤と併用することが多い。
8. 重要な基本的注意
8.1 連用する場合、高カリウム血症等の電解質異常があらわれることがあるので、定期的に検査を行うこと。[11.1.1参照]
8.2 降圧作用に基づくめまい等があらわれることがあるので、高所作業、自動車の運転等危険を伴う機械を操作する際には注意させること。
8.3 夜間の休息が特に必要な患者には、夜間の排尿を避けるため、午前中に投与することが望ましい。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 重篤な冠動脈硬化症又は脳動脈硬化症のある患者
急激な利尿があらわれた場合、急速な血漿量減少、血液濃縮を来し、血栓塞栓症を誘発するおそれがある。
9.1.2 減塩療法中の患者
水分・電解質が欠乏し、脱水症状や低ナトリウム血症等があらわれやすくなる。[11.1.1参照]
9.2 腎機能障害患者
9.2.1 急性腎不全の患者
9.2.2 重篤な腎障害のある患者
腎機能を更に悪化させるおそれがある。また、腎からのカリウム排泄が低下しているため高カリウム血症を誘発又は増悪させるおそれがある。
9.3 肝機能障害患者
高カリウム血症が発現するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。カンレノ酸(スピロノラクトンの主要な活性代謝物)はヒト乳汁中へ移行することが認められている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。乳児は電解質バランスがくずれやすい。[11.1.1参照]
9.8 高齢者
次の点に注意し、少量から投与を開始するなど患者の状態を観察しながら慎重に投与すること。
9.8.1 急激な利尿は血漿量の減少を来し、脱水、低血圧等による立ちくらみ、めまい、失神等を起こすことがある。
9.8.2 心疾患がある又は心疾患等で浮腫がある場合は急激な利尿は急速な血漿量の減少と血液濃縮を来し、脳梗塞等の血栓塞栓症を誘発するおそれがある。
9.8.3 一般に過度の降圧は好ましくないとされている。脳梗塞等が起こるおそれがある。
9.8.4 腎機能又肝機能が低下していることが多いため、高カリウム血症があらわれやすい。
10. 相互作用
10.1 併用禁忌
10.2 併用注意
| 降圧剤 ACE阻害剤 カルシウム拮抗剤 β-遮断剤 利尿降圧剤等 | 降圧作用を増強することがあるので、用量を調節するなど注意する。 | これらの薬剤と本剤の相加・相乗作用 |
| カリウム製剤 塩化カリウム グルコン酸カリウム アスパラギン酸カリウム 等 ACE阻害剤 カプトプリル エナラプリル リシノプリル等 アンジオテンシンII受容体拮抗剤 ロサルタンカリウム カンデサルタンシレキセチル バルサルタン等 アリスキレン カリウム保持性利尿剤 トリアムテレン カンレノ酸カリウム シクロスポリン ボクロスポリン ドロスピレノン | 高カリウム血症を誘発することがあるので、血清カリウム値を観察するなど十分注意する。 | これらの薬剤と本剤の相加・相乗作用による血清カリウム値の上昇。 危険因子:腎障害患者、高齢者 |
| フィネレノン | 血清カリウム値上昇及び高カリウム血症が発現する危険性が増大するおそれがあるので、治療上必要と判断される場合にのみ併用すること。併用する場合には、血清カリウム値をより頻回に測定するなど患者の状態を慎重に観察すること。 | これらの薬剤と本剤の相加・相乗作用による血清カリウム値の上昇。 危険因子:腎障害患者、高齢者 |
| ノルエピネフリン | ノルエピネフリンの血管反応性を低下させるとの報告がある。 | 本剤が心血管反応性を低下させる機序は完全には解明されていない。 危険因子:麻酔施行患者 |
| 乳酸ナトリウム | 乳酸ナトリウムのアルカリ化作用を減弱することがある。 | 本剤により高カリウム性アシドーシスが惹起され、乳酸ナトリウムのアルカリ化作用と拮抗する可能性がある。 |
| 塩化アンモニウム コレスチラミン | 代謝性アシドーシスを来すとの報告がある。 | これらの薬剤と本剤の相加・相乗作用 |
| ジゴキシン メチルジゴキシン | 血中ジゴキシン及びメチルジゴキシン濃度が上昇することがある。 | 本剤がジゴキシン及びメチルジゴキシンの腎からの排泄を低下させるため、血中ジゴキシン及びメチルジゴキシン濃度を上昇させることがある。 |
| ジギトキシン | ジギトキシンの作用を増強又は減弱するおそれがあるので、併用する場合にはジギトキシンの血中濃度の測定を行うなど、観察を十分に行い慎重に投与すること。1)2) | 本剤の肝酵素誘導によりジギトキシンの血中濃度半減期が短縮すると考えられる報告がある。また、機序は不明であるが、ジギトキシンの血中濃度半減期が延長したとの報告がある。 |
| リチウム製剤 炭酸リチウム | 利尿剤又はACE阻害剤との併用により、リチウム中毒を起こすことが報告されているので、血中リチウム濃度に注意すること。 | ナトリウムイオン不足はリチウムイオンの貯留を促進するといわれているため、ナトリウム排泄を促進することにより起こると考えられる。 |
| 非ステロイド性消炎鎮痛剤 インドメタシン等 | カリウム保持性利尿剤との併用により、その降圧作用の減弱、腎機能障害患者における重度の高カリウム血症の発現が報告されている。 | プロスタグランジン産生が抑制されることによって、ナトリウム貯留作用による降圧作用の減弱、カリウム貯留作用による血清カリウム値の上昇が起こると考えられる。 危険因子:腎機能障害 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 電解質異常(高カリウム血症、低ナトリウム血症、代謝性アシドーシス等)(頻度不明)
11.1.2 急性腎不全(頻度不明)
11.1.3 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(いずれも頻度不明)
11.2 その他の副作用
| 0.1〜5%未満a) | 頻度不明 | |
| 内分泌 | 女性型乳房b)、乳房腫脹、性欲減退、陰萎、多毛、月経不順、無月経、閉経後の出血、音声低音化 | 乳房腫瘤、乳房痛 |
| 過敏症 | 発疹、蕁麻疹 | そう痒 |
| 精神神経系 | 眩暈、頭痛、四肢しびれ感、神経過敏、うつ状態、不安感、精神錯乱、運動失調、傾眠 | |
| 肝臓 | AST上昇、ALT上昇、γ-GTP上昇、Al-P上昇、LDH上昇、ビリルビン上昇 | |
| 腎臓 | BUN上昇 | |
| 消化器 | 食欲不振、悪心・嘔吐、口渇、下痢、便秘 | |
| 血液 | 白血球減少、血小板減少 | |
| その他 | 倦怠感、心悸亢進、発熱、肝斑 | 筋痙攣、脱毛 |
13. 過量投与
13.1 症状
本剤の過量投与により悪心、嘔吐、傾眠状態、精神錯乱、斑状丘疹、紅斑、下痢、電解質失調、脱水を起こす可能性がある。
13.2 処置
本剤の投与を中止し、食事を含むカリウムの摂取を制限すること。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 長期間服用した患者(男女とも)に乳癌が発生したとする症例報告がある。
15.1.2 アビラテロン酢酸エステルとの併用時に、前立腺特異抗原(PSA)の上昇が認められた症例が報告されている。本剤はアンドロゲン受容体と結合し、アビラテロン酢酸エステルを投与中の前立腺癌患者において、PSAを上昇させる可能性がある。
15.2 非臨床試験に基づく情報
ラットに24ヵ月経口投与した癌原性試験において内分泌臓器の腫瘍及び肝臓の増殖性変化がみられたとの報告がある。
16. 薬物動態
16.1 血中濃度
健康成人男性(10名)にスピロノラクトン100mgを1回経口投与したときの血漿中濃度の推移は以下のとおりであり、血漿中からの消失は二相性を示した3)。
注:本剤の承認された用量は「1日50〜100mgを分割経口投与」である。
| tmax | Cmax | 消失半減期 |
| 2.8時間 | 461ng/mL | α相:1.8時間 β相:11.6時間 |
16.4 代謝
尿中の主な代謝物は、カンレノン、6β-ヒドロキシ-7α-メチルスルフィニル体及びカンレノ酸のグルクロン酸抱合体であった4)(外国人データ)。
16.5 排泄
健康成人男性に[20-3H]スピロノラクトン200mgを1回経口投与したところ、5日間に放射活性の31.6%が尿中に、22.7%が糞中に排泄された4)(外国人データ)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
再評価申請時における各種疾患に対する有効率は以下のとおりであった。
注:本剤の承認された用量は「1日50〜100mgを分割経口投与」であるが、本集計では、投与量が50〜400mg/日の症例も含む。
| 疾患名 | 有効率 |
| 原発性アルドステロン症 | 100%(5/5) |
| 高血圧症 | 58.2%(53/91) |
| 心性浮腫、腎性浮腫、肝性浮腫等 | 70.5%(31/44) |
18. 薬効薬理
18.1 作用機序
19. 有効成分に関する理化学的知見
19.1. スピロノラクトン
20. 取扱い上の注意
<細粒>
瓶の開封後は光を避けて保存すること。
<錠>
瓶又はPTPの開封後は湿気を避けて保存すること。
22. 包装
<アルダクトンA細粒10%>
100g(瓶)
<アルダクトンA錠25mg>
100錠[10錠(PTP)×10]
300錠[10錠(PTP)×30]
100錠(瓶)
<アルダクトンA錠50mg>
100錠[10錠(PTP)×10]
23. 主要文献
- Carruthers,S.G.et al., Clin Pharmacol Ther., 27 (2), 184-187, (1980) »PubMed
- Wirth,K.E.et al., Eur J Clin Pharmacol., 9, 345-354, (1976)
- 社内資料:健康成人における血漿中濃度
- Karim,A.et al., Clin Pharmacol Ther., 19 (2), 158-169, (1976) »PubMed
- Kagawa,C.M., Endocrinology., 67, 125-132, (1960) »PubMed
- Fukuchi,S.et al., Tohoku J Exp Med., 76, 195-203, (1962) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
ファイザー株式会社
Pfizer Connect/メディカル・インフォメーション
〒151-8589
東京都渋谷区代々木3-22-7
電話:0120-664-467
製品情報問い合わせ先
ファイザー株式会社
Pfizer Connect/メディカル・インフォメーション
〒151-8589
東京都渋谷区代々木3-22-7
電話:0120-664-467
26. 製造販売業者等
26.1 製造販売元
ファイザー株式会社
東京都渋谷区代々木3-22-7