医薬品情報
| 総称名 | フロベン |
|---|---|
| 一般名 | フルルビプロフェン |
| 欧文一般名 | Flurbiprofen |
| 製剤名 | フルルビプロフェン製剤 |
| 薬効分類名 | 鎮痛・抗炎症剤 |
| 薬効分類番号 | 1149 |
| ATCコード | M01AE09 M02AA19 |
| KEGG DRUG |
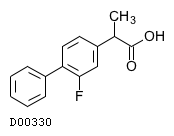
D00330
フルルビプロフェン
|
| KEGG DGROUP |
DG00755
フルルビプロフェン
DG01504
非ステロイド性抗炎症薬 (NSAID)
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年10月 改訂(第2版)

|
2.禁忌 4.効能または効果 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| フロベン錠40 | FROBEN Tablets | 科研製薬 | 1149011F1076 | 15.7円/錠 | 劇薬 |
| フロベン顆粒8% | FROBEN Granules | 科研製薬 | 1149011D1032 | 劇薬 |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
6. 用法及び用量
<フロベン錠40>
通常成人1回1錠、1日3回食後経口投与する。
なお、年齢、症状により適宜増減する。頓用の場合には、1回1〜2錠を経口投与する。
なお、年齢、症状により適宜増減する。頓用の場合には、1回1〜2錠を経口投与する。
<フロベン顆粒8%>
通常成人1回0.5g、1日3回食後経口投与する。
なお、年齢、症状により適宜増減する。頓用の場合には、1回0.5g〜1gを経口投与する。
なお、年齢、症状により適宜増減する。頓用の場合には、1回0.5g〜1gを経口投与する。
7. 用法及び用量に関連する注意
他の消炎鎮痛剤との併用は避けることが望ましい。
8. 重要な基本的注意
8.1 消炎鎮痛剤による治療は原因療法ではなく対症療法であることに留意すること。
8.2 慢性疾患(関節リウマチ、変形性関節症等)に対し本剤を用いる場合には、次の事項を考慮すること。
・長期投与する場合には定期的に尿検査、血液検査及び肝機能検査等を行うこと。
・薬物療法以外の療法も考慮すること。
8.3 急性疾患に対し本剤を用いる場合には、次の事項を考慮すること。
・急性炎症、疼痛の程度を考慮し投与すること。
・原則として同一の薬剤の長期投与を避けること。
・原因療法があればこれを行うこと。
8.4 過度の体温下降、虚脱、四肢冷却等があらわれることがあるので、特に高熱を伴う小児及び高齢者又は消耗性疾患の患者においては、投与後の患者の状態に十分注意すること。
8.5 急性腎障害、ネフローゼ症候群等の重篤な腎障害があらわれることがあるので、定期的に腎機能検査を行うなど観察を十分に行うこと。[11.1.2参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 非ステロイド性消炎鎮痛剤の長期投与による消化性潰瘍のある患者で、本剤の長期投与が必要であり、かつミソプロストールによる治療が行われている患者
本剤を継続投与する場合には、十分経過を観察し、慎重に投与すること。ミソプロストールは非ステロイド性消炎鎮痛剤により生じた消化性潰瘍を効能・効果としているが、ミソプロストールによる治療に抵抗性を示す消化性潰瘍もある。[2.1参照]
9.1.2 消化性潰瘍の既往歴のある患者
消化性潰瘍を再発させることがある。
9.1.3 血液の異常又はその既往歴のある患者(重篤な血液の異常のある患者を除く)
9.1.4 出血傾向のある患者
血小板機能低下が起こることがあるので、出血傾向を助長するおそれがある。
9.1.5 心機能異常のある患者(重篤な心機能不全のある患者を除く)
プロスタグランジン合成阻害作用による水・ナトリウム貯留傾向があるため、心機能異常を悪化させるおそれがある。[2.5参照]
9.1.6 高血圧症のある患者(重篤な高血圧症のある患者を除く)
プロスタグランジン合成阻害作用による水・ナトリウム貯留傾向があるため、血圧を上昇させるおそれがある。[2.6参照]
9.1.7 気管支喘息のある患者(アスピリン喘息又はその既往歴のある患者を除く)
9.1.8 感染症を合併している患者
9.1.9 潰瘍性大腸炎の患者
他の非ステロイド性消炎鎮痛剤で症状が悪化したとの報告がある。
9.1.10 クローン病の患者
他の非ステロイド性消炎鎮痛剤で症状が悪化したとの報告がある。
9.2 腎機能障害患者
9.2.1 重篤な腎障害のある患者
9.2.2 腎障害又はその既往歴のある患者あるいは腎血流量が低下している患者(重篤な腎障害のある患者を除く)
腎障害を悪化又は再発あるいは誘発させるおそれがある。[11.1.2参照]
9.3 肝機能障害患者
9.3.1 重篤な肝障害のある患者
投与しないこと。副作用として肝機能異常があらわれることがあるので、肝障害を更に悪化させるおそれがある。[2.3参照]
9.3.2 肝障害又はその既往歴のある患者(重篤な肝障害のある患者を除く)
肝障害を悪化又は再発させるおそれがある。
9.5 妊婦
9.5.1 妊娠後期の女性
9.5.2 妊婦(妊娠後期を除く)又は妊娠している可能性のある女性
治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。投与する際には、必要最小限にとどめ、羊水量、胎児の動脈管収縮を疑う所見を妊娠週数や投与日数を考慮して適宜確認するなど慎重に投与すること。シクロオキシゲナーゼ阻害剤(経口剤、坐剤)を妊婦に使用し、胎児の腎機能障害及び尿量減少、それに伴う羊水過少症が起きたとの報告がある。シクロオキシゲナーゼ阻害剤(全身作用を期待する製剤)を妊娠中期の妊婦に使用し、胎児の動脈管収縮が起きたとの報告がある。周産期・授乳期投与試験では、ラット(経口投与)の2.5mg/kg以上の投与群で、少数例に母体の死亡、衰弱、哺育不良が認められている3)。[9.6参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。母乳中へ移行することが報告されている。[9.5.2参照]
9.7 小児等
9.7.1 小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
9.7.2 副作用の発現に特に注意し、必要最小限の使用にとどめるなど慎重に投与すること。
9.8 高齢者
副作用の発現に特に注意し、少量から投与を開始するなど必要最小限の使用にとどめ患者の状態を観察しながら慎重に投与すること。
10. 相互作用
相互作用序文
本剤は、主として肝代謝酵素CYP2C9によって代謝される。
薬物代謝酵素用語
CYP2C9
10.1 併用禁忌
10.2 併用注意
| ニューキノロン系抗菌剤(ただし、エノキサシン水和物、ロメフロキサシン、ノルフロキサシン、プルリフロキサシンは併用禁忌) オフロキサシン等 [9.1.8、10.1、11.1.7参照] | 痙攣があらわれるおそれがある。併用は避けることが望ましい。 | ニューキノロン系抗菌剤のGABA阻害作用が併用により増強されるためと考えられる。 |
| クマリン系抗凝血剤 ワルファリン | クマリン系抗凝血剤(ワルファリン)の作用を増強するとの報告があるので、用量を調節するなど注意すること。 | ワルファリンの血漿蛋白結合と競合し、遊離型ワルファリンが増加するためと考えられる。 |
| メトトレキサート | メトトレキサートの作用が増強され、中毒症状(貧血、血小板減少等)があらわれたとの報告があるので、用量を調節するなど注意すること。 | プロスタグランジン合成阻害作用により腎血流が減少し、メトトレキサートの腎排泄が抑制されることにより、メトトレキサートの血中濃度が上昇すると考えられる。 |
| リチウム製剤 炭酸リチウム | リチウムの血中濃度が上昇し、リチウム中毒を呈するおそれがあるので、併用する場合にはリチウムの血中濃度をモニターするなど観察を十分に行い、慎重に投与すること。 | プロスタグランジン合成阻害作用により、腎でのナトリウム排泄が減少してリチウムクリアランスを低下させ、リチウムの血中濃度が上昇すると考えられる。 |
| チアジド系利尿薬 ヒドロクロロチアジド等 ループ利尿薬 フロセミド | これら利尿薬の作用を減弱するとの報告がある。 | プロスタグランジン合成阻害作用により、水・塩類の体内貯留が生じるためと考えられる。 |
| 副腎皮質ホルモン剤 メチルプレドニゾロン等 [11.1.3参照] | 相互に消化器系の副作用(消化性潰瘍、消化管出血等)が増強されるおそれがある。 | 両薬剤の消化器系の副作用が併用により増強されると考えられる。 |
| CYP2C9阻害作用を有する薬剤 フルコナゾール等 | 本剤の血中濃度が上昇するおそれがある。 | 代謝酵素(CYP2C9)の競合により、本剤の代謝が阻害されると考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
胸内苦悶、悪寒、冷汗、呼吸困難、四肢しびれ感、血圧低下、血管浮腫、蕁麻疹等があらわれた場合には投与を中止し、適切な処置を行うこと。
11.1.2 急性腎障害、ネフローゼ症候群(いずれも頻度不明)
11.1.3 胃腸出血(頻度不明)[10.2参照]
11.1.5 喘息発作(頻度不明)
11.1.6 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、剥脱性皮膚炎(いずれも頻度不明)
11.1.7 痙攣(頻度不明)
11.1.8 心筋梗塞、脳血管障害(いずれも頻度不明)
心筋梗塞、脳血管障害等の心血管系血栓塞栓性事象があらわれることがある4)。
11.2 その他の副作用
| 1%以上 | 1%未満 | 頻度不明 | |
| 過敏症 | 発疹、そう痒感 | ||
| 消化器 | 嘔気・嘔吐、胃部不快感、食欲不振、胃痛 | 下痢、便秘、口渇、腹痛、胃・腹部膨満感 | 口内炎 |
| 肝臓 | AST上昇、ALT上昇、Al-P上昇 | ||
| 精神神経系 | 頭痛、眠気、めまい、ふらつき感、倦怠感 | ||
| 循環器 | 動悸 | ||
| 血液 | 血小板減少、血小板機能低下(出血時間の延長) | ||
| 耳 | 耳鳴り | ||
| その他 | 浮腫 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
14.2 薬剤投与時の注意
食道に停留し崩壊すると、食道潰瘍を起こすおそれがあるので、多めの水で服用させ、特に就寝直前の服用等には注意すること。
15. その他の注意
15.1 臨床使用に基づく情報
非ステロイド性消炎鎮痛剤を長期間投与されている女性において、一時的な不妊が認められたとの報告がある。
16. 薬物動態
16.1 血中濃度
健康成人10例にフロベン錠40(フルルビプロフェン40mg)1錠を単回経口投与したときの血漿中フルルビプロフェン濃度は以下のとおりであった。顆粒剤についてもほぼ同様のパターンであった5)。
フルルビプロフェン40mg(フロベン錠40 1錠)経口投与後の血漿中濃度推移
| Cmax(μg/mL) | Tmax(hr) | T1/2(hr) |
| 5.6±0.5 | 1.4±0.2 | 2.7±0.2 |
16.4 代謝
健康成人にフルルビプロフェン40mgを単回経口投与したところ、尿中に未変化体、3種類の代謝物(4'-ヒドロキシ体、3',4'-ジヒドロキシ体及び3'-ヒドロキシ-4'-メトキシ体)及びこれらの抱合体が確認された6)。
16.5 排泄
健康成人にフルルビプロフェン40mgを単回経口投与したところ、尿中には投与後24時間以内に投与量の約73%が排泄された6)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床試験
二重盲検比較試験及び一般臨床試験において、本剤の有用性が認められている。本剤の疾患別有効率は次のとおりである7)8)9)10)11)12)13)14)15)16)。
| 疾患名\有効率(%) | 有効以上 | やや有効以上 |
| 関節リウマチ | 34/74(45.9) | 62/74(83.8) |
| 変形性関節症 | 57/123(46.3) | 94/123(76.4) |
| 腰痛症 | 194/326(59.5) | 286/326(87.7) |
| 歯髄炎 | 88/165(53.3) | 136/165(82.4) |
| 歯根膜炎 | 95/155(61.3) | 140/155(90.3) |
| 抜歯並びに歯科領域における小手術後の鎮痛・消炎 | 276/407(67.8) | 355/407(87.2) |
18. 薬効薬理
18.1 作用機序
プロスタグランジン(PG)生合成の律速酵素であるシクロオキシゲナーゼ(COX)を阻害し、PGの産生を抑制することにより、抗炎症作用、解熱作用、鎮痛作用を現す17)。
18.2 抗炎症作用
カラゲニン浮腫(ラット)、紫外線紅斑(モルモット)の急性炎症に対するID50(経口投与)は、それぞれ0.48mg/kg、0.19mg/kgで、アスピリン(それぞれ122.0mg/kg、150.0mg/kg)及びインドメタシン(それぞれ6.8mg/kg、4.8mg/kg)に比し強力である。
アジュバンド関節炎(ラット)の慢性炎症に対しては、3mg/kg/日の経口投与で約50%の抑制作用を示し、インドメタシンと同程度の作用を示す18)。
アジュバンド関節炎(ラット)の慢性炎症に対しては、3mg/kg/日の経口投与で約50%の抑制作用を示し、インドメタシンと同程度の作用を示す18)。
18.3 鎮痛作用
酢酸ライシング法(マウス)によるID50(経口投与)は3.1mg/kgで、アスピリン(255.0mg/kg)に比し少量で作用を示す19)。
ラット足蹠の炎症性疼痛(Randall-Selitto法)に対する最小有効量(経口投与)は0.33mg/kgで、アスピリン(90mg/kg)に比し強い作用を示す20)。
18.4 プロスタグランジン生合成阻害作用
関節リウマチ患者の滑液膜細胞のミクロソームでのプロスタグランジン生合成の50%阻害濃度は0.06μMで、インドメタシン(0.54μM)、ジクロフェナクナトリウム(0.2μM)より強い作用を示す21)。
19. 有効成分に関する理化学的知見
19.1. フルルビプロフェン
22. 包装
<フロベン錠40>
100錠[10錠(PTP)×10]
500錠[10錠(PTP)×50]
1,000錠[10錠(PTP)×100]
<フロベン顆粒8%>
100g[プラスチック容器]
23. 主要文献
- 門間和夫 他, 日本新生児学会雑誌, 20, 508-518, (1984)
- 門間和夫 他, 小児科の進歩, 2, 95-101, (1983)
- 吉中一朗 他, 薬理と治療, 4, 2187-2223, (1976)
- データベース調査結果の概要(NDBを用いた非ステロイド性抗炎症薬による心血管系イベント発現のリスク評価), (https://www.pmda.go.jp/files/000270714.pdf)
- 社内資料:フロベン顆粒血中濃度比較試験
- 社内資料:ヒト内服時の吸収、代謝および排泄について
- 辻本正記 他, 臨牀と研究, 53, 255-260, (1976)
- 広畑和志, 薬理と治療, 4, 687-699, (1976)
- 石川武憲 他, 診療と新薬, 13, 1493-1506, (1976)
- 大橋靖 他, 日本口腔外科学会雑誌, 22, 880-887, (1976) »DOI
- 福田仁一 他, 歯界展望, 47, 641-644, (1976)
- 志村介三 他, 臨牀と研究, 53, 610-619, (1976)
- 花岡英弥 他, 薬理と治療, 8, 4365-4377, (1980)
- 榊田喜三郎 他, 薬理と治療, 8, 4379-4388, (1980)
- 神山義信 他, 歯界展望, 56, 849-858, (1980)
- 堀亘孝 他, 歯科ジャーナル, 12, 377-385, (1980)
- 第十八改正日本薬局方解説書, (廣川書店)
- 高瀬健一郎 他, 日本薬理学雑誌, 71, 573-583, (1975) »PubMed
- Adams SS,et al., Arzneim.-Forsch.(Drug Res.), 25, 1786-1791, (1975) »PubMed
- 吉中一朗 他, 薬理と治療, 4, 1931-1942, (1976)
- Steele L,et al., J.Pharmacol.Methods., 5, 341-345, (1981) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
科研製薬株式会社
医薬品情報サービス室
〒113-8650
東京都文京区本駒込二丁目28番8号
電話:フリーダイヤル 0120-519-874
製品情報問い合わせ先
科研製薬株式会社
医薬品情報サービス室
〒113-8650
東京都文京区本駒込二丁目28番8号
電話:フリーダイヤル 0120-519-874
26. 製造販売業者等
26.1 製造販売元
科研製薬株式会社
東京都文京区本駒込二丁目28番8号