医薬品情報
| 総称名 | ジルテック |
|---|---|
| 一般名 | セチリジン塩酸塩 |
| 欧文一般名 | Cetirizine Hydrochloride |
| 薬効分類名 | 持続性選択H1受容体拮抗・アレルギー性疾患治療剤 |
| 薬効分類番号 | 4490 |
| ATCコード | R06AE07 |
| KEGG DRUG |
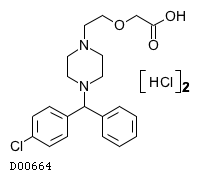
D00664
セチリジン塩酸塩
|
| KEGG DGROUP |
DG01482
ヒスタミンH1受容体拮抗薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年9月 改訂(第3版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ジルテック錠5 | Zyrtec Tablets | ユーシービージャパン | 4490020F1020 | 11.9円/錠 | |
| ジルテック錠10 | Zyrtec Tablets | ユーシービージャパン | 4490020F2027 | 16.3円/錠 |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
ジルテック錠5
ジルテック錠10
〔成人〕
○蕁麻疹、湿疹・皮膚炎、痒疹、皮膚そう痒症
6. 用法及び用量
ジルテック錠5
<5mg錠>
〔成人〕
通常、成人にはセチリジン塩酸塩として1回10mgを1日1回、就寝前に経口投与する。
なお、年齢、症状により適宜増減するが、最高投与量は1日20mgとする。
なお、年齢、症状により適宜増減するが、最高投与量は1日20mgとする。
〔小児〕
通常、7歳以上15歳未満の小児にはセチリジン塩酸塩として1回5mgを1日2回、朝食後及び就寝前に経口投与する。
ジルテック錠10
<10mg錠>
通常、成人にはセチリジン塩酸塩として1回10mgを1日1回、就寝前に経口投与する。
なお、年齢、症状により適宜増減するが、最高投与量は1日20mgとする。
なお、年齢、症状により適宜増減するが、最高投与量は1日20mgとする。
7. 用法及び用量に関連する注意
8. 重要な基本的注意
<効能共通>
8.1 眠気を催すことがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械の操作には従事させないよう十分注意すること。
8.2 効果が認められない場合には、漫然と長期にわたり投与しないように注意すること。
<アレルギー性鼻炎>
8.3 季節性の患者に投与する場合は、好発季節を考えて、その直前から投与を開始し、好発季節終了時まで続けることが望ましい。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 てんかん等の痙攣性疾患又はこれらの既往歴のある患者
痙攣を発現するおそれがある。[11.1.2参照]
9.2 腎機能障害患者
9.2.1 重度の腎機能障害患者(クレアチニンクリアランス10mL/min未満)
9.2.2 中等度又は軽度の腎機能障害患者(クレアチニンクリアランス10mL/min以上60mL/min以下)
9.3 肝機能障害患者
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
動物実験(ラット)で胎盤を通過することが報告されている。
動物実験(ラット)で胎盤を通過することが報告されている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
ヒト乳汁中へ移行することが報告されている。
ヒト乳汁中へ移行することが報告されている。
9.7 小児等
9.7.1 2歳以上7歳未満の小児に対してはセチリジン塩酸塩ドライシロップを投与すること。
9.7.2 低出生体重児、新生児、乳児又は2歳未満の幼児を対象とした臨床試験は実施していない。
9.8 高齢者
10. 相互作用
10.2 併用注意
| テオフィリン | テオフィリンの薬物動態に変化はないが、本剤の曝露量の増加が報告されている。 | 機序は明らかではないが、本剤のクリアランスが16%減少する。 |
| リトナビル | 本剤の曝露量の増加(40%)及びリトナビルの曝露量のわずかな変化(−11%)が報告されている。 | リトナビルにより本剤の腎排泄が阻害される可能性が考えられる。 |
| 中枢神経抑制剤 アルコール | 中枢神経系に影響を与える可能性がある。 | 中枢神経抑制作用が増強される可能性がある。 |
| ピルシカイニド塩酸塩水和物 | 両剤の血中濃度が上昇し、ピルシカイニド塩酸塩水和物の副作用が発現したとの報告がある。 | 機序は明らかではない。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
ショック、アナフィラキシー(呼吸困難、血圧低下、蕁麻疹、発赤等)があらわれることがある。
11.1.2 痙攣(頻度不明)[9.1.1参照]
11.1.3 肝機能障害、黄疸(いずれも頻度不明)
AST、ALT、γ-GTP、LDH、Al-Pの上昇等の肝機能障害(初期症状:全身倦怠感、食欲不振、発熱、嘔気等)、黄疸があらわれることがある。
11.1.4 血小板減少(頻度不明)
11.2 その他の副作用
| 0.1%〜5%未満 | 0.1%未満 | 頻度不明 | |
| 精神神経系 | 眠気、倦怠感 | 頭痛、頭重感、ふらふら感、しびれ感、めまい、浮遊感 | 不眠、振戦、抑うつ、激越、攻撃性、無力症、錯感覚、幻覚、不随意運動、意識消失、健忘、自殺念慮、悪夢 |
| 消化器 | 口渇、嘔気、食欲不振 | 胃不快感、下痢、消化不良、腹痛、腹部不快感、胃痛、口唇炎、便秘、口唇乾燥感、嘔吐、味覚異常、口内炎 | 腹部膨満感、食欲亢進 |
| 循環器 | 動悸、血圧上昇、不整脈(房室ブロック、期外収縮、頻脈、発作性上室性頻拍、心房細動) | ||
| 血液 | 好酸球増多 | 好中球減少、リンパ球増多、白血球増多、白血球減少、単球増多、血小板増加、血小板減少 | |
| 過敏症 | 発疹、蕁麻疹、浮腫、かぶれ、そう痒感、血管浮腫 | 多形紅斑 | |
| 眼 | 結膜充血、霧視 | 眼球回転発作 | |
| 肝臓 | ALT上昇、AST上昇、総ビリルビン上昇 | Al-P上昇 | |
| 腎臓・泌尿器 | 尿蛋白、BUN上昇、尿糖、ウロビリノーゲンの異常、頻尿、血尿 | 排尿困難、遺尿、尿閉 | |
| その他 | 耳鳴、月経異常、胸痛、ほてり、息苦しさ | 関節痛、手足のこわばり、嗅覚異常、鼻出血、脱毛、咳嗽、体重増加、筋肉痛 |
12. 臨床検査結果に及ぼす影響
アレルゲン皮内反応を抑制するため、アレルゲン皮内反応検査を実施する3〜5日前より本剤の投与を中止することが望ましい。
13. 過量投与
13.1 症状
錯乱、散瞳、落ち着きのなさ、鎮静、傾眠、昏迷、尿閉があらわれることがある。
13.2 処置
本剤の特異的な解毒剤はなく、また本剤は透析で除去されない。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
16.1.1 成人
健康成人にセチリジン塩酸塩錠10mgを単回経口投与した場合、速やかに吸収され、投与約1.4時間後に最高血漿中濃度(Cmax)214.5ng/mLに達し、血漿中濃度消失半減期は約7時間であった。また、20mgを単回経口投与した場合、投与量の増加に伴ってCmaxの上昇、AUCの増大が認められた。健康成人に1日1回20mgを7日間連続経口投与した場合、蓄積性は認められなかった1)。
成人におけるセチリジン塩酸塩錠単回投与時の血漿中濃度の推移
| 投与量 | Tmax(hr) | Cmax(ng/mL) | T1/2(hr) | AUC(mg・hr/L) |
| 10mg | 1.44±0.50 | 214.5±35.3 | 6.73±2.30 | 2.0±0.3 |
| 20mg | 1.50±0.38 | 438.1±111.8 | 6.79±1.85 | 3.9±0.9 |
また、健康成人にセチリジン塩酸塩ドライシロップ0.8gを単回経口投与した場合、速やかに吸収され、投与約0.82時間後に最高血漿中濃度(Cmax)413.6ng/mLに達し、血漿中濃度消失半減期は約8時間であった2)。
成人におけるセチリジン塩酸塩錠・ドライシロップ単回投与時の血漿中濃度の推移
| 投与量 | Tmax(hr) | Cmax(ng/mL) | T1/2(hr) | AUC(mg・hr/L) |
| 10mg錠 | 1.13±0.52 | 440.9±144.7 | 8.36±1.63 | 3.0±0.8 |
| ドライシロップ0.8g | 0.82±0.39 | 413.6±130.5 | 8.03±1.45 | 2.8±0.8 |
16.1.2 小児
日本人の通年性アレルギー性鼻炎患児又は皮膚疾患患児を対象とした臨床試験5試験、570例から得られた血清中濃度値994点を用い、母集団薬物動態解析(非線形混合効果モデル法、NONMEM)を行った。その結果、体重が共変量として認められ、2〜6歳の小児(本年齢層における体重の中央値:18.0kg)の全身クリアランス(CL/F)は1.64L/hr、分布容積(V/F)は11.9L、7〜14歳の小児(同:31.0kg)のCL/Fは2.11L/hr、V/Fは17.7Lと推定された。また、セチリジン塩酸塩2.5mg 1日2回投与時の定常状態時最低血清中濃度(Css min)及び最高血清中濃度(Css max)は、それぞれ58±25ng/mL及び214±50ng/mL(平均±標準偏差注)、以下同様)と推定され、セチリジン塩酸塩5mg 1日2回投与時のCss min及びCss maxは、それぞれ100±40ng/mL及び308±74ng/mLと推定された3)。
注)1000例の血清中濃度推移をシミュレーションしたときの推定値
16.3 分布
16.3.1 血漿蛋白結合率
14C標識−セチリジン0.1、1及び10μg/mL濃度のin vitroにおけるヒト血漿蛋白との結合率は、平均92%(90.7〜92.5%)であった(平衡透析法)4)。
16.4 代謝
健康成人に1日1回セチリジン塩酸塩20mgを7日間連続経口投与した場合、血漿中に酸化的脱アルキル体がわずかに認められた1)。
16.5 排泄
健康成人にセチリジン塩酸塩10mg又は20mgを単回経口投与した場合、24時間後までに投与量の約50%が未変化体として尿中に排泄された。また、健康成人に1日1回20mgを7日間連続経口投与した場合、未変化体の1日投与量に対する尿中排泄率は、1日目は24時間後までに約58%、7日目は約70%であった1)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
腎機能障害患者(クレアチニンクリアランス:7〜60mL/min)にセチリジン塩酸塩10mgを単回経口投与した場合、腎機能正常者に比べ血清中濃度は持続し、血清中濃度消失半減期の延長が認められた5)(外国人データ)。
| クレアチニンクリアランス(mL/min) | Tmax(hr) | Cmax(ng/mL) | T1/2(hr) | AUC(mg・hr/L) |
| >90 | 0.9±0.2 | 313±45 | 7.4±3.0 | 2.7±0.4 |
| 31〜60 | 1.1±0.2 | 356±64 | 19.2±3.3 | 6.9±1.8 |
| 7〜30 | 2.2±1.1 | 357±172 | 20.9±4.4 | 10.7±2.4 |
16.6.2 肝機能障害患者での体内動態
16.6.3 高齢者
高齢者(年齢:平均77歳、クレアチニンクリアランス:平均53mL/min)にセチリジン塩酸塩10mgを単回経口投与した場合、成人(年齢:平均53歳、クレアチニンクリアランス:平均87mL/min)に比べ、血清中濃度消失半減期の延長とCmaxの上昇が認められ、これらの薬物動態パラメータの変化は、腎機能の低下によるものと考えられた5)(外国人データ)。[7.3、9.8参照]
| 投与量(被験者、例数) | Tmax(hr) | Cmax(ng/mL) | T1/2(hr) | AUC(mg・hr/L) |
| 10mg(成人、n=14) | 1.0±0.5 | 384±103 | 7.4±1.6 | 3.3±0.9 |
| 10mg(高齢者、n=16) | 0.9±0.3 | 460±59 | 11.8±5.4 | 5.6±1.8 |
17. 臨床成績
17.1 有効性及び安全性に関する試験
<アレルギー性鼻炎>
17.1.1 国内後期第II相試験(二重盲検比較試験、成人)
本剤10mgを1日1回2週間投与したとき、最終全般改善度の中等度改善以上の割合は53.8%(21/39例)であった8)。
副作用発現頻度は13.0%(6/46例)であり、主な副作用は眠気4.3%(2/46例)であった。
17.1.2 国内第III相試験(二重盲検比較試験、成人)
本剤10mgを1日1回4週間投与したとき、最終全般改善度の中等度改善以上の割合は47.9%(45/94例)であった9)。
副作用発現頻度は5.5%(6/110例)であり、主な副作用は眠気3.6%(4/110例)であった。
17.1.3 国内第III相試験(二重盲検比較試験、小児)
セチリジン塩酸塩ドライシロップ[2歳以上7歳未満:1回0.2g(セチリジン塩酸塩として2.5mg)を1日2回、7歳以上15歳未満:1回0.4g(セチリジン塩酸塩として5mg)を1日2回]あるいはプラセボを2週間投与した。総合鼻症状スコア(くしゃみ発作、鼻汁、鼻閉、鼻内そう痒感)の変化量(解析対象122例)を下表に示した。その結果から、プラセボに対する本薬の優越性が検証された10)。
| 群 | 例数 | ベースライン評価期間 | 全治療評価期間 | 変化量b) | |
| 平均値(標準偏差) | 平均値(標準偏差) | 平均値(標準偏差) | 調整済み平均値c)(標準誤差) | ||
| セチリジン塩酸塩 | 122 | 6.66(1.26) | 4.79(1.96) | 1.87(1.79) | 1.85(0.18) |
| プラセボ | 117 | 6.84(1.52) | 5.51(2.04) | 1.33(1.79) | 1.25(0.18) |
| セチリジン塩酸塩vsプラセボ | 点推定値c) | 95%信頼区間c) | p値 |
| 0.60 | [0.15〜1.05] | p=0.0087 |
a)総合鼻症状スコアが10を超える患児は組入れから除外
b)変化量={ベースライン評価期間(治験薬投与開始日の前3日間)−全治療評価期間}
c)ベースライン評価期間スコア及び年齢層を共変量とした共分散分析により算出
副作用発現頻度は9.8%(12/122例)であり、主な副作用はALT増加5.7%(7/122例)、AST増加1.6%(2/122例)であった。
17.1.4 国内第III相試験(一般臨床試験、小児)
セチリジン塩酸塩ドライシロップ[2歳以上7歳未満:1回0.2g(セチリジン塩酸塩として2.5mg)を1日2回、7歳以上15歳未満:1回0.4g(セチリジン塩酸塩として5mg)を1日2回]を12週間投与した。総合鼻症状スコアのベースライン評価期間からの変化量の推移(平均値±標準偏差、解析対象36例)は、投与4週時:2.81±2.62、投与8週時:3.66±2.75、投与12週時:3.40±3.01であり、効果は投与終了時まで減弱することなく、安定していた11)。
副作用発現頻度は2.8%(1/36例)であり、主な副作用は白血球数増加2.8%(1/36例)であった。
<蕁麻疹>
17.1.5 国内後期第II相試験(二重盲検比較試験、成人)
本剤10mgを1日1回投与したとき、投与3日後、投与1週後及び投与2週後における全般改善度の中等度改善以上の割合は、それぞれ、47.9%(34/71例)、64.9%(48/74例)及び71.6%(48/67例)であった12)。
副作用発現頻度は10.8%(9/83例)であり、主な副作用は眠気4.8%(4/83例)であった。
17.1.6 国内第III相試験(二重盲検比較試験、成人)
本剤10mgを1日1回投与したとき、投与3日後、投与1週後及び投与2週後における全般改善度の中等度改善以上の割合は、それぞれ、56.4%(53/94例)、71.3%(77/108例)及び82.2%(88/107例)であった13)。
副作用発現頻度は15.9%(21/132例)であり、主な副作用は眠気10.6%(14/132例)であった。
17.1.7 国内第III相試験(一般臨床試験、成人)
本剤10mgを1日1回投与したとき、投与3日後、投与1週後及び投与2週後における全般改善度の中等度改善以上の割合は、それぞれ、46.7%(14/30例)、53.2%(33/62例)及び72.9%(43/59例)であった14)。
副作用発現頻度は4.4%(3/68例)であり、主な副作用は眠気2.9%(2/68例)であった。
17.1.8 国内第III相試験(一般臨床試験、成人)
本剤10mgを1日1回投与したとき、投与3日後、投与1週後及び投与2週後における全般改善度の中等度改善以上の割合は、それぞれ、66.7%(24/36例)、70.8%(34/48例)及び80.0%(32/40例)であった15)。
副作用発現頻度は7.8%(4/51例)であり、主な副作用は眠気3.9%(2/51例)であった。
<湿疹・皮膚炎、痒疹、皮膚そう痒症>
17.1.9 国内第III相試験(一般臨床試験、成人)
本剤10mgを1日1回2週間投与したとき、最終全般改善度の中等度改善以上の割合は、湿疹・皮膚炎群で65.9%(81/123例)、痒疹群で57.7%(30/52例)、皮膚そう痒症で74.5%(41/55例)であった16)。
副作用発現頻度は全体で5.5%(13/236例)であり、主な副作用は眠気3.4%(8/236例)であった。
<蕁麻疹、皮膚疾患(湿疹・皮膚炎、皮膚そう痒症)に伴うそう痒>
17.1.10 国内第III相試験(二重盲検比較試験、小児)
アトピー性皮膚炎を対象とした二重盲検比較試験において、セチリジン塩酸塩ドライシロップ[3歳以上7歳未満:1回0.2g(セチリジン塩酸塩として2.5mg)を1日2回、7歳以上15歳未満:1回0.4g(セチリジン塩酸塩として5mg)を1日2回]あるいはケトチフェンフマル酸塩ドライシロップ[3歳以上7歳未満:1回0.6g(ケトチフェンとして0.6mg)を1日2回、7歳以上15歳未満:1回1g(ケトチフェンとして1mg)を1日2回]を2週間投与した。そう痒の重症度の変化量(解析対象134例)を下表に示した。その結果から、ケトチフェンフマル酸塩に対する本薬の非劣性が検証された17)。
| 群 | 例数a) | ベースライン評価期間 | 全治療評価期間 | 変化量b) | |
| 平均値(標準偏差) | 平均値(標準偏差) | 平均値(標準偏差) | 調整済み平均値c)(標準誤差) | ||
| セチリジン塩酸塩 | 134 | 2.41(0.52) | 1.96(0.64) | 0.45(0.67) | 0.43(0.05) |
| ケトチフェンフマル酸塩 | 126 | 2.40(0.52) | 1.88(0.63) | 0.52(0.62) | 0.51(0.05) |
| セチリジン塩酸塩vsケトチフェンフマル酸塩 | 点推定値c) | 95%信頼区間c) |
| −0.08 | [−0.22〜0.06] |
a)変化量が算出可能な被験者数
b)変化量={ベースライン評価期間(治験薬投与開始日の前3日間)−全治療評価期間}
c)ベースライン評価期間のそう痒の重症度及び年齢層を共変量とした共分散分析により算出
副作用発現頻度は2.7%(4/148例)であり、主な副作用は傾眠1.4%(2/148例)であった。
17.1.11 国内第III相試験(一般臨床試験、小児)
蕁麻疹、湿疹・皮膚炎、痒疹、皮膚そう痒症を対象とした試験において、セチリジン塩酸塩ドライシロップ[2歳以上7歳未満:1回0.2g(セチリジン塩酸塩として2.5mg)を1日2回、7歳以上15歳未満:1回0.4g(セチリジン塩酸塩として5mg)を1日2回]を12週間投与した。そう痒の重症度の治療期開始日からの変化量の推移(平均値±標準偏差)は、投与4週時:0.83±0.79、投与8週時:0.97±0.90、投与12週時:1.03±0.90であり、効果は投与終了時まで減弱することなく、安定していた18)。
副作用発現頻度は1.4%(1/73例)であり、傾眠1例であった。
17.3 その他
18. 薬効薬理
18.1 作用機序
ヒスタミンH1受容体に選択的に結合することにより、ヒスタミンの作用を阻害する。
18.2 ヒスタミンH1受容体拮抗作用
18.3 好酸球に対する作用
18.4 メディエーター遊離抑制作用
ヒト肺切片からのロイコトリエン及びプロスタグランジンD2遊離を抑制した27)。
19. 有効成分に関する理化学的知見
19.1. セチリジン塩酸塩
22. 包装
<ジルテック錠5>
100錠[10錠(PTP)×10]、500錠[10錠(PTP)×50]
<ジルテック錠10>
100錠[10錠(PTP)×10]
23. 主要文献
- 笹 征史 他, 臨床薬理, 26, 509-522, (1995) »DOI
- 社内資料:ドライシロップ剤及び錠剤の生物学的同等性試験
- 社内資料:Retrospective population pharmacokinetic analysis of cetirizine in Japanese children
- 水野佳子 他, 基礎と臨床, 28, 1951-1961, (1994)
- Matzke G R,et al., Ann Allergy., 59, 25-30, (1987) »PubMed
- Awni W M,et al., Eur J Clin Pharmacol., 38, 67-69, (1990) »PubMed
- Simons F E R,et al., J Clin Pharmacol., 33, 949-954, (1993)
- 奥田 稔 他, 耳鼻咽喉科展望, 37, 754-779, (1994) »DOI
- 奥田 稔 他, 耳鼻咽喉科展望, 38, 116-136, (1995) »DOI
- 斎藤博久, 臨床医薬, 26, 141-154, (2010)
- 斎藤博久 他, 臨床医薬, 26, 127-139, (2010)
- 吉田彦太郎 他, 基礎と臨床, 28, 2107-2129, (1994)
- 吉田彦太郎 他, 基礎と臨床, 28, 2131-2145, (1994)
- 吉田彦太郎 他, 基礎と臨床, 28, 2163-2173, (1994)
- 社内資料:セチリジン円形錠(5mg錠)の慢性蕁麻疹に対する臨床試験
- 吉田彦太郎 他, 基礎と臨床, 28, 2147-2162, (1994)
- 中川秀己 他, 臨床医薬, 26, 155-167, (2010)
- 中川秀己 他, 臨床医薬, 26, 169-181, (2010)
- 社内資料:小児アレルギー性鼻炎を対象とした二重盲検比較試験(2009年4月22日承認、CTD 2.7.6.3)
- Advenier C,et al., J Allergy Clin Immunol., 88, 104-113, (1991) »PubMed
- Simons F E R,et al., J Allergy Clin Immunol., 86, 540-547, (1990)
- Braunstein G,et al., Br J Clin Pharmacol., 33, 445-448, (1992) »PubMed
- 内田昌子 他, 基礎と臨床, 28, 1795-1812, (1994)
- Snyder S H,et al., Ann Allergy., 59, 4-8, (1987) »PubMed
- Okada C,et al., Int Arch Allergy Immunol., 103, 384-390, (1994) »PubMed
- Fadel R,et al., Clin Allergy., 17, 373-379, (1987) »PubMed
- Fabre J M,et al., Allergy., 50, 362-365, (1995) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
グラクソ・スミスクライン株式会社
カスタマー・ケア・センター
東京都港区赤坂1-8-1
電話:0120-561-007(9:00〜17:45/土日祝日及び当社休業日を除く)
製品情報問い合わせ先
グラクソ・スミスクライン株式会社
カスタマー・ケア・センター
東京都港区赤坂1-8-1
電話:0120-561-007(9:00〜17:45/土日祝日及び当社休業日を除く)
26. 製造販売業者等
26.1 製造販売元
ユーシービージャパン株式会社
東京都新宿区西新宿8丁目17番1号
26.2 販売元
グラクソ・スミスクライン株式会社
東京都港区赤坂1-8-1