医薬品情報
| 総称名 | エリスロシン |
|---|---|
| 一般名 | エリスロマイシンラクトビオン酸塩 |
| 欧文一般名 | Erythromycin Lactobionate |
| 製剤名 | 注射用エリスロマイシンラクトビオン酸塩 |
| 薬効分類名 | マクロライド系抗生物質製剤 |
| 薬効分類番号 | 6141 |
| ATCコード | D10AF02 J01FA01 |
| KEGG DRUG |
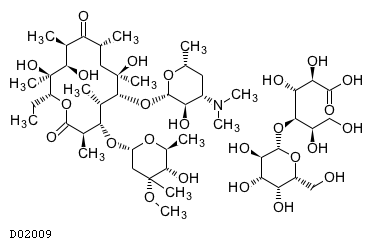
D02009
エリスロマイシンラクトビオン酸塩
|
| KEGG DGROUP |
DG00436
エリスロマイシン
DG01551
マクロライド系抗生物質
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年7月 改訂(第3版)

|
2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| エリスロシン点滴静注用500mg | Erythrocin for Intravenous Infusion | ヴィアトリス・ヘルスケア | 6141400D1031 | 1369円/瓶 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 エルゴタミン酒石酸塩・無水カフェイン・イソプロピルアンチピリン、ジヒドロエルゴタミンメシル酸塩、ピモジド、ロミタピドメシル酸塩、アミオダロン(注射剤)、クリンダマイシン(注射剤、経口剤)、リンコマイシン塩酸塩水和物を投与中の患者[10.1参照]
4. 効能または効果
5. 効能または効果に関連する注意
経口投与が困難な場合、あるいは、緊急を要する場合に本剤を使用すること。
6. 用法及び用量
通常、成人にはエリスロマイシンとして1日600〜1500mg(力価)を2〜3回に分けて1回2時間以上かけて点滴静注する。
なお、年齢、症状により適宜増減する。
なお、年齢、症状により適宜増減する。
7. 用法及び用量に関連する注意
8. 重要な基本的注意
8.1 本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
8.2 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、次の措置をとること。[11.1.3参照]
8.2.1 事前に既往歴等について十分な問診を行うこと。なお、抗生物質等によるアレルギー歴は必ず確認すること。
8.2.2 投与に際しては、必ずショック等に対する救急処置のとれる準備をしておくこと。
8.2.3 投与開始から投与終了後まで、患者を安静の状態に保たせ、十分な観察を行うこと。特に、投与開始直後は注意深く観察すること。
8.3 急性腎障害(急性間質性腎炎)があらわれることがあるので、定期的に検査を行うこと。[11.1.5参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 心疾患のある患者
QT延長、心室頻拍(Torsade de pointesを含む)を起こすことがある。[7.、11.1.2参照]
9.3 肝機能障害患者
血中濃度が上昇するおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒト母乳中へ移行することが報告されている1)。
9.7 小児等
嘔吐等の症状に注意すること。新生児、乳児で、肥厚性幽門狭窄があらわれたとの報告がある2)。
9.8 高齢者
用量に留意するなど慎重に投与すること。一般に生理機能が低下していることが多い。
10. 相互作用
相互作用序文
本剤はCYP3Aで代謝される。また、本剤はCYP3A、P-糖蛋白質を阻害する。[16.4参照]
薬物代謝酵素用語
CYP3A
薬物代謝酵素用語
P-糖蛋白質
10.1 併用禁忌
| エルゴタミン酒石酸塩・無水カフェイン・イソプロピルアンチピリン (クリアミン) ジヒドロエルゴタミンメシル酸塩 [2.2参照] | 四肢の虚血、血管攣縮等が報告されている。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| ピモジド [2.2参照] | QT延長、心室性不整脈(Torsade de pointesを含む)等が発現するおそれがある。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| ロミタピドメシル酸塩 (ジャクスタピッド) [2.2参照] | ロミタピドメシル酸塩の血中濃度が著しく上昇するおそれがある。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| アミオダロン(注射剤) (アンカロン注) [2.2参照] | 併用によりTorsade de pointesのリスクが増加する。 | 併用によりQT延長作用が相加的に増加することがある。 |
| クリンダマイシン(注射剤、経口剤) (ダラシンS注射液、ダラシンカプセル) リンコマイシン塩酸塩水和物 (リンコシン) [2.2参照] | 併用してもこれらの薬剤の効果があらわれないと考えられる。 | 本剤の細菌のリボゾーム50S Subunitへの親和性がこれらの薬剤より高いと考えられる。 |
10.2 併用注意
| ジソピラミド キニジン硫酸塩水和物 | QT延長、心室性不整脈(Torsade de pointesを含む)等が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| テオフィリン3)4) アミノフィリン水和物 | 悪心・嘔吐、不整脈、痙攣等が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| シクロスポリン タクロリムス水和物 | 腎障害等が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| ワルファリンカリウム | 出血傾向、プロトロンビン時間延長等が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| イリノテカン塩酸塩水和物 | 骨髄機能抑制、下痢等の副作用を増強するおそれがあるため、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| ビンカアルカロイド ビンブラスチン硫酸塩 ビノレルビン酒石酸塩等 | 好中球減少、筋肉痛等が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| バルプロ酸ナトリウム | 傾眠、運動失調等が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| フェロジピン | 降圧作用の増強が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| ベラパミル塩酸塩 | 血圧低下、徐脈性不整脈、乳酸アシドーシス等が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| ミダゾラム5) トリアゾラム6) | 鎮静作用の増強が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| カルバマゼピン | めまい、運動失調等が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| コルヒチン | 下痢、腹痛、発熱、筋肉痛、汎血球減少、呼吸困難等が報告されているので、減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| シンバスタチン7) アトルバスタチンカルシウム水和物8) | シンバスタチン、アトルバスタチンカルシウム水和物との併用により、筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇を特徴とし、急激な腎機能悪化を伴う横紋筋融解症があらわれたとの報告がある。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| ピタバスタチンカルシウム水和物 | シンバスタチン、アトルバスタチンカルシウム水和物との併用により、筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇を特徴とし、急激な腎機能悪化を伴う横紋筋融解症があらわれたとの報告がある。 | 本剤がピタバスタチンの肝臓への取り込みを阻害するためと考えられる。 |
| ブロモクリプチンメシル酸塩9) ドセタキセル水和物 パクリタキセル セレギリン塩酸塩 シルデナフィルクエン酸塩10) バルデナフィル塩酸塩水和物 タダラフィル シロスタゾール | 減量するなど慎重に投与すること。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| ブロナンセリン クロザピン ゾピクロン アルプラゾラム エプレレノン エレトリプタン臭化水素酸塩 エベロリムス サキナビルメシル酸塩 | これらの薬剤の作用が増強するおそれがある。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| ドンペリドン | ドンペリドンの血中濃度が上昇する。また、ドンペリドンとの併用により、QT延長が報告されている。 | 本剤はCYP3Aと結合し、複合体を形成するため、これらの薬剤の代謝を抑制し、血中濃度が上昇することがある。 |
| 副腎皮質ホルモン剤 メチルプレドニゾロン11)等 | これらの薬剤の消失半減期が延長するとの報告があるので、減量するなど慎重に投与すること。 | 本剤はこれらの薬剤の代謝を抑制することがある。 |
| エバスチン12) | エバスチンの代謝物カレバスチンの血中濃度が上昇するとの報告がある。 | 本剤はこれらの薬剤の代謝を抑制することがある。 |
| エドキサバントシル酸塩水和物 | 出血のリスクを増大させるおそれがある。併用する場合、エドキサバントシル酸塩水和物の用量は、エドキサバントシル酸塩水和物の電子添文を参照すること。 | 本剤がP-糖蛋白質を阻害し、エドキサバンの血中濃度を上昇させるためと考えられる。 |
| ジゴキシン | ジゴキシンの作用増強による嘔気、嘔吐、不整脈等の中毒症状が報告されているので、減量するなど慎重に投与すること。 | 本剤の腸内細菌叢への影響により、ジゴキシンの代謝が抑制される。 |
| ザフィルルカスト | ザフィルルカストの血中濃度が低下するとの報告がある。 | 機序は不明である。 |
| シメチジン | 難聴が報告されているので、減量するなど慎重に投与すること。 | これらの薬剤のCYP3A阻害作用により、本剤の代謝が抑制され、血中濃度が上昇すると考えられる。 |
| リトナビル | 本剤のAUCが上昇することが予想される。 | これらの薬剤のCYP3A阻害作用により、本剤の代謝が抑制され、血中濃度が上昇すると考えられる。 |
| クリンダマイシン(外用剤) | 併用してもクリンダマイシンの効果があらわれないと考えられる。 | 本剤の細菌のリボゾーム50S Subunitへの親和性がクリンダマイシンより高いと考えられる。 |
| リバーロキサバン | リバーロキサバンの血中濃度が上昇したとの報告がある。 | 本剤がCYP3A4及びP-糖蛋白質を阻害することによりリバーロキサバンのクリアランスが減少する。 |
| フェキソフェナジン塩酸塩 | フェキソフェナジンの血漿中濃度を上昇させるとの報告がある。 | P-糖蛋白質の阻害によるフェキソフェナジンのクリアランスの低下及び吸収率の増加に起因するものと推定される。 |
| CYP3A4誘導作用を有する薬剤 リファンピシン、リファブチン、フェニトイン、フェノバルビタール等 セイヨウオトギリソウ(St.John's Wort,セント・ジョーンズ・ワート)含有食品 | 本剤の作用が減弱するおそれがある。 | これらの薬剤のCYP3A誘導作用により、本剤の代謝を促進し、本剤の血中濃度を低下させる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 偽膜性大腸炎等の血便を伴う重篤な大腸炎(頻度不明)
腹痛、頻回の下痢があらわれた場合には、直ちに投与を中止するなど適切な処置を行うこと。
11.1.2 心室頻拍(Torsade de pointesを含む)、心室細動、QT延長(頻度不明)[7.、9.1.1参照]
11.1.3 ショック、アナフィラキシー(頻度不明)
呼吸困難、胸内苦悶、血圧低下等があらわれた場合には投与を中止し、適切な処置を行うこと。[8.2参照]
11.1.4 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)
11.1.5 急性腎障害(急性間質性腎炎)(頻度不明)[8.3参照]
11.1.6 肝機能障害、黄疸(頻度不明)
AST、ALT、ALPの上昇等を伴う肝機能障害や黄疸があらわれることがある。
11.2 その他の副作用
| 頻度不明 | |
| 過敏症 | 発疹、蕁麻疹、血管性浮腫 |
| 消化器 | 食欲不振、悪心・嘔吐、胃痛、下痢、膵炎 |
| 聴覚 | 難聴注) |
| 眼 | 視力低下、霧視 |
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.1 注射液は注射用水で5%溶液をつくり、これをブドウ糖注射液、生理食塩液等で希釈して点滴静注溶液とする。5%溶液を調製するには、本剤1バイアルに注射用水10mLを加える。
14.1.2 5%溶液調製の際には、生理食塩液あるいは無機塩類を含有する溶液を使用しないこと。5%溶液をさらに希釈する際には、注射用水を使用しないこと(低張になる)。
14.1.3 5%溶液は冷蔵庫内で2週間安定である。
14.2 薬剤投与時の注意
血管痛、血栓、静脈炎を起こすことがあるので注意すること。
15. その他の注意
15.1 臨床使用に基づく情報
外国で重症筋無力症が悪化したとの報告がある。
16. 薬物動態
16.1 血中濃度
患者(外国人)3例に本剤400mg(力価)を5%ブドウ糖注射液500mLで溶解し、1.5時間かけて点滴静注した場合、点滴終了直後の血清中濃度は平均7.8μg/mLであった14)。
16.3 分布
16.4 代謝
16.5 排泄
16.5.1 排泄経路
尿中、胆汁中
16.5.2 排泄率
患者(外国人)3例に本剤400mg(力価)を5%ブドウ糖注射液500mLで溶解し、1.5時間かけて点滴静注した場合、点滴静注後24時間までに投与量の5.5%が尿中に排泄されたが、その89%は12時間までに排泄された14)。
18. 薬効薬理
18.1 作用機序
18.2 抗菌作用
19. 有効成分に関する理化学的知見
19.1. エリスロマイシンラクトビオン酸塩
22. 包装
500mg×10バイアル
23. 主要文献
- 森操七郎, 日本産科婦人科学会雑誌, 23 (7), 547-555, (1971)
- Honein MA, et al., Lancet., (354), 2101-2105, (1999)
- Reisz G,et al., Am Rev Respir Dis., (127), 581-584, (1983) »PubMed »DOI
- 前田昇三, Chemotherapy., 41 (7), 765-769, (1993) »DOI
- Olkkola KT,et al., Clin Pharmacol Ther., 53 (3), 298-305, (1993) »PubMed »DOI
- Phillips JP,et al., J Clin Psychopharmacol., 6 (5), 297-299, (1986) »PubMed
- Kantola T,et al., Clin Pharmacol Ther., 64 (2), 177-182, (1998) »PubMed »DOI
- Siedlik PH,et al., J Clin Pharmacol., (39), 501-504, (1999)
- Nelson MV,et al., Clin Pharmacol Ther., 47 (6), 694-697, (1990) »PubMed »DOI
- Zusman RM,et al., Am J Cardiol., 83 (5A), 35C-44C, (1999)
- Laforce CF,et al., J Allergy Clin Immunol., 72 (1), 34-39, (1983) »PubMed »DOI
- 長澤紘一ほか, 臨床医薬, 11 (6), 1213-1226, (1995)
- Quinnan GV&McCabe WR., Lancet., 1 (8074), 1160-1161, (1978) »PubMed »DOI
- Lopez-Belio M&Takimura Y., Antibiot Annu., 295-311, (1954-1955)
- Lopez-Belio M,et al., Antibiot Annu., 152-158, (1956-1957)
- Simon C&Clasen I., Curr Med Res Opin., 5 (suppl.2), 19-22, (1978)
- Takimura Y&Lopez-Belio M., Antibiot Med., 1 (10), 561-566, (1955) »PubMed
- Prandota J,et al., J Int Med Res., 8 (suppl.2), 1-8, (1980) »PubMed
- Mao JCH,et al., Biochem Pharmacol., 14, 1049-1058, (1965)
- Watkins PB,et al., Proc Natl Acad Sci USA., 82, 6310-6314, (1985) »PubMed »DOI
- Brian WR,et al., Biochemistry., 29 (51), 11280-11292, (1990) »PubMed »DOI
- Brock TD,et al., Biochim Biophys Acta., 33, 274-275, (1959) »PubMed »DOI
- Mao JCH., Biochem Pharmacol., 16, 2441-2443, (1967)
- 日本抗生物質医薬品基準解説, 723-728, (1971), (薬業時報社)
- GOODMAN and GILMAN's The Pharmacological Basis of Therapeutics 8th ed., 1130-1134, (1990), (Pergamon Press.)
- McCall CE,et al., Am J Med Sci., 254 (2), 144-155, (1967) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
ヴィアトリス製薬合同会社
メディカルインフォメーション部
〒106-0041
東京都港区麻布台一丁目3番1号
電話:フリーダイヤル 0120-419-043
製品情報問い合わせ先
ヴィアトリス製薬合同会社
メディカルインフォメーション部
〒106-0041
東京都港区麻布台一丁目3番1号
電話:フリーダイヤル 0120-419-043
26. 製造販売業者等
26.1 製造販売元
ヴィアトリス・ヘルスケア合同会社
東京都港区麻布台一丁目3番1号
26.2 販売元
ヴィアトリス製薬合同会社
東京都港区麻布台一丁目3番1号