医薬品情報
| 総称名 | ビクシリン |
|---|---|
| 一般名 | アンピシリン水和物 クロキサシリンナトリウム水和物 |
| 欧文一般名 | Ampicillin Hydrate Cloxacillin Sodium Hydrate |
| 製剤名 | アンピシリン水和物・クロキサシリンナトリウム水和物錠 |
| 薬効分類名 | 複合ペニシリン系抗生物質製剤 |
| 薬効分類番号 | 6191 |
| ATCコード | J01CA51 J01CR50 J01RA01 |
| KEGG DRUG |
D02502
アンピシリン・クロキサシリン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年5月 改訂(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ビクシリンS配合錠 (後発品) | VICCILLIN-S COMBINATION TABLETS | Meiji Seikaファルマ | 6191001F1036 | 19円/錠 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 伝染性単核症のある患者[アンピシリンの投与により発疹の発現頻度を高めることがある。]
4. 効能または効果
6. 用法及び用量
通常、成人1回合剤(アンピシリン水和物・クロキサシリンナトリウム水和物)として250mg(力価)〜500mg(力価)を6時間ごとに経口投与する。
ただし、年齢、症状により適宜増減する。
ただし、年齢、症状により適宜増減する。
8. 重要な基本的注意
8.1 本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
8.2 ショックを起こすおそれがあるので、十分な問診を行うこと。[11.1.1参照]
8.3 無顆粒球症、溶血性貧血があらわれることがあるので、定期的に検査を行うこと。[11.1.3参照]
8.4 急性腎障害等の重篤な腎障害があらわれることがあるので、定期的に検査を行うこと。[11.1.4参照]
8.5 肝機能障害があらわれることがあるので、定期的に検査を行うこと。[11.1.6参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 ペニシリン系又はセフェム系抗生物質に対し過敏症の既往歴のある患者(ただし、本剤に対し過敏症の既往歴のある患者には投与しないこと)
9.1.2 本人又は両親、兄弟に気管支喘息、発疹、蕁麻疹等のアレルギー症状を起こしやすい体質を有する患者
9.1.3 経口摂取の不良な患者又は非経口栄養の患者、全身状態の悪い患者
観察を十分に行うこと。アンピシリンの投与によりビタミンK欠乏症状があらわれることがある。
9.2 腎機能障害患者
9.2.1 高度の腎障害のある患者
投与間隔をあけて使用すること。血中濃度が持続する。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。アンピシリンの大量(3,000mg/kg/day)投与でラットに催奇形性が報告されている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。母乳中へ移行することが報告されている。
9.8 高齢者
次の点に注意し、用量並びに投与間隔に留意するなど患者の状態を観察しながら慎重に投与すること。
・生理機能が低下していることが多く副作用が発現しやすい。
・ビタミンK欠乏による出血傾向があらわれることがある。
10. 相互作用
10.2 併用注意
| 経口避妊薬 | 経口避妊薬の効果が減弱するおそれがある。 | 腸内細菌叢を変化させ、経口避妊薬の腸肝循環による再吸収を抑制すると考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも0.1%未満)
不快感、口内異常感、喘鳴、眩暈、便意、耳鳴等があらわれた場合には、投与を中止し、適切な処置を行うこと。[8.2参照]
11.1.2 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)1)(0.1%未満)、皮膚粘膜眼症候群(Stevens-Johnson症候群)2)3)(0.1%未満)、急性汎発性発疹性膿疱症(頻度不明)
11.1.3 無顆粒球症、溶血性貧血(いずれも0.1%未満)[8.3参照]
11.1.4 急性腎障害等の重篤な腎障害(0.1%未満)[8.4参照]
11.1.5 偽膜性大腸炎等の血便を伴う重篤な大腸炎4)(0.1%未満)
腹痛、頻回の下痢があらわれた場合には、直ちに投与を中止し、適切な処置を行うこと。
11.1.6 肝機能障害(頻度不明)
AST、ALTの上昇等を伴う肝機能障害があらわれることがある。[8.5参照]
11.2 その他の副作用
| 5%以上又は頻度不明 | 0.1〜5%未満 | 0.1%未満 | |
| 過敏症 | 発熱、発疹、蕁麻疹等 | ||
| 血液 | 好酸球増多、顆粒球減少、血小板減少、貧血 | ||
| 肝臓 | AST上昇 | ||
| 消化器 | 下痢、悪心、食欲不振等 | ||
| 菌交代症注) | 口内炎、カンジダ症 | ||
| ビタミン欠乏症注) | ビタミンK欠乏症状(低プロトロンビン血症、出血傾向等)、ビタミンB群欠乏症状(舌炎、口内炎、食欲不振、神経炎等) |
12. 臨床検査結果に及ぼす影響
本剤の投与により、ベネディクト試薬、フェーリング試薬による尿糖検査では偽陽性を呈することがあるので注意すること。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
アンピシリンとアロプリノールとの併用により、発疹の発現が増加するとの報告がある。
16. 薬物動態
16.1 血中濃度
健康成人に本剤250mg又は500mg(力価)(各々n=2)1回経口投与したときの最高血中濃度は1〜2時間後にみられ、各々4.1μg/mL、9.2μg/mLの値を示し、以後漸減し、6時間後は各々0.56μg/mL、0.52μg/mLであった5)。
16.5 排泄
健康成人に本剤250mg(力価)(n=3)を1回経口投与後6時間までの尿中排泄率は21%であった6)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
肺膿瘍(肺化膿症)、慢性呼吸器病変の二次感染(気管支拡張症)、肺炎(細菌性肺炎)に対する成績では有効率90.0%(18/20例)を示した。
18. 薬効薬理
18.1 作用機序
アンピシリンは、細菌の細胞壁合成阻害により殺菌的に作用する。
クロキサシリンは、細菌の細胞壁合成阻害により殺菌的に作用し、細菌が産生するペニシリン分解酵素に対し抵抗性を有する。
クロキサシリンは、細菌の細胞壁合成阻害により殺菌的に作用し、細菌が産生するペニシリン分解酵素に対し抵抗性を有する。
18.2 in vitro抗菌作用
アンピシリン/クロキサシリンは、グラム陽性菌及びグラム陰性菌に抗菌作用を示し、多剤耐性ブドウ球菌にも抗菌作用を示した。
| 被験菌 | 最小発育阻止濃度(μg/mL) | ||
| アンピシリン/クロキサシリン | アンピシリン | クロキサシリン | |
| Staphylococcus aureus 209P | 0.062 | 0.062 | 0.5 |
| S.aureus 樋口株注) | 0.16 | 0.62 | 0.16 |
| S.aureus 有富株注) | 0.31 | 1.25 | 0.31 |
| S.aureus 久家株注) | 0.31 | 1.25 | 0.31 |
| Streptococcus hemolyticus D90 | 0.25 | 0.5 | >1.0 |
| S.hemolyticus Cook | 0.005 | 0.005 | 0.04 |
| S.pneumoniae type 3 IID | 0.125 | 0.125 | 0.5 |
| Escherichia coli IAM 1253 | 0.62 | 1.25 | >10 |
19. 有効成分に関する理化学的知見
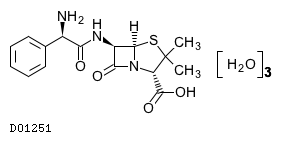
19.1. アンピシリン水和物
19.2. クロキサシリンナトリウム水和物
| 一般的名称 | クロキサシリンナトリウム水和物 | ||||||
|---|---|---|---|---|---|---|---|
| 一般的名称(欧名) | Cloxacillin Sodium Hydrate | ||||||
| 略号 | MCIPC | ||||||
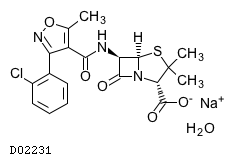
| 化学名 | Monosodium(2S,5R,6R)-6-{[3-(2-chlorophenyl)-5-methylisoxazole-4-carbonyl]amino}-3,3-dimethyl-7-oxo-4-thia-1-azabicyclo[3.2.0]heptane-2-carboxylate monohydrate | ||||||
| 分子式 | C19H17ClN3NaO5S・H2O | ||||||
| 分子量 | 475.88 | ||||||
| 物理化学的性状 | クロキサシリンナトリウム水和物は白色〜淡黄白色の結晶又は結晶性の粉末である。 本品は水、N,N-ジメチルホルムアミド又はメタノールに溶けやすく、エタノール(95)にやや溶けにくい。 |
||||||
| 分配係数 |
|
||||||
| 理化学知見その他 | 19.2 クロキサシリンナトリウム水和物 | ||||||
| KEGG DRUG |
|
20. 取扱い上の注意
光により徐々に退色することがあるので、アルミピロー開封後の保存には注意すること。
22. 包装
PTP包装 100錠(10錠×10)
23. 主要文献
- 立田京子ほか, 臨床皮膚科, 35 (4), 339-342, (1981)
- Howell,C.G.,et al., J.Pediatr.Surg., 22 (11), 994-995, (1987) »PubMed
- Frank,S.,et al., Clin.Pediatr., 23 (7), 412-414, (1984)
- Keating,J.P.,et al., Am.J.Dis.Child., 128 (3), 369-370, (1974) »PubMed
- 石神襄次ほか, Jpn.J.Antibiot., 22 (5), 372-377, (1969) »PubMed
- 角田和之ほか, 西日本泌尿器科, 31 (3), 432-438, (1969)
24. 文献請求先及び問い合わせ先
文献請求先
Meiji Seikaファルマ株式会社
くすり相談室
〒104-8002
東京都中央区京橋2-4-16
電話:フリーダイヤル0120-093-396
03-3273-3539
03-3273-3539
FAX:03-3272-2438
製品情報問い合わせ先
Meiji Seikaファルマ株式会社
くすり相談室
〒104-8002
東京都中央区京橋2-4-16
電話:フリーダイヤル0120-093-396
03-3273-3539
03-3273-3539
FAX:03-3272-2438
26. 製造販売業者等
26.1 製造販売元
Meiji Seikaファルマ株式会社
東京都中央区京橋2-4-16