医薬品情報
| 総称名 | ペレックス |
|---|---|
| 一般名 | サリチルアミド アセトアミノフェン 無水カフェイン クロルフェニラミンマレイン酸塩 |
| 欧文一般名 | Salicylamide Acetaminophen Anhydrous Caffeine Chlorpheniramine Maleate |
| 製剤名 | サリチルアミド・アセトアミノフェン・無水カフェイン・クロルフェニラミンマレイン酸塩配合顆粒剤 |
| 薬効分類名 | 感冒剤 |
| 薬効分類番号 | 1180 |
| ATCコード | N02BA55 R06AB54 |
| KEGG DRUG |
D04044
クロルフェニラミンマレイン酸塩・アセトアミノフェン・サリチルアミド・無水カフェイン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年10月 改訂(第2版)

|
1.警告 2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 13.過量投与 15.その他の注意 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ペレックス配合顆粒 | Pelex combination granules | 大鵬薬品工業 | 1180105D1035 | 6.9円/g | 劇薬 |
1. 警告
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
感冒もしくは上気道炎に伴う下記症状の改善及び緩和
鼻汁、鼻閉、咽・喉頭痛、咳、痰、頭痛、関節痛、筋肉痛、発熱
6. 用法及び用量
通常、成人1回1gを1日3〜4回経口投与する。
なお、年齢、症状により適宜増減する。
なお、年齢、症状により適宜増減する。
8. 重要な基本的注意
眠気を催すことがあるので、本剤投与中の患者には自動車の運転等、危険を伴う機械の操作に従事させないよう十分に注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 出血傾向のある患者
血小板機能異常があらわれ、出血傾向が悪化するおそれがある。[10.2参照]
9.1.2 気管支喘息の患者(アスピリン喘息(非ステロイド性消炎鎮痛剤等による喘息発作の誘発)又はその既往歴のある患者を除く)
9.1.3 アルコール多量常飲者
9.1.4 絶食・低栄養状態・摂食障害等によるグルタチオン欠乏、脱水症状のある患者
肝障害があらわれやすくなる。[11.1.6参照]
9.1.5 開放隅角緑内障の患者
抗コリン作用により眼圧が上昇し、症状を悪化させることがある。
9.2 腎機能障害患者
腎障害が悪化するおそれがある。[11.1.7参照]
9.3 肝機能障害患者
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。投与する際には、必要最小限にとどめ、羊水量、胎児の動脈管収縮を疑う所見を妊娠週数や投与日数を考慮して適宜確認するなど慎重に投与すること。シクロオキシゲナーゼ阻害剤(経口剤、坐剤)を妊婦に使用し、胎児の腎機能障害及び尿量減少、それに伴う羊水過少症が起きたとの報告がある。シクロオキシゲナーゼ阻害剤を妊娠中期以降の妊婦に使用し、胎児の動脈管収縮が起きたとの報告があり、また妊娠後期はその発現リスクがより高くなることが知られている。サリチル酸系製剤(アスピリン等)の動物実験(ラット)で催奇形作用が、また、ヒトで妊娠後期に投与された患者及びその新生児に出血異常があらわれたとの報告がある1)2)3)4)5)6)7)8)9)。妊娠後期の女性へのアセトアミノフェンの投与により胎児に動脈管収縮を起こすことがある10)11)12)。アセトアミノフェンを妊娠後期のラットに投与した実験で、弱い胎児の動脈管収縮が報告されている13)。
9.6 授乳婦
9.7 小児等
9.7.1 15歳未満の水痘、インフルエンザ患者
投与しないことを原則とするが、やむを得ず投与する場合には、慎重に投与し、投与後の患者の状態を十分に観察すること。サリチル酸系製剤の使用実態は我が国と異なるものの、米国においてサリチル酸系製剤とライ症候群との関連性を示す疫学調査報告がある。(ライ症候群:小児において極めてまれに水痘、インフルエンザ等のウイルス性疾患の先行後、激しい嘔吐、意識障害、痙攣(急性脳浮腫)と肝臓ほか諸臓器の脂肪沈着、ミトコンドリア変形、AST・ALT・LDH・CKの急激な上昇、高アンモニア血症、低プロトロンビン血症、低血糖等の症状が短期間に発現する高死亡率の病態である。)
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下していることが多い。
10. 相互作用
10.2 併用注意
| クマリン系抗凝血剤 ワルファリン [9.1.1参照] | クマリン系抗凝血剤の作用が増強されることがあるので、減量するなど慎重に投与すること。 | サリチル酸系製剤(アスピリン等)は血小板凝集抑制作用、消化管刺激による出血作用を有する。また、血漿蛋白に結合したクマリン系抗凝血剤と置換し、これらの薬剤を遊離させる。 |
| 糖尿病用剤 インスリン製剤 トルブタミド | 糖尿病用剤の作用が増強されることがあるので、減量するなど慎重に投与すること。 | サリチル酸系製剤(アスピリン等)は血漿蛋白に結合した糖尿病用剤と置換し、これらの薬剤を遊離させる。 |
| 中枢神経抑制剤 フェノチアジン誘導体 バルビツール酸誘導体等 | 相互に中枢神経抑制作用が増強されることがあるので、減量するなど慎重に投与すること。 | クロルフェニラミンマレイン酸塩は中枢神経抑制作用を有する。 |
| アルコール [9.1.3参照] | (1)相互に中枢神経抑制作用が増強されることがあるので、減量するなど慎重に投与すること。 (2)アルコール多量常飲者がアセトアミノフェンを服用したところ肝不全を起こしたとの報告がある。 | (1)クロルフェニラミンマレイン酸塩は中枢神経抑制作用を有する。 (2)アルコールによりアセトアミノフェンから肝毒性を持つN-アセチル-p-ベンゾキノンイミンへの代謝が促進される。 |
| MAO阻害剤 | 相互に作用が増強されることがあるので、減量するなど慎重に投与すること。 | クロルフェニラミンマレイン酸塩の抗コリン作用が増強されると考えられている。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
呼吸困難、全身潮紅、血管浮腫、蕁麻疹等があらわれることがある。
11.1.2 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、急性汎発性発疹性膿疱症、剥脱性皮膚炎(いずれも頻度不明)
11.1.3 再生不良性貧血、無顆粒球症(いずれも頻度不明)
11.1.5 間質性肺炎(頻度不明)
発熱、咳嗽、呼吸困難、胸部X線異常、好酸球増多を伴う間質性肺炎があらわれることがあるので、このような症状があらわれた場合には投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.1.6 劇症肝炎、肝機能障害、黄疸(いずれも頻度不明)
11.1.7 間質性腎炎、急性腎障害(いずれも頻度不明)[9.2参照]
11.1.8 横紋筋融解症(頻度不明)
筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇を特徴とする横紋筋融解症があらわれることがある。
11.1.9 薬剤性過敏症症候群(頻度不明)
初期症状として発疹、発熱がみられ、更に肝機能障害、リンパ節腫脹、白血球増加、好酸球増多、異型リンパ球出現等を伴う遅発性の重篤な過敏症状があらわれることがある。なお、ヒトヘルペスウイルス6(HHV-6)等のウイルスの再活性化を伴うことが多く、投与中止後も発疹、発熱、肝機能障害等の症状が再燃あるいは遷延化することがあるので注意すること。
注1)発現頻度は小児用製剤(本剤の1/6量)の情報を含む。
11.2 その他の副作用
| 0.1〜5%未満 | 頻度不明 | |
| 過敏症 | 発疹 | 浮腫、鼻炎様症状、結膜炎 |
| 血液 | 血小板減少、貧血、チアノーゼ | |
| 消化器 | 食欲不振、胃部不快感、悪心・嘔吐、下痢、便秘 | 胸やけ、胃痛、口渇、消化管出血 |
| 精神神経系 | 眠気 | 耳鳴、難聴、めまい、頭痛、興奮、神経過敏、焦躁感、複視 |
| 肝臓 | 肝障害 | |
| 腎臓 | 腎障害 | |
| 泌尿器 | 多尿、排尿困難 | |
| その他 | 心悸亢進 | 過呼吸注2)、代謝性アシドーシス注2) |
13. 過量投与
13.1 症状
13.1.2 総合感冒剤や解熱鎮痛剤等の配合剤には、アセトアミノフェンを含むものがあり、本剤とアセトアミノフェン又はその配合剤との偶発的な併用により、アセトアミノフェンの過量投与による重篤な肝障害が発現するおそれがある。[1.2参照]
13.2 処置
アセトアミノフェン過量投与時の解毒(肝障害の軽減等)には、アセチルシステインの投与を考慮すること。[1.2参照]
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 腎盂及び膀胱腫瘍の患者を調査したところ、アセトアミノフェンの類似化合物(フェナセチン)製剤を長期・大量に使用(例:総服用量1.5〜27kg、服用期間4〜30年)していた人が多いとの報告がある21)22)23)。
15.1.2 アセトアミノフェンの類似化合物(フェナセチン)の長期投与により、血色素異常を起こすことがあるので、長期投与を避けること。
15.1.3 非ステロイド性消炎鎮痛剤を長期間投与されている女性において、一時的な不妊が認められたとの報告がある。
15.2 非臨床試験に基づく情報
15.2.1 アセトアミノフェンの類似化合物(フェナセチン)を長期・大量投与した動物実験(マウス、ラット)で、腫瘍発生が認められたとの報告がある24)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
18. 薬効薬理
18.1 作用機序
19. 有効成分に関する理化学的知見
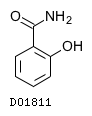
19.1. サリチルアミド
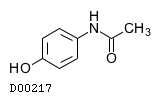
19.2. アセトアミノフェン
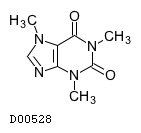
19.3. 無水カフェイン
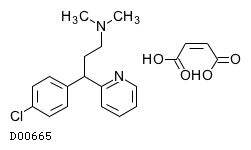
19.4. クロルフェニラミンマレイン酸塩
22. 包装
ヒートシール
1g×1000包、1g×2000包
バラ包装
500g(プラスチックボトル)、5kg(アルミ袋:1kg×5袋)
23. 主要文献
- Larsson,K.S.et al., Acta Paediat.Scand., 54, 43-48, (1965) »PubMed
- Eriksson,M., Acta Path.Microbiol.Scand., 76, 164-170, (1969) »PubMed
- Lansdown,A.B.G., Food Cosmet.Toxicol., 8, 647-653, (1970) »PubMed
- Eriksson,M., Acta Paediat.Scand., 59, 517-522, (1970) »PubMed
- Eriksson,M., Acta Pharmacol.Toxicol., 29, 241-249, (1971) »PubMed
- Eriksson,M., Acta Pharmacol.Toxicol., 29, 250-255, (1971) »PubMed
- Tanaka,S.et al., 先天異常, 13 (2), 73-84, (1973) »DOI
- Tagashira,E.et al., Jpn.J.Pharmacol., 31 (4), 563-571, (1981) »DOI
- Stuart,M.J.et al., New Engl.J.Med., 307 (15), 909-912, (1982) »PubMed
- 西原正泰 他, 和歌山医学, 56 (2), 121, (2005)
- 平川健一郎 他, 日本未熟児新生児学会雑誌, 22 (3), 601, (2010)
- 松沢麻衣子 他, 日本未熟児新生児学会雑誌, 22 (3), 602, (2010)
- 門間和夫 他, 小児科の進歩, 2, 95-101, (1983)
- Bailey,D.N.et al., J.Analyt.Toxicol., 6, 64-68, (1982) »PubMed
- Schilf,E.et al., Arch.Gynaekol., 134, 201-204, (1928)
- Davidson,D.G.D.et al., Br.Med.J., 2 (5512), 497-499, (1966) »PubMed
- Krikler,D.M., Br.Med.J., 2 (5552), 615-616, (1967) »PubMed
- Proudfoot,A.T.et al., Br.Med.J., 3 (5722), 557-558, (1970) »PubMed
- Edwards,O.M.et al., Br.Med.J., 2 (5753), 87-89, (1971) »PubMed
- Will,E.J.et al., Br.Med.J., 4 (5784), 430-431, (1971) »PubMed
- Taylor,J.S.et al., Med.J.Aust., 1 (9), 407-409, (1972) »PubMed
- Leistenschneider,W.et al., Schweiz.Med.Wschr., 103 (12), 433-439, (1973)
- Johansson,S.et al., Cancer., 33 (3), 743-753, (1974) »PubMed
- 井坂英彦, 厚生省がん研究助成金による研究報告集(昭和52年度), 751-753, (1978)
- 小沢正人 他, 臨牀と研究, 55 (2), 586-590, (1978)
- 綾部長徳, 新薬と臨牀, 25 (11), 1975-1977, (1976)
- 辰口益三, 基礎と臨床, 11 (2), 633-635, (1977)
- 浅子由己, 基礎と臨床, 11 (2), 636-638, (1977)
- 江頭洋祐, 新薬と臨牀, 26 (4), 791-793, (1977)
- 河村信治 他, 新薬と臨牀, 26 (5), 993-995, (1977)
- 赤松春義, 新薬と臨牀, 26 (5), 996-998, (1977)
- 中村泰郎, 新薬と臨牀, 26 (8), 1586-1588, (1977)
- 島本暉朗 他, 薬理学, 151-167,471-479, (1968)
- 亀山勉 他, 応用薬理, 13 (6), 845-850, (1977)
24. 文献請求先及び問い合わせ先
文献請求先
大鵬薬品工業株式会社
医薬品情報課
〒101-8444
東京都千代田区神田錦町1-27
電話:0120-20-4527
製品情報問い合わせ先
大鵬薬品工業株式会社
医薬品情報課
〒101-8444
東京都千代田区神田錦町1-27
電話:0120-20-4527
26. 製造販売業者等
26.1 製造販売元
大鵬薬品工業株式会社
東京都千代田区神田錦町1-27