医薬品情報
| 総称名 | サム |
|---|---|
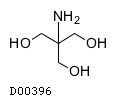
| 一般名 | トロメタモール |
| 欧文一般名 | Trometamol |
| 薬効分類名 | アシドーシス治療剤 |
| 薬効分類番号 | 3399 |
| KEGG DRUG |
D04981
トロメタモール・塩化ナトリウム・塩化カリウム
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年12月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| サム点滴静注セット | THAM Injection SET | 大塚製薬工場 | 3399400X1035 | 734円/管 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 代謝性及び呼吸性アルカローシスのある患者[症状が悪化するおそれがある。]
2.2 無尿、尿毒症などの腎機能障害のある患者[9.2.1参照]
4. 効能または効果
○代謝性アシドーシス(アシデミアを認めるとき)
○体外循環、低体温による手術及び保存血大量注入によるアシドーシスの治療
6. 用法及び用量
投与に当たっては、まず投与量の半量から投与を開始し、必要に応じて、適宜追加補正することが望ましい。
通常成人の投与量は一般に次式による。
投与量(mEq)=不足塩基量(Base Deficit mEq/L)×0.3×体重(kg)
トロメタモールの0.3モル溶液の場合は次式による。
投与量(mL)=不足塩基量(Base Deficit mEq/L)×体重(kg)
投与はなるべく太い静脈に直接又は静脈カテーテルを用いて0.2mL/kg/分以下の速度で注射する。
なお、投与量、投与速度は年齢、症状、細胞外液量等に応じて適宜増減する。
なお、投与量、投与速度は年齢、症状、細胞外液量等に応じて適宜増減する。
8. 重要な基本的注意
8.1 本剤及び本剤の補正液は濃厚液のため、そのまま注射しないこと。必ず希釈して使用すること。
8.2 呼吸の抑制があらわれることがあるので、使用にあたっては人工呼吸器等の準備が望ましい。
9. 特定の背景を有する患者に関する注意
9.2 腎機能障害患者
9.2.1 無尿、尿毒症などの腎機能障害のある患者
投与しないこと。水分、電解質代謝異常が悪化するおそれがある。[2.2参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.7 小児等
9.7.1 小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
9.7.2 新生児への投与で、出血性肝壊死が報告されている1)。
9.8 高齢者
投与速度を緩徐にし、減量するなど注意すること。一般に生理機能が低下している。
11. 副作用
11.2 その他の副作用
| 頻度不明 | |
| 大量・急速投与 | 呼吸の抑制、低血圧、低血糖 |
| 注射部位 細い血管 | 血管痙攣、静脈炎 |
| 注射部位 血管外漏出 | 組織の炎症、壊死 |
| 電解質異常 | 浸透圧性利尿作用による血清電解質の減少、腎障害や乏尿のある患者では高カリウム血症 |
14. 適用上の注意
14.1 全般的な注意
使用時には、感染に対する配慮をすること。
14.2 薬剤調製時の注意
14.2.1 使用時に調製し、調製液は速やかに使用すること。
14.2.2 添付のラベルは、pH約10で使用するときはpH=8の部分を切り取り、pH約8で使用するときはpH=10の部分を切り取って希釈液の瓶に貼って使用すること。
14.3 薬剤投与時の注意
14.3.1 血管外に漏出させないよう注意すること。
14.3.2 残液は使用しないこと。
16. 薬物動態
16.1 血中濃度
14C標識トロメタモール(THAM)を含む本剤をウサギに静脈投与した結果、血中濃度は投与6時間後までに急速に減少し、48時間後にはほとんど残存していなかった2)。
16.5 排泄
14C標識THAMを含む本剤をウサギに静脈内投与した結果、投与された放射能は投与後24時間までに尿中に52〜76%が排泄された2)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
18. 薬効薬理
18.1 作用機序
トロメタモール(THAM)は酸(HA)の存在下で次のような反応をする。
(CH2OH)3C-NH2+HA→←(CH2OH)3C-NH3++A−
また、血中の炭酸ガスと反応して
(CH2OH)3C-NH2+CO2+H2O→←(CH2OH)3C-NH3++HCO3−
すなわち、THAMは血中の酸やCO2と反応して、これらを減少させる5)。
18.2 アシドーシス改善効果
18.3 細胞内アシドーシス改善効果
本剤を静注したヒトにおいて、赤血球内pHの著明な上昇が認められ、細胞外液のみならず細胞内液のアシドーシスの改善効果が示唆された9)。
19. 有効成分に関する理化学的知見
19.1. トロメタモール
20. 取扱い上の注意
以下の場合には使用しないこと。
・容器から薬液が漏れている場合
・性状その他薬液に異状が認められる場合
22. 包装
1セット
サム点滴静注(50mL)1管 ガラスアンプル
サム希釈液(450mL)1本 プラボトル(PLABOTTLE)
サム補正液(20mL)1管 ガラスアンプル
23. 主要文献
- Goldenberg V.E.,et al., J Am Med Assoc., 205, 81-84, (1968)
- (株)大塚製薬工場 社内資料:薬物動態
- 五十川久士, 新潟医学会雑誌, 81, 228-243, (1967)
- 田中 孝,他, 麻酔, 16, 343-347, (1967) »PubMed
- Nahas,G.G., Clin Pharm & Therap, 4, 784-803, (1963)
- (株)大塚製薬工場 社内資料:薬効薬理(実験的代謝性アシドーシス)
- (株)大塚製薬工場 社内資料:薬効薬理(実験的出血性ショック)
- 桑原茂夫,他, 麻酔, 17, 155-159, (1968) »PubMed
- 三村 久,他, 麻酔, 18, 486-491, (1969) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
株式会社大塚製薬工場
輸液DIセンター
〒101-0048
東京都千代田区神田司町2-2
電話:0120-719-814
FAX:03-5296-8400
製品情報問い合わせ先
株式会社大塚製薬工場
輸液DIセンター
〒101-0048
東京都千代田区神田司町2-2
電話:0120-719-814
FAX:03-5296-8400
26. 製造販売業者等
26.1 製造販売元
株式会社大塚製薬工場
徳島県鳴門市撫養町立岩字芥原115
26.2 販売提携
大塚製薬株式会社
東京都千代田区神田司町2-9