医薬品情報
| 総称名 | コンビビル |
|---|---|
| 一般名 | ジドブジン ラミブジン |
| 欧文一般名 | Zidovudine Lamivudine |
| 製剤名 | ジドブジン・ラミブジン製剤 |
| 薬効分類名 | 抗ウイルス化学療法剤 |
| 薬効分類番号 | 6250 |
| ATCコード | J05AR01 |
| KEGG DRUG |
D07507
ジドブジン・ラミブジン
|
| KEGG DGROUP |
DG03107
抗HIV薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年8月 改訂(第7版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| コンビビル配合錠 | Combivir Combination Tablets | ヴィーブヘルスケア | 6250100F1032 | 885円/錠 | 劇薬, 処方箋医薬品注) |
1. 警告
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
5. 効能または効果に関連する注意
5.1 無症候性ヒト免疫不全ウイルス(HIV)感染症に関する治療開始については、CD4リンパ球数及び血漿中HIV RNA量が指標とされている。よって、本剤の使用にあたっては、患者のCD4リンパ球数及び血漿中HIV RNA量を確認するとともに、最新のガイドライン1)2)3)を確認すること。
5.2 本剤はジドブジン及びラミブジンの固定用量を含有する配合剤であるので、ジドブジン又はラミブジンの用量調節が必要な次の患者には個別のジドブジン製剤(レトロビルカプセル)又はラミブジン製剤(エピビル錠)を用いること。
・体重30kg未満の小児患者[9.7参照]
・肝硬変等の重篤な肝疾患を有する患者[9.1.7参照]
5.3 HIVによる神経機能障害に対する本剤の有効性は確認されていない。
6. 用法及び用量
通常、成人には1回1錠(ジドブジンとして300mg及びラミブジンとして150mg)を1日2回経口投与する。
7. 用法及び用量に関連する注意
7.2 本剤投与中貧血(ヘモグロビン値が9.5g/dL未満)又は好中球減少(1000/mm3未満)が認められた場合は、本剤の投与を中止し、個別のジドブジン製剤(レトロビルカプセル)又はラミブジン製剤(エピビル錠)を用いて用量調節を行うこと。[2.1、5.4、9.1.1-9.1.3参照]
7.3 本剤と他の抗HIV薬との併用療法において、因果関係が特定されない重篤な副作用が発現し、治療の継続が困難であると判断された場合には、本剤若しくは併用している他の抗HIV薬の一部を減量又は休薬するのではなく、原則として本剤及び併用している他の抗HIV薬の投与をすべて一旦中止すること。
7.4 本剤はジドブジン及びラミブジンの固定用量を含有する配合剤であるので、本剤に加えてジドブジン含有製剤(レトロビルカプセル)又はラミブジン含有製剤を併用投与しないこと。
7.5 ラミブジンの薬剤耐性プロファイル等のウイルス学的特性はエムトリシタビンと類似しているので、本剤とエムトリシタビンを含む製剤を併用しないこと。また、エムトリシタビンを含む抗HIV療法においてウイルス学的効果が得られず、HIV-1逆転写酵素遺伝子のM184V/I変異が認められた場合、エムトリシタビンを本剤に変更するのみで効果の改善は期待できない。[18.3.2参照]
8. 重要な基本的注意
8.1 本剤の使用に際しては、国内外のガイドライン等の最新の情報を参考に、患者又は患者に代わる適切な者に、次の事項についてよく説明し同意を得た後、使用すること。
・本剤の日本人における薬物動態及び有効性・安全性は確認されておらず、外国人における成績しか得られていないこと。
・本剤はHIV感染症の根治療法薬ではないことから、日和見感染症を含むHIV感染症の進展に伴う疾病を発症し続ける可能性があるので、本剤投与開始後の身体状況の変化については、すべて担当医に報告すること。
・本剤はジドブジン及びラミブジンの固定用量を含有する配合剤であるので、本剤に加えてジドブジン含有製剤(レトロビルカプセル)又はラミブジン含有製剤をさらに追加して服用しないこと。
・本剤の有効成分であるジドブジンは相互作用が多く知られていることから、他院で処方された薬剤又は市販薬を服用中の場合は、すべて担当医に報告すること。
8.3 重篤な血液障害、乳酸アシドーシス、脂肪沈着による重度の肝腫大(脂肪肝)、横紋筋融解症、ニューロパシー、錯乱、痙攣、てんかん様発作、心不全があらわれることがあるので、定期的に検査を行うなど観察を十分に行うこと。[9.2.2、11.1.1、11.1.2、11.1.4-11.1.6参照]
8.4 本剤の投与により、脂肪組織萎縮症があらわれることがあるので、脂肪組織萎縮症の徴候を判定するための検査を行うなど、脂肪組織萎縮症の徴候に十分注意するとともに、身体状態の変化について定期的に問診すること。
8.5 本剤を含む抗HIV薬の多剤併用療法を行った患者で、免疫再構築症候群が報告されている。投与開始後、免疫機能が回復し、症候性のみならず無症候性日和見感染(マイコバクテリウムアビウムコンプレックス、サイトメガロウイルス、ニューモシスチス等によるもの)等に対する炎症反応が発現することがある。また、免疫機能の回復に伴い自己免疫疾患(甲状腺機能亢進症、多発性筋炎、ギラン・バレー症候群、ブドウ膜炎等)が発現するとの報告があるので、これらの症状を評価し、必要時には適切な治療を考慮すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 好中球数750/mm3未満又はヘモグロビン値が7.5g/dL未満に減少した患者(ただし原疾患であるHIV感染症に起因し、本剤又は他の抗HIV薬による治療経験が無いものを除く)
9.1.3 好中球数750/mm3以上1000/mm3未満又はヘモグロビン値が7.5g/dL以上9.5g/dL未満の患者
ジドブジンにより好中球数、ヘモグロビン値が更に減少することがある。[7.2参照]
9.1.4 ビタミンB12欠乏患者
ジドブジンにより貧血が発現するおそれがある。
9.1.5 膵炎を発症する可能性のある患者(膵炎の既往歴のある患者、膵炎を発症させることが知られている薬剤との併用療法を受けている患者)
9.1.6 B型肝炎ウイルス感染を合併している患者
本剤の投与を中断する場合には十分注意すること。B型慢性肝炎を合併している患者では、本剤の投与中止により、B型慢性肝炎が再燃するおそれがある。特に非代償性の場合、重症化するおそれがある。[1.2参照]
9.1.7 肝硬変等の重篤な肝疾患を有する患者
肝臓におけるグルクロン酸抱合低下により、ジドブジンの高い血中濃度が持続するおそれがある。[5.2参照]
9.2 腎機能障害患者
9.2.1 腎機能障害(Ccrが30mL/min未満)を有する患者
9.2.2 腎機能障害(Ccrが30〜49mL/min)を有する患者
9.3 肝機能障害患者
9.3.1 肝機能障害のある患者
ジドブジンの高い血中濃度が持続するおそれがある。
9.5 妊婦
9.5.1 妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
(1)ジドブジン
ジドブジンはヒト胎盤を通過する。出生児の血漿中ジドブジン濃度は、分娩時の母親の血漿中濃度と同じであることが報告されている4)(外国人データ)。
ジドブジンが胎児臍帯血白血球のDNAに取り込まれたという報告がある5)(外国人データ)。
ラットの受胎能及び一般生殖能試験(50、150、450mg/kg/日、1日2回投与)では、中及び高用量群に胚吸収率の増加、高用量群に胎児平均体重の減少がみられた。
サルを用いた試験で、胎児にミトコンドリア障害(心筋及び骨格筋におけるミトコンドリアミオパシー)が認められたとの報告がある6)。
(2)ラミブジン
ラミブジンはヒト胎盤を通過する。出生児の血清中ラミブジン濃度は、分娩時の母親の血清中及び臍帯血中の濃度と同じであることが報告されている(外国人データ)。
動物実験(ウサギ)で胎児毒性(早期の胚死亡数の増加)が報告されている。
(3)ジドブジン/ラミブジン共通
ヌクレオシド系逆転写酵素阻害剤(NRTI)を子宮内曝露又は周産期曝露された新生児及び乳児において、ミトコンドリア障害によると考えられる軽微で一過性の血清乳酸値の上昇が報告されている。
非常にまれに発育遅延、てんかん様発作、他の神経疾患も報告されている。しかしながら、これら事象とNRTIの子宮内曝露、周産期曝露との関連性は確立していない。
9.5.2 本剤を投与された妊婦より出生した児に貧血があらわれることがある。定期的に検査を行うなど児の状態を十分に観察し、異常が認められた場合には適切な処置を行うこと。
9.6 授乳婦
9.6.1 授乳を避けさせること。
(1)ジドブジン
経口投与されたジドブジン(200mg、単回投与)は、ヒト乳汁中に排泄され、血清中の濃度と同じであることが報告されている(外国人データ)。
ジドブジンの母体血漿中濃度に対する乳汁中濃度の比は0.4〜3.2であることが報告されている(外国人データ)。
乳児の血清中のジドブジン濃度は24ng/mLであったとの報告がある7)(外国人データ)。
(2)ラミブジン
経口投与されたラミブジンはヒト乳汁中に排泄されることが報告されている(乳汁中濃度:<0.5-8.2μg/mL)8)(外国人データ)。
ラミブジンの母体血漿中濃度に対する乳汁中濃度の比は0.6〜3.3であることが報告されている(外国人データ)。
乳児の血清中のラミブジン濃度は18〜28ng/mLであったとの報告がある(外国人データ)。
9.7 小児等
本剤はジドブジン及びラミブジンの固定用量を含有する配合剤であるので、ジドブジン又はラミブジンの用量調節が必要である体重30kg未満の小児患者には、個別のジドブジン製剤(レトロビルカプセル)又はラミブジン製剤(エピビル錠)を用いること。[5.2参照]
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。肝機能又は腎機能が低下していることが多いため高い血中濃度が持続するおそれがある。
10. 相互作用
10.1 併用禁忌
| イブプロフェン(ブルフェン) [2.3参照] | ジドブジンと併用投与した場合、血友病患者において出血傾向が増強することがある。 | 機序は不明である。 |
10.2 併用注意
| ペンタミジンイセチオン酸塩、ピリメタミン(国内未発売)、スルファメトキサゾール・トリメトプリム、フルシトシン、ガンシクロビル、インターフェロン、ビンクリスチン硫酸塩、ビンブラスチン硫酸塩、ドキソルビシン塩酸塩 | ジドブジンの毒性作用が増強されることがある。 | 機序は不明であるが、ともに腎毒性又は骨髄毒性を有するためと考えられている。 |
| プロベネシド | ジドブジンの全身クリアランスが約1/3に減少し半減期が約1.5倍延長したとの報告があるので、投与間隔を適宜あけること。 | ジドブジンのグルクロン酸抱合が競合的に阻害される。また、本剤のグルクロン酸抱合体の腎排泄が抑制されることが考えられている。 |
| フルコナゾール、ホスフルコナゾール | ジドブジンの最高血中濃度が84%上昇するとの報告がある9)。 | ジドブジンのグルクロン酸抱合が競合的に阻害されることが考えられている。 |
| リトナビル | ジドブジンの最高血中濃度が27%減少し、AUCが25%減少するとの報告がある10)。 | ジドブジンのグルクロン酸抱合が促進されることが考えられている。 |
| リファンピシン | ジドブジンの全身クリアランスが約2.5倍増加し、AUCが約1/2減少するとの報告がある11)。 | 機序は不明である。 |
| フェニトイン | 血中フェニトイン濃度が約1/2に減少するとの報告がある12)。また、上昇するとも報告されているので、血中フェニトイン濃度を注意深く観察すること。 | 機序は不明である。 |
| サニルブジン | 細胞内におけるサニルブジン三リン酸化体が減少し、サニルブジンの効果が減弱するとの報告があるので、ジドブジンとサニルブジンとの併用療法は避けることが望ましい。 | ジドブジンが細胞内におけるサニルブジンのリン酸化を抑制することが考えられている。 |
| リバビリン | In vitroにおいてリバビリンとの併用によりジドブジンの効果が減弱するとの報告があるので、ジドブジンとリバビリンの併用療法は避けることが望ましい。 | ジドブジンの細胞内におけるリン酸化が競合的に阻害されることが考えられている。 |
| アトバコン | ジドブジンのAUCが33%上昇し、グルクロン酸抱合体の最高血中濃度が19%低下した。ジドブジン500又は600mg/日を3週間投与した場合では、ジドブジンの血中濃度の上昇により、副作用の発現頻度が上昇する可能性は低いと考えられるが、アトバコンをより長期に投与する場合には、十分注意すること。 | ジドブジンのグルクロン酸抱合が阻害されることが考えられている。 |
| スルファメトキサゾール・トリメトプリム | ラミブジンのAUCが43%増加し、全身クリアランスが30%、腎クリアランスが35%減少したとの報告がある。 | 腎臓における排泄がラミブジンとトリメトプリムで競合すると考えられている。 |
| ソルビトール | 経口ソルビトール溶液(ソルビトールとして3.2g、10.2g、13.4g)とラミブジンの併用により、ラミブジンのAUCが減少した(それぞれ18%、36%、42%減少)との報告がある。 | ソルビトールによりラミブジンの吸収が抑制されると考えられている。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 重篤な血液障害
11.1.2 乳酸アシドーシス(0.2%)、脂肪沈着による重度の肝腫大(脂肪肝)(0.2%)
乳酸アシドーシス又は肝毒性が疑われる臨床症状や検査値異常が認められた場合には、本剤の投与を一時中止すること。特に、肝疾患の危険因子を有する患者においては注意すること。本剤を含むNRTIの単独投与又はこれらの併用療法により、重篤な乳酸アシドーシス(全身倦怠、食欲不振、急な体重減少、胃腸障害、呼吸困難、頻呼吸等)及び肝毒性(脂肪沈着による重度の肝腫大、脂肪肝を含む)が、女性に多く報告されている。[8.3参照]
11.1.3 膵炎(0.4%)
11.1.4 横紋筋融解症(頻度不明)[8.3参照]
11.1.5 ニューロパシー(0.4%)、錯乱、痙攣、てんかん様発作(いずれも頻度不明)[8.3参照]
11.1.6 心不全(頻度不明)[8.3参照]
注)発現頻度には使用成績調査の結果を含む
11.2 その他の副作用
| 1〜11%未満 | 1%未満 | 頻度不明 | |
| 血液 | 平均赤血球容積(MCV)増加注1)、リンパ球減少注2)、リンパ節症注2) | ||
| 消化器 | 嘔気、下痢、腹痛、嘔吐、食欲不振、胃炎、鼓腸放屁 | 消化不良、便秘、口内潰瘍 | 嚥下困難、口唇浮腫、舌浮腫、あい気、歯肉出血、直腸出血、痔核注2)、腹部痙直注2) |
| 全身症状 | 倦怠感・疲労、体脂肪の再分布/蓄積(胸部、体幹部の脂肪増加、末梢部、顔面の脂肪減少、野牛肩、血清脂質増加、血糖増加)、発熱 | 疼痛、頭痛、体重減少、無力症 | 胸痛、全身痛、悪寒、感冒症状、背痛、体温調節障害注2)、インフルエンザ様疾患 |
| 肝臓 | 肝機能検査値異常(AST、ALT等の上昇) | ||
| 筋骨格 | 骨痛・筋痛 | ミオパシー、CK上昇を伴う筋脱力、筋痙直注2)、関節痛注2) | |
| 精神神経系 | めまい | うつ病、錯感覚、不眠、末梢神経障害、傾眠、失神 | 痙攣等の脳症状、活動低下、手足のしびれ感、情緒不安、筋痙攣、振戦、攣縮、痛覚過敏、神経過敏症、健忘症、見当識障害、嗄声、ストレス反応、空間の広がり感、睡眠障害注2)、不安注2)、感情障害注2) |
| 呼吸器 | 呼吸困難、肺炎、鼻出血、咽頭炎、鼻炎注1)、咳注2)、咽頭痛注2)、気管支炎注2)、副鼻腔炎注2)、耳管炎注2)、呼吸障害注2)、上気道炎注2) | ||
| 皮膚 | 発疹 | 湿疹、ざ瘡・毛嚢炎、そう痒、皮膚炎、脱毛 | じん麻疹、体臭変化、爪・皮膚・口腔粘膜の色素沈着、発汗注2) |
| 過敏症 | アレルギー反応 | ||
| 腎臓 | 頻尿、排尿障害、腎不全、無尿、多尿、血清クレアチニン上昇注2) | ||
| 循環器 | 心筋症、血管拡張 | ||
| 代謝・内分泌系 | トリグリセリド上昇・血清コレステロール上昇、血中尿酸上昇 | CK上昇、高乳酸塩血症 | 血清アミラーゼ上昇、脱水、高血糖注1)、重炭酸塩低下注1)、総蛋白低下注2)、重炭酸塩上昇注2)、総蛋白上昇注2)、血糖値低下注2) |
| その他 | 味覚倒錯、霧視 | 羞明、弱視、難聴、敗血症、女性化乳房 |
13. 過量投与
13.1 処置
血液透析及び腹膜透析はジドブジンの除去には一部しか関与しないが、グルクロン酸抱合体の排泄を亢進する。ラミブジンは血液透析により一部除去される(ラミブジン300mg投与時に、投与約2時間後から4時間血液透析したとき、AUC0-infが約24%低下することが報告されている)51)。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.2 非臨床試験に基づく情報
15.2.1 ジドブジンについては、がん原性試験で試験末期に雌動物(ラット及びマウス)に膣腫瘍が発生したとの報告がある。
マウス(20、30、40mg/kg/日、1日1回経口投与)及びラット(80、220、300mg/kg/日、1日1回経口投与)におけるがん原性試験で、膣扁平上皮癌(マウス高用量群5/60例、ラット高用量群2/60例)が認められた13)。[15.2.2参照]
マウス(20、30、40mg/kg/日、1日1回経口投与)及びラット(80、220、300mg/kg/日、1日1回経口投与)におけるがん原性試験で、膣扁平上皮癌(マウス高用量群5/60例、ラット高用量群2/60例)が認められた13)。[15.2.2参照]
15.2.2 ジドブジンについては、マウスにおける経胎盤曝露によるがん原性試験で次の報告がある。
・最大耐量(420mg/kg/周産期体重)を妊娠12〜18日(妊娠中〜末期)に投与された母動物からの出生児において、出生1年後、肺、肝及び雌性生殖器の腫瘍発生率の増加が認められた14)。
15.2.3 ジドブジンの変異原性について、次の報告がある。
・Ames試験では変異原性は認められなかったが、マウスリンパ腫細胞を用いた遺伝子突然変異試験において弱い変異原性を示し、in vitroの細胞形質転換試験において陽性を示した13)。
・ラットを用いたin vivo染色体異常試験では染色体の損傷は認められなかったが、ヒト培養リンパ球を用いたin vitro染色体異常試験、ラット及びマウスを用いたin vivo小核試験で染色体異常誘発作用が認められた13)。また、11人のAIDS患者の末梢血リンパ球において、ジドブジン服用患者は非服用患者と比較して染色体異常頻度が高かったとの報告がある16)。
・ジドブジンが成人AIDS患者の白血球のDNA及びその胎児臍帯血白血球のDNAに取り込まれたとの報告がある5)。
15.2.4 ラミブジンについては、遺伝毒性試験において弱い染色体異常誘発作用を示したとの報告がある。また、長期のがん原性試験において発がん性を認めなかったとの報告がある。
ヒト末梢血リンパ球を用いた染色体異常試験では300μg/mL以上、マウスリンパ腫細胞を用いた遺伝子突然変異試験では2000μg/mL以上で陽性を示した。
マウス及びラットを用いた長期のがん原性試験では、臨床用量におけるヒト全身曝露量(AUC)の10倍(マウス)及び58倍(ラット)までの曝露量において、発がん性は認められなかった。
ヒト末梢血リンパ球を用いた染色体異常試験では300μg/mL以上、マウスリンパ腫細胞を用いた遺伝子突然変異試験では2000μg/mL以上で陽性を示した。
マウス及びラットを用いた長期のがん原性試験では、臨床用量におけるヒト全身曝露量(AUC)の10倍(マウス)及び58倍(ラット)までの曝露量において、発がん性は認められなかった。
16. 薬物動態
16.1 血中濃度
16.1.1 単回経口投与
健康成人76例にドルテグラビル・ラミブジン50mg・300mgを空腹時に単回経口投与した時のラミブジンの血漿中濃度の推移を図-1に、薬物動態パラメータを表-1に示した52)(外国人データ)。
図-1 健康成人にドルテグラビル・ラミブジンを単回経口投与した時のラミブジンの血漿中濃度の推移(平均値+標準偏差)
| AUC0-inf(μg・h/mL) | Cmax(μg/mL) | Tmax(h)注1) | t1/2(h) |
| 13.59(17.99) | 3.22(29.30) | 1.00(0.50,3.50) | 18.63(26.85) |
16.1.2 反復経口投与
HIV感染症患者6例に対し、ジドブジン100mg注)1日4回とラミブジン150mg1日2回を25日間以上連続経口投与した時のジドブジン、ラミブジンの血漿中薬物濃度の推移を図-2に、薬物動態パラメータを表-2に示した。ジドブジンは投与後0.8時間で、ラミブジンは投与後1.3時間で最高血漿中濃度(Cmax)に達し、ジドブジン、ラミブジンのCmax平均はそれぞれ0.549μg/mL、1.547μg/mLであった。ジドブジン、ラミブジンの平均半減期はそれぞれ1.1時間、2.3時間であった17)。
図-2 血漿中薬物濃度の推移(平均値±標準偏差、6例)
| Cmax(μg/mL) | Tmax(h) | t1/2(h) | AUC0-6(μg・h/mL) | AUC0-12(μg・h/mL) | |
| ジドブジン | 0.549±0.261 | 0.8±0.3 | 1.1±0.1 | 0.858±0.266 | − |
| ラミブジン | 1.547±0.302 | 1.3±0.6 | 2.3±0.6 | 5.089±1.692 | 6.165±2.312 |
ラミブジンとジドブジンの併用投与を行なった時、ジドブジンの最高血中濃度が28%上昇したが、ラミブジン及びジドブジンのAUCに有意な変化は認められなかった18)(外国人データ)。
成人HIV感染症患者にジドブジンを反復経口投与後のCmax及びAUCは、2.0mg/kgを8時間毎〜10mg/kg注)を4時間毎の投与量範囲で投与量に比例して増加し、0.5〜1.5時間で最高血漿中濃度に達し、半減期約1時間(0.78〜1.93時間)で消失した(外国人データ)。
成人HIV感染症患者にラミブジン2mg/kg注)を1日2回15日間経口投与した時、初回投与時では投与1.5時間後に最高血中濃度の1.5μg/mLに達し、半減期は2.6時間であり、15日間投与後では血中濃度は定常状態に達し、最高血中濃度は1.9μg/mLであった19)(外国人データ)。
16.1.3 単回静脈内投与
ジドブジンを静脈内投与注)した場合、1〜5mg/kgの範囲で線形の薬物動態を示し、半減期は約1.1時間(0.48〜2.86時間)、全身クリアランス(CL)は1900mL/min/70kg、みかけの分布容積(Vd)は1.6L/kgであった21)(外国人データ)。
16.1.4 生物学的同等性
健康成人24例に、空腹時に本剤(ジドブジン300mg及びラミブジン150mgを含有する配合剤)1錠、及び、空腹時にジドブジン製剤(ジドブジン300mgを含有する錠剤)及びラミブジン製剤(ラミブジン150mgを含有する錠剤)各1錠を投与し、生物学的同等性を評価した。本剤投与時とジドブジン製剤及びラミブジン製剤の併用投与時のジドブジン及びラミブジンのAUClast、AUC∞及びCmaxは、生物学的同等性の判定基準(平均値の比の90%信頼区間が0.8〜1.25の範囲内)を満たし、生物学的同等性が示された(外国人データ)。
16.2 吸収
16.2.1 食事の影響
健康成人24例に、標準朝食(炭水化物58g、蛋白質33g、脂肪67g)摂取後に本剤(ジドブジン300mg及びラミブジン150mgを含有する配合剤)を投与した時、一晩絶食後に投与した時と比較して、ジドブジンのCmaxは45%低下し、Tmaxは30分から1時間(中央値)に遅延し、ラミブジンのCmaxは15%低下した。一方AUC∞はラミブジンでは変化が認められず、ジドブジンでは10%の低下であり、食事摂取により曝露量はほとんど変化しなかった(外国人データ)。
16.2.2 バイオアベイラビリティ
16.3 分布
16.3.1 ジドブジン
(1)髄液への移行
ヒトにジドブジンを投与したとき髄液中への移行が認められ、2mg/kg注)経口投与1.8時間後におけるジドブジンの髄液中/血漿中濃度比は0.15であり、2.5及び5.0mg/kg静脈内投与注)2〜4時間後の髄液中/血漿中濃度比はそれぞれ0.20及び0.64であった21)(外国人データ)。
(2)血漿蛋白結合率
In vitroにおけるジドブジンの血漿蛋白結合率は34〜38%であった。
(3)結合蛋白
In vitroにおけるジドブジンの結合蛋白はアルブミンと同定された22)。
16.3.2 ラミブジン
(1)脳脊髄液への移行
成人HIV感染症患者にラミブジン4〜10mg/kg注)を1日2回2週間以上反復経口投与した時、投与2時間後の脳脊髄液中濃度は血中濃度の約6%であった23)(外国人データ)。
16.4 代謝
16.4.1 ジドブジン
ジドブジンは吸収後、主にUDP-glucuronosyl transferaseによってグルクロン酸抱合をうけ、主代謝物3'-azido-3'-deoxy-5'-O-β-D-glucopyranuronosyl thymidine(GZDV)に速やかに代謝される。副代謝経路として3'-amino-3'-deoxythymidine(AMT)及びそのグルクロン酸抱合体(GAMT)に代謝される経路も存在する24)。
静脈内投与後のGZDVのAUCは未変化体のAUCの約3倍であり、AMTのAUCは未変化体のAUCの1/5であった。
静脈内投与後のGZDVのAUCは未変化体のAUCの約3倍であり、AMTのAUCは未変化体のAUCの1/5であった。
16.4.2 ラミブジン
ヒトでの主代謝物はトランス−スルホキシド体(1-[(2R,5S)-trans-2-hydroxymethyl-1,3-oxathiolan-3-oxide-5-yl]cytosine)であった25)(外国人データ)。
16.5 排泄
16.5.1 ジドブジン
HIV感染症患者にジドブジンを経口投与後の未変化体及びGZDVの尿中排泄率はそれぞれ14.3%及び75.2%であった。ジドブジンの腎クリアランスは400mL/min/70kgであり、糸球体濾過及び能動的尿細管分泌による排泄機構が示唆される21)(外国人データ)。
16.5.2 ラミブジン
成人HIV感染症患者にラミブジン2mg/kg注)を経口投与した時、投与後12時間尿中にトランス−スルホキシド体が投与量の5.2%排泄された。また、血中濃度が定常状態での未変化体の尿中排泄率は投与量の約70%であり、腎排泄がラミブジンの体内からの除去の主要な経路であることが示された25)(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
(1)ジドブジン
(2)ラミブジン
16.7 薬物相互作用
16.7.1 In vitro試験
アスピリン、インドメタシン等のグルクロン酸抱合により代謝される薬剤がジドブジンのグルクロン酸抱合を阻害したとの報告がある27)。
注)本剤の承認された用法及び用量は「通常、成人には1回1錠(ジドブジンとして300mg及びラミブジンとして150mg)を1日2回経口投与する。」である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第II相試験
本剤を用いた日本人における臨床試験成績は得られていないため、参考までに、HIV感染症を対象としたジドブジン100mg注)1日4回及びラミブジン150mg1日2回の併用投与を行った国内臨床試験の結果を示す。
試験開始前のCD4リンパ球数が100〜400/mm3の12歳以上のHIV感染症患者42例を対象とした多施設共同オープン試験(ラミブジン150mg1日2回とジドブジン100mg1日4回注)を併用投与)で、有効性評価対象症例37例での臨床評価の概要は次のとおりである。
CD4リンパ球数は、試験開始時の平均220.8/mm3から4週後には約25/mm3増加し、8週後から24週後までの増加量は4.6〜34.0/mm3で推移した。CD4リンパ球数の推移を図-1に示した。
CD4パーセントは、開始時の18.81%から4週後には20.03%へ有意に増加し、8週後から24週後まではほとんど変動なく約20%で推移した。血漿中HIV RNA量は、試験開始時の平均3.8log10 copies/mLから4週後には1.6log10 copies/mL有意に減少し、8週後から24週後までは0.7〜1.2log10 copies/mL減少した。血漿中HIV RNA量の推移を図-2に示した。
図-1 CD4リンパ球数の推移(平均値±標準偏差)
図-2 血漿中HIV RNA量の推移(平均値±標準偏差)
42例中30例(71.4%)に副作用が認められ、主な副作用は赤血球減少等の貧血(22件)、空腹時血糖値上昇(6件)、嘔気(4件)、食欲不振(3件)であった17)。
17.1.2 海外第III相試験(B3027)
抗レトロウイルス薬による治療経験のないウイルス量が10000copies/mL以上、及びCD4リンパ球数が200/mm3以上の診断が確定したHIV感染症患者75例を対象とした無作為多施設オープン試験において、ジドブジン200mg注)1日3回及びラミブジン150mg1日2回の併用投与又は本剤(ジドブジン300mg+ラミブジン150mg1日2回)の単独投与を12週間行い有効性を比較した。投与開始12週後における血漿中HIV RNA量の平均変化量を表-1に示した。両群において血漿中HIV RNA量の平均変化量に有意な差は認められなかった。
| ジドブジン+ラミブジン併用投与群 | 本剤投与群 | 95%信頼区間 | ||
| Intent-to-treat analysis | 例数 | 38 | 33 | [−0.301、0.298]注1) |
| HIV RNA量の平均変化量(log10 copies/mL) | −1.36 | −1.36 | ||
| Per-protocol analysis | 例数 | 33 | 30 | [−0.364、0.283]注1) |
| HIV RNA量の平均変化量(log10 copies/mL) | −1.37 | −1.41 | ||
17.1.3 海外臨床試験(NUCA3001,NUCB3001,NUCB3002,NUCA3002の4試験)のmeta-analysis
欧米で行われた4つの無作為化、二重盲検比較試験についてmeta-analysisを行った。ジドブジン200mg注)1日3回にラミブジン150mg又は300mg注)1日2回を併用投与した群(ラミブジン併用群)における症例数は569例、ジドブジン200mg1日3回の単独投与又はジドブジンにザルシタビンを併用投与した群(比較対照群)は316例で、両群の患者背景には差を認めなかった。
試験期間中、CDC分類のB/Cあるいは新たなB/C症状に進展した患者数は計118例、また、Cへの進展は計28例に認められた。meta-analysisの結果、ラミブジン併用群は比較対照群に比し、CDC分類のB/Cへの進展は49%減少し(p<0.0001)、CDC分類Cへの進展は66%減少した(p=0.003)28)。
試験期間中、CDC分類のB/Cあるいは新たなB/C症状に進展した患者数は計118例、また、Cへの進展は計28例に認められた。meta-analysisの結果、ラミブジン併用群は比較対照群に比し、CDC分類のB/Cへの進展は49%減少し(p<0.0001)、CDC分類Cへの進展は66%減少した(p=0.003)28)。
17.1.4 海外第III相試験(B3007:CAESAR)
CD4リンパ球数が25〜250/mm3かつkarnofsky scoreが70以上のHIV感染症患者1840例を対象とした無作為化、二重盲検比較試験において、ジドブジン1日500〜600mg注)とプラセボを併用投与した群(プラセボ併用群)注1)は471例、ジドブジンにラミブジン150mg1日2回を併用投与した群(ラミブジン併用群)は907例、ジドブジンにラミブジンとloviride注2)100mg1日3回を併用投与した群(ラミブジン+loviride併用群)は462例であった。52週間の試験期間中に、AIDS若しくは死亡へ進行した患者(Intent-to-treat解析)は、プラセボ併用群で95例(20%)、ラミブジン併用群で86例(9%)、ラミブジン+loviride併用群で42例(9%)であり、ラミブジンが併用された群では、いずれもプラセボ併用群に比較して有意にAIDS若しくは死亡への進行が抑えられた(p<0.0001)29)。
注1)ジドブジンにザルシタビン又はジダノシンの併用投与は可能とした。
注2)国内では未承認の非ヌクレオシド系逆転写酵素阻害剤
17.1.5 海外臨床試験(進行性エイズ関連症候群[ARC]患者、ジドブジンの投与量変更)
エイズ患者及び進行性ARC患者320例を対象とした二重盲検比較試験において、ジドブジン300mgを1日2回12時間毎に投与した群(1日2回投与群)は162例で、100mg注)を1日6回4時間毎に投与した群(1日6回投与群)は158例であった。
48週間の試験期間中に発現した死亡症例数及び日和見感染症発症例数等について、両群間に差は認められなかった(表-2)。
48週間の試験期間中に発現した死亡症例数及び日和見感染症発症例数等について、両群間に差は認められなかった(表-2)。
| 1日2回投与群 (n=162) | 1日6回投与群 (n=158) | |
| 死亡症例数 | 5 | 5 |
| 日和見感染症発症例数 | 33 | 29 |
| 平均体重増加量(第20週)(kg) | 1.9 | 3.2 |
| CD4リンパ球数増加量(/mm3) | 22(最高値、第4週)注1) | 29(最高値、第8週)注1) |
副作用発現頻度について、両群間に差は認められなかった(表-3)。
| 1日2回投与群 (n=162) | 1日6回投与群 (n=158) | |
| 貧血(Hgb<8.0g/dL) | 14% | 16% |
| 好中球減少(<1000/mm3) | 42% | 42% |
| 嘔気 | 15% | 18% |
| 頭痛 | 12% | 11% |
| 無力症 | 6% | 5% |
| 筋肉痛 | 1% | 5% |
| 嘔吐 | 4% | 4% |
注)本剤の承認された用法及び用量は「通常、成人には1回1錠(ジドブジンとして300mg及びラミブジンとして150mg)を1日2回経口投与する。」である。
18. 薬効薬理
18.1 作用機序
18.1.1 ジドブジン
18.1.2 ラミブジン
18.2 抗ウイルス作用
18.2.1 ジドブジン
ジドブジンのHIVに対するin vitroにおけるIC50値は、CD4リンパ球系細胞を用いた系では0.13μg/mL(0.49μM)以下であった34)。
In vitroでジドブジンとアバカビル、ラミブジン、ジダノシン等の抗HIV薬あるいはインターフェロンαとの相加又は相乗作用が認められた。
マウスにマウスレトロウイルス(Rauscherマウス白血病ウイルス)を接種し、接種4時間目より、ジドブジンを1.0mg/mLの割合で飲用水に混入して投与することにより、平均脾臓重量、脾臓細胞感染率、及び血中ウイルス力価が対照群に比し著しく低下した。また感染後生存日数も延長した35)。
18.2.2 ラミブジン
In vitroでのラミブジンのHIV-1(RF、GB8、U455及びIIIB)に対するIC50値は670nM以下、HIV-2 RODに対するIC50値は40nMであった33)。
In vitroでアバカビル、ジダノシン、ネビラピン、ザルシタビン及びジドブジンとの相加又は相乗作用が認められた36)。また、in vitroにおいて、ラミブジンは単独で、ジドブジン耐性臨床分離株の平均p24抗原量を薬物無処置群に比べ66〜80%低下させた。
In vitroでの26種のHIV-1臨床分離株[グループM(サブタイプA、B、C、D、E、F、G)]並びに3種類のHIV-2臨床分離株に対するラミブジンのIC50値(平均値)はHIV-1株及びHIV-2株でそれぞれ40nM(範囲は1〜120nM)及び42nM(範囲は2〜120nM)であった。
18.3 薬剤耐性
18.3.1 ジドブジン
ジドブジンを含むチミジンアナログに対する耐性は、HIV逆転写酵素の41、67、70、210、215及び219番目のアミノ酸の変異によって生じ、これらのうち41番目と215番目の変異あるいは4個以上の変異によってウイルスは表現型として耐性を示す37)38)。なお、これらチミジンアナログの変異を有するウイルスは高度の交差耐性を示さない39)。[7.1参照]
また、62、75、77、116及び151番目のアミノ酸の変異、並びに69番目のアミノ酸のスレオニンからセリンへの変異とそれに加えて同じ個所への6塩基対の挿入により、ウイルスはジドブジンを含むヌクレオシド系逆転写酵素阻害剤に対し多剤耐性を示す40)41)42)。
また、62、75、77、116及び151番目のアミノ酸の変異、並びに69番目のアミノ酸のスレオニンからセリンへの変異とそれに加えて同じ個所への6塩基対の挿入により、ウイルスはジドブジンを含むヌクレオシド系逆転写酵素阻害剤に対し多剤耐性を示す40)41)42)。
18.3.2 ラミブジン
ラミブジンを含む抗HIV薬で治療を受けたHIV-1感染症患者で発現するラミブジン耐性HIV-1には、HIV逆転写酵素の活性部位に近い184番目のアミノ酸のメチオニンからバリンへの変異(M184V)がみられる43)。このM184V変異の結果、ウイルスのラミブジンに対する感受性は著明に低下し43)44)、in vitroでのウイルスの複製能力は低下する45)。
In vitroにおいて、ジドブジン耐性臨床分離株にラミブジン耐性変異を導入すると、ジドブジンに対する感受性は回復することが確認されている。また、抗HIV薬の治療経験のない患者にジドブジン及びラミブジンを併用することにより、ジドブジン耐性ウイルスの出現が遅延する46)。さらに、抗HIV薬(ラミブジンを含む)の多剤併用療法はM184V変異ウイルスを有する患者と同様、抗HIV薬の治療経験のない患者においても有効性が確認されている47)48)。[7.1、7.5参照]
In vitroにおいて、ジドブジン耐性臨床分離株にラミブジン耐性変異を導入すると、ジドブジンに対する感受性は回復することが確認されている。また、抗HIV薬の治療経験のない患者にジドブジン及びラミブジンを併用することにより、ジドブジン耐性ウイルスの出現が遅延する46)。さらに、抗HIV薬(ラミブジンを含む)の多剤併用療法はM184V変異ウイルスを有する患者と同様、抗HIV薬の治療経験のない患者においても有効性が確認されている47)48)。[7.1、7.5参照]
18.4 交差耐性
19. 有効成分に関する理化学的知見
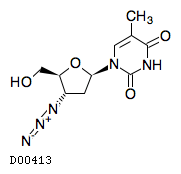
19.1. ジドブジン
| 一般的名称 | ジドブジン |
|---|---|
| 一般的名称(欧名) | Zidovudine |
| 化学名 | 3'-Azido-3'-deoxythymidine |
| 分子式 | C10H13N5O4 |
| 分子量 | 267.24 |
| 融点 | 約124℃ |
| 物理化学的性状 | 白色〜微黄白色の粉末。 エタノール(99.5)にやや溶けやすく、水にやや溶けにくい。 光によって分解する。 |
| KEGG DRUG |
|
19.2. ラミブジン
22. 包装
100錠[10錠(PTP)×10]
23. 主要文献
- DHHS:Guidelines for Using Antiretroviral Agents Among HIV-Infected Adults and Adolescents., (http://www.aidsinfo.nih.gov/Guidelines/)
- 抗HIV治療ガイドライン, (http://www.haart-support.jp/)
- HIV感染症「治療の手引き」, (http://www.hivjp.org/)
- O'Sullivan MJ,et al., Am J Obstet Gynecol., 168, 1510-1516, (1993) »PubMed »DOI
- Olivero OA,et al., AIDS., 13, 919-925, (1999) »PubMed »DOI
- Gerschenson M,et al., AIDS Res Hum Retroviruses., 16, 635-644, (2000) »PubMed »DOI
- Mirochnick M,et al., Antimicrob Agents Chemother., 53 (3), 1170-1176, (2009) »PubMed »DOI
- Moodley J,et al., J Infect Dis., 178, 1327-1333, (1998) »PubMed »DOI
- Sahai J,et al., J Infect Dis., 169, 1103-1107, (1994) »PubMed »DOI
- Norvir PDR 52版, (1998)
- Burger DM,et al., Antimicrob Agents Chemother., 37, 1426-1431, (1993) »PubMed »DOI
- Burger DM,et al., Pharm Weekbl., 126, 454-461, (1991)
- Ayers KM,et al., Fundam Appl Toxicol., 32, 148-158, (1996) »PubMed »DOI
- Diwan BA,et al., Toxicol Appl Pharmacol., 161, 82-99, (1999) »PubMed »DOI
- Ayers KM,et al., Fundam Appl Toxicol., 38, 195-198, (1997) »PubMed »DOI
- Shafik HM,et al., Antiviral Res., 16, 205-212, (1991) »PubMed »DOI
- 木村 哲ほか, 化学療法の領域, 14, 1419-1432, (1998)
- Horton CM,et al., Clin Pharmacol Ther., 55, 198, (1994)
- Pluda JM,et al., J Infect Dis., 171, 1438-1447, (1995) »PubMed »DOI
- van Leeuwen R,et al., AIDS., 6, 1471-1475, (1992) »PubMed »DOI
- Retrovir PDR 52版, (1998)
- Luzier A,et al., Antiviral Res., 21, 267-280, (1993) »PubMed »DOI
- van Leeuwen R,et al., J Infect Dis., 171, 1166-1171, (1995) »PubMed »DOI
- Acosta EP,et al., Clin Pharmacokinet., 30, 251-262, (1996) »PubMed »DOI
- Johnson MA,et al., Clin Pharmacokinet., 36, 41-66, (1999) »PubMed
- Heald AE,et al., Antimicrob Agents Chemother., 40, 1514-1519, (1996) »PubMed »DOI
- Sim SM,et al., Br J Clin Pharmacol., 32, 17-21, (1991) »PubMed »DOI
- Staszewski S,et al., AIDS., 11, 477-483, (1997) »PubMed »DOI
- CAESAR Coordinating Committee, Lancet., 349, 1413-1421, (1997)
- Furman PA,et al., Proc Natl Acad Sci USA., 83, 8333-8337, (1986) »PubMed »DOI
- Cammack N,et al., Biochem Pharmacol., 43, 2059-2064, (1992) »PubMed »DOI
- Hart GJ,et al., Antimicrob Agents Chemother., 36, 1688-1694, (1992) »PubMed »DOI
- Coates JAV,et al., Antimicrob Agents Chemother., 36, 733-739, (1992)
- Mitsuya H,et al., Proc Natl Acad Sci USA., 82, 7096-7100, (1985) »PubMed »DOI
- Ruprecht RM,et al., Nature., 323, 467-469, (1986) »PubMed »DOI
- Merrill DP,et al., J Infect Dis., 173, 355-364, (1996) »PubMed »DOI
- Hooker DJ,et al., J Virol., 70, 8010-8018, (1996) »PubMed »DOI
- Kellam P,et al., J Gen Virol., 75, 341-351, (1994) »PubMed »DOI
- Schinazi RF,et al., Int Antiviral News., 8, 65-91, (2000)
- Iversen AKN.et al., J Virol., 70, 1086-1090, (1996)
- Winters MA.et al., J Clin Invest., 102, 1769-1775, (1998) »PubMed »DOI
- De Antoni A,et al., J Infect Dis., 176, 899-903, (1997) »PubMed »DOI
- Schuurman R,et al., J Infect Dis., 171, 1411-1419, (1995) »PubMed »DOI
- Tisdale M,et al., Proc Natl Acad Sci USA., 90, 5653-5656 , (1993) »PubMed »DOI
- Back NKT,et al., EMBO J., 15, 4040-4049, (1996)
- Larder BA,et al., Science., 269, 696-699, (1995) »PubMed »DOI
- Maguire M.et al., AIDS., 14, 1195-1201, (2000) »PubMed »DOI
- Kuritzkes DR,et al., AIDS., 10, 975-981, (1996) »PubMed »DOI
- Tisdale M,et al., Antimicrob Agents Chemother., 41, 1094-1098, (1997) »PubMed »DOI
- Miller V,et al., AIDS., 12, 705-712, (1998) »PubMed »DOI
- Johnson MA,et al., Br J Clin Pharmacol., 46, 21-27, (1998) »PubMed
- 社内資料:海外臨床試験(204994)
24. 文献請求先及び問い合わせ先
文献請求先
グラクソ・スミスクライン株式会社
ヴィーブヘルスケア・カスタマー・サービス
東京都港区赤坂1-8-1
電話:0120-066-525 (9:00〜17:45/土日祝日及び当社休業日を除く)
製品情報問い合わせ先
グラクソ・スミスクライン株式会社
ヴィーブヘルスケア・カスタマー・サービス
東京都港区赤坂1-8-1
電話:0120-066-525 (9:00〜17:45/土日祝日及び当社休業日を除く)
26. 製造販売業者等
26.1 製造販売元
ヴィーブヘルスケア株式会社
東京都港区赤坂1-8-1
26.2 販売元
グラクソ・スミスクライン株式会社
東京都港区赤坂1-8-1