医薬品情報
| 総称名 | ウラリット |
|---|---|
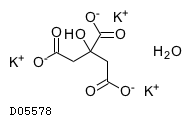
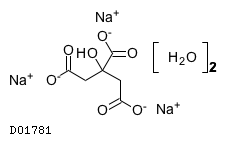
| 一般名 | クエン酸カリウム クエン酸ナトリウム水和物 |
| 欧文一般名 | Potassium Citrate Sodium Citrate Hydrate |
| 製剤名 | クエン酸カリウム・クエン酸ナトリウム水和物配合製剤 |
| 薬効分類名 | アルカリ化療法剤−酸性尿・アシドーシス改善− |
| 薬効分類番号 | 3949 |
| KEGG DRUG |
D05624
クエン酸カリウム・クエン酸ナトリウム水和物
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年12月 改訂(第2版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ウラリット−U配合散 | Uralyt-U Combination Powder | 日本ケミファ | 3949101A1149 | 9.9円/g | 処方箋医薬品注) |
| ウラリット配合錠 | Uralyt Combination Tablets | 日本ケミファ | 3949101F1073 | 6.3円/錠 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 ヘキサミンを投与中の患者[10.1参照]
4. 効能または効果
○痛風並びに高尿酸血症における酸性尿の改善
○アシドーシスの改善
6. 用法及び用量
ウラリット−U配合散
| 効能又は効果 | 用法及び用量 |
| ウラリット−U配合散 | |
| 痛風並びに高尿酸血症における酸性尿の改善 | 通常成人1回1gを1日3回経口投与するが、尿検査でpH6.2から6.8の範囲に入るよう投与量を調整する。 |
| アシドーシスの改善 | 原則として成人1日量6gを3〜4回に分けて経口投与するが、年齢、体重、血液ガス分析結果などから患者の状況に応じ適宜増減する。 |
ウラリット配合錠
| 効能又は効果 | 用法及び用量 |
| ウラリット配合錠 | |
| 痛風並びに高尿酸血症における酸性尿の改善 | 通常成人1回2錠を1日3回経口投与するが、尿検査でpH6.2から6.8の範囲に入るよう投与量を調整する。 |
| アシドーシスの改善 | 原則として成人1日量12錠を3〜4回に分けて経口投与するが、年齢、体重、血液ガス分析結果などから患者の状況に応じ適宜増減する。 |
8. 重要な基本的注意
8.1 本剤の投与に際しては、患者の血清電解質の変化に注意すること。特に、腎機能障害のある患者に投与する場合や、長期間投与する場合には、血中のカリウム値、腎機能等を定期的に検査すること。[9.2、11.1.1参照]
8.2 リン酸カルシウムは、アルカリ側で不溶性となることが知られているので、結石防止のため過度の尿アルカリ化は避けるべきである。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 尿路感染症の患者
感染を助長するおそれがある。
9.2 腎機能障害患者
9.3 肝機能障害患者
肝疾患・肝機能障害の症状を悪化させるおそれがある。
9.8 高齢者
減量するなど注意すること。生理機能が低下していることが多く、副作用があらわれやすい。
10. 相互作用
10.1 併用禁忌
| ヘキサミン (ヘキサミン静注液) [2.1参照] | ヘキサミンの効果を減弱することがあるので併用は避けること。 | ヘキサミンは酸性尿下で効果を発現するので、尿pHの上昇により効果が減弱することがある。 |
10.2 併用注意
| 水酸化アルミニウムゲル | 他のクエン酸製剤との併用でアルミニウムの吸収が促進されたとの報告があるので、併用する場合には2時間以上投与間隔を置くこと。 | クエン酸がアルミニウムとキレート化合物を形成し、アルミニウムの吸収を促進させるとの報告がある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 高カリウム血症(0.54%)
11.2 その他の副作用
| 0.1%〜2%未満 | 頻度不明 | |
| 肝臓 | AST上昇、ALT上昇、Al-P上昇、γ-GTP上昇 | LDH上昇 |
| 腎臓 | 血中クレアチニン上昇、BUN上昇 | |
| 消化器 | 胃不快感、下痢、悪心、胸やけ、嘔吐、食欲不振 | 嘔気、口内炎、腹部膨満感、胃痛、舌炎 |
| 皮膚 | 発疹 | そう痒感 |
| 泌尿器 | 排尿障害注) | |
| その他 | 頻脈、残尿感、眠気 | 貧血、全身倦怠感 |
14. 適用上の注意
14.1 薬剤交付時の注意
<散剤>
14.1.1 服用しにくい場合は、水などに溶かして服用すること。本剤は、塩味が強く服用しにくいことがある。また、痛風・高尿酸血症の患者においては、尿量の増加をはかることが望ましいとされている。
<錠剤>
14.1.2 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
本剤の体内薬物動態は、本剤の成分及び代謝産物がすべて生体常在物質であることをふまえて解析された。
16.1.1 単回投与
16.1.2 反復投与
健常成人5名にウラリット−U配合散1日3g(分3)、4g(分4)、9g(分3)を5日間連続経口投与した時、血中クエン酸濃度は用量依存的に増加したが、血中ナトリウム、カリウム、重炭酸濃度に大きな変動はなかった3)。
16.3 分布
ラットに[1,5-14C]クエン酸を含有するウラリット−U配合散を250mg/kg単回経口投与したところ、放射能は速やかに血中に出現し、全身に分布した4)。
16.4 代謝
本剤の成分であるクエン酸塩は生体常在物質であり、細胞内に存在するTCA回路などで通常の代謝を受け、代謝産物として重炭酸塩を産生すると考えられる。
16.5 排泄
17. 臨床成績
17.1 有効性及び安全性に関する試験
<酸性尿の改善効果>
17.1.1 国内臨床試験
比較試験を含む臨床試験において痛風、高尿酸血症等の患者411例を対象にウラリット−U配合散を通常1日3gあるいはウラリット配合錠を通常1日6錠経口投与した結果、酸性尿の改善効果は有効率94.2%(387/411例)であった6)7)。
また、ウラリット−U配合散は炭酸水素ナトリウムを対照とした比較試験の結果、有用性が認められた7)。
また、ウラリット−U配合散は炭酸水素ナトリウムを対照とした比較試験の結果、有用性が認められた7)。
| 基礎疾患名 | 有効率(%) |
| 痛風 | 93.3(180/193) |
| 無症候性高尿酸血症 | 98.1(51/52) |
| 高尿酸血症を伴う高血圧症 | 91.2(31/34) |
| 高尿酸血症を伴う腎障害 | 87.5(21/24) |
| Lesch-Nyhan症候群 | 100.0(5/5) |
| 小児急性白血病 | 100.0(7/7) |
| 尿酸結石ほか | 95.8(92/96) |
<アシドーシスの改善効果>
17.1.2 国内臨床試験
比較試験を含む臨床試験において腎尿細管性アシドーシス等の代謝性アシドーシス患者126例を対象にウラリット−U配合散を原則として1日6gあるいはウラリット配合錠を原則として1日12錠経口投与した結果、アシドーシスの改善効果は有効率89.7%(113/126例)であった6)8)。
また、ウラリット−U配合散は炭酸水素ナトリウムを対照とした比較試験の結果、有用性が認められた8)。
また、ウラリット−U配合散は炭酸水素ナトリウムを対照とした比較試験の結果、有用性が認められた8)。
| 基礎疾患名 | 有効率(%) |
| ファンコニー症候群 | 90.5(19/21) |
| ロウ症候群 | 92.9(13/14) |
| 糖原病 | 100.0(12/12) |
| シスチン症 | 100.0(4/4) |
| 腎尿細管性アシドーシス | 88.6(39/44) |
| 高クロール血症性アシドーシス※ | 66.7(10/15) |
| その他のアシドーシス※※ | 100.0(16/16) |
18. 薬効薬理
18.1 作用機序
本剤の作用は、主として代謝産物の重炭酸塩(HCO3−)が、生体において塩基として作用することに基づくと考えられる。
18.2 酸性尿改善作用
18.3 アシドーシス改善作用
マレイン酸誘発アシドーシスラットにおいて、低下した血液pH、重炭酸濃度、base excessを用量依存的に増加させた9)。
19. 有効成分に関する理化学的知見
19.1. クエン酸カリウム
19.2. クエン酸ナトリウム水和物
20. 取扱い上の注意
<錠剤>
20.1 開封後は湿気を避けて保存すること。
22. 包装
<ウラリットU−配合散>
1g×90包
1g×300包
500g[ポリエチレン瓶、バラ、乾燥剤入り]
<ウラリット配合錠>
100錠[10錠(PTP)×10]
500錠[10錠(PTP)×50]
1,000錠[10錠(PTP)×100]
23. 主要文献
- 小川由英、他, 薬理と治療, 14, 5251-5272, (1986)
- 日本ケミファ(株):生物学的同等性に関する資料(社内資料)
- 小川由英、他, 薬理と治療, 14, 5273-5293, (1986)
- 春木左千夫、他, 基礎と臨床, 20, 5308-5318, (1986)
- 春木左千夫、他, 基礎と臨床, 20, 5330-5338, (1986)
- 日本ケミファ(株):臨床試験に関する資料(社内資料)
- 上田 泰、他, 臨床評価, 9, 421-433, (1981)
- 北川照男、他, 小児科臨床, 39, 2257-2266, (1986)
- 服部新三郎、他, 腎と透析, 22, 335-340, (1987)
- 日本ケミファ(株):薬効薬理に関する資料(社内資料)
- 細谷龍男、他, 尿酸, 10, 75-79, (1986) »DOI
24. 文献請求先及び問い合わせ先
文献請求先
日本ケミファ株式会社
安全管理部
〒101−0032
東京都千代田区岩本町2丁目2-3
電話:0120-47-9321
03-3863-1225
03-3863-1225
FAX:03-3861-9567
製品情報問い合わせ先
日本ケミファ株式会社
安全管理部
〒101−0032
東京都千代田区岩本町2丁目2-3
電話:0120-47-9321
03-3863-1225
03-3863-1225
FAX:03-3861-9567
26. 製造販売業者等
26.1 製造販売元
日本ケミファ株式会社
東京都千代田区岩本町2丁目2-3
26.2 提携
マダウス社
ドイツ