医薬品情報
| 総称名 | セロクエル |
|---|---|
| 一般名 | クエチアピンフマル酸塩 |
| 欧文一般名 | Quetiapine Fumarate |
| 薬効分類名 | 抗精神病剤 |
| 薬効分類番号 | 1179 |
| ATCコード | N05AH04 |
| KEGG DRUG |
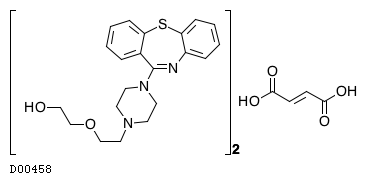
D00458
クエチアピンフマル酸塩
|
| KEGG DGROUP |
DG01482
ヒスタミンH1受容体拮抗薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年4月 改訂(第5版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| セロクエル25mg錠 | Seroquel 25mg Tablets | LTLファーマ | 1179042F1020 | 13.7円/錠 | 劇薬, 処方箋医薬品注) |
| セロクエル100mg錠 | Seroquel 100mg Tablets | LTLファーマ | 1179042F2026 | 26.2円/錠 | 劇薬, 処方箋医薬品注) |
| セロクエル200mg錠 | Seroquel 200mg Tablets | LTLファーマ | 1179042F3022 | 48.1円/錠 | 劇薬, 処方箋医薬品注) |
| セロクエル細粒50% | Seroquel Fine Granules 50% | LTLファーマ | 1179042C1023 | 185.4円/g | 劇薬, 処方箋医薬品注) |
1. 警告
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
6. 用法及び用量
通常、成人にはクエチアピンとして1回25mg、1日2又は3回より投与を開始し、患者の状態に応じて徐々に増量する。通常、1日投与量は150〜600mgとし、2又は3回に分けて経口投与する。
なお、投与量は年齢・症状により適宜増減する。ただし、1日量として750mgを超えないこと。
なお、投与量は年齢・症状により適宜増減する。ただし、1日量として750mgを超えないこと。
7. 用法及び用量に関連する注意
8. 重要な基本的注意
8.1 本剤の投与により、著しい血糖値の上昇から、糖尿病性ケトアシドーシス、糖尿病性昏睡等の致命的な経過をたどることがあるので、本剤投与中は、血糖値の測定や口渇、多飲、多尿、頻尿等の観察を十分に行うこと。特に、高血糖、肥満等の糖尿病の危険因子を有する患者では、血糖値が上昇し、代謝状態を急激に悪化させるおそれがある。[1.1、1.2、8.3、9.1.5、11.1.1参照]
8.2 本剤の投与により、低血糖があらわれることがあるので、本剤投与中は、脱力感、倦怠感、冷汗、振戦、傾眠、意識障害等の低血糖症状に注意するとともに、血糖値の測定等の観察を十分に行うこと。[8.3、11.1.2参照]
8.3 本剤の投与に際し、あらかじめ上記8.1及び8.2の副作用が発現する場合があることを、患者及びその家族に十分に説明し、高血糖症状(口渇、多飲、多尿、頻尿等)、低血糖症状(脱力感、倦怠感、冷汗、振戦、傾眠、意識障害等)に注意し、このような症状があらわれた場合には、直ちに投与を中断し、医師の診察を受けるよう、指導すること。[1.1、1.2、8.1、8.2、9.1.5、11.1.1、11.1.2参照]
8.4 本剤の投与により体重増加を来すことがあるので、肥満に注意し、肥満の徴候があらわれた場合は、食事療法、運動療法等の適切な処置を行うこと。
8.6 本剤は主として中枢神経系に作用するため、眠気、注意力・集中力・反射運動能力等の低下が起こることがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械の操作に従事させないように注意すること。
8.7 前治療薬からの切り替えの際、精神症状が悪化する可能性があるので観察を十分行いながら前治療薬の用量を減らしつつ、本薬を徐々に増量することが望ましい。また、症状の悪化が認められた場合には、他の治療法に切り替えるなど適切な処置を行うこと。
8.8 投与量の急激な減少ないし投与の中止により、不眠、悪心、頭痛、下痢、嘔吐等の離脱症状があらわれることがある。投与を中止する場合には、徐々に減量するなど慎重に行うこと。
8.9 無顆粒球症、白血球減少があらわれることがあるので、血液検査を行うなど、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。[11.1.6参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 心・血管疾患、脳血管障害、低血圧又はそれらの疑いのある患者
9.1.2 てんかん等の痙攣性疾患、又はこれらの既往歴のある患者
痙攣閾値を低下させるおそれがある。
9.1.3 不整脈又はその既往歴のある患者、先天性QT延長症候群の患者
QT間隔が延長する可能性がある。[10.2参照]
9.1.4 自殺企図の既往及び自殺念慮を有する患者
症状を悪化させるおそれがある。
9.1.6 不動状態、長期臥床、肥満、脱水状態等の危険因子を有する患者
肺塞栓症、静脈血栓症等の血栓塞栓症が報告されている。[11.1.10参照]
9.3 肝機能障害患者
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。動物実験(ラット及びウサギ)で胎児への移行が報告されている。また、妊娠後期に抗精神病薬が投与されている場合、新生児に哺乳障害、傾眠、呼吸障害、振戦、筋緊張低下、易刺激性等の離脱症状や錐体外路症状があらわれたとの報告がある。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒトで母乳中へ移行することが報告されている。
9.7 小児等
小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
9.8 高齢者
10. 相互作用
相互作用序文
本剤の代謝に関与する主なP450酵素はCYP3A4である。[16.4.1参照]
薬物代謝酵素用語
CYP3A4
10.1 併用禁忌
10.2 併用注意
| 中枢神経抑制剤 アルコール | 中枢神経抑制作用が増強することがあるので、個々の患者の症状及び忍容性に注意し、慎重に投与すること。 | 薬力学的相互作用を起こすことがある。 |
| CYP3A4誘導作用を有する薬剤注) フェニトイン カルバマゼピン バルビツール酸誘導体 リファンピシン 等 [16.7.1参照] | 本剤の作用が減弱することがある。 | 本剤の主要代謝酵素であるCYP3A4の誘導により、本剤のクリアランスが増加することがある。 |
| 強いCYP3A4阻害作用を有する薬剤 イトラコナゾール 等 [16.7.2参照] | 本剤の作用を増強するおそれがあるので、個々の患者の症状及び忍容性に注意し、本剤を減量するなどして慎重に投与すること。 併用により本剤の血漿中濃度が高値となり、QT間隔が延長するおそれがある。 | 本剤の主要代謝酵素であるCYP3A4を強く阻害するため、血漿中濃度が上昇する可能性がある。 |
| CYP3A4阻害作用を有する薬剤 エリスロマイシン 等 | 本剤の作用を増強するおそれがあるので、個々の患者の症状及び忍容性に注意し、慎重に投与すること。 | 本剤の主要代謝酵素であるCYP3A4を阻害するため、血漿中濃度が上昇する可能性がある。 |
| QT延長を起こすことが知られている薬剤 [9.1.3参照] | QT延長があらわれるおそれがある。 | 併用によりQT延長作用が相加的に増加するおそれがある。 |
| アドレナリン含有歯科麻酔剤 リドカイン・アドレナリン | 重篤な血圧降下を起こすことがある。 | アドレナリンはアドレナリン作動性α、β-受容体の刺激剤であり、本剤のα-受容体遮断作用により、β-受容体の刺激作用が優位となり、血圧降下作用が増強されるおそれがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 高血糖、糖尿病性ケトアシドーシス、糖尿病性昏睡(いずれも頻度不明)
11.1.2 低血糖(頻度不明)
11.1.3 悪性症候群(Syndrome malin)(0.2%)
無動緘黙、強度の筋強剛、嚥下困難、頻脈、血圧の変動、発汗等が発現し、それにひきつづき発熱がみられる場合は、投与を中止し、体冷却、水分補給等の全身管理とともに適切な処置を行うこと。本症発症時には、白血球の増加やCKの上昇がみられることが多く、また、ミオグロビン尿を伴う腎機能低下がみられることがある。
なお、高熱が持続し、意識障害、呼吸困難、循環虚脱、脱水症状、急性腎障害へと移行し、死亡した例が報告されている。
なお、高熱が持続し、意識障害、呼吸困難、循環虚脱、脱水症状、急性腎障害へと移行し、死亡した例が報告されている。
11.1.4 横紋筋融解症(頻度不明)
筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇等が認められた場合には投与を中止し、適切な処置を行うこと。また、横紋筋融解症による急性腎障害の発症に注意すること。
11.1.5 痙攣(頻度不明)
11.1.6 無顆粒球症、白血球減少(いずれも頻度不明)[8.9参照]
11.1.7 肝機能障害、黄疸(いずれも頻度不明)
AST、ALT、γ-GTP、Al-Pの上昇等を伴う肝機能障害、黄疸があらわれることがある。
11.1.8 麻痺性イレウス(頻度不明)
腸管麻痺(食欲不振、悪心・嘔吐、著しい便秘、腹部の膨満あるいは弛緩及び腸内容物のうっ滞等の症状)を来し、麻痺性イレウスに移行することがあるので、腸管麻痺があらわれた場合には、投与を中止するなど適切な処置を行うこと。
11.1.9 遅発性ジスキネジア(0.9%)
口周部等の不随意運動があらわれ、投与中止後も持続することがある。
11.1.10 肺塞栓症、深部静脈血栓症(いずれも頻度不明)
肺塞栓症、静脈血栓症等の血栓塞栓症が報告されているので、息切れ、胸痛、四肢の疼痛、浮腫等が認められた場合には、投与を中止するなど適切な処置を行うこと。[9.1.6参照]
11.1.11 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、多形紅斑(いずれも頻度不明)
11.2 その他の副作用
| 5%以上 | 1〜5%未満 | 1%未満 | 頻度不明 | |
| 精神神経系 | 不眠(19.3%)、易刺激性、傾眠(14.2%)、不安、頭痛、めまい | 幻覚の顕在化、健忘、攻撃的反応、昏迷、神経症、妄想の顕在化、リビドー亢進、感情不安定、激越、錯乱、思考異常、自殺企図、人格障害、躁病反応、多幸症、舞踏病様アテトーシス、片頭痛、悪夢、うつ病、独語、衝動行為、自動症 | 統合失調性反応、協調不能、レストレスレッグス症候群、軽躁、注意力障害、過眠症、自殺念慮、自傷行動、焦躁感、鎮静、意識レベルの低下、せん妄、敵意 | |
| 錐体外路症状 | アカシジア、振戦、構音障害 | 筋強剛、流涎過多、運動緩慢、歩行障害、ジスキネジア、嚥下障害 | ジストニア、眼球回転発作 | 構語障害、錐体外路障害、パーキンソン症候群 |
| 血液 | 顆粒球減少 | 白血球数増加、好酸球増加症、貧血、血小板減少 | ||
| 循環器系 | 頻脈 | 起立性低血圧、心悸亢進、心電図異常 | 低血圧、高血圧、徐脈、不整脈、失神 | 血管拡張、動悸、心電図QT延長 |
| 肝臓 | AST上昇、ALT上昇、LDH上昇 | Al-P上昇、γ-GTP上昇 | ビリルビン血症 | 肝機能検査異常 |
| 呼吸器系 | 去痰困難、鼻炎 | 咳増加、鼻閉 | ||
| 消化器系 | 便秘、食欲減退 | 悪心 | 食欲亢進、嘔吐、腹痛、下痢、消化不良 | 鼓腸放屁、消化管障害、吐血、直腸障害、過食、腹部膨満、胃食道逆流性疾患、膵炎、胃炎、胃不快感 |
| 眼 | 瞳孔反射障害 | 弱視、結膜炎 | ||
| 代謝・内分泌 | 高プロラクチン血症、T4減少 | 高コレステロール血症 | 月経異常、甲状腺疾患、高脂血症、高カリウム血症、肥満症 | T3減少、痛風、低ナトリウム血症、水中毒、多飲症、TSH減少、TSH上昇、高トリグリセリド血症、高尿酸血症、尿糖陽性、FT4減少、乳汁漏出症 |
| 過敏症 | 発疹 | 血管浮腫、そう痒、湿疹 | ||
| 泌尿器系 | 排尿障害、排尿困難、尿失禁、尿閉、BUN上昇 | 持続勃起、射精異常、インポテンス、頻尿、膀胱炎、尿蛋白陽性 | ||
| その他 | 倦怠感、無力症、CK上昇 | 口内乾燥、体重増加 | 多汗、発熱、体重減少、胸痛、筋肉痛、舌麻痺、しびれ感、背部痛、浮腫、ほてり、歯痛 | 顔面浮腫、頸部硬直、腫瘤、過量投与、骨盤痛、歯牙障害、関節症、滑液包炎、筋無力症、痙縮、悪化反応、偶発外傷、耳の障害、味覚倒錯、ざ瘡、脱毛症、薬剤離脱症候群(不眠、悪心、頭痛、下痢、嘔吐)、口渇、回転性めまい、悪寒、靭帯捻挫、意欲低下、末梢性浮腫、関節痛 |
13. 過量投与
13.1 症状
主な症状は傾眠、鎮静、頻脈、低血圧等である。まれに昏睡、死亡に至る症例が報告されている。
13.2 処置
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 本剤による治療中、原因不明の突然死が報告されている。
15.1.2 国内臨床試験において、本剤と因果関係が不明の心筋梗塞、出血性胃潰瘍が報告されている。また、申請時に用いた外国長期投与試験において、急性腎障害が報告されている。
15.1.3 外国で実施された高齢認知症患者を対象とした17の臨床試験において、本剤を含む非定型抗精神病薬投与群はプラセボ投与群と比較して死亡率が1.6〜1.7倍高かったとの報告がある。また、外国での疫学調査において、定型抗精神病薬も非定型抗精神病薬と同様に死亡率の上昇に関与するとの報告がある。
15.2 非臨床試験に基づく情報
15.2.1 イヌで長期大量(100mg/kg/日を6及び12カ月間)経口投与により、コレステロール合成阻害によると考えられる三角状後白内障が認められた。しかし、カニクイザル(最大225mg/kg/日を56週間)及びげっ歯類に投与しても白内障は認められなかった。また、臨床試験においても、本剤と関連した角膜混濁は認められなかった。
15.2.2 ラットに24カ月間経口投与したがん原性試験において、20mg/kg/日以上の雌の投与群で乳腺腫瘍の発現頻度の上昇が報告されている。これらの腫瘍の所見は、げっ歯類においてプロラクチンと関連した所見として報告されているが1)、ヒトではプロラクチン濃度の上昇と腫瘍形成の関連性は明確にされていない。
16. 薬物動態
16.1 血中濃度
16.1.1 反復投与(錠剤投与時)
(1)統合失調症患者にクエチアピンを1回用量25〜100mgの範囲で漸増して1日2回反復経口投与した。100mgの用量で7回反復投与した後の血漿中クエチアピン濃度推移及び薬物動態パラメータは図1及び表1のとおりである2)。
非高齢者では、投与約2.6時間後に最高血漿中濃度(平均397ng/mL)に達した。血漿中からのクエチアピンの消失は速やかであり、半減期は3.5時間であった。[16.6.2参照]
非高齢者では、投与約2.6時間後に最高血漿中濃度(平均397ng/mL)に達した。血漿中からのクエチアピンの消失は速やかであり、半減期は3.5時間であった。[16.6.2参照]
図1 統合失調症患者にクエチアピン100mgを1日2回反復投与時の血漿中クエチアピン濃度推移
(平均値±標準誤差、非高齢者:n=12、高齢者:n=11)
| 群 | n | Cmax(ng/mL) | Tmax(h) | AUC0-12h(μg・h/mL) | t1/2(h) | CL/F(L/h) |
| 非高齢者 | 12 | 397±57 | 2.6±0.7 | 1.69±0.19 | 3.5±0.2 | 67.1±7.1 |
| 高齢者 | 11 | 483±96 | 2.9±0.3 | 2.59±0.54 | 3.6±0.3 | 50.9±6.7 |
(2)外国人統合失調症患者にクエチアピンを1回用量25〜250mgの範囲で漸増して1日3回反復経口投与した。1回用量を75mg、150mg及び250mgとしたときの定常状態における薬物動態パラメータは表2のとおりである。血漿中クエチアピン濃度は用量に比例して増加し、男女差は認められなかった。
| 用量 | 性 | Cmax(ng/mL) | Tmax(h)a) | AUC0-8h(μg・h/mL) | t1/2(h) | CL/F(L/h) |
| 75mg tid | 男 | 277±54 | 1.0(0.5-3.0) | 1.07±0.19 | 2.7±0.1b) | 89±12 |
| 女 | 294±41 | 1.0(0.5-3.0) | 1.20±0.17 | 3.4±0.3b) | 86±16 | |
| 150mg tid | 男 | 625±121 | 1.0(0.5-4.0) | 2.30±0.33 | 3.0±0.3b) | 78±10 |
| 女 | 572±63 | 1.5(0.5-4.0) | 2.41±0.34 | 4.4±0.8b) | 73±8 | |
| 250mg tid | 男 | 778±108 | 1.5(0.5-4.0) | 3.38±0.46 | 5.8±0.3c) | 87±10 |
| 女 | 879±72 | 1.5(1.0-3.0) | 4.08±0.53 | 6.6±0.8c) | 72±9 |
16.1.2 単回投与(細粒投与時)
健康成人男子にクエチアピン25mgを単回経口投与したときの薬物動態パラメータは表3のとおりである3)。
| Cmax(ng/mL) | Tmax(h) | AUC0-24h(ng・h/mL) | t1/2(h) |
| 65.29±31.43 | 0.72±0.19 | 172.0±77.1 | 2.88±0.59 |
16.2 吸収
クエチアピンの経口吸収性は良好であり、クエチアピンのCmax及びAUCに及ぼす食事の影響は認められなかった。(錠剤投与時のデータ)
16.3 分布
ヒト血漿中におけるクエチアピンの蛋白結合率は83.0%であった4)(in vitro)。
16.4 代謝
16.4.2 ヒト血漿中の主要代謝物は有意な薬理活性を示さなかった5)。
16.4.3 In vitro試験において、未変化体及び代謝物はCYP1A2、CYP2C9、CYP2C19、CYP2D6及びCYP3A4活性に対して弱い阻害作用を示したが、ヒトでの血漿中濃度の約10倍以上の濃度でみられる作用であり、薬物相互作用の惹起を示唆するものではないと考えられた5)。
16.5 排泄
16.5.1 健康成人男子にクエチアピン20mgを単回経口投与したところ、尿中への未変化体の排泄率は投与量の1%未満であった6)。(錠剤投与時のデータ)
16.5.2 外国人統合失調症患者に14C標識クエチアピンを経口投与したところ、尿及び糞中への放射能排泄率はそれぞれ投与量の72.8%及び20.2%であった。また、尿糞中放射能に占める未変化体の割合は1%未満であった7)。(錠剤投与時のデータ)
16.6 特定の背景を有する患者
16.6.1 肝機能障害患者
肝機能障害患者(アルコール性肝硬変)にクエチアピン25mgを単回経口投与したところ、クエチアピンのCmax及びAUCinfは健康成人よりも高く(約1.5倍)、t1/2は健康成人よりも長かった(約1.8倍)8)(外国人データ)。(錠剤投与時のデータ)[7.1、9.3参照]
| 被験者 | Cmax(ng/mL) | Tmax(h)a) | AUCinf(μg・h/mL) | t1/2(h) | CL/F(L/h) |
| 肝機能障害患者 | 78.5±14.4 | 1.0(0.5-1.5) | 0.386±0.077 | 5.5±1.0 | 79.4±10.7 |
| 健康成人 | 53.0±3.5 | 1.25(0.6-3.0) | 0.248±0.020 | 3.1±0.2 | 105±8 |
16.6.2 高齢者
16.7 薬物相互作用
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相二重盲検比較試験(ハロペリドール)
統合失調症患者197例を対象としてクエチアピンの有効性及び安全性についてハロペリドールを対照に多施設二重盲検比較試験を行った。投与期間は8週とした。その結果、最終全般改善度を指標とした改善率はクエチアピン群38.1%(37/97例)、ハロペリドール群25.8%(24/93例)であり、同等性(非劣性)が検証された。副作用の発現率はクエチアピン群67.0%(67/100例)、ハロペリドール群82.5%(80/97例)であり、本剤投与群で有意に低かった(p=0.014)。本剤投与群における主な副作用は、不眠症21例(21.0%)、傾眠19例(19.0%)、倦怠感15例(15.0%)、神経過敏症14例(14.0%)、振戦12例(12.0%)、不安10例(10.0%)、無力症10例(10.0%)であった10)。
17.1.2 国内第III相二重盲検比較試験(モサプラミン)
統合失調症患者181例を対象としてクエチアピンの有効性及び安全性についてモサプラミンを対照に多施設二重盲検比較試験を行った。投与期間は8週とした。その結果、最終全般改善度を指標とした改善率はクエチアピン群37.2%(32/86例)、モサプラミン群28.8%(23/80例)であり、同等性(非劣性)が検証された。副作用の発現率はクエチアピン群61.1%(55/90例)、モサプラミン群81.1%(73/90例)であり、本剤投与群で有意に低かった(p=0.004)。本剤投与群における主な副作用は、神経過敏症22例(24.4%)、不眠症19例(21.1%)、不安17例(18.9%)、めまい11例(12.2%)、振戦10例(11.1%)、倦怠感10例(11.1%)、無力症10例(11.1%)、アカシジア9例(10.0%)であった11)。
17.1.3 国内第III相一般臨床試験
他の抗精神病薬において寛解を示さなかった(治療抵抗性)統合失調症患者32例を対象とし、有効性及び安全性を検討することを目的とした多施設オープン試験を実施した。投与期間は8週とした。その結果、最終全般改善度を指標とした改善率は40.9%(9/22例)であった。副作用の発現率は46.9%(15/32例)であった。主な副作用は、不眠症8例(25.0%)、神経過敏症7例(21.9%)、不安5例(15.6%)、振戦3例(9.4%)であった12)。
18. 薬効薬理
18.1 作用機序
本薬の薬理学的特徴はドパミンD2受容体に比してセロトニン5-HT2A受容体に対する親和性が高いこと、及び種々の受容体に対して親和性があることであり、これらが臨床における作用に寄与しているものと考えられている13)。
18.2 受容体親和性
ラット脳組織を用いた試験で、ドパミンD1及びD2受容体、セロトニン5-HT1及び5-HT2受容体、ヒスタミンH1受容体、アドレナリンα1及びα2受容体に対して親和性を示したが、ムスカリン受容体及びベンゾジアゼピン受容体に対してはほとんど親和性を示さなかった。また、ドパミンD2受容体に比して、セロトニン5-HT2受容体に対する親和性は高かった13)(in vitro)。
18.3 ドパミン及びセロトニン受容体拮抗作用
18.4 錐体外路系に対する作用
18.4.1 ヒトでの作用
統合失調症患者を対象とした海外のプラセボ対照二重盲検比較試験において、錐体外路障害の発現頻度には、プラセボ投与群との間に有意な差を認めなかった。
18.4.2 動物での作用
サルにおけるジストニア惹起作用及びラットにおけるカタレプシー惹起作用は、ハロペリドールに比べて弱かった。ラットでの電気生理学的試験では辺縁系に対し選択的な作用を示し、錐体外路症状との関連が深いとされる黒質線条体系に対しては作用を示さなかった13)。
18.5 血漿中プロラクチンに対する作用
18.5.1 ヒトでの作用
統合失調症患者を対象とした海外のプラセボ対照二重盲検比較試験において、プロラクチン濃度には、プラセボ投与群との間に有意な差を認めなかった。
18.5.2 動物での作用
ラットにおいて、血漿中プロラクチン濃度推移はハロペリドールと異なり、持続的な上昇を示さなかった13)。
19. 有効成分に関する理化学的知見
19.1. クエチアピンフマル酸塩
22. 包装
<セロクエル25mg錠>
100錠[10錠(PTP)×10]
500錠[10錠(PTP)×50]
1,000錠[瓶、バラ]
<セロクエル100mg錠>
100錠[10錠(PTP)×10]
500錠[10錠(PTP)×50]
1,000錠[瓶、バラ]
<セロクエル200mg錠>
100錠[10錠(PTP)×10]
500錠[瓶、バラ]
<セロクエル細粒50%>
100g[瓶、乾燥剤セットキャップ]
23. 主要文献
- Vonderhaar,B.K., Pharmacol.Ther., 79 (2), 169-178, (1998) »PubMed »DOI
- 社内資料:統合失調症患者・第III相多施設共同オープン試験
- 社内報告書:健康成人・薬物動態
- 社内資料:ヒト血漿・蛋白結合
- 社内資料:ヒト肝ミクロソーム・代謝
- 村崎光邦 他, 臨床評価, 27 (1), 101-144, (1999)
- 社内資料:海外統合失調症患者・排泄
- 社内資料:海外肝障害患者・薬物動態
- 社内資料:薬物相互作用
- 村崎光邦 他, 臨床精神薬理, 4 (1), 127-155, (2001)
- 工藤義雄 他, 臨床医薬, 16 (12), 1807-1842, (2000)
- 前田久雄 他, 臨床精神薬理, 2 (6), 653-668, (1999)
- Goldstein,J.M., Schizophrenia,Breaking Down Barriers, 177-208, (1996), (Wiley)
- 社内資料:ラット・薬理作用
24. 文献請求先及び問い合わせ先
文献請求先
LTLファーマ株式会社
コールセンター
〒160-0023
東京都新宿区西新宿6丁目10番1号
電話:フリーダイヤル 0120-303-711
製品情報問い合わせ先
LTLファーマ株式会社
コールセンター
〒160-0023
東京都新宿区西新宿6丁目10番1号
電話:フリーダイヤル 0120-303-711
26. 製造販売業者等
26.1 製造販売
LTLファーマ株式会社
東京都新宿区西新宿6丁目10番1号