医薬品情報
| 総称名 | アクトス |
|---|---|
| 一般名 | ピオグリタゾン塩酸塩 |
| 欧文一般名 | Pioglitazone Hydrochloride |
| 製剤名 | ピオグリタゾン塩酸塩口腔内崩壊錠 |
| 薬効分類名 | インスリン抵抗性改善剤−2型糖尿病治療剤− |
| 薬効分類番号 | 3969 |
| ATCコード | A10BG03 |
| KEGG DRUG |
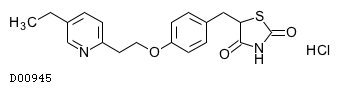
D00945
ピオグリタゾン塩酸塩
|
| KEGG DGROUP |
DG02044
血糖降下薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年3月 改訂(第4版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アクトスOD錠15 | ACTOS OD Tablets | T’s製薬 | 3969007F3027 | 16.3円/錠 | 処方箋医薬品注) |
| アクトスOD錠30 | ACTOS OD Tablets | T’s製薬 | 3969007F4023 | 29.9円/錠 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 心不全の患者及び心不全の既往歴のある患者[動物試験において循環血漿量の増加に伴う代償性の変化と考えられる心重量の増加がみられており、また、臨床的にも心不全を増悪あるいは発症したとの報告がある。][11.1.1、11.1.2参照]
2.2 重症ケトーシス、糖尿病性昏睡又は前昏睡、1型糖尿病の患者[輸液、インスリンによる速やかな高血糖の是正が必須となる。]
2.3 重篤な肝機能障害のある患者[9.3.1参照]
2.4 重篤な腎機能障害のある患者[9.2.1参照]
2.5 重症感染症、手術前後、重篤な外傷のある患者[インスリン注射による血糖管理が望まれるので本剤の投与は適さない。]
2.6 本剤の成分に対し過敏症の既往歴のある患者
2.7 妊婦又は妊娠している可能性のある女性[9.5参照]
4. 効能または効果
2型糖尿病
ただし、下記のいずれかの治療で十分な効果が得られずインスリン抵抗性が推定される場合に限る。
1.
[1]食事療法、運動療法のみ
[2]食事療法、運動療法に加えてスルホニルウレア剤を使用
[3]食事療法、運動療法に加えてα-グルコシダーゼ阻害剤を使用
[4]食事療法、運動療法に加えてビグアナイド系薬剤を使用
2.食事療法、運動療法に加えてインスリン製剤を使用
5. 効能または効果に関連する注意
本剤を使用する場合は、インスリン抵抗性が推定される患者に限定すること。インスリン抵抗性の目安は肥満度(Body Mass Index=BMI kg/m2)で24以上あるいはインスリン分泌状態が空腹時血中インスリン値で5μU/mL以上とする。
6. 用法及び用量
<食事療法、運動療法のみの場合及び食事療法、運動療法に加えてスルホニルウレア剤又はα-グルコシダーゼ阻害剤若しくはビグアナイド系薬剤を使用する場合>
通常、成人にはピオグリタゾンとして15〜30mgを1日1回朝食前又は朝食後に経口投与する。なお、性別、年齢、症状により適宜増減するが、45mgを上限とする。
<食事療法、運動療法に加えてインスリン製剤を使用する場合>
通常、成人にはピオグリタゾンとして15mgを1日1回朝食前又は朝食後に経口投与する。なお、性別、年齢、症状により適宜増減するが、30mgを上限とする。
7. 用法及び用量に関連する注意
7.3 インスリンとの併用時においては、浮腫が多く報告されていることから、1日1回15mgから投与を開始すること。本剤を増量する場合は浮腫及び心不全の症状・徴候を十分に観察しながら慎重に行うこと。ただし、1日量として30mgを超えないこと。[8.1、11.1.1、11.1.2参照]
7.4 高齢者では、1日1回15mgから投与を開始することが望ましい。[9.8参照]
8. 重要な基本的注意
8.1 循環血漿量の増加によると考えられる浮腫が短期間に発現し、また心不全が増悪あるいは発症することがあるので、服用中の浮腫、急激な体重増加、症状の変化に注意し、異常がみられた場合には直ちに本剤の服用を中止し、受診するよう患者を指導すること。[7.1-7.3、9.1.1、11.1.1、11.1.2参照]
8.2 心電図異常や心胸比増大があらわれることがあるので、定期的に心電図検査を行うなど十分に観察し、異常が認められた場合には投与を一時中止するかあるいは減量するなど慎重に投与すること。[11.2参照]
8.3 基礎に肝機能障害を有するなど必要な場合には定期的に肝機能検査を実施し、異常が認められた場合には投与を中止するなど適切な処置を行うこと。[11.1.3参照]
8.5 本剤を投与された患者で膀胱癌の発生リスクが増加する可能性が完全には否定できないので、以下の点に注意すること。[15.1、15.2.1参照]
・膀胱癌治療中の患者には投与を避けること。また、特に、膀胱癌の既往を有する患者には本剤の有効性及び危険性を十分に勘案した上で、投与の可否を慎重に判断すること。
・投与開始に先立ち、患者又はその家族に膀胱癌発症のリスクを十分に説明してから投与すること。また、投与中に血尿、頻尿、排尿痛等の症状が認められた場合には、直ちに受診するよう患者に指導すること。
・投与中は、定期的に尿検査等を実施し、異常が認められた場合には、適切な処置を行うこと。また、投与終了後も継続して、十分な観察を行うこと。
8.6 投与する場合には、血糖、尿糖を定期的に検査し、薬剤の効果を確かめ、3ヵ月間投与して効果が不十分な場合には、速やかに他の治療薬への切り替えを行うこと。
8.7 急激な血糖下降に伴い、糖尿病性網膜症が悪化する例があることが知られており、本剤においても報告例があるので留意すること。
8.8 低血糖症状を起こすことがあるので、高所作業、自動車の運転等に従事している患者に投与するときには注意すること。[11.1.4参照]
8.9 α-グルコシダーゼ阻害剤と本剤1日45mgの併用における安全性は確立していない(使用経験はほとんどない)。
8.10 α-グルコシダーゼ阻害剤、スルホニルウレア系薬剤及び本剤の3剤を併用投与する場合の安全性は確立していない。臨床試験成績より、副作用発現率が高くなる傾向が認められている。
8.11 ビグアナイド系薬剤と本剤1日45mgの併用における安全性は確立していない(使用経験はほとんどない)。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 心不全発症のおそれのある心筋梗塞、狭心症、心筋症、高血圧性心疾患等の心疾患のある患者
9.1.2 低血糖を起こすおそれのある以下の患者又は状態
9.2 腎機能障害患者
9.3 肝機能障害患者
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。ラット器官形成期投与試験では、40mg/kg以上の群で胚・胎児死亡率の高値、出生児の生存率の低値が、ウサギ器官形成期投与試験では、160mg/kg群で親動物の死亡又は流産がそれぞれ1例、胚・胎児死亡率の高値がみられている。[2.7参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中へ移行することが報告されている1)。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
副作用発現に留意し、経過を十分に観察しながら慎重に投与すること。一般に生理機能が低下している。[7.4参照]
10. 相互作用
相互作用序文
本剤は主として肝薬物代謝酵素CYP2C8で代謝され、他に複数の分子種が代謝に関与する。[16.4参照]
薬物代謝酵素用語
CYP2C8
10.2 併用注意
| 糖尿病用薬 スルホニルウレア系薬剤 ビグアナイド系薬剤 速効型インスリン分泌促進薬 α-グルコシダーゼ阻害剤 DPP-4阻害剤 GLP-1アナログ製剤 インスリン製剤 [11.1.4、16.7.1-16.7.3参照] | 低血糖を発現するおそれがあるので、低用量から投与を開始するなど慎重に投与すること。 | 併用時には、血糖降下作用の増強により、低血糖のリスクが増加するおそれがある。 |
| 糖尿病用薬及びその血糖降下作用を増強又は減弱する薬剤を併用している場合 糖尿病用薬の血糖降下作用を増強する薬剤 β-遮断剤 サリチル酸剤 モノアミン酸化酵素阻害剤 フィブラート系の高脂血症治療剤 ワルファリン等 糖尿病用薬の血糖降下作用を減弱する薬剤 アドレナリン 副腎皮質ホルモン 甲状腺ホルモン等 | 左記の併用に加え更に本剤を併用する場合には、糖尿病用薬の使用上の注意に記載の相互作用に留意するとともに、本剤のインスリン抵抗性改善作用が加わることによる影響に十分注意すること。 | 血糖降下作用の増強又は減弱による。 |
| リファンピシン等のCYP2C8を誘導する薬剤 | リファンピシンと併用するとピオグリタゾンのAUCが54%低下するとの報告があるので、リファンピシンと併用する場合は血糖管理状況を十分に観察し、必要な場合には本剤を増量すること。 | CYP2C8を誘導することにより、本剤の代謝が促進されると考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 心不全(頻度不明)
11.1.2 浮腫(8.2%)
11.1.3 肝機能障害、黄疸(頻度不明)
AST、ALT、Al-P等の著しい上昇を伴う肝機能障害、黄疸があらわれることがある。[8.3参照]
11.1.4 低血糖(0.1〜5%未満)
11.1.5 横紋筋融解症(頻度不明)
筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇を特徴とする横紋筋融解症があらわれることがある。
11.1.6 間質性肺炎(頻度不明)
発熱、咳嗽、呼吸困難、肺音の異常(捻髪音)等が認められた場合には、速やかに胸部X線、胸部CT、血清マーカー等の検査を実施し、異常が認められた場合には、投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.1.7 胃潰瘍の再燃(0.1%未満)
11.2 その他の副作用
| 5%以上 | 0.1〜5%未満 | 0.1%未満 | 頻度不明 | |
| 血液注1) | 貧血、白血球減少、血小板減少 | |||
| 循環器 | 血圧上昇、心胸比増大注2)、心電図異常注2)、動悸、胸部圧迫感、顔面潮紅 | |||
| 過敏症 | 発疹、湿疹、そう痒 | |||
| 消化器 | 悪心・嘔吐、胃部不快感、胸やけ、腹痛、腹部膨満感、下痢、便秘、食欲亢進、食欲不振 | |||
| 肝臓 | AST、ALT、Al-P、γ-GTPの上昇 | |||
| 精神神経系 | めまい、ふらつき、頭痛、眠気、倦怠感、脱力感、しびれ | |||
| その他 | LDH及びCKの上昇 | BUN及びカリウムの上昇、総蛋白及びカルシウムの低下、体重及び尿蛋白の増加、息切れ | 関節痛、ふるえ、急激な血糖下降に伴う糖尿病性網膜症の悪化 | 骨折注3)、糖尿病性黄斑浮腫の発症又は増悪注4) |
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
14.1.2 本剤は舌の上にのせて唾液を浸潤させると崩壊するため、水なしで服用可能である。また、水で服用することもできる。
15. その他の注意
15.1 臨床使用に基づく情報
15.2 非臨床試験に基づく情報
16. 薬物動態
16.1 血中濃度
16.1.1 生物学的同等性試験
健康成人男子(62例)にアクトスOD錠30を水なしで、あるいはアクトス錠30を水ありでクロスオーバー法にて、朝絶食下に単回投与した時、未変化体の血中濃度は次図のとおりであり、生物学的同等性が認められた。また、未変化体、活性代謝物(M-II〜IV)の薬物動態学的パラメータは下表のとおりである。なお、Wistar fattyラットで調べた血糖低下作用において、M-II〜IVの活性は未変化体より弱い。
| Cmax(ng/mL) | Tmax(h) | AUC0-72(ng・h/mL) | T1/2(h) | ||
| 未変化体 | アクトスOD錠 | 1,548.6±477.92 | 2.726±1.0852 | 16,842.9±6,540.00 | 6.727±2.3160 |
| アクトス錠 | 1,468.7±380.39 | 2.105±1.0368 | 15,536.7±4,889.06 | 6.788±2.3785 | |
| M-II | アクトスOD錠 | 40.5±13.73 | 8.279±2.9616 | 666.8±392.04 | 21.387±23.0671 |
| アクトス錠 | 38.5±11.52 | 7.475±3.2094 | 619.8±325.19 | 18.830±11.9439 | |
| M-III | アクトスOD錠 | 271.8±77.76 | 16.742±6.2958 | 11,809.6±3,372.04 | 26.199±5.2975 |
| アクトス錠 | 251.6±66.43 | 15.645±6.3918 | 11,122.3±3,002.30 | 26.939±6.6344 | |
| M-IV | アクトスOD錠 | 568.0±112.73 | 17.032±7.1677 | 25,103.8±5,060.23 | 25.683±6.0510 |
| アクトス錠 | 535.6±107.02 | 15.097±6.8202 | 23,676.3±4,341.39 | 25.426±5.5472 | |
16.1.2 反復投与
健康成人男子(6例)に1日1回ピオグリタゾンとして30mgを9日間(2日目は休薬)反復経口投与した時、未変化体及び活性化合物合計(未変化体+M-II〜IV)の血中濃度は6〜7日目でほぼ定常状態に達し、反復投与による蓄積性はないものと考えられる9)。
16.2 吸収
健康成人男子(8例)に空腹時又は食後にピオグリタゾンとして1回30mgを単回経口投与した時、食後投与において未変化体のTmaxの延長がみられた以外に未変化体の薬物速度論的パラメータに大きな差はなく、摂食による影響はほとんどないと考えられる9)。
16.4 代謝
ピオグリタゾンの代謝にはチトクロームP450 1A1、1A2、2C8、2C9、2C19、2D6、3A4の複数の分子種が関与している。また、ピオグリタゾンはヒトチトクロームP450分子種発現ミクロゾームの代謝活性に対して、チトクロームP450 1A1、1A2、2A6、2B6、2C8、2C9、2C19、2D6、2E1、3A4にほとんど影響を与えない(in vitro)。[10.参照]
16.5 排泄
健康成人男子(14例)に空腹時にピオグリタゾンとして1回30mgを単回経口投与した時、尿中には主としてM-IV〜VIが排泄され、投与後48時間までの累積尿中排泄率は約30%である10)。
16.7 薬物相互作用
16.7.1 スルホニルウレア剤
16.7.2 α-グルコシダーゼ阻害剤
16.7.3 ビグアナイド系薬剤
メトホルミン反復投与中の健康成人男子(14例)に対して、1日1回ピオグリタゾンとして30mgを経口投与した時、本剤の活性化合物合計(未変化体+M-II〜IV)の血中濃度は本剤単独投与時の健康成人男子(8例)での結果と近似している。[10.2参照]
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内後期第II相試験、第III相試験
2型糖尿病患者を対象に、1日1回ピオグリタゾンとして15mg、30mg又は45mgを投与した二重盲検比較試験を含む各種臨床試験において、総合血糖改善度が評価された821例の改善率(「中等度改善」以上)は50.8%(417/821例)である12)13)14)15)16)17)18)19)。
さらに、長期投与試験(28〜48週間以上投与)でも、空腹時血糖及びHbA1cの下降は持続し、作用の減弱はみられず、安定した血糖コントロールが得られている18)19)。
さらに、長期投与試験(28〜48週間以上投与)でも、空腹時血糖及びHbA1cの下降は持続し、作用の減弱はみられず、安定した血糖コントロールが得られている18)19)。
副作用発現頻度は13.2%(128/969例)で、主な副作用は浮腫・むくみ(79例)であった。
<食事療法、運動療法のみの2型糖尿病>
17.1.2 国内第III相試験
1日1回ピオグリタゾンとして30mgを12週間投与した結果、HbA1c(JDS値)は1.08±1.47%(63例の平均値±標準偏差)の下降が認められている。
副作用発現頻度は、16.9%(13/77例)で、主な副作用は浮腫・むくみ(9例)であった。
<食事療法、運動療法に加えてスルホニルウレア剤を使用中の2型糖尿病>
17.1.3 国内第III相試験
1日1回ピオグリタゾンとして30mgを12週間投与した結果、HbA1c(JDS値)は1.24±1.33%(56例の平均値±標準偏差)の下降が認められている。
副作用発現頻度は、10.5%(8/76例)で、主な副作用は浮腫・むくみ(3例)であった。
<食事療法、運動療法に加えてα-グルコシダーゼ阻害剤を使用中の2型糖尿病>
17.1.4 国内第III相試験
1日1回ピオグリタゾンとして30mgを16週間投与した結果、HbA1c(JDS値)は0.91±0.89%(55例の平均値±標準偏差)の下降が認められている。
臨床検査値の異常を含む副作用が67.2%(43/64例)に認められ、主な副作用は浮腫(6例)であった。
<食事療法、運動療法に加えてビグアナイド系薬剤を使用中の2型糖尿病>
17.1.5 国内第III相試験
1日1回ピオグリタゾンとして15mgを12週間、その後30mgを16週間投与した結果、HbA1c(JDS値)は0.67±0.80%(83例の平均値±標準偏差)の下降が認められている。
臨床検査値の異常を含む副作用が15.7%(13/83例)に認められ、主な副作用は浮腫(3例)、末梢性浮腫、上腹部痛及びBNP上昇(各2例)などであった。
<食事療法、運動療法に加えてインスリン製剤を使用中の2型糖尿病>
17.1.6 国内第III相試験
1日1回ピオグリタゾンとして30mgを16週間投与した結果、HbA1c(JDS値)は1.22±1.11%(45例の平均値±標準偏差)の下降が認められている。
臨床検査値の異常を含む副作用が66.7%(40/60例)に認められ、主な副作用は低血糖症(20例)、末梢性浮腫及び血中LDH増加(各11例)などであった。
18. 薬効薬理
18.1 作用機序
本剤はインスリン受容体のインスリン結合部以降に作用してインスリン抵抗性を軽減し、肝における糖産生を抑制し、末梢組織における糖利用を高め血糖を低下させる。この作用は、インスリン抵抗性の主因である細胞内インスリン情報伝達機構を正常化することによると推測される。
18.1.1 末梢組織におけるインスリン作用増強
Wistar fattyラットの後肢ヒラメ筋において、インスリンの作用(グリコーゲン合成及び解糖亢進作用)を増強する(ex vivo)。また、Wistar fattyラットの副睾丸周囲脂肪組織由来の単離脂肪細胞において、インスリンの作用(グルコース酸化及び総脂質合成亢進作用)を増強する20)(ex vivo)。
18.1.2 肝におけるインスリン作用増強
Wistar fattyラットにおいて、肝におけるグルコキナーゼの活性を亢進し、グルコース-6-ホスファターゼの活性を低下させ、糖産生を抑制する21)(in vivo)。
18.1.3 インスリン受容体作用増強
Wistar fattyラットの骨格筋において、低下したインスリン受容体及びインスリン受容体基質のリン酸化を正常化し、ホスファチジルイノシトール-3-キナーゼの活性を亢進する22)(in vivo)。
18.1.4 TNF-α産生抑制作用
Wistar fattyラットに認められる骨格筋TNF-α産生亢進を抑制し、これと並行して高血糖を軽減する23)(in vivo)。
18.2 糖代謝改善作用
18.2.1 食事療法、運動療法のみの2型糖尿病患者に1日1回ピオグリタゾンとして30mgを12週間投与した二重盲検比較試験において、空腹時血糖、HbA1cの下降、1,5-AGの上昇が認められている15)。
18.2.2 食事療法、運動療法に加えてスルホニルウレア剤を使用中の2型糖尿病患者に1日1回ピオグリタゾンとして30mgを12週間併用投与した二重盲検比較試験において、空腹時血糖、HbA1cの下降、1,5-AGの上昇、血中インスリンの下降が認められている16)。
18.2.3 食事療法、運動療法に加えてボグリボースを使用中の2型糖尿病患者に1日1回ピオグリタゾンとして30mgを16週間併用投与した二重盲検比較試験において、空腹時血糖、HbA1cの下降が認められている。
18.2.4 食事療法、運動療法に加えてメトホルミンを使用中の2型糖尿病患者に1日1回ピオグリタゾンとして15mgを12週間、その後30mgを16週間併用投与した二重盲検比較試験において、空腹時血糖、HbA1cの下降が認められている。
18.2.5 食事療法、運動療法に加えてインスリン製剤を使用中の2型糖尿病患者に1日1回ピオグリタゾンとして30mgを16週間併用投与した二重盲検比較試験において、空腹時血糖、HbA1cの下降が認められている。
18.3 耐糖能改善作用
18.4 インスリン抵抗性改善作用
18.4.1 食事療法、運動療法のみ又は食事療法、運動療法に加えてスルホニルウレア剤を使用中の2型糖尿病患者に1日1回ピオグリタゾンとして30mgを12週間投与した臨床薬理試験(グルコース・クランプ法)において、末梢組織及び肝の糖取り込み率の上昇が認められている25)26)。
18.4.2 インスリン抵抗性を有し、肥満型糖尿病であるWistar fattyラット及び肥満であるZucker fattyラットにピオグリタゾンを14日間投与し、20時間絶食後にインスリンを投与したところ、インスリン投与後の血糖低下の増強が認められている20)24)。
18.4.3 肥満型糖尿病であるKKAyマウスの横隔膜のグリコーゲン画分及び副睾丸周囲脂肪組織の総脂肪画分へのインスリン刺激時の糖取り込みを増加させる24)。
18.4.4 肥満型糖尿病であるWistar fattyラットの肝からの糖産生を抑制し、末梢組織における糖の利用を高める21)。
19. 有効成分に関する理化学的知見
19.1. ピオグリタゾン塩酸塩
20. 取扱い上の注意
開封後も湿気を避けて保存すること。本品は高防湿性の内袋により品質保持をはかっている。
22. 包装
<アクトスOD錠15>
100錠[10錠(PTP)×10、乾燥剤入り]、500錠[10錠(PTP)×50、乾燥剤入り]
<アクトスOD錠30>
100錠[10錠(PTP)×10、乾燥剤入り]
23. 主要文献
- 前芝良宏 他, 薬理と治療, 24, 2597-2617, (1996)
- NDBを用いた調査結果の概要(ピオグリタゾン塩酸塩による骨折発現のリスク評価), (https://www.pmda.go.jp/files/000279371.pdf)
- Lewis J.D.et al., JAMA., 314, 265-277, (2015)
- Korhonen P.et al., BMJ., 354, i3903, (2016)
- Azoulay L.et al., BMJ., 344, e3645, (2012)
- Hsiao F.Y.et al., Drug Safety., 36, 643-649, (2013)
- Saez E.et al., Nature Medicine., 4, 1058-1061, (1998)
- Lefebvre A.M.et al., Nature Medicine., 4, 1053-1057, (1998)
- 平賀興吾, 臨牀と研究, 74, 1184-1201, (1997)
- 東 純一 他, 臨牀と研究, 74, 1627-1637, (1997)
- 播 穣治 他, 臨牀と研究, 74, 1217-1226, (1997)
- 兼子俊男 他, 臨牀と研究, 74, 1540-1556, (1997)
- 兼子俊男 他, 臨牀と研究, 74, 1250-1277, (1997)
- 兼子俊男 他, 臨牀と研究, 74, 1278-1306, (1997)
- 兼子俊男 他, 臨牀と研究, 74, 1491-1514, (1997)
- 兼子俊男 他, 臨牀と研究, 74, 1515-1539, (1997)
- 高科成良 他, 臨牀と研究, 74, 1614-1626, (1997)
- 兼子俊男 他, 臨牀と研究, 74, 1557-1588, (1997)
- 兼子俊男 他, 臨牀と研究, 74, 1589-1613, (1997)
- Sugiyama Y.et al., Arzneimittelforschung., 40, 263-267, (1990)
- Sugiyama Y.et al., Arzneimittelforschung., 40, 436-440, (1990)
- Hayakawa T.et al., Biochem.Biophys.Res.Commun., 223, 439-444, (1996)
- Murase K.et al., Diabetologia., 41, 257-264, (1998)
- 池田 衡 他, 薬理と治療, 25, 337-343, (1997)
- Kawamori R.et al., Diabetes Research and Clinical Practice., 41, 35-43, (1998)
- Yamasaki Y.et al., Tohoku J.Exp.Med., 183, 173-183, (1997) »DOI
24. 文献請求先及び問い合わせ先
文献請求先
T's製薬株式会社
ティーズDIセンター
〒451-0045
名古屋市西区名駅二丁目27番8号
電話:0120-923-093 受付時間 9:00〜17:30(土日祝日・弊社休業日を除く)
製品情報問い合わせ先
T's製薬株式会社
ティーズDIセンター
〒451-0045
名古屋市西区名駅二丁目27番8号
電話:0120-923-093 受付時間 9:00〜17:30(土日祝日・弊社休業日を除く)
26. 製造販売業者等
26.1 製造販売元
T's製薬株式会社
大阪市中央区道修町四丁目1番1号
26.2 販売
武田薬品工業株式会社
大阪市中央区道修町四丁目1番1号