医薬品情報
| 総称名 | ワンタキソテール |
|---|---|
| 一般名 | ドセタキセル水和物 |
| 欧文一般名 | Docetaxel Hydrate |
| 薬効分類名 | タキソイド系抗悪性腫瘍剤 |
| 薬効分類番号 | 4240 |
| ATCコード | L01CD02 |
| KEGG DRUG |
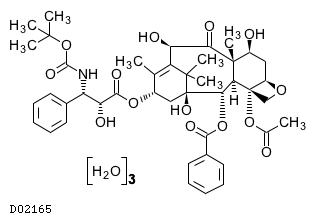
D02165
ドセタキセル水和物
|
| KEGG DGROUP |
DG00694
ドセタキセル
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年6月 改訂(第5版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ワンタキソテール点滴静注20mg/1mL | ONETAXOTERE I.V.Infusion | サノフィ | 4240405A3021 | 4622円/瓶 | 毒薬, 処方箋医薬品 |
| ワンタキソテール点滴静注80mg/4mL | ONETAXOTERE I.V.Infusion | サノフィ | 4240405A4028 | 16163円/瓶 | 毒薬, 処方箋医薬品 |
1. 警告
本剤の用量規制因子(Dose Limiting Factor,DLF)は好中球減少であり、本剤の使用により重篤な骨髄抑制(主に好中球減少)、重症感染症等の重篤な副作用及び本剤との因果関係が否定できない死亡例が認められている。したがって、本剤を含むがん化学療法は、緊急時に十分対応できる医療施設において、がん化学療法に十分な知識・経験を持つ医師のもとで、本剤の投与が適切と判断される症例についてのみ実施すること。また、下記の患者には投与しないなど適応患者の選択を慎重に行うこと。
・重篤な骨髄抑制のある患者
・感染症を合併している患者
・発熱を有し感染症の疑われる患者
2. 禁忌
次の患者には投与しないこと
2.1 重篤な骨髄抑制のある患者[重症感染症等を併発し、致命的となることがある。][1.参照]
2.2 感染症を合併している患者[感染症が増悪し、致命的となることがある。][1.参照]
2.3 発熱を有し感染症の疑われる患者[感染症が増悪し、致命的となることがある。][1.参照]
2.4 本剤又はポリソルベート80含有製剤に対し重篤な過敏症の既往歴のある患者[本剤はポリソルベート80を含有する。]
2.5 妊婦又は妊娠している可能性のある女性[9.5参照]
4. 効能または効果
5. 効能または効果に関連する注意
<前立腺癌>
遠隔転移を有する又は去勢抵抗性の患者に投与すること。
6. 用法及び用量
| 効能又は効果 | 用法及び用量 |
| 乳癌 非小細胞肺癌 胃癌 頭頸部癌 | 通常、成人に1日1回、ドセタキセルとして60mg/m2(体表面積)を1時間以上かけて3〜4週間間隔で点滴静注する。なお、患者の状態により適宜増減すること。ただし、1回最高用量は75mg/m2とする。 |
| 卵巣癌 | 通常、成人に1日1回、ドセタキセルとして70mg/m2(体表面積)を1時間以上かけて3〜4週間間隔で点滴静注する。なお、患者の状態により適宜増減すること。ただし、1回最高用量は75mg/m2とする。 |
| 食道癌 子宮体癌 | 通常、成人に1日1回、ドセタキセルとして70mg/m2(体表面積)を1時間以上かけて3〜4週間間隔で点滴静注する。なお、患者の状態により適宜減量すること。 |
| 前立腺癌 | 通常、成人に1日1回、ドセタキセルとして75mg/m2(体表面積)を1時間以上かけて3週間間隔で点滴静注する。なお、患者の状態により適宜減量すること。 |
7. 用法及び用量に関連する注意
7.1 本剤の投与にあたっては、特に本剤の用量規制因子である好中球数の変動に十分留意し、投与当日の好中球数が2,000/mm3未満であれば、投与を延期すること。
8. 重要な基本的注意
8.1 重篤な骨髄抑制が高頻度に起こるので、下記の点に留意すること。[1.、7.2、9.1.1、11.1.1、11.1.15参照]
・投与後は頻回に臨床検査(血液検査等)を行うなど、患者の状態を十分に観察すること。
・特に感染症の発現に十分注意し、好中球減少、CRP上昇、発熱等の有無を確認すること。
・本剤の投与にあたってはG-CSF製剤の適切な使用に関しても考慮すること。
8.2 脳転移病巣に対する効果は確立されていないので、脳転移病巣に対しては他の治療法を考慮すること。
8.3 本剤による重篤な過敏症状があらわれることがあるので、特に本剤の初回及び第2回目の投与時は、観察を十分に行うこと。過敏症状は本剤の投与開始から数分以内に起こることがあるので、本剤投与開始後1時間は頻回にバイタルサイン(血圧、脈拍数等)のモニタリングを行うなど、患者の状態を十分に観察すること。重篤な過敏症状(呼吸困難、気管支痙攣、血圧低下、胸部圧迫感、発疹等)が認められた場合は、直ちに本剤の投与を中止し、適切な処置を行うこと。なお、重篤な過敏症状が発現した症例には、本剤を再投与しないこと。[11.1.2、15.1.1参照]
8.4 心・循環器系に対する観察を十分に行うこと。ときに心不全、血圧低下、不整脈、動悸等があらわれることがある。[11.1.6参照]
8.5 重篤な肝障害があらわれることがあるので、肝機能検査の値に注意して観察を十分に行うこと。[11.1.3参照]
8.7 播種性血管内凝固症候群(DIC)があらわれることがあるので、血小板数、血清FDP値、血漿フィブリノーゲン濃度等の血液検査を適宜行うこと。[11.1.7参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 骨髄抑制のある患者
9.1.2 間質性肺炎又は肺線維症のある患者
症状を増悪させるおそれがある。[11.1.5参照]
9.1.3 浮腫のある患者
9.1.4 アルコールに過敏な患者
本剤を投与する場合には問診により適切かどうか判断すること。本剤は溶剤として無水エタノールを含有するため、アルコールの中枢神経系への影響が強くあらわれるおそれがある。
9.2 腎機能障害患者
9.3 肝機能障害患者
9.4 生殖能を有する者
9.4.1 以下の点に留意すること。[9.5、15.2参照]
・投与開始にあたっては、妊娠していないことを確認すること。
・妊娠する可能性のある患者に対しては投与しないことを原則とする。やむを得ず投与する場合には、本剤が妊娠の維持、胎児の発育等に障害を与える可能性があることを十分に説明すること。また、本剤投与中及び最終投与後2ヵ月間において避妊する必要性及び適切な避妊法について説明すること。
・本剤投与中に妊娠が確認された場合又は疑われた場合には直ちに投与を中止すること。
9.4.2 生殖可能な年齢の患者に投与する必要がある場合には性腺に対する影響を考慮すること。動物実験(マウス、ラット、イヌ)において精巣毒性が認められている。
9.4.3 男性には、本剤投与中及び最終投与後1ヵ月間においてバリア法(コンドーム)を用いて避妊する必要性について説明すること。[15.2参照]
9.5 妊婦
9.6 授乳婦
授乳しないことが望ましい。動物実験(ラット)で乳汁中への移行が報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
副作用の発現に注意し、投与間隔及び投与量に留意すること。副作用があらわれた場合には、休薬、投与間隔の延長等の適切な処置を行うこと。一般に高齢者では生理機能が低下している。
10. 相互作用
相互作用序文
本剤は、主として薬物代謝酵素CYP3A4で代謝されるので、本酵素の活性に影響を及ぼす薬剤と併用する場合には注意して投与すること。[16.4参照]
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| 他の抗悪性腫瘍剤 | 骨髄抑制等の副作用が増強することがあるので、併用療法を行う場合には、患者の状態を観察し、減量するか又は投与間隔を延長すること。 | 共に骨髄抑制作用を有する。 |
| 放射線照射 [11.1.5参照] | 放射線療法を併用している患者で放射線肺臓炎があらわれることがある。併用療法を行う場合には、患者の状態を観察し、肺陰影等が認められた場合には、本剤の投与及び放射線照射を中止するなど適切な処置を行うこと。 | 機序不明 |
| 放射線照射 [11.1.5参照] | 骨髄抑制等の副作用が増強することがあるので、併用療法を行う場合には、患者の状態を観察し、減量するか又は投与間隔を延長すること。 | 共に骨髄抑制作用を有する。 |
| アゾール系抗真菌剤 ミコナゾール等 エリスロマイシン、クラリスロマイシン、シクロスポリン、ミダゾラム | 副作用が強くあらわれることが考えられる。 | これらの薬剤がCYP3A4を阻害又はドセタキセルとの競合により、ドセタキセルの代謝が阻害され、その結果としてドセタキセルの血中濃度が上昇することが考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 骨髄抑制
11.1.2 ショック症状(0.1%)・アナフィラキシー(0.3%)
呼吸困難、気管支痙攣、血圧低下、胸部圧迫感、発疹等のショック症状・アナフィラキシーがあらわれることがある。[8.3参照]
11.1.3 黄疸、肝不全、肝機能障害(頻度不明)
黄疸、肝不全、AST・ALT・Al-Pの著しい上昇等の重篤な肝障害があらわれることがある。[8.5参照]
11.1.4 急性腎障害(0.1%)
11.1.5 間質性肺炎(0.4%)、肺線維症(頻度不明)
11.1.6 心不全(0.2%)[8.4参照]
11.1.7 播種性血管内凝固症候群(DIC)(0.1%)[8.7参照]
11.1.8 腸管穿孔(0.1%)、胃腸出血(0.6%)、虚血性大腸炎(頻度不明)、大腸炎(0.1%)
腹痛、吐血、下血、下痢等の症状があらわれた場合には投与を中止するなど適切な処置を行うこと。
11.1.9 イレウス(頻度不明)
11.1.10 急性呼吸促迫症候群(頻度不明)
呼吸障害等がみられた場合には、投与を中止するなど適切な処置を行うこと。
11.1.11 急性膵炎(頻度不明)
血清アミラーゼ値等に異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.12 皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)、中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(頻度不明)、多形紅斑(頻度不明)
皮膚粘膜眼症候群(Stevens-Johnson症候群)、中毒性表皮壊死融解症(TEN)、多形紅斑等の水疱性・滲出性皮疹があらわれることがある。
11.1.13 心タンポナーデ(頻度不明)、肺水腫(頻度不明)、浮腫・体液貯留(0.7%注))
11.1.14 心筋梗塞(頻度不明)、静脈血栓塞栓症(頻度不明)
11.1.15 感染症(2.3%注))
敗血症、肺炎等の感染症が報告されている。発症又は増悪した場合には、直ちに抗生剤の投与等の適切な処置を行うこと。日本人を対象とした臨床試験において、前立腺癌患者(70mg/m2)では他癌腫の患者(70mg/m2)よりも感染症等の発現割合が高かった。[8.1参照]
11.1.16 抗利尿ホルモン不適合分泌症候群(SIADH)(頻度不明)
低浸透圧血症を伴う低ナトリウム血症、尿中ナトリウム排泄量の増加、痙攣、意識障害等の症状があらわれた場合には投与を中止し、水分摂取の制限等適切な処置を行うこと。
11.1.17 重篤な口内炎等の粘膜炎(頻度不明)
11.1.18 血管炎(頻度不明)
11.1.19 末梢神経障害(頻度不明)
11.1.20 四肢の脱力感等の末梢性運動障害(頻度不明)
11.1.21 Radiation Recall現象(頻度不明)
注)Grade3以上の副作用から頻度を算出した。
乳癌、非小細胞肺癌、胃癌、頭頸部癌、卵巣癌、食道癌、子宮体癌及び前立腺癌を対象とした国内前・後期第2相臨床試験で認められた副作用に基づき算出した。
11.2 その他の副作用
| 50%以上 | 5〜50%未満 | 5%未満 | 頻度不明 | |
| 消化器 | 食欲不振 | 悪心・嘔吐、下痢、口内炎、便潜血 | 腹痛、腹部膨満感、便秘、舌炎、口内乾燥 | 胃・十二指腸潰瘍、食道炎、しゃっくり |
| 過敏症 | アレルギー、発赤 | そう痒感、潮紅 | ||
| 皮膚 | 脱毛 | 皮疹 | 色素沈着、爪疾患(爪剥離、変形、変色、爪下出血、爪下血腫、爪下膿瘍等) | 皮膚剥離、手足症候群、皮膚エリテマトーデス、強皮症様変化 |
| 精神・神経系 | しびれ感 | 頭痛、意識喪失、見当識障害、めまい、昏迷、難聴、耳鳴、味覚異常、不眠 | 傾眠 | |
| 眼 | 羞明、視力異常、流涙、結膜炎 | 視覚障害(閃光、光のちらつき、暗点)、涙道閉塞、黄斑浮腫 | ||
| 神経・筋症状 | 筋肉痛、関節痛、筋力低下・脱力感、背部痛、痙攣 | 筋炎 | ||
| 肝臓 | AST・ALT・γ-GTP・Al-P・LDH上昇 | 総ビリルビン上昇 | ||
| 腎臓 | 蛋白尿、K・Na・Cl・Caの異常、BUN上昇 | クレアチニン上昇、尿糖、血尿、乏尿、頻尿 | ||
| 循環器 | 血圧低下、血圧上昇、不整脈、動悸、頻脈 | |||
| 呼吸器 | 呼吸困難、咽頭炎、咳嗽 | 血痰 | ||
| その他 | 全身倦怠感 | 発熱、浮腫、総蛋白・アルブミン・A/G比・CK異常 | 静脈炎、疼痛、胸痛、全身痛、熱感、腰痛、鼻出血、ほてり | 脱水 |
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.1 本剤と薬剤濃度の異なるドセタキセル製剤を同時に使用しないこと。
14.1.2 必要量を注射筒で抜き取り、直ちに250又は500mLの輸液(生理食塩液又は5%ブドウ糖液)と混和した後は速やかに使用すること。
14.1.3 他剤との混注を行わないこと。
14.1.4 本剤が皮膚に付着した場合には、直ちに石鹸及び多量の流水で洗い流すこと。また、粘膜に付着した場合には、直ちに多量の流水で洗い流すこと。
14.2 薬剤投与時の注意
14.2.1 静脈内投与に際し、薬液が血管外に漏れると、注射部位に硬結・壊死をおこすことがあるので薬液が血管外に漏れないように投与すること。また、以前に同反応を発現した注射部位とは異なる部位に本剤を再投与した場合、以前の注射部位に同反応を再発するといった、いわゆる「Recall現象」が認められたとの報告がある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 外国における前投与
本剤の1回最大投与量を100mg/m2としている欧米においては注)、浮腫の発現率及び重篤度が高く、浮腫並びに過敏症状の軽減を目的として、副腎皮質ホルモン剤による前投与が行われている。前投与としては、デキサメタゾン(16mg/日、8mg1日2回)等を、本剤の投与前日から3日間、単独経口投与することが望ましいとされている。なお、前投与を実施した症例においても、重篤な過敏症(アナフィラキシーショック)による死亡例が報告されている。また、浮腫に関しては以下のような報告がある。[8.3、9.1.3、11.1.13参照]
・本剤100mg/m2を3週間間隔で点滴静脈内投与したところ、上記前投与を受けた患者では累積投与量(中央値)として818.9mg/m2以上、受けない患者では489.7mg/m2以上投与したときに浮腫の発現率が高くなった。
・本剤の投与を中止すると、浮腫は徐々に軽快する。浮腫は下肢から発現し、3kg以上の体重増加を伴う全身性のものになる場合があるが、急性の乏尿や低血圧は伴わない。まれに脱水症及び肺水腫が報告されている。
15.1.2 外国での肝機能異常患者への投与
外国において、本剤100mg/m2を3週間間隔で点滴静脈内投与注)したところ、血中アルカリホスファターゼ高値(正常域上限の2.5倍以上)を伴うトランスアミナーゼ高値(正常域上限の1.5倍以上)患者、又は血中ビリルビン高値(正常域上限以上)患者に本剤を投与した場合、重篤な副作用の発現や副作用の増強・増悪が認められている。報告された副作用は、Grade4の好中球減少、発熱性好中球減少、感染症、重篤な血小板減少、重篤な口内炎、並びに皮膚剥離を伴う皮膚症状等であり、治療関連死の危険性が増加すると警告されている。[9.3参照]
15.1.3 本剤を単独投与した患者あるいは本剤と他の抗悪性腫瘍剤や放射線療法を併用した患者で、急性白血病、骨髄異形成症候群(MDS)等の二次性悪性腫瘍が発生したとの報告がある。
15.1.4 国内での非小細胞肺癌に対する35mg/m2の週1回投与法注)(1日1回35mg/m2、1、8、15日目投与、4週毎に繰り返し)による第2相臨床試験において、間質性肺炎が48例中6例に認められた。[11.1.5参照]
15.1.5 乳癌の術後補助化学療法に関する海外臨床試験において、本剤と他の抗悪性腫瘍剤を併用した患者で観察期間終了時点においても脱毛が継続していた症例が報告されている(3.9%(29/744)、観察期間中央値:96ヵ月)1)。
15.2 非臨床試験に基づく情報
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
国内の各種固形癌患者24例にドセタキセル10〜90mg/m2を60分以上かけて単回点滴静脈内投与注2)したとき、血漿中濃度は点滴終了後漸減した。最高血漿中濃度(Cmax)及びAUC0-∞は投与量依存的に増加した2)。
NONMEM解析によるpopulation pharmacokinetic parametersを用い、60mg/m2、60分点滴静脈内投与時注2)をシミュレーションして求めた薬物動態パラメータは以下のようであった。α1-酸性糖蛋白(AAG)と肝機能障害がドセタキセルのクリアランス(CL)の主要な変動因子と考えられ、AST又はALTが60IU/L以上の患者ではクリアランスが21%減少した。
NONMEM解析によるpopulation pharmacokinetic parametersを用い、60mg/m2、60分点滴静脈内投与時注2)をシミュレーションして求めた薬物動態パラメータは以下のようであった。α1-酸性糖蛋白(AAG)と肝機能障害がドセタキセルのクリアランス(CL)の主要な変動因子と考えられ、AST又はALTが60IU/L以上の患者ではクリアランスが21%減少した。
| 対象 | Cmax(μg/mL) | AUC0-∞(μg・hr/mL) | t1/2α(min) | t1/2β(min) | t1/2γ(hr) | CL(L/hr/m2) |
| 母集団 | 2.0 | 2.9 | 6.3 | 46.4 | 18.8 | 20.4 |
| 肝機能障害時注1) | 2.3 | 3.7 | 7.1 | 47.8 | 20.2 | 16.2 |
16.1.2 反復投与
国内の各種固形癌患者6例にドセタキセル20、50及び70mg/m2を3又は4週間隔で2コースから最大4コースまで反復点滴静脈内投与注2)したとき、初回投与時と最終回投与時の血漿中濃度の推移に差はみられず、反復投与による体内動態の変化は認められなかった。
海外の各種固形癌患者24例にドセタキセル35mg/m2を1週間隔、75mg/m2及び100mg/m2を3週間隔で反復点滴静脈内投与注2,注3)したとき、終末相半減期は61〜120時間であったとの報告がある3)。
海外の各種固形癌患者24例にドセタキセル35mg/m2を1週間隔、75mg/m2及び100mg/m2を3週間隔で反復点滴静脈内投与注2,注3)したとき、終末相半減期は61〜120時間であったとの報告がある3)。
16.3 分布
16.3.1 組織移行
担癌マウスにドセタキセルを単回静脈内投与したとき、肝等の広範な臓器・組織に速やかな分布が認められた。腫瘍組織における消失半減期(t1/2β)は20hr以上で他の臓器・組織に比べ長かった4)。
16.3.2 血漿蛋白結合率
100mg/m2を60分間単回点滴静脈内投与注2)した外国人の各種固形癌患者3例において、ドセタキセルの血漿蛋白結合率を検討したところ、点滴終了8時間までの測定において90%以上であった5)。
16.4 代謝
16.5 排泄
国内の各種固形癌患者19例にドセタキセル10〜90mg/m2を60〜160分間かけて単回点滴静脈内投与注2)したときの尿中排泄率を検討した結果、未変化体の48時間までの尿中排泄率はいずれも5%以下であった。
14C-ドセタキセル100mg/m2を60分間単回点滴静脈内投与注2)した外国人の各種固形癌患者での薬物動態を検討した。投与後168時間までの尿中及び糞中排泄率はそれぞれ6.0%(n=3)及び74.1%(n=2)で、主排泄経路は糞中排泄であった。
注2)本剤の承認された1回用量は60、70及び75mg/m2(体表面積)である。
注3)ドセタキセル35mg/m2及び75mg/m2を投与された患者においては初回投与後、並びに100mg/m2を投与された患者においては初回投与後又は2回目の投与後に測定された血漿中濃度に基づき算出された。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<乳癌>
17.1.1 国内後期第2相臨床試験
乳癌を対象とした非盲検法による後期第2相臨床試験で、本剤60mg/m2の用量を3〜4週間間隔で、2コース以上単独で静脈内投与し、適宜増減(50〜70mg/m2)した。本剤の奏効率(有効性解析対象例139例)は、48.2%(67/139例)であった。主な副作用は、137例中、脱毛89.1%(122例)、食欲不振67.9%(93例)、悪心・嘔吐60.6%(83例)、発熱44.5%(61例)、下痢25.5%(35例)、口内炎16.1%(22例)及び浮腫15.3%(21例)であった。主な臨床検査値異常は、白血球数減少98.5%(135/137例)、好中球数減少95.6%(130/136例)及びヘモグロビン減少61.3%(84/137例)であった8)9)。[17.1.10参照]
<非小細胞肺癌>
17.1.2 国内後期第2相臨床試験
非小細胞肺癌を対象とした非盲検法による後期第2相臨床試験で、本剤60mg/m2の用量を3〜4週間間隔で、2コース以上単独で静脈内投与し、適宜増減(50〜70mg/m2)した。本剤の奏効率(有効性解析対象例150例)は、21.3%(32/150例)であった。主な副作用は、149例中、脱毛81.9%(122例)、食欲不振56.4%(84例)、全身倦怠感43.0%(64例)、発熱42.3%(63例)、悪心・嘔吐34.9%(52例)、下痢15.4%(23例)及び皮疹・発赤15.4%(23例)であった。主な臨床検査値異常は、白血球数減少95.3%(142/149例)、好中球数減少96.6%(144/149例)、赤血球数異常67.8%(101/149例)、ヘモグロビン減少54.4%(81/149例)、LDH異常20.8%(31/149例)、アルブミン異常20.1%(29/144例)、総蛋白異常19.5%(29/149例)、ALT上昇15.4%(23/149例)、AST上昇12.1%(18/149例)及びγ-GTP異常10.1%(15/149例)であった10)11)。[17.1.10参照]
<胃癌>
17.1.3 国内後期第2相臨床試験
胃癌を対象とした非盲検法による後期第2相臨床試験で、本剤60mg/m2の用量を3〜4週間間隔で、4コース以上単独で静脈内投与し、適宜増減(50〜70mg/m2)した。本剤の奏効率(有効性解析対象例129例)は、17.1%(22/129例)であった。主な副作用は、124例中、脱毛74.2%(92例)、発熱54.0%(67例)、悪心・嘔吐50.8%(63例)、食欲不振49.2%(61例)及び全身倦怠感48.4%(60例)であった。主な臨床検査値異常は、白血球数減少98.4%(122/124例)、好中球数減少95.2%(118/124例)、ヘモグロビン減少32.3%(40/124例)及び赤血球数異常31.5%(39/124例)であった12)。[17.1.10参照]
<頭頸部癌>
17.1.4 国内後期第2相臨床試験
頭頸部癌を対象とした非盲検法による後期第2相臨床試験で、本剤60mg/m2の用量を3〜4週間間隔で、2コース以上単独で静脈内投与し、適宜増減(50〜70mg/m2)した。本剤の奏効率(有効性解析対象例63例)は、20.6%(13/63例)であった。主な副作用は、62例中、脱毛80.6%(50例)、全身倦怠感66.1%(41例)、食欲不振62.9%(39例)、発熱59.7%(37例)及び悪心・嘔吐43.5%(27例)であった。主な臨床検査値異常は、白血球数減少95.2%(59/62例)、好中球数減少90.3%(56/62例)、赤血球数54.8%(34/62例)、ヘモグロビン減少40.3%(25/62例)、LDH40.0%(24/60例)、アルブミン36.1%(22/61例)、総蛋白33.3%(20/60例)、ALT上昇32.3%(20/62例)及びAST上昇30.6%(19/62例)であった13)。[17.1.10参照]
<卵巣癌>
17.1.5 国内後期第2相臨床試験
卵巣癌を対象とした非盲検法による後期第2相臨床試験で、本剤70mg/m2の用量を3週間間隔で、2コース以上単独で静脈内投与した。本剤の奏効率(有効性解析対象例63例)は、23.8%(15/63例)であった。主な副作用は、62例中、脱毛67.7%(42例)、食欲不振51.6%(32例)、全身倦怠感50.0%(31例)、悪心・嘔吐48.4%(30例)及び発熱46.8%(29例)であった。主な臨床検査値異常は、白血球数減少98.4%(61/62例)、好中球数減少98.4%(61/62例)、ヘモグロビン減少69.4%(43/62例)及び赤血球数66.1%(41/62例)であった14)。[17.1.10参照]
<食道癌>
17.1.6 国内後期第2相臨床試験
<子宮体癌>
17.1.7 国内後期第2相臨床試験
<前立腺癌>
17.1.8 国内後期第2相臨床試験
ホルモン不応性転移性前立腺癌患者(対象の組織型は腺癌のみ)を対象としたプレドニゾロンとの併用下の非盲検法による後期第2相臨床試験で本剤70mg/m2注1)が静脈内投与(3週毎に1回、最大10サイクル)され、奏効率(有効性解析対象例43例)は44.2%(19/43例)であった。主な副作用は、43例中、脱毛88.4%(38例)、食欲不振65.1%(28例)及び疲労53.5%(23例)で、Grade3以上では好中球減少を伴わない感染14.0%(6例)があった。主な臨床検査値異常は、白血球減少症97.7%(42例)、好中球減少症95.3%(41例)、リンパ球減少症79.1%(34例)及びCRP増加48.8%(21例)で、Grade3以上では発熱性好中球減少症16.3%(7例)があった17)。[17.1.10参照]
17.1.9 海外第3相臨床試験
ホルモン不応性転移性前立腺癌(対象の組織型は腺癌のみ)患者を対象にプレドニゾン又はプレドニゾロンとの併用下にミトキサントロンを対照薬とした非盲検法による第3相臨床試験で、本剤75mg/m2投与群(75mg/m2を3週間隔で静脈内投与し、最大10サイクル)、30mg/m2投与群注1)(30mg/m2を5週連続隔週で静脈内投与後1週休薬し、最大5サイクル)の有効性及び安全性が比較検討された。本剤75mg/m2投与群(有効性解析対象例335例)は、対照群(ミトキサントロン投与群、有効性解析対象例337例)に比べ全生存期間の延長を示した18)。
注1)前立腺癌で承認された本剤の1回用量は75mg/m2(体表面積)である。
| ドセタキセル投与群 (n=335) | ミトキサントロン投与群 (n=337) | |
| 生存期間中央値(月) [95%信頼区間] | 18.9 [17.0-21.2] | 16.5 [14.4-18.6] |
| ハザード比 [95%信頼区間] | 0.76 [0.62-0.94] | |
| P値注2) | P=0.009 | |
本剤75mg/m2を投与した安全性評価対象例332例中、治療関連死の疑われた症例は1例(0.3%)であった。主な副作用は、脱毛216例(65.1%)、全身倦怠感142例(42.8%)、悪心118例(35.5%)等であった。Grade3以上の発現率では全身倦怠感13例(3.9%)が最も高かった。また、臨床検査値異常については、検査を実施した328例中、主なものはヘモグロビン減少218例(66.5%)、Al-P上昇204例(62.2%)、好中球減少134例(40.9%)、白血球減少132例(40.2%)等であった。Grade3以上の主なものは、好中球減少105例(32.0%)、白血球減少79例(24.1%)、Al-P上昇38例(11.6%)等であった。
<効能共通>
17.1.10 国内前・後期第2相臨床試験
国内前・後期第2相臨床試験において、次のような臨床検査値異常が認められた。70mg/m2の用量では、60mg/m2投与時に比べ骨髄抑制がさらに強くあらわれ、好中球減少、ヘモグロビン減少等の発現率が高かった。[17.1.1-17.1.8参照]
| 検査項目 | 60mg/m2 | 70mg/m2注3) | 70mg/m2 (前立腺癌) | |
| 白血球減少 | 全体 | 97.2% (733/754) | 97.9% (188/192) | 97.7% (42/43) |
| 2,000/mm3未満 | 65.3% (492/754) | 81.8% (157/192) | 81.4% (35/43) | |
| 1,000/mm3未満 | 14.7% (111/754) | 27.1% (52/192) | 20.9% (9/43) | |
| 好中球減少 | 全体 | 95.2% (711/747) | 98.4% (187/190) | 95.3% (41/43) |
| 1,000/mm3未満 | 84.6% (632/747) | 90.0% (171/190) | 93.0% (40/43) | |
| 500/mm3未満 | 60.6% (453/747) | 73.7% (140/190) | 74.4% (32/43) | |
| ヘモグロビン減少 | 全体 | 50.9% (384/754) | 78.1% (150/192) | 76.7% (33/43) |
| 8.0g/dL未満 | 7.7% (58/754) | 16.7% (32/192) | 9.3% (4/43) | |
| 血小板減少 | 全体 | 11.7% (88/753) | 13.0% (25/192) | 9.3% (4/43) |
| 50×103/μL未満 | 3.2% (24/753) | 1.6% (3/192) | 0.0% (0/43) | |
| AST上昇 | 全体 | 20.1% (151/752) | 31.8% (61/192) | 39.5% (17/43) |
| 501U以上 | 0.4% (3/752) | 0.0% (0/192) | 0.0% (0/43) | |
| ALT上昇 | 全体 | 20.2% (152/753) | 26.6% (51/192) | 46.5% (20/43) |
| 501U以上 | 0.3% (2/753) | 0.0% (0/192) | 0.0% (0/43) | |
| BUN上昇 | 全体 | 4.1% (31/754) | 10.4% (20/192) | −注4) |
| 61mg/dL以上 | 0.7% (5/753) | 0.5% (1/192) | −注4) | |
| 用量 | 好中球のNadir注5) | Nadirまでの期間 | Nadirから2,000/mm3以上に回復するまでの期間 |
| 60mg/m2 | 527.5/mm3 | 9日 | 8日注7) |
| 70mg/m2注6) | 412.0/mm3 | 8日 | 6日注8) |
| 70mg/m2 (前立腺癌) | 594.0/mm3 | 9日 | 6日注9) |
18. 薬効薬理
18.1 作用機序
ドセタキセルはチューブリンの重合を促進し、安定な微小管を形成するとともに、その脱重合を抑制する。また、細胞内においては形態的に異常な微小管束を形成する。以上の作用により細胞の有糸分裂を停止させる19)。
18.2 抗腫瘍効果
In vivoにおいて、ドセタキセルはマウスのMA16/C乳癌、MA13/C乳癌、MA44乳癌、Lewis肺癌に対して退縮を含む抗腫瘍作用を示した。また、ヒト乳癌株であるMC-8-JCK(充実腺管癌)、MC-2-JCK(充実腺管癌)、H-31(乳頭腺管癌)、及びヒト非小細胞肺癌株であるLu-99(大細胞癌)、Lu-61(中分化扁平上皮癌)、LC-11-JCK(乳頭型腺癌)に対し、腫瘍増殖抑制効果にとどまらず、腫瘍縮小効果を示した。この他にヒト胃癌細胞株(MKN-28、MKN-45、KKLS)、ヒト卵巣癌株(OVCAR-3)、ヒト食道癌株(H-190、H-204)、ヒト子宮体癌株(AN3CA)、ヒト前立腺癌株(DU145)等にも抗腫瘍効果が認められている。In vitroにおいて、ドセタキセルはドキソルビシン耐性P388白血病細胞では部分交叉耐性を示したが、カンプトテシン耐性株及び白金製剤耐性株に対する交叉耐性は認められなかった4)20)21)22)23)24)25)26)27)28)。
19. 有効成分に関する理化学的知見
19.1. ドセタキセル水和物
20. 取扱い上の注意
遮光を保つため、包装開封後はバイアルを箱に入れて保存すること。
22. 包装
<ワンタキソテール点滴静注20mg/1mL>
1mL×1バイアル
<ワンタキソテール点滴静注80mg/4mL>
4mL×1バイアル
23. 主要文献
- 社内資料:乳癌の術後補助化学療法に関する海外第3相臨床試験
- 田口鐵男 他, 癌と化学療法, 21 (12), 1997-2005, (1994) »PubMed
- Baker S D,et al., Clin Cancer Res., 10 (6), 1976-83, (2004) »PubMed
- Bissery M C,et al., Anti-Cancer Drugs., 6 (3), 339-68, (1995) »PubMed
- de Valeriola D,et al., Proceedings of the American Association for Cancer Research., 34, 373, (1993)
- Shou M,et al., Pharmacogenetics., 8, 391-401, (1998) »PubMed
- Sparreboom A,et al., Drug Metab Dispos., 24 (6), 655-8, (1996) »PubMed
- 田口鐵男 他, 癌と化学療法, 21 (15), 2625-32, (1994) »PubMed
- Adachi I,et al., British Journal of Cancer., 73, 210-6, (1996) »PubMed
- 工藤翔二 他, 癌と化学療法, 21 (15), 2617-23, (1994) »PubMed
- 大熨泰亮 他, 癌と化学療法, 22 (1), 59-65, (1995) »PubMed
- 社内資料:進行・再発胃癌に対する後期第2相臨床試験
- 社内資料:進行・再発頭頸部癌に対する後期第2相臨床試験
- 社内資料:卵巣癌に対する後期第2相臨床試験
- Muro K,et al., Annals of Oncology., 15, 955-9, (2004) »PubMed
- Katsumata N,et al., British Journal of Cancer., 93, 999-1004, (2005) »PubMed
- Naito S,et al., Jpn J Clin Oncol., 38 (5), 365-72, (2008) »PubMed
- Tannock I F,et al., New England Journal of Medicine., 351 (15), 1502-12, (2004) »PubMed
- Ringel I,et al., Journal of the National Cancer Institute., 83 (4), 288-91, (1991) »PubMed
- Bissery M C,et al., Cancer Research., 51 (18), 4845-52, (1991) »PubMed
- Bissery M C,et al., Proceedings of the American Association for Cancer Research., 35, 327, (1994)
- Riou J F,et al., Biochemical and Biophysical Research Communications., 187 (1), 164-70, (1992) »PubMed
- Tanaka M,et al., European Journal of Cancer., 32A (2), 226-30, (1996) »PubMed
- Dykes D J,et al., Investigational New Drugs., 13, 1-11, (1995) »PubMed
- Kelland L R,et al., Cancer Chemotherapy and Pharmacology., 30 (6), 444-50, (1992) »PubMed
- 赤藤修司 他, 癌と化学療法, 33 (3), 337-43, (2006) »PubMed
- 赤藤修司 他, 癌と化学療法, 32 (10), 1437-42, (2005) »PubMed
- Kraus L A,et al., Investigational New Drugs., 21, 259-68, (2003) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
サノフィ株式会社
くすり相談室
〒163-1488
東京都新宿区西新宿三丁目20番2号
電話:フリーダイヤル 0120-109-905
製品情報問い合わせ先
サノフィ株式会社
くすり相談室
〒163-1488
東京都新宿区西新宿三丁目20番2号
電話:フリーダイヤル 0120-109-905
26. 製造販売業者等
26.1 製造販売元
サノフィ株式会社
〒163-1488
東京都新宿区西新宿三丁目20番2号
その他の説明
ワンタキソテール点滴静注20mg/1mL、80mg/4mL 調製方法
[1]
ワンタキソテール点滴静注バイアルを用意します。
[2]
必要量を注射筒で抜き取ってください。
抜き取りには21G針が推奨されます(19G以上の太い注射針を使用した場合にゴム栓のコアリングの報告があります)。
抜き取りには21G針が推奨されます(19G以上の太い注射針を使用した場合にゴム栓のコアリングの報告があります)。
溶液1mL中に20mgのドセタキセルを含有します。
また、溶液1mL中に0.395gの無水エタノールを予め含有します。
タキソテール点滴静注用20mg、80mgのプレミックス液とはドセタキセル濃度、及びエタノールの含有量が異なります。
詳しくはワンタキソテール点滴静注20mg/1mL、80mg/4mL及びタキソテール点滴静注用20mg、80mgの添付文書をご参照ください。
また、溶液1mL中に0.395gの無水エタノールを予め含有します。
タキソテール点滴静注用20mg、80mgのプレミックス液とはドセタキセル濃度、及びエタノールの含有量が異なります。
詳しくはワンタキソテール点滴静注20mg/1mL、80mg/4mL及びタキソテール点滴静注用20mg、80mgの添付文書をご参照ください。
[3]
輸液には250又は500mLの生理食塩液又は5%ブドウ糖液を用い、混和調製してください。
調製後は速やかに使用してください。
調製後は速やかに使用してください。
本剤はドセタキセル注射液で、最高用量は食道癌・子宮体癌では70mg/m2、その他の癌腫では75mg/m2です。