医薬品情報
| 総称名 | ウルソデオキシコール酸 |
|---|---|
| 一般名 | ウルソデオキシコール酸 |
| 欧文一般名 | Ursodeoxycholic Acid |
| 薬効分類名 | 肝・胆・消化機能改善剤 |
| 薬効分類番号 | 2362 |
| ATCコード | A05AA02 |
| KEGG DRUG |
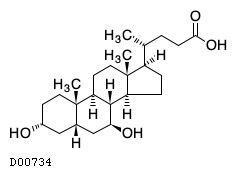
D00734
ウルソデオキシコール酸
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年12月 改訂(第3版)

|
2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ウルソデオキシコール酸錠50mg「JG」 | Ursodeoxycholic Acid Tablets | 日本ジェネリック | 2362001F1100 | 10.8円/錠 | |
| ウルソデオキシコール酸錠100mg「JG」 | Ursodeoxycholic Acid Tablets | 日本ジェネリック | 2362001F2190 | 10.8円/錠 |
2. 禁忌
4. 効能または効果
○下記疾患における利胆
胆道(胆管・胆のう)系疾患及び胆汁うっ滞を伴う肝疾患
○慢性肝疾患における肝機能の改善
○下記疾患における消化不良
小腸切除後遺症、炎症性小腸疾患
○外殻石灰化を認めないコレステロール系胆石の溶解
○原発性胆汁性肝硬変における肝機能の改善
○C型慢性肝疾患における肝機能の改善
5. 効能または効果に関連する注意
<C型慢性肝疾患における肝機能の改善>
5.1 C型慢性肝疾患においては、まずウイルス排除療法を考慮することが望ましい。本薬にはウイルス排除作用はなく、現時点ではC型慢性肝疾患の長期予後に対する肝機能改善の影響は明らかではないため、ウイルス排除のためのインターフェロン治療無効例若しくはインターフェロン治療が適用できない患者に対して本薬の投与を考慮すること。
5.2 非代償性肝硬変患者に対する有効性及び安全性は確立していない。[9.3.5参照]
6. 用法及び用量
| 効能又は効果 | 用法及び用量 |
| ・下記疾患における利胆 胆道(胆管・胆のう)系疾患及び胆汁うっ滞を伴う肝疾患 ・慢性肝疾患における肝機能の改善 ・下記疾患における消化不良 小腸切除後遺症、炎症性小腸疾患 | ウルソデオキシコール酸として、通常、成人1回50mgを1日3回経口投与する。なお、年齢、症状により適宜増減する。 |
| ・外殻石灰化を認めないコレステロール系胆石の溶解 | 外殻石灰化を認めないコレステロール系胆石の溶解には、ウルソデオキシコール酸として、通常、成人1日600mgを3回に分割経口投与する。なお、年齢、症状により適宜増減する。 |
| ・原発性胆汁性肝硬変における肝機能の改善 | 原発性胆汁性肝硬変における肝機能の改善には、ウルソデオキシコール酸として、通常、成人1日600mgを3回に分割経口投与する。なお、年齢、症状により適宜増減する。増量する場合の1日最大投与量は900mgとする。 |
| ・C型慢性肝疾患における肝機能の改善 | C型慢性肝疾患における肝機能の改善には、ウルソデオキシコール酸として、通常、成人1日600mgを3回に分割経口投与する。なお、年齢、症状により適宜増減する。増量する場合の1日最大投与量は900mgとする。 |
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 重篤な膵疾患のある患者
原疾患が悪化するおそれがある。
9.1.2 消化性潰瘍のある患者
粘膜刺激作用があるため、症状が増悪するおそれがある。
9.3 肝機能障害患者
9.3.1 完全胆道閉塞のある患者
投与しないこと。利胆作用があるため、症状が増悪するおそれがある。[2.1参照]
9.3.2 劇症肝炎の患者
投与しないこと。症状が増悪するおそれがある。[2.2参照]
9.3.3 胆管に胆石のある患者
利胆作用があるため、胆汁うっ滞を惹起するおそれがある。
9.3.4 原発性胆汁性肝硬変の硬変期で高度の黄疸のある患者
血清ビリルビン値の上昇等がみられた場合には、投与を中止するなど適切な処置を行うこと。症状が悪化するおそれがある。
9.3.5 C型慢性肝疾患で高度の黄疸のある患者
血清ビリルビン値の上昇等がみられた場合には、投与を中止するなど適切な処置を行うこと。症状が悪化するおそれがある。[5.2参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。動物実験(ラット)で妊娠前及び妊娠初期の大量(2,000mg/kg/日)投与により胎児毒性が報告されている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒトで母乳への移行が認められている。
9.8 高齢者
用量に注意して投与すること。一般に生理機能が低下している。
10. 相互作用
10.2 併用注意
| コレスチラミン コレスチミド | 本剤の作用を減弱するおそれがあるので、可能な限り間隔をあけて投与すること。 | 本剤と結合し、本剤の吸収を遅滞あるいは減少させるおそれがある。 |
| 制酸剤 水酸化アルミニウムゲル 合成ケイ酸アルミニウム 水酸化アルミニウムゲル・水酸化マグネシウム | 本剤の作用を減弱するおそれがある。 | アルミニウムを含有する制酸剤は、本剤を吸着し、本剤の吸収を阻害するおそれがある。 |
| 脂質低下剤 クロフィブラート ベザフィブラート フェノフィブラート | 本剤をコレステロール胆石溶解の目的で使用する場合は、本剤の作用を減弱するおそれがある。 | クロフィブラート等は胆汁中へのコレステロール分泌を促進するため、コレステロール胆石形成が促進されるおそれがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 間質性肺炎(頻度不明)
発熱、咳嗽、呼吸困難、胸部X線異常を伴う間質性肺炎があらわれることがあるので、このような症状があらわれた場合には、投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
注)発現頻度は製造販売後調査の結果を含む。
11.2 その他の副作用
| 1〜5%未満 | 0.1〜1%未満 | 0.1%未満 | 頻度不明 | |
| 消化器 | 下痢 | 悪心、食欲不振、便秘、胸やけ、胃不快感、腹痛、腹部膨満 | 嘔吐 | |
| 過敏症 | そう痒、発疹 | 蕁麻疹等 | 紅斑(多形滲出性紅斑等) | |
| 肝臓 | AST上昇、ALT上昇、ALP上昇 | ビリルビン上昇、γ-GTP上昇 | ||
| その他 | 全身倦怠感、めまい | 白血球数減少 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
過去に胆石治療のための十二指腸乳頭部の処置(内視鏡的乳頭切開術や胆道と十二指腸との吻合術など)を受けた患者において、本剤を長期使用した際に、ウルソデオキシコール酸を主成分とする胆石の形成が報告されている。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人を対象とし、ウルソデオキシコール酸200mgを投与(100mg錠を2錠、6例)したとき、最高血清中濃度は1.90±0.25μg/mLであった。また、400mgを投与(100mg錠を4錠、6例)したとき、最高血清中濃度は7.09±1.43μg/mLであった1)。
16.1.2 生物学的同等性試験
<ウルソデオキシコール酸錠50mg「JG」>
ウルソデオキシコール酸錠50mg「JG」とウルソ錠50mgを、クロスオーバー法によりそれぞれ2錠(ウルソデオキシコール酸として100mg)健康成人男性に絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について分散分析にて統計解析を行った結果、両剤の生物学的同等性が確認された2)。
| 判定パラメータ | ||
| AUC0-240min(μg・min/mL) | Cmax(μg/mL) | |
| ウルソデオキシコール酸錠50mg「JG」 | 303±37 | 2.44±0.40 |
| ウルソ錠50mg | 317±35 | 2.43±0.34 |
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
<ウルソデオキシコール酸錠100mg「JG」>
ウルソデオキシコール酸錠100mg「JG」とウルソ錠100mgを、クロスオーバー法によりそれぞれ1錠(ウルソデオキシコール酸として100mg)健康成人男性に絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について分散分析にて統計解析を行った結果、両剤の生物学的同等性が確認された3)。
| 判定パラメータ | ||
| AUC0-240min(μg・min/mL) | Cmax(μg/mL) | |
| ウルソデオキシコール酸錠100mg「JG」 | 360±34 | 3.04±0.29 |
| ウルソ錠100mg | 349±21 | 2.87±0.21 |
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.2 吸収
健康成人にウルソデオキシコール酸1g/日を2週間経口投与後、14C-ウルソデオキシコール酸を静注し、同位体希釈分析法を用いてその吸収量などを測定した。腸肝循環中のウルソデオキシコール酸のプールサイズは約940mgであり、投与されたウルソデオキシコール酸はそのほとんどが腸肝循環を行っていた。また、胆汁中胆汁酸分画に占めるウルソデオキシコール酸は最大56%でありケノデオキシコール酸(CDCA)とコール酸(CA)の比率はともに減少した4)(外国人のデータ)。
16.4 代謝
健康成人6例を対象とし、ウルソデオキシコール酸400mg(100mg錠を4錠)を投与したとき、血清中の主な代謝物は、グリコウルソデオキシコール酸(GUDCA)及びその硫酸抱合体(GUDCA-S)であった。また、尿中の主な代謝物はGUDCA-S及びウルソデオキシコール酸のN-アセチルグルコサミン抱合体であった1)。
16.5 排泄
健康成人6例を対象とし、ウルソデオキシコール酸400mg(100mg錠を4錠)を投与したとき、投与後24時間のGUDCA-S及びウルソデオキシコール酸のN-アセチルグルコサミン抱合体の尿中排泄率は0.5%であった1)。
注)本剤の最大承認用量は900mgである。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 二重盲検試験
(1)胆道系疾患(胆石症、胆道炎、胆道ジスキネジー、胆のう切除後症候群)患者にウルソデオキシコール酸150mg/日を2週間投与し、自覚症状に対する改善効果を検討したところ、右季肋部痛などに対してプラセボ投与群に比し有意な改善効果を認めた5)。
(2)慢性肝疾患(慢性肝炎、肝硬変)患者にウルソデオキシコール酸150mg/日を4週間投与したところ、ウルソデオキシコール酸投与群はプラセボ投与群に比しAST、ALT値が有意に低下した6)。
(3)コレステロール系胆石症患者にウルソデオキシコール酸150mg/日、600mg/日を6〜12ヵ月間投与し、胆石溶解効果を検討したところ、X線造影像による胆石の消失、縮小・減少を合わせた有効率は150mg/日投与群17.4%(4/23例)、600mg/日投与群34.5%(10/29例)、プラセボ投与群5.0%(1/20例)で、600mg/日投与群はプラセボ投与群に比し有意な溶解効果を認めた7)。
(4)原発性胆汁性肝硬変(PBC)患者にウルソデオキシコール酸150mg/日、600mg/日を24週間投与し肝機能改善効果を検討したところ、改善以上の改善率は150mg/日投与群22.7%(5/22例)、600mg/日投与群92.0%(23/25例)で、600mg/日投与群は150mg/日投与群に比し、有意な改善効果を認めた8)。
(5)C型慢性肝炎患者にウルソデオキシコール酸150mg/日、600mg/日、900mg/日を24週間投与し、ALTの変化率(中央値)を比較検討したところ、150mg/日投与群(195例)−15.3%、600mg/日投与群(198例)−29.2%、900mg/日投与群(193例)−36.2%であり、600mg/日投与群、900mg/日投与群は150mg/日投与群に比し、有意な改善効果を認めた。副作用の発現頻度は150mg/日投与群、600mg/日投与群、900mg/日投与群それぞれ18.1%(36/199例)、21.5%(43/200例)、17.8%(35/197例)と全体ではほぼ同様で、各群間に有意差は認められなかった。なお、下痢については高用量で発現頻度が高い傾向が認められた9)。
17.1.2 長期投与試験
18. 薬効薬理
18.1 作用機序
18.2 利胆作用及び胆汁うっ滞改善作用
胆石摘出術後患者5例にT-チューブドレナージを設置し、ウルソデオキシコール酸150mg/日を14日間経口投与したところ、肝胆汁流量は投与5日目より増加した12)。
18.3 肝機能改善作用
18.3.1 肝の摂取・排泄機能改善作用
慢性肝疾患患者にウルソデオキシコール酸150mg/日を3ヵ月間経口投与し、その前後に99mTc-PMTを静注して動態解析を行ったところ、肝の摂取排泄曲線のピークタイムが有意に短縮した13)。
18.3.2 動物モデルにおける肝障害抑制作用
(1)自己免疫性肝炎モデルマウスに0.3%濃度になるように調製したウルソデオキシコール酸飼料を摂取させたところ、リポポリサッカライド投与による生存率の低下、血中AST及びALTの上昇、肝組織における壊死及び炎症細胞浸潤を抑制した14)。
(2)コンカナバリンA誘発肝障害モデルマウスにウルソデオキシコール酸50及び150mg/kgを経口投与したところ、血中AST及びALTの上昇を抑制した。また、本モデルにウルソデオキシコール酸150mg/kgを経口投与したところ、血中TNF-α、IL-6及びMIP-2(ヒトのIL-8に相当)上昇を抑制した。さらに、肝臓において好中球浸潤の指標となるミエロペルオキシダーゼ(MPO)活性の上昇を抑制した15)。
(3)ケノデオキシコール酸(CDCA)誘発肝障害モデルハムスターにウルソデオキシコール酸50及び150mg/kgを経口投与したところ、血中ALTの上昇を抑制した16)。
18.3.3 疎水性胆汁酸の肝細胞障害性に対する軽減作用
ヒト肝細胞由来のChang細胞を用いたin vitro実験で、培養液中にCA、CDCAあるいはウルソデオキシコール酸を添加して細胞障害性を検討したところ、細胞障害性の強さはCDCAが最も強く、CAとウルソデオキシコール酸は同程度に弱かった。また、CDCAによる細胞障害性はウルソデオキシコール酸の添加により有意に低下した17)。
18.4 消化吸収改善作用
18.4.1 回腸切除患者12例にウルソデオキシコール酸150mg/日を1ヵ月間経口投与し、その前後で血中高級脂肪酸、脂溶性ビタミン濃度を測定したところ、血中リノール酸、リノレン酸、ビタミンD、Eの各濃度が上昇した18)。
18.4.2 膵液分泌促進作用
ラット及びイヌの十二指腸内に2.55×10−2Mに調製したウルソデオキシコール酸溶液2.5mL/kgを投与したところ、ラットにおいて膵液量の増加を、またイヌでは重炭酸濃度の増加及びアミラーゼなど膵酵素活性の上昇を認めた19)。
18.5 胆石溶解作用
18.5.1 胆のう胆汁のコレステロール不飽和化作用
コレステロール系胆石症患者5例にウルソデオキシコール酸300mg/日を2ヵ月間、その後増量し、600mg/日を2ヵ月間経口投与したところ、いずれの用量においても胆のう胆汁中のコレステロールの相対比率は低下し、Lithogenic Indexの改善を認めた20)。
18.5.2 液晶形成作用
コレステロール系胆石症患者5例にウルソデオキシコール酸600mg/日を1週間経口投与し、胆のう胆汁を採取し、偏光顕微鏡で観察したところ、胆汁中に多成分型の液晶が認められ、コレステロールはこの液晶中に多量に可溶化されていた21)。
18.5.3 コレステロールの腸管吸収抑制作用
健康成人6例にウルソデオキシコール酸600mg/日を1ヵ月間経口投与したところ、腸管におけるコレステロール吸収を抑制した22)。
19. 有効成分に関する理化学的知見
19.1. ウルソデオキシコール酸
22. 包装
<ウルソデオキシコール酸錠50mg「JG」>
100錠[10錠(PTP)×10]
1000錠[10錠(PTP)×100]
1000錠[プラスチック容器、バラ]
<ウルソデオキシコール酸錠100mg「JG」>
100錠[10錠(PTP)×10]
1000錠[10錠(PTP)×100]
1000錠[プラスチック容器、バラ]
23. 主要文献
- 永松信哉 他, 薬理と治療, 25 (6), 1637-1651, (1997)
- 社内資料:生物学的同等性試験(錠50mg)
- 社内資料:生物学的同等性試験(錠100mg)
- Fedorowski,T.et al., Gastroenterology., 73 (5), 1131-1137, (1977) »PubMed
- 戸田安士 他, 基礎と臨床, 10 (1), 103-119, (1976)
- 宮地一馬 他, 臨床と研究, 53 (5), 1395-1403, (1976)
- 芦沢真六 他, 医学のあゆみ, 101 (13), 922-936, (1977)
- 戸田剛太郎 他, 肝胆膵, 37 (3), 443-460, (1998)
- Omata,M.et al., Gut., 56 (12), 1747-1753, (2007) »PubMed
- 戸田剛太郎 他, 医学と薬学, 41 (4), 609-633, (1999)
- 長期投与試験(ウルソ錠:2007年3月2日承認、審査報告書)
- 吉岡正智 他, 診断と治療, 64 (10), 1953-1963, (1976)
- 早川富博 他, 日本消化器病学会雑誌, 85 (11), 2389-2395, (1988) »DOI
- 武内喜茂 他, 薬理と治療, 26 (2), 169-176, (1998)
- Ishizaki,K.et al., Eur.J.Pharmacol., 578 (1), 57-64, (2008) »PubMed
- Iwaki,T.et al., World J.Gastroenterol., 13 (37), 5003-5008, (2007) »PubMed
- 木村恒夫, 日本消化器病学会雑誌, 77 (2), 185-194, (1980) »DOI
- 土屋周二 他, 厚生省特定疾患消化吸収障害調査研究班 昭和57年度業績集, 99-104, (1982)
- 原泰寛 他, 福岡医誌, 65 (12), 933-940, (1974)
- 菅田文夫 他, 日本消化器病学会雑誌, 75 (4), 492-499, (1978) »DOI
- Igimi,H.et al., Gastroenterol.Jpn., 18 (2), 93-97, (1983) »PubMed
- 堀内至, 胆道, 2 (3), 239-247, (1988) »DOI
- Crosignani,A.et al., Hepatology., 14 (6), 1000-1007, (1991) »PubMed
- Terasaki,S.et al., Am.J.Gastroenterol., 86 (9), 1194-1199, (1991) »PubMed
- Yoshikawa,M.et al., Hepatology., 16 (2), 358-364, (1992) »PubMed
- Tanaka,H.et al., J.Immunol., 156 (4), 1601-1608, (1996) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
日本ジェネリック株式会社
お客さま相談室
〒108-0014
東京都港区芝五丁目33番11号
電話:0120-893-170
FAX:0120-893-172
製品情報問い合わせ先
日本ジェネリック株式会社
お客さま相談室
〒108-0014
東京都港区芝五丁目33番11号
電話:0120-893-170
FAX:0120-893-172
26. 製造販売業者等
26.1 製造販売元
日本ジェネリック株式会社
東京都港区芝五丁目33番11号