医薬品情報
| 総称名 | アデムパス |
|---|---|
| 一般名 | リオシグアト |
| 欧文一般名 | Riociguat |
| 製剤名 | リオシグアト錠 |
| 薬効分類名 | 可溶性グアニル酸シクラーゼ(sGC)刺激剤 |
| 薬効分類番号 | 2190 |
| ATCコード | C02KX05 |
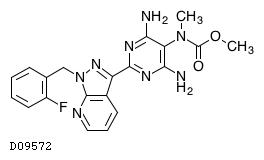
| KEGG DRUG |
D09572
リオシグアト
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年2月 改訂(第6版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アデムパス錠0.5mg | Adempas tablets 0.5mg | バイエル薬品 | 2190034F1027 | 685.9円/錠 | 劇薬, 処方箋医薬品注) |
| アデムパス錠1.0mg | Adempas tablets 1.0mg | バイエル薬品 | 2190034F2023 | 1371.7円/錠 | 劇薬, 処方箋医薬品注) |
| アデムパス錠2.5mg | Adempas tablets 2.5mg | バイエル薬品 | 2190034F3020 | 3429.3円/錠 | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
○外科的治療不適応又は外科的治療後に残存・再発した慢性血栓塞栓性肺高血圧症
5. 効能または効果に関連する注意
<効能共通>
5.1 本剤の使用にあたっては、最新の慢性血栓塞栓性肺高血圧症又は肺動脈性肺高血圧症に対する治療ガイドラインを参考に投与の要否を検討すること。
<肺動脈性肺高血圧症>
5.2 肺動脈性肺高血圧症のWHO機能分類クラスIVにおける有効性及び安全性は確立していない。
6. 用法及び用量
用量調節期
通常、成人にはリオシグアトとして1回1.0mg1日3回経口投与から開始する。2週間継続して収縮期血圧が95mmHg以上で低血圧症状を示さない場合には、2週間間隔で1回用量を0.5mgずつ増量するが、最高用量は1回2.5mg1日3回までとする。収縮期血圧が95mmHg未満でも低血圧症状を示さない場合は、現行の用量を維持するが、低血圧症状を示す場合には、1回用量を0.5mgずつ減量する。
用量維持期
用量調節期に決定した用量を維持する。用量維持期においても、最高用量は1回2.5mg1日3回までとし、低血圧症状を示すなど、忍容性がない場合には、1回用量を0.5mgずつ減量する。
7. 用法及び用量に関連する注意
7.2 投与間隔は約6〜8時間間隔とすることが望ましい。ただし、1回の服用を忘れた場合には、次回の服用時刻に1回用量を服用させる。
7.3 3日間以上投与が中断した場合、再開時には、開始時の用量を考慮し、「6.用法及び用量」に従い用量調節を行う。
8. 重要な基本的注意
8.1 本剤の投与により肺水腫の徴候がみられた場合には、肺静脈閉塞性疾患との関連性を疑い、投与を中止すること。[9.1.3参照]
8.2 本剤は血管を拡張して血圧を低下させる作用を有している。本剤の投与に際しては、血管拡張作用により患者が有害な影響を受ける状態(降圧剤投与中、安静時低血圧、血液量減少、重度の左室流出路閉塞、自律神経機能障害等)にあるかどうかを十分検討すること。
8.3 臨床試験において、めまい等が認められているので、高所作業、自動車の運転等危険を伴う機械を操作する際には注意させること。
8.4 特発性間質性肺炎に伴う症候性肺高血圧症を対象とした国際共同試験において、本剤投与群ではプラセボ投与群と比較して重篤な有害事象及び死亡が多く認められた。間質性肺病変を伴う肺動脈性肺高血圧症の患者に本剤を投与する場合は、間質性肺疾患の治療に精通した専門医に相談するなど、本剤投与によるリスクとベネフィットを考慮した上で、投与の可否を慎重に検討すること。[15.1参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 抗凝固療法中の患者
気道出血が起こる可能性が高くなるため、喀血が起こりやすく、重篤で致死的な喀血の危険性が高まる可能性がある。患者ごとに本剤投与のリスク・ベネフィットを定期的に評価すること。[11.1参照]
9.1.2 投与前の収縮期血圧が95mmHg未満の患者
過度の血圧低下が起こるおそれがある。本剤の投与に際しては、患者における治療上のリスク・ベネフィットを考慮して慎重に判断すること。国際共同第III相試験では除外されている。[7.1参照]
9.1.3 肺静脈閉塞性疾患の患者
本剤を投与しないことが望ましい。心血管系の状態を著しく悪化させるおそれがある。[8.1参照]
9.1.4 喫煙者
禁煙させることが望ましい。非喫煙者に比べて本剤の血漿中濃度が低下する。[16.6.1参照]
9.2 腎機能障害患者
9.2.1 重度の腎機能障害患者又は透析中の患者
9.2.2 軽度又は中等度の腎機能障害患者
9.3 肝機能障害患者
9.3.1 重度の肝機能障害患者
Child-Pugh分類Cの患者には投与しないこと。血中濃度が著しく上昇するおそれがある。国際共同第III相試験では除外されている。[2.3参照]
9.3.2 軽度又は中等度の肝機能障害患者
9.4 生殖能を有する者
妊娠する可能性のある女性に以下について説明及び指導し、必要に応じて妊娠検査を行い、妊娠していないことを確認すること。[9.5参照]
・妊娠中に本剤を服用した場合に胎児に影響を及ぼす危険性があること。
・本剤の服用開始後は確実な避妊法を用いること。
・妊娠した場合若しくはその疑いがある場合には、直ちに医師に連絡すること。
9.5 妊婦
9.6 授乳婦
授乳しないことが望ましい。動物実験(ラット、経口投与)で乳汁中に投与量の2.2%が移行することが報告されている3)。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
10. 相互作用
相互作用序文
本剤は、主にCYP1A1で代謝され、一部はCYP3Aにより代謝される。本剤はP-糖タンパク/乳癌耐性タンパク(P-gp/BCRP)の基質である。また、本剤及び主代謝物M-1はCYP1A1阻害作用がある。
薬物代謝酵素用語
CYP1A1
薬物代謝酵素用語
CYP3A
薬物代謝酵素用語
P-糖タンパク(P-gp)
薬物代謝酵素用語
乳癌耐性タンパク(BCRP)
10.1 併用禁忌
| 硝酸剤及びNO供与剤 ニトログリセリン、亜硝酸アミル、硝酸イソソルビド、ニコランジル等 [2.5、16.7.1参照] | 本剤単回投与後にニトログリセリンを舌下投与したときに、プラセボ投与に比べて有意な収縮期血圧の低下が認められている。 | 細胞内cGMP濃度が増加し、降圧作用を増強する。 |
| PDE5阻害剤 シルデナフィルクエン酸塩(バイアグラ、レバチオ) タダラフィル含有製剤(シアリス、アドシルカ、ザルティア、ユバンシ) バルデナフィル塩酸塩水和物 [2.6、16.7.2参照] | 症候性低血圧を起こすことがある。 | 細胞内cGMP濃度が増加し、全身血圧に相加的な影響を及ぼすおそれがある。 |
| 可溶性グアニル酸シクラーゼ(sGC)刺激薬 ベルイシグアト(ベリキューボ) [2.7参照] | 症候性低血圧を起こすおそれがある。 | 細胞内cGMP濃度が増加し、降圧作用を増強するおそれがある。 |
10.2 併用注意
| CYP1A1阻害剤 エルロチニブ、ゲフィチニブ [7.1参照] | 本剤の血中濃度が上昇するおそれがあるので、強いCYP1A1阻害薬との併用には注意すること。 | CYP1A1阻害により本剤のクリアランスが低下する。 |
| リトナビル含有製剤 アタザナビル リルピビリン含有製剤 コビシスタット含有製剤 アバカビル含有製剤 ダルナビル含有製剤 ホスアンプレナビル [7.1参照] | 本剤の血中濃度が上昇するおそれがある4)。 これらの薬剤を投与中の患者に本剤の投与を開始する場合は、1回0.5mg1日3回からの開始も考慮すること。 本剤を投与中にこれらの薬剤を開始する場合は、本剤の減量を考慮すること。 | これら薬剤のCYP1A1及び/又はCYP3A阻害により本剤のクリアランスが低下する。 |
| イトラコナゾール、ボリコナゾール [7.1、16.7.3参照] | 本剤の血中濃度が上昇するおそれがある。 これらの薬剤を投与中の患者に本剤の投与を開始する場合は、1回0.5mg1日3回からの開始も考慮すること。 本剤を投与中にこれらの薬剤を開始する場合は、本剤の減量を考慮すること。 | これら薬剤のCYP1A1及び/又はCYP3A阻害により本剤のクリアランスが低下する。 |
| エンシトレルビル フマル酸、ロナファルニブ [7.1参照] | 本剤の血中濃度が上昇するおそれがある。 これらの薬剤を投与中の患者に本剤の投与を開始する場合は、1回0.5mg1日3回からの開始も考慮すること。 本剤を投与中にこれらの薬剤を開始する場合は、本剤の減量を考慮すること。 | これらの薬剤のCYP3A阻害により本剤のクリアランスが低下する。 |
| CYP1A1で代謝される薬剤 イストラデフィリン、グラニセトロン、エルロチニブ | これら薬剤の血中濃度が上昇するおそれがある。 | 本剤及びM-1のCYP1A1阻害によりこれら薬剤のクリアランスが低下する。 |
| シクロスポリン [7.1参照] | 本剤の血中濃度が上昇するおそれがあるので、強いP-gp/BCRP阻害薬との併用には注意すること。 | P-gp/BCRP阻害により本剤のクリアランスが低下する。 |
| 制酸剤 水酸化アルミニウム/水酸化マグネシウム合剤等 [16.7.4参照] | 水酸化アルミニウム/水酸化マグネシウム合剤との併用により本剤のAUCが34%減少し、Cmaxは56%低下した。 制酸剤は本剤投与後1時間以上経過してから服用させること。 | 消化管内pHの上昇により本剤のバイオアベイラビリティが低下する。 |
| CYP3A阻害剤 クラリスロマイシン、エリスロマイシン等 [7.1、16.7.7参照] | 本剤の血中濃度が上昇するおそれがあるので、強いCYP3A阻害薬との併用には注意すること。 | CYP3A阻害により本剤のクリアランスが低下する。 |
| ボセンタン [16.7.5参照] | ボセンタンを併用した肺動脈性肺高血圧症患者において、本剤のAUCが27%減少した。 | CYP3Aの誘導により本剤のクリアランスが上昇する。 |
| CYP3A誘導薬 フェニトイン、カルバマゼピン、フェノバルビタール、セイヨウオトギリソウ(St.John's Wort、セント・ジョーンズ・ワート)含有食品等 | 強いCYP3A誘導薬との併用により本剤の血中濃度が低下する可能性がある。 | CYP3A誘導により本剤のクリアランスが上昇する。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 喀血(0.2%)、肺出血(頻度不明)[9.1.1参照]
11.2 その他の副作用
| 10%以上 | 1〜10%未満 | 1%未満 | 頻度不明 | |
| 精神神経系 | 頭痛、浮動性めまい | |||
| 感覚器 | 鼻閉 | 鼻出血 | ||
| 消化器 | 消化不良 | 悪心、胃・腹部痛、下痢、嘔吐、胃食道逆流、便秘、嚥下障害、胃炎、腹部膨満 | 胃腸炎 | |
| 循環器 | 低血圧、動悸、潮紅、失神 | |||
| 呼吸器 | 呼吸困難 | |||
| 血液 | 貧血 | |||
| その他 | 末梢性浮腫、疲労、顔面浮腫 |
13. 過量投与
13.1 症状
過度の血圧低下等が起こる可能性がある。
13.2 処置
特異的な解毒薬はない。また、本剤はタンパク結合率が高いので、血液透析による除去は期待できない。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
適応外であるが、特発性間質性肺炎に伴う症候性肺高血圧症患者147例を対象とした国際共同プラセボ対照比較試験において、プラセボ投与群に比較して本剤投与群では重篤な有害事象及び死亡が多く認められ、試験が早期に中止された。主要投与期(二重盲検下)では、重篤な有害事象は本剤投与群で73例中27例(37.0%)、プラセボ投与群で74例中17例(23.0%)、死亡は本剤投与群で73例中8例(11.0%)、プラセボ投与群で74例中3例(4.1%)認められた。長期継続投与期(二重盲検期及び非盲検期)では、重篤な有害事象は本剤投与継続群で32例中12例(37.5%)、プラセボから本剤への切替え群で38例中21例(55.3%)、死亡は本剤投与継続群で32例中1例(3.1%)、プラセボから本剤への切替え群で38例中8例(21.1%)認められた。[8.4参照]
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
日本人健康成人男性27例に本剤0.5、1.0及び2.5mgを空腹時単回経口投与したとき、本剤は速やかに吸収され、血漿中リオシグアト濃度は投与1〜1.5時間後にピークに達し、Cmax及びAUCは用量に応じて増加した5)。
| 投与量 | Cmax(μg/L) | tmax※(h) | AUC(μg・h/L) | t1/2(h) |
| 0.5mg | 22.9/31.5 | 1.0(0.5-1.5) | 106/56.4 | 4.15/46.1 |
| 1.0mg | 49.7/23.6 | 1.0(0.5-1.5) | 272/101 | 6.33/86.4 |
| 2.5mg | 126/17.1 | 1.5(0.75-4.0) | 824/70.9 | 7.59/47.2 |
16.1.2 反復投与
日本人健康成人男性15例に本剤1.0及び1.5mgを1日3回7日間反復投与したとき、血漿中リオシグアト濃度は、投与開始7日後までに定常状態に達した。定常状態におけるCmaxは初回投与に比べて1.18〜1.25倍増加したが、AUCはほとんど変動しなかった6)。
| 投与量 | Cmax(μg/L) | tmax※(h) | AUC(0-7)(μg・h/L) | t1/2(h) |
| 1.0mg 1日3回 | 59.9/35.8 | 1.50(0.5-4.0) | 325/40.3 | 9.69/28.7 |
| 1.5mg 1日3回 | 101/27.6 | 1.50(0.5-4.0) | 516/29.3 | 9.17/25.7 |
16.1.3 母集団薬物動態解析
母集団薬物動態の結果、国際共同第III相試験に組み入れられた慢性血栓塞栓性肺高血圧症患者及び肺動脈性肺高血圧症患者における定常状態のAUCは、健康成人の約3倍と推定された。
16.2 吸収
16.2.1 バイオアベイラビリティ
本剤の絶対的バイオアベイラビリティは94%であった(外国人データ)。
16.2.2 食事の影響
健康成人男性23例に本剤2.5mgを高脂肪食・高カロリー食摂取後に単回経口投与したとき、空腹時と比較して、本剤のCmaxはおよそ35%低下したが、AUCは低下しなかった(外国人データ)。
16.3 分布
本剤の定常状態での分布容積は30Lである。本剤の血漿タンパク結合率は約95%であり、主に血清アルブミン及びα1-酸性糖タンパクと結合した(in vitro)。
16.4 代謝
本剤は、主にCYP1A1、CYP2J2及びCYP3Aによって脱メチル化され、主代謝物M-1が生成される(in vitro)。その後、薬理活性のないN-グルクロン酸抱合体に代謝される。肝臓及び肺において主代謝物の生成に関わるCYP1A1は、タバコの煙等に含まれる多環芳香族炭化水素によって誘導されることが報告されている。
16.6 特定の背景を有する患者
16.6.1 喫煙者
16.6.2 腎機能障害患者
16.6.3 肝機能障害患者
16.6.4 高齢者
16.7 薬物相互作用
16.7.1 ニトログリセリン
16.7.2 シルデナフィルクエン酸塩
16.7.3 ケトコナゾール(経口剤:国内未発売)
16.7.4 制酸剤
16.7.5 ボセンタン
16.7.6 オメプラゾール
健康成人12例を対象としたクロスオーバー試験により本剤2.5mgを単独で又はオメプラゾール40mgを1日1回4日間投与後に空腹時単回投与した。オメプラゾール併用による本剤のCmax及びAUCの低下はそれぞれ35%及び26%であった16)(外国人データ)。
16.7.7 クラリスロマイシン
16.7.8 その他の薬剤
アセチルサリチル酸、ミダゾラム、ワルファリンの併用において、臨床的に意味のある相互作用はみられなかった。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<慢性血栓塞栓性肺高血圧症>
17.1.1 国際共同第III相試験
肺動脈血栓内膜摘除術不適応又は本手術後に残存・再発した慢性血栓塞栓性肺高血圧症患者261例(日本人16例を含む)を対象とした比較試験において、本剤(用量調節法:被験者の血圧、忍容性等に応じて1.0〜2.5mgを1日3回8週間投与し、8週時点の用量をさらに8週間投与)又はプラセボを16週間投与した。その結果、有効性主要評価項目である6分間歩行距離のベースラインからの変化は、プラセボ投与群と比べ本剤投与群において有意に大きかった(p<0.0001、層別Wilcoxon検定)。さらに、副次的評価項目[肺血管抵抗、ヒト脳性ナトリウム利尿ペプチド前駆体N端フラグメント(NT-proBNP)、WHO機能分類]においても、本剤投与群ではプラセボ投与群に比べて有意な改善効果を示し、6分間歩行距離と一貫した結果であった18)。
| 評価項目(単位) | 本剤投与群 [症例数] | プラセボ投与群 [症例数] |
| 主要評価項目 | ||
| 6分間歩行距離(m) 平均値±SD | 38.9±79.3 [173] | −5.5±84.3 [88] |
| 投与群間の比較:45.69(24.74〜66.63)※1 p<0.0001※2 | ||
| 主な副次的評価項目 | ||
| 肺血管抵抗(dynes・sec・cm−5) 平均値±SD | −225.7±247.5 [151] | 23.1±273.5 [82] |
| 投与群間の比較:−246.43(−303.33〜−189.53)※1 p<0.0001※2 | ||
| NT-proBNP(pg/mL) 平均値±SD | −290.7±1716.9 [150] | 76.4±1446.6 [73] |
| 投与群間の比較:−443.99(−842.95〜−45.03)※1 p<0.0001※2 | ||
| WHO機能分類※3 症例数(%) | ||
| 改善 | 57(32.9%) | 13(14.9%) |
| 不変 | 107(61.8%) | 68(78.2%) |
| 悪化 | 9(5.2%) | 6(6.9%) |
| 投与群間の比較:p=0.0026※2 | ||
日本人部分集団は少数例(本剤投与群:11例、プラセボ投与群:5例)であり、ばらつきが大きく、主要評価項目である6分間歩行距離のベースラインからの変化量(平均値±標準偏差)は、本剤投与群で31.9±148.6m(中央値:64.0m)、プラセボ投与群で36.0±36.4m(中央値:14.0m)であった。しかしながら、主な副次的評価項目である肺血管抵抗の変化量は、本剤投与群で−129.6±122.5(dynes・sec・cm−5)、プラセボ投与群では15.7±120.8(dynes・sec・cm−5)であり、全体集団と同様に血行動態改善効果が認められた18)。
17.1.2 国際共同第III相試験(長期継続投与試験)
プラセボ対照二重盲検比較試験に参加した慢性血栓塞栓性肺高血圧症患者237例を対象に、本剤0.5〜2.5mg1日3回の用量で適宜漸増する長期継続投与試験を実施した。237例(日本人14例を含む)を対象とした中間解析の結果、6分間歩行距離のベースラインからの平均変化量は、6ヵ月後(218例)で56.5m、9ヵ月後(215例)で49.7m、12ヵ月後(172例)で51.3m、18ヵ月後(114例)で51.1mであった。プラセボ対照二重盲検比較試験で認められた本剤投与による6分間歩行距離の改善は、長期継続投与においても維持されていることが示された。日本人部分集団(14例)においては、6分間歩行距離のベースラインからの平均変化量は、6ヵ月後(11例)で86.3m、9ヵ月後(12例)で80.9m、12ヵ月後(12例)で62.9m、18ヵ月後(9例)で89.6mであった19)。
<肺動脈性肺高血圧症>
17.1.3 国際共同第III相試験
肺動脈性肺高血圧症患者443例(日本人26例を含む)を対象とした比較試験において、本剤[用量調節法1(用量調節群):被験者の血圧、忍容性等に応じて1.0〜2.5mgを1日3回8週間投与し、8週時点の用量をさらに4週間投与、用量調節法2(1.5mg群、探索的用量群〔63例〕):被験者の血圧、忍容性等に応じて最大1.5mgまでを1日3回8週間投与し、8週時点の用量をさらに4週間投与]又はプラセボを12週間投与した。その結果、有効性主要評価項目である6分間歩行距離のベースラインからの変化は、プラセボ投与群と比べ用量調節群において有意に大きかった(p<0.0001、層別Wilcoxon検定)。さらに、副次的評価項目[肺血管抵抗、NT-proBNP、WHO機能分類]においても、用量調節群ではプラセボ投与群に比べて有意な改善効果を示し、6分間歩行距離と一貫した結果であった20)。
| 評価項目(単位) | 本剤投与群 [症例数] | プラセボ投与群 [症例数] |
| 主要評価項目 | ||
| 6分間歩行距離(m) 平均値±SD | 29.6±65.8 [254] | −5.6±85.5 [126] |
| 投与群間の比較:35.78(20.06〜51.51)※1 p<0.0001※2 | ||
| 主な副次的評価項目 | ||
| 肺血管抵抗(dynes・sec・cm−5) 平均値±SD | −223.3±260.1 [232] | −8.9±316.6 [107] |
| 投与群間の比較:−225.72(−281.37〜−170.08)※1 p<0.0001※2 | ||
| NT-proBNP(pg/mL) 平均値±SD | −197.9±1721.3 [228] | 232.4±1011.1 [106] |
| 投与群間の比較:−431.81(−781.52〜−82.10)※1 p<0.0001※2 | ||
| WHO機能分類※3 症例数(%) | ||
| 改善 | 53(20.9%) | 18(14.4%) |
| 不変 | 192(75.6%) | 89(71.2%) |
| 悪化 | 9(3.5%) | 18(14.4%) |
| 投与群間の比較:p=0.0033※2 | ||
日本人部分集団は少数例(用量調節群:16例、プラセボ投与群:7例、1.5mg群:3例)であり、ばらつきが大きく、主要評価項目である6分間歩行距離のベースラインからの変化量(平均値±標準偏差)は、用量調節群で21.4±35.7m(中央値:23.0m)、プラセボ投与群で40.1±49.4m(中央値:32.0m)であり、明らかな差は認められなかった。しかしながら、主な副次的評価項目である肺血管抵抗の変化量は、用量調節群で−160.6±161.7(dynes・sec・cm−5)、プラセボ投与群では−73.9±163.1(dynes・sec・cm−5)であり、全体集団と同様に、本剤投与による血行動態改善効果が認められた20)。
17.1.4 国際共同第III相試験(長期継続投与試験)
プラセボ対照二重盲検比較試験に参加した肺動脈性肺高血圧症患者396例を対象に、本剤0.5〜2.5mg1日3回の用量で適宜漸増する長期継続投与試験を実施した。396例(日本人21例を含む)を対象とした中間解析の結果、6分間歩行距離のベースラインからの平均変化量は、6ヵ月後(366例)で52.8m、9ヵ月後(354例)で52.2m、12ヵ月後(327例)で51.4m、18ヵ月後(245例)で49.6mであった。プラセボ対照二重盲検比較試験で認められた本剤投与による6分間歩行距離の改善は、長期継続投与においても維持されていることが示された。日本人部分集団(21例)においては、6分間歩行距離のベースラインからの平均変化量は、6ヵ月後(18例)で60.8m、9ヵ月後(18例)で57.3m、12ヵ月後(18例)で50.2m、18ヵ月後(10例)で69.7mであった21)。
18. 薬効薬理
18.1 作用機序
内因性一酸化窒素(NO)に対する可溶性グアニル酸シクラーゼ(sGC)の感受性を高める作用とNO非依存的に直接sGCを刺激する作用の2つの機序を介し、環状グアノシン一リン酸(cGMP)の産生を促進する22)。
18.2 肺高血圧症モデルに対する作用
低酸素誘発肺高血圧症マウスモデル及びモノクロタリン誘発肺高血圧症ラットモデルにおいて、経口投与で右室収縮期圧の上昇、右室肥大及び肺血管リモデリングを抑制した22)。
19. 有効成分に関する理化学的知見
19.1. リオシグアト
22. 包装
<アデムパス錠0.5mg>
100錠[10錠(PTP)×10]
<アデムパス錠1.0mg>
100錠[10錠(PTP)×10]
<アデムパス錠2.5mg>
100錠[10錠(PTP)×10]
23. 主要文献
- 社内資料:ラットにおける胚・胎児発生に関する毒性試験(2014年1月17日承認、CTD2.6.6.6.2)
- 社内資料:ウサギにおける胚・胎児発生に関する毒性試験(2014年1月17日承認、CTD2.6.6.6.3)
- 社内資料:ラットにおける乳汁中分泌に関する試験(2014年1月17日承認、CTD2.6.4.6.4)
- DeJesus E,et al., Pulm Circ., 9, 1-10, (2019)
- 社内資料:健康成人における単回投与試験(2014年1月17日承認、CTD2.7.6.9)
- 社内資料:健康成人における反復投与試験(2014年1月17日承認、CTD2.7.6.10)
- 社内資料:外国人健康被験者における薬物動態の統合解析レポート(2014年1月17日承認、CTD2.7.2.3.4)
- 社内資料:外国人腎障害患者を対象とした臨床薬理試験(2014年1月17日承認、CTD2.7.6.17)
- 社内資料:外国人肝障害患者を対象とした臨床薬理試験(2014年1月17日承認、CTD2.7.6.19)
- 社内資料:外国人高齢者における薬物動態試験(2014年1月17日承認、CTD2.7.6.15)
- 社内資料:ニトログリセリンとの薬物相互作用試験(2014年1月17日承認、CTD2.7.2.2.3.3.3)
- 社内資料:シルデナフィルクエン酸塩との薬物相互作用試験(2014年1月17日承認、CTD2.7.2.2.3.3.4)
- 社内資料:ケトコナゾールとの薬物相互作用試験(2014年1月17日承認、CTD2.7.2.2.3.2.1)
- 社内資料:制酸剤との薬物相互作用試験(2014年1月17日承認、CTD2.7.2.2.3.1.2)
- 社内資料:肺動脈性肺高血圧症患者における第III相試験の母集団PK/PD解析レポート(2014年1月17日承認、CTD2.7.2.3.4.2.2.2.3)
- 社内資料:オメプラゾールとの薬物相互作用試験(2014年1月17日承認、CTD2.7.2.2.3.1.1)
- 社内資料:クラリスロマイシンとの薬物相互作用試験(2014年1月17日承認、CTD2.7.2.2.3.2.2)
- 社内資料:慢性血栓塞栓性肺高血圧症患者におけるプラセボ対照二重盲検比較試験(2014年1月17日承認、CTD2.7.6.36)
- 社内資料:慢性血栓塞栓性肺高血圧症患者における長期継続投与試験(2014年1月17日承認、CTD2.7.6.37)
- 社内資料:肺動脈性肺高血圧症患者におけるプラセボ対照二重盲検比較試験(2015年2月20日承認、CTD2.7.6.39)
- 社内資料:肺動脈性肺高血圧症患者における長期継続投与試験(2015年2月20日承認、CTD2.7.6.40)
- Schermuly RT,et al., Eur Respir J., 32, 881-891, (2008) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
MSD株式会社
MSDカスタマーサポートセンター
東京都千代田区九段北1-13-12
電話:医療関係者の方:フリーダイヤル 0120-024-961
製品情報問い合わせ先
MSD株式会社
MSDカスタマーサポートセンター
東京都千代田区九段北1-13-12
電話:医療関係者の方:フリーダイヤル 0120-024-961
26. 製造販売業者等
26.1 製造販売元
バイエル薬品株式会社
大阪市北区梅田二丁目4番9号
26.2 販売提携
MSD株式会社
東京都千代田区九段北1-13-12