医薬品情報
| 総称名 | シングレア |
|---|---|
| 一般名 | モンテルカストナトリウム |
| 欧文一般名 | Montelukast Sodium |
| 製剤名 | モンテルカストナトリウム錠・モンテルカストナトリウム口腔内崩壊錠 |
| 薬効分類名 | ロイコトリエン受容体拮抗薬 気管支喘息・アレルギー性鼻炎治療薬 |
| 薬効分類番号 | 4490 |
| ATCコード | R03DC03 |
| KEGG DRUG |
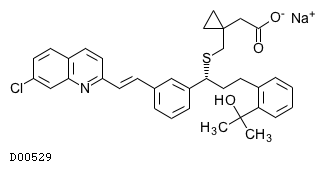
D00529
モンテルカストナトリウム
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年4月 改訂(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| シングレア錠5mg | SINGULAIR Tablets 5mg | オルガノン | 4490026F3039 | 46円/錠 | |
| シングレア錠10mg | SINGULAIR Tablets 10mg | オルガノン | 4490026F2059 | 41.9円/錠 | |
| シングレアOD錠10mg | SINGULAIR OD Tablets 10mg | オルガノン | 4490026F4035 | 41.9円/錠 |
2. 禁忌
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
6. 用法及び用量
<気管支喘息>
通常、成人にはモンテルカストとして10mgを1日1回就寝前に経口投与する。
<アレルギー性鼻炎>
通常、成人にはモンテルカストとして5〜10mgを1日1回就寝前に経口投与する。
7. 用法及び用量に関連する注意
<効能共通>
7.1 気管支喘息及びアレルギー性鼻炎を合併し本剤を気管支喘息の治療のために用いる成人患者には、モンテルカストとして10mgを1日1回就寝前に経口投与すること。
7.2 モンテルカストフィルムコーティング錠はモンテルカストチュアブル錠と生物学的に同等でなく、モンテルカストチュアブル錠はモンテルカストフィルムコーティング錠と比較してバイオアベイラビリティが高いため、モンテルカストフィルムコーティング錠5mgとモンテルカストチュアブル錠5mgをそれぞれ相互に代用しないこと1)。
<気管支喘息>
8. 重要な基本的注意
<効能共通>
8.1 本剤投与によりステロイド維持量を減量し得た患者で、本剤の投与を中止する場合は、原疾患再発のおそれがあるので注意すること。
8.2 本剤との因果関係は明らかではないが、うつ病、自殺念慮、自殺及び攻撃的行動を含む精神症状が報告されているので、患者の状態を十分に観察すること。[15.1参照]
8.3 本剤を含めロイコトリエン拮抗剤使用時に好酸球性多発血管炎性肉芽腫症様の血管炎を生じたとの報告がある。これらの症状は、おおむね経口ステロイド剤の減量・中止時に生じている。本剤使用時は、特に好酸球数の推移及びしびれ、四肢脱力、発熱、関節痛、肺の浸潤影等の血管炎症状に注意すること。
8.4 本剤投与により効果が認められない場合には、漫然と長期にわたり投与しないように注意すること。
<気管支喘息>
8.5 本剤は、喘息の悪化時ばかりでなく、喘息が良好にコントロールされている場合でも継続して服用するよう、患者に十分説明しておくこと。
8.6 本剤は気管支拡張剤、ステロイド剤等と異なり、すでに起こっている喘息発作を緩解する薬剤ではないので、このことは患者に十分説明しておく必要がある。
8.7 本剤を投与中、大発作をみた場合は、気管支拡張剤あるいはステロイド剤を投与する必要がある。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 長期ステロイド療法を受けている患者
本剤投与によりステロイドの減量をはかる場合は十分な管理下で徐々に行うこと。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。海外の市販後において、妊娠中に本剤を服用した患者から出生した新生児に先天性四肢奇形がみられたとの報告がある。これらの妊婦のほとんどは妊娠中、他の喘息治療薬も服用していた。本剤とこれらの事象の因果関係は明らかにされていない。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で乳汁中への移行が報告されている。
9.7 小児等
10. 相互作用
相互作用序文
本剤は、主として薬物代謝酵素チトクロームP450(CYP)3A4で代謝される。[16.4参照]
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| フェノバルビタール [16.7.1参照] | 本剤の作用が減弱するおそれがある。 | フェノバルビタールがCYP3A4を誘導し、本剤の代謝が促進される。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 アナフィラキシー(頻度不明)
11.1.2 血管浮腫(頻度不明)
11.1.3 劇症肝炎、肝炎、肝機能障害、黄疸(いずれも頻度不明)
11.1.4 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、多形紅斑(いずれも頻度不明)
11.1.5 血小板減少(頻度不明)
初期症状として、紫斑、鼻出血、歯肉出血等の出血傾向があらわれることがある。
11.2 その他の副作用
| 0.1〜5%未満注) | 頻度不明 | |
| 過敏症 | 皮疹 | そう痒、蕁麻疹、肝臓の好酸球浸潤 |
| 精神神経系 | 頭痛、傾眠 | 異夢、易刺激性、情緒不安、痙攣、不眠、幻覚、めまい、感覚異常(しびれ等)、激越、振戦、夢遊症、失見当識、集中力低下、記憶障害、せん妄、強迫性症状 |
| 呼吸器 | 肺好酸球増多症 | |
| 消化器系 | 下痢、腹痛、胃不快感、嘔気、胸やけ、嘔吐、便秘 | 消化不良、口内炎 |
| 肝臓 | 肝機能異常、AST上昇、ALT上昇、Al-P上昇、γ-GTP上昇、総ビリルビン上昇 | |
| 筋骨格系 | 筋痙攣を含む筋痛、関節痛 | |
| その他 | 口渇、尿潜血、血尿、尿糖、浮腫、倦怠感、白血球数増加、尿蛋白、トリグリセリド上昇 | 出血傾向(鼻出血、紫斑等)、挫傷、動悸、頻尿、発熱、脱力、疲労、脱毛、遺尿 |
14. 適用上の注意
14.1 薬剤交付時の注意
<製剤共通>
14.1.1 食事の有無にかかわらず投与できる。
<フィルムコーティング錠>
14.1.2 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
<OD錠>
14.1.3 以下の点について指導すること。
・ブリスターシートから取り出して服用すること。ブリスター包装の誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
・ブリスターシートからの取り出しは、裏面のシートを完全に剥がした後、錠剤をていねいに取り出すこと。OD錠は錠剤と比べて性質上柔らかく、割れることがあるので、シートを剥がさずに押し出さないこと。欠けや割れが生じた場合は全量服用すること。
・吸湿性を有するため、使用直前にブリスターシートから取り出すこと。
14.1.4 本剤は舌の上にのせて唾液を浸潤させると崩壊するため、水なしで服用可能である。また、水で服用することもできる。
15. その他の注意
15.1 臨床使用に基づく情報
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人8例にモンテルカストフィルムコーティング錠10mgを空腹時に単回経口投与したとき、モンテルカストの血漿中濃度は投与3.9時間後に最高値(Cmax)526ng/mLに達し、消失半減期(t1/2)4.6時間で消失した(図1)。Cmax及び血漿中濃度−時間曲線下面積(AUC0-∞)は2〜50mg注)の範囲で投与量に比例して増大した(表1)4)。
図1 健康成人におけるモンテルカストフィルムコーティング錠10mg経口投与後の血漿中濃度推移
| 投与量(mg) | Tmax(hr) | Cmax(ng/mL) | t1/2(hr) | AUC0-∞(ng・hr/mL) |
| 2 | 2.8±0.9 | 108±23.1 | 4.34±0.76 | 753±242 |
| 10 | 3.9±1.5 | 526±138 | 4.57±0.39 | 3840±906 |
| 50 | 3.6±1.2 | 2550±1250 | 4.63±0.41 | 19100±7910 |
16.1.2 反復投与
健康成人8例にモンテルカストフィルムコーティング錠10mgを1日1回7日間反復経口投与したときのCmaxは1日目が580±136ng/mL、7日目が660±124ng/mLであったが、投与7日目のAUC0-24hrは投与1日目のAUC0-∞と一致しており、連続投与による蓄積性は認められなかった4)。
16.1.3 生物学的同等性試験
クロスオーバー法により健康成人男性(120例)に空腹時、モンテルカストOD錠10mg(1錠、水なし若しくは水あり)又はモンテルカストフィルムコーティング錠10mg(1錠、水あり)でそれぞれ単回経口投与したとき、モンテルカストの薬物動態パラメータ及び血漿中濃度推移は以下のとおりであった。得られた薬物動態パラメータ(Cmax及びAUC0-t)の幾何平均比について、90%信頼区間法にて統計解析を行った結果、Log(0.80)〜Log(1.25)の範囲内であり、モンテルカストOD錠10mgは水なし又は水とともに服用した場合のいずれにおいても、モンテルカストフィルムコーティング錠10mg(水あり)と生物学的に同等であることが示された5)。
| 飲水 | N | Cmax(ng/mL) | AUC0-t(ng・hr/mL) | Tmax(hr) | t1/2(hr) | |
| OD錠10mg (算術平均±標準偏差) | なし | 120 | 588±129 | 3917±1001 | 2.4±1.1 | 4.6±2.4 |
| あり | 119 | 531±138 | 3638±1036 | 2.1±0.9 | 4.2±0.5 | |
| フィルムコーティング錠10mg (算術平均±標準偏差) | あり | 119 | 495±105 | 3517±878 | 3.6±1.4 | 4.2±0.6 |
| OD錠10mg(水なし)/フィルムコーティング錠10mg幾何平均比 (90%信頼区間) | 1.17 (1.10-1.24) | 1.10 (1.05-1.15) | − | − | ||
| OD錠10mg(水あり)/フィルムコーティング錠10mg幾何平均比 (90%信頼区間) | 1.06 (1.01-1.11) | 1.03 (0.99-1.07) | − | − | ||
図2 健康成人におけるOD錠10mg及びフィルムコーティング錠10mg経口投与後の血漿中濃度推移(空腹時)
16.2 吸収
16.2.1 食事の影響
健康成人8例にモンテルカストフィルムコーティング錠10mgを食後投与したとき、空腹時に比べてAUC0-∞は3420±598ng・hr/mLから4240±1120ng・hr/mLに24%増加した。最高血漿中濃度到達時間(Tmax)(空腹時:4.0±1.1時間、食後:4.4±1.8時間)及びt1/2(空腹時:4.31±0.58時間、食後:4.30±0.35時間)には差がなかった4)。
16.2.2 生物学的利用率
健康成人における生物学的利用率は、58〜67%であった6)(外国人データ)。
16.3 分布
16.3.1 蛋白結合率
モンテルカストのヒト血漿蛋白との結合率は99.6%であった。モンテルカストは生理的な濃度のアルブミン及びα1-酸性糖蛋白質の両方に99%以上結合した7)(in vitro)。
16.4 代謝
ヒトにおけるモンテルカストの主要代謝物は側鎖メチル基の水酸化体及びベンジル位メチレン基の水酸化体であった。これら代謝物の生成にはそれぞれチトクロームP450(CYP)の分子種であるCYP2C8/2C9及び3A4が関与しており、CYP2C8がモンテルカストの主要代謝酵素であった。[10.参照]
更に側鎖メチル基の水酸化体はカルボン酸体まで酸化的代謝を受けることが確認されている。In vitro試験により治療時の血漿中濃度では、モンテルカストはCYP3A4、2C9、1A2、2A6、2C19又は2D6を阻害しないことが示された8)9)10)11)。
また、in vitro試験によりモンテルカストはCYP2C8を阻害することが示されたが、in vivoにおいてはモンテルカストは主にCYP2C8で代謝される代表的な薬剤であるロシグリタゾンとの臨床薬物相互作用試験で、CYP2C8を阻害しないことが示された12)(外国人データ)。したがって、モンテルカストはCYP2C8で代謝される薬剤(パクリタキセル等)の代謝に影響を及ぼさないと考えられる。
更に側鎖メチル基の水酸化体はカルボン酸体まで酸化的代謝を受けることが確認されている。In vitro試験により治療時の血漿中濃度では、モンテルカストはCYP3A4、2C9、1A2、2A6、2C19又は2D6を阻害しないことが示された8)9)10)11)。
また、in vitro試験によりモンテルカストはCYP2C8を阻害することが示されたが、in vivoにおいてはモンテルカストは主にCYP2C8で代謝される代表的な薬剤であるロシグリタゾンとの臨床薬物相互作用試験で、CYP2C8を阻害しないことが示された12)(外国人データ)。したがって、モンテルカストはCYP2C8で代謝される薬剤(パクリタキセル等)の代謝に影響を及ぼさないと考えられる。
16.5 排泄
16.5.1 健康成人にモンテルカストカプセル剤400mg注)を単回経口投与したとき尿中に未変化体は検出されなかった4)。
16.5.2 健康成人に14C標識モンテルカストカプセル剤102mg注)を単回経口投与した後5日間の糞中及び尿中放射能排泄率はそれぞれ約86%及び0.1%であった13)(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 肝機能障害患者
軽度から中等度の肝機能障害のある肝硬変患者にモンテルカストフィルムコーティング錠10mgを単回経口投与したとき、4.0時間後にCmax 313ng/mLに達し、t1/2 8.6時間で消失した。t1/2は健康成人の4.7時間に比べて遅くなり、AUC0-∞は2248.7±812.1ng・hr/mLから3167.2±1300.5ng・hr/mLに41%増加した14)(外国人データ)。
16.6.2 高齢者
健康高齢者(65歳〜73歳)にモンテルカストフィルムコーティング錠10mgを単回経口投与したとき、2.8時間後にCmax 495ng/mLに達し、t1/2 6.6時間で消失した。高齢者のAUC0-∞(3423.2±1344.7ng・hr/mL)は健康非高齢者(20歳〜48歳)のAUC0-∞(3624.0±1257.8ng・hr/mL)と比較して有意差はなかった15)(外国人データ)。
16.7 薬物相互作用
16.7.1 フェノバルビタール
16.7.2 テオフィリン
健康成人にモンテルカストカプセル剤を高用量(200mg注)を1日1回6週間反復あるいは1日3回8日間反復)で経口投与し、テオフィリンの経口投与(250mg単回)あるいは静脈内投与(5mg/kg単回)を併用したとき、血漿中テオフィリン濃度の低下が認められたが、モンテルカストフィルムコーティング錠10mg(10日間反復)の経口投与とテオフィリン5mg/kg(単回)の静脈内投与の併用では血漿中テオフィリン濃度の変化は認められなかった17)(外国人データ)。
16.7.3 プレドニゾン、プレドニゾロン
健康成人にモンテルカストカプセル剤200mg注)(6週間反復)とプレドニゾン20mg(単回)を経口投与により併用したとき、プレドニゾンのAUC0-∞がプラセボ群と比較して有意に低下したが、同一被験者のモンテルカストカプセル剤200mg注)投与前後の比較では変化はなく、活性代謝物であるプレドニゾロンの薬物動態も変化はなかった。また、健康成人にモンテルカストカプセル剤200mg注)(6週間反復)とプレドニゾロン20mg(単回)を静脈内投与により併用したとき、プレドニゾン及びプレドニゾロンの薬物動態はいずれも影響を受けなかった(外国人データ)。
16.7.4 経口避妊薬(エチニルエストラジオール35μg/ノルエチンドロン1mg)
健康成人にモンテルカストカプセル剤100mg注)(8日間反復)と経口避妊薬(エチニルエストラジオール35μg/ノルエチンドロン1mg単回)を経口投与により併用したとき、エチニルエストラジオール及びノルエチンドロンの薬物動態はいずれも影響を受けなかった18)(外国人データ)。
16.7.5 ジゴキシン
健康成人にモンテルカストフィルムコーティング錠10mg(7日間反復)とジゴキシン0.5mg(単回)を経口投与により併用したとき、免疫反応性ジゴキシンの薬物動態は影響を受けなかった19)(外国人データ)。
16.7.6 ワルファリン
健康成人にモンテルカストフィルムコーティング錠10mg(7日間反復)とワルファリン30mg(単回)を経口投与により併用したとき、ワルファリンの血漿中総薬物濃度は影響を受けなかった。また、プロトロンビン時間への影響もなかった20)(外国人データ)。
注)
成人の気管支喘息における承認用量は1回10mgである。
成人のアレルギー性鼻炎における承認用量は1回5〜10mgである。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<気管支喘息>
17.1.1 国内臨床試験
二重盲検比較試験を含む成人気管支喘息患者を対象とした臨床試験におけるモンテルカストフィルムコーティング錠10mg群の最終全般改善度の有効率は55.6%(145/261例)であった。
17.1.2 国内第III相二重盲検比較試験
気管支喘息患者を対象とした第III相二重盲検比較試験におけるモンテルカストフィルムコーティング錠10mg群の最終全般改善度の有効率は58.5%(83/142例)であり、プランルカスト水和物450mg群[46.0%(63/137例)]に対する非劣性が検証された(非劣性マージンΔ=10%)21)。
副作用発現率は11.0%(20/182例)であり、主な副作用は胸やけ3例(1.6%)、眼瞼浮腫、胃痛、胃不快感、食欲不振、嘔気、下痢が各2例(1.1%)であった。また臨床検査値異常変動は8.8%(16/182例)であり、主な臨床検査値異常変動はALT上昇2.3%(4/178例)、尿潜血1.9%(3/156例)であった。
副作用発現率は11.0%(20/182例)であり、主な副作用は胸やけ3例(1.6%)、眼瞼浮腫、胃痛、胃不快感、食欲不振、嘔気、下痢が各2例(1.1%)であった。また臨床検査値異常変動は8.8%(16/182例)であり、主な臨床検査値異常変動はALT上昇2.3%(4/178例)、尿潜血1.9%(3/156例)であった。
<アレルギー性鼻炎>
17.1.3 国内第II相至適用量設定試験
季節性アレルギー性鼻炎患者における第II相至適用量設定試験(約900例)の結果、総合鼻症状点数[日中鼻症状点数注1)と夜間鼻症状点数注2)の平均(治療期2週間の平均)]のベースラインからの変化量の最小二乗平均(LS mean)は、モンテルカストフィルムコーティング錠5mg群で−0.47点、10mg群で−0.47点であり、プラセボ群(−0.37点)と比較して有意に改善した22)。
副作用発現率は、5mg群で4.7%(15/318例)、10mg群で4.2%(13/310例)であった。主な副作用は、5mg群で1%以上発現した副作用はなく、10mg群で口渇4例(1.3%)、頭痛、傾眠が各3例(1.0%)であった。また臨床検査値異常変動の副作用発現率は、5mg群で1.9%(6/318例)、10mg群で5.8%(18/310例)であった。主な臨床検査値異常の副作用は、5mg群で1%以上発現した臨床検査値異常はなく、10mg群で尿潜血陽性、尿中蛋白陽性が各4例(1.3%)、血中ビリルビン増加、血中トリグリセリド増加が各3例(1.0%)であった。
副作用発現率は、5mg群で4.7%(15/318例)、10mg群で4.2%(13/310例)であった。主な副作用は、5mg群で1%以上発現した副作用はなく、10mg群で口渇4例(1.3%)、頭痛、傾眠が各3例(1.0%)であった。また臨床検査値異常変動の副作用発現率は、5mg群で1.9%(6/318例)、10mg群で5.8%(18/310例)であった。主な臨床検査値異常の副作用は、5mg群で1%以上発現した臨床検査値異常はなく、10mg群で尿潜血陽性、尿中蛋白陽性が各4例(1.3%)、血中ビリルビン増加、血中トリグリセリド増加が各3例(1.0%)であった。
17.1.4 国内第III相二重盲検比較試験
季節性アレルギー性鼻炎患者における第III相二重盲検比較試験(約1,400例)の結果、総合鼻症状点数[日中鼻症状点数注1)と夜間鼻症状点数注2)の平均(治療期2週間の平均)]のベースラインからの変化量のLS meanは、モンテルカストフィルムコーティング錠5mg群で−0.19点、10mg群で−0.19点であり、プランルカスト水和物450mg群(−0.20点)に対する非劣性が検証された(非劣性マージンΔ=0.085点)23)。
副作用発現率は、5mg群で4.8%(22/462例)、10mg群で4.2%(19/457例)であった。主な副作用は、5mg群で口渇6例(1.3%)、傾眠5例(1.1%)であり、10mg群で傾眠5例(1.1%)であった。また臨床検査値異常変動の副作用発現率は、5mg群で2.4%(11/459例)、10mg群で2.0%(9/456例)であった。5mg群、10mg群のいずれにおいても1%以上発現した臨床検査値異常の副作用はなかった。
副作用発現率は、5mg群で4.8%(22/462例)、10mg群で4.2%(19/457例)であった。主な副作用は、5mg群で口渇6例(1.3%)、傾眠5例(1.1%)であり、10mg群で傾眠5例(1.1%)であった。また臨床検査値異常変動の副作用発現率は、5mg群で2.4%(11/459例)、10mg群で2.0%(9/456例)であった。5mg群、10mg群のいずれにおいても1%以上発現した臨床検査値異常の副作用はなかった。
注1)鼻閉、鼻汁、くしゃみ発作の症状点数を集計
注2)鼻閉、入眠困難度、夜間覚醒度の症状点数を集計
18. 薬効薬理
18.1 作用機序
<気管支喘息>
18.1.1 モンテルカストは、システイニルロイコトリエン タイプ1受容体(Cys LT1受容体)に選択的に結合し、炎症惹起メディエーターであるLTD4やLTE4による病態生理学的作用(気管支収縮、血管透過性の亢進、及び粘液分泌促進)を抑制する。この作用機序に基づき、モンテルカストは抗喘息作用として、喘息性炎症の種々の因子を改善する。
<アレルギー性鼻炎>
18.1.2 アレルギー性鼻炎では、抗原曝露後に、即時相及び遅発相のいずれにおいてもシステイニルロイコトリエンが鼻粘膜から放出される。その放出はアレルギー性鼻炎の症状発現と関連がある。また、システイニルロイコトリエンの鼻腔内投与は鼻腔通気抵抗を上昇させ、鼻閉症状を増悪させることが示されている。モンテルカストはロイコトリエン受容体の作用を遮断することにより、アレルギー性鼻炎症状の緩和に重要な役割を果たすことが示唆されている。
18.2 LT受容体拮抗作用(受容体結合試験)
受容体結合試験(モルモット肺細胞膜、U937細胞膜及びTHP-1細胞膜)で、LTD4の受容体結合を強力に阻害し、その作用は血液成分による影響を受けなかった。LTC4及びLTB4に対する受容体拮抗作用は弱かった24)。
18.3 気管支収縮抑制作用(摘出臓器及び動物試験)
モルモット摘出気管におけるLTD4の収縮を競合的に阻害した。また、モルモット及びリスザルにおいてLTD4誘発気管支収縮反応に対して強力かつ持続的な阻害作用を示した。一方、モンテルカストは、LTC4(LTC4の代謝を阻害した条件下)による摘出組織の収縮を阻害しなかった。また、モルモットを用いたヒスタミン、アラキドン酸、セロトニン及びアセチルコリン誘発の気管支収縮をほとんど阻害しなかった24)。
18.4 抗原誘発による気管支収縮抑制作用
18.5 即時型及び遅発型気管支収縮反応に対する抑制作用
感作リスザルの抗原誘発による即時型及び遅発型気管支収縮反応を経口投与で抑制した24)。
18.6 アナフィラキシーショックに対する抑制作用
感作モルモットの卵アルブミンによるアナフィラキシーショックを部分的に抑制した26)。
18.7 抗原誘発による鼻腔通気抵抗上昇(鼻閉)に対する抑制効果
感作モルモットを用い、卵アルブミン吸入で誘発される鼻腔通気抵抗の上昇(鼻閉)に対し、モンテルカスト1及び3mg/kg(腹腔内投与)は、それぞれ55%、85%の抑制効果を示した27)。
18.8 肺機能の改善作用
軽症から中等症の慢性気管支喘息患者において、1秒量及び最大呼気流量を改善した28)。
18.9 好酸球に対する効果
19. 有効成分に関する理化学的知見
19.1. モンテルカストナトリウム
20. 取扱い上の注意
<フィルムコーティング錠>
アルミニウム袋開封後は、湿気を避けて遮光して保存すること。
22. 包装
<シングレア錠5mg>
100錠[10錠(PTP)×10]
<シングレア錠10mg>
100錠[10錠(PTP)×10]
140錠[14錠(PTP)×10]
<シングレアOD錠10mg>
60錠[10錠(ブリスター)×6]
23. 主要文献
- Knorr B,et al., J Clin Pharmacol., 39, 786-93, (1999) »PubMed
- Philip G,et al., J Allergy Clin Immunol., 124, 691-6, (2009) »PubMed
- Philip G,et al., J Allergy Clin Immunol., 124, 699-706, (2009) »PubMed
- 大西明弘、他, 臨床医薬, 17, 443-70, (2001)
- 社内資料:モンテルカストの生物学的同等性試験
- 社内資料:モンテルカストの生物学的利用率
- 社内資料:モンテルカストの蛋白との結合
- Filppula AM,et al., Drug Metab Dispos., 39, 904-11, (2011) »PubMed
- Karonen T,et al., Br J Clin Pharmacol., 73, 257-67, (2012) »PubMed
- Karonen T,et al., Clin Pharmacol Ther., 88, 223-30, (2010) »PubMed
- Chiba M,et al., Drug Metab Dispos., 25, 1022-31, (1997) »PubMed
- Friedman E,et al., Clin Pharmacol Ther., 79, 72, (2006)
- Balani SK,et al., Drug Metab Dispos., 25, 1282-7, (1997) »PubMed
- 社内資料:モンテルカストの肝機能障害患者における薬物動態
- Zhao JJ,et al., Biopharm Drug Dispos., 18, 769-77, (1997) »PubMed
- Holland S,et al., Clin Pharmacol Ther., 63, 231, (1998)
- Malmstrom K,et al., Am J Ther., 5, 189-95, (1998) »PubMed
- Schwartz J,et al., Clin Pharmacol Ther., 61, 162, (1997)
- Depre M,et al., J Clin Pharmacol., 39, 941-4, (1999) »PubMed
- Van Hecken A,et al., J Clin Pharmacol., 39, 495-500, (1999) »PubMed
- 宮本昭正、他, 臨床医薬, 17, 519-58, (2001)
- Okubo K,et al., Allergol Int., 57, 247-55, (2008) »PubMed
- Okubo K,et al., Allergol Int., 57, 383-90, (2008) »PubMed
- Jones TR,et al., Can J Physiol Pharmacol., 73, 191-201, (1995) »PubMed
- Diamant Z,et al., Clin Exp Allergy., 29, 42-51, (1999) »PubMed
- 社内資料:モンテルカストのアナフィラキシーショックに対する抑制作用
- 社内資料:モンテルカストの抗原誘発による鼻腔通気抵抗上昇(鼻閉)に対する抑制効果(2008年1月25日承認、CTD2.6.2.2)
- 宮本昭正、他, 臨床医薬, 17, 577-95, (2001)
- Minoguchi K,et al., Chest., 121, 732-8, (2002) »PubMed
- 古庄巻史、他, 臨床医薬, 17, 609-21, (2001)
- 古庄巻史、他, 臨床医薬, 21, 1019-29, (2005)
24. 文献請求先及び問い合わせ先
文献請求先
オルガノン株式会社
カスタマーサポートセンター
東京都港区南青山1-24-3
電話:フリーダイヤル 0120-095-213
製品情報問い合わせ先
オルガノン株式会社
カスタマーサポートセンター
東京都港区南青山1-24-3
電話:フリーダイヤル 0120-095-213
26. 製造販売業者等
26.1 製造販売元
オルガノン株式会社
東京都港区南青山1-24-3