医薬品情報
| 総称名 | アレルゲンスクラッチエキス |
|---|---|
| 一般名 | ヒスタミン二塩酸塩 |
| 欧文一般名 | Histamine dihydrochloride |
| 製剤名 | ヒスタミン二塩酸塩液 |
| 薬効分類名 | アレルゲン検査陽性対照薬 |
| 薬効分類番号 | 7290 |
| KEGG DRUG |
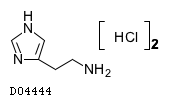
D04444
ヒスタミン二塩酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年12月 改訂(第3版)

|
4.効能または効果 6.用法及び用量 7.用法及び用量に関連する注意 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アレルゲンスクラッチエキス陽性対照液「トリイ」ヒスタミン二塩酸塩 | Allergen Scratch Extract Positive Control (Torii) Histamine Dihydrochloride | 塩野義製薬 | 7290417A1027 | 7913円/瓶 | 処方箋医薬品注) |
4. 効能または効果
診断
アレルゲンによる皮膚反応の陽性対照
6. 用法及び用量
診断
通常乱刺(プリック)又は切皮(スクラッチ)法により皮膚面に出血しない程度に傷をつけ,本剤1滴を滴下し,アレルゲン検査時の陽性対照とする。
7. 用法及び用量に関連する注意
7.1 本剤を滴下すると,15分後に通常3mm以上の膨疹が形成される。
7.2 正確な皮膚反応テストを行うため,実施部位に皮膚病変がないことを十分に確認すること。
7.3 正確な皮膚反応テストを行うため,皮膚反応テスト前日から抗ヒスタミン薬やメディエータ遊離抑制薬等の投与を中止すること。また,皮膚反応テストを実施する約1週間前から投与を中止することが望ましい薬剤があるので注意すること。
7.4 陽性反応を示さない場合は,日を改めて再検査することが望ましい。
8. 重要な基本的注意
8.1 皮膚反応テスト実施後,実施部位の観察を十分に行うこと。皮膚反応テスト実施部位に発生する皮膚症状(かゆみ)や軽微な疼痛(痛み)が数時間持続する場合がある。
9. 特定の背景を有する患者に関する注意
9.5 妊婦
診断上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
診断上の有益性及び母乳栄養の有益性を考慮し,授乳の継続又は中止を検討すること。
9.7 小児等
低出生体重児又は新生児を対象とした臨床試験を実施していない。
9.8 高齢者
検査に際しては注意すること。一般に生理機能が低下していることが多い。
11. 副作用
11.2 その他の副作用
| 頻度不明 | |
| 過敏症 | 過敏症,呼吸困難,紅斑 |
14. 適用上の注意
14.1 診断上の注意
皮膚反応テスト実施時には,スクラッチエキス用対照液(アレルゲンスクラッチエキス対照液「トリイ」)を同時に用いて反応を比較すること。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験(350-3-1試験)
健康成人男女30例を対象に,本剤と陰性対照薬(アレルゲンスクラッチエキス対照液「トリイ」)を用いた無作為化二重盲検試験による皮膚反応テスト(プリックテスト)を行った。テスト実施15分後の結果は,30例すべてで本剤の膨疹(平均径)が3mm以上であり,陽性率は100%であった1)。
安全性評価対象30例において,副作用は認められなかった。
安全性評価対象30例において,副作用は認められなかった。
18. 薬効薬理
18.1 測定法
ヒスタミンが皮下注射されると,ヒスタミンの直接的な血管拡張効果による局所性赤色斑,間接的な血管拡張効果による発赤,浮腫誘発による膨疹等の症状が受容体を介して発現することが知られている2)。
19. 有効成分に関する理化学的知見
19.1. ヒスタミン二塩酸塩
20. 取扱い上の注意
20.1 バイアル開封後は,キャップをよく締め,2〜8℃で遮光保存すること。
20.2 バイアル開封後6ヵ月間経過した場合は,残液を使用しないこと。
22. 包装
2mL[1バイアル(点滴用スポイトキャップ付属)]
23. 主要文献
- 社内資料:第III相臨床試験(2015年9月28日承認,CTD2.7.3.2)
- Owen,DA.,et al., Br J Pharmacol., 69 (4), 615-623, (1980) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
鳥居薬品株式会社
お客様相談室
〒103-8439
東京都中央区日本橋本町3-4-1
電話:0120-316-834
FAX:03-3231-6890
製品情報問い合わせ先
鳥居薬品株式会社
お客様相談室
〒103-8439
東京都中央区日本橋本町3-4-1
電話:0120-316-834
FAX:03-3231-6890
26. 製造販売業者等
26.1 製造販売元
塩野義製薬株式会社
大阪市中央区道修町3丁目1番8号
26.2 販売元
鳥居薬品株式会社
東京都中央区日本橋本町3-4-1
その他の説明
<初回使用時の準備>
キャップ(白,グレー)をはずし,付属のスポイトキャップ(青)を取り付ける。
※キャップをはずす際,キャップ(白)とキャップ(グレー)が同時にはずれる場合がある。
※使用後は,スポイトキャップ(青)をしっかり締めて遮光し,2〜8℃で保管する。