医薬品情報
| 総称名 | シプロキサン |
|---|---|
| 一般名 | シプロフロキサシン |
| 欧文一般名 | Ciprofloxacin |
| 製剤名 | シプロフロキサシン注射剤 |
| 薬効分類名 | ニューキノロン系注射用抗菌剤 |
| 薬効分類番号 | 6241 |
| ATCコード | J01MA02 S01AE03 S02AA15 S03AA07 |
| KEGG DRUG |
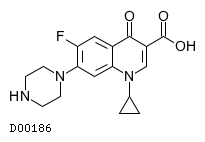
D00186
シプロフロキサシン
|
| KEGG DGROUP |
DG00617
シプロフロキサシン
DG01549
ニューキノロン系抗生物質
|
| JAPIC | 添付文書(PDF) |
添付文書情報2022年9月 改訂(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| シプロキサン注200mg | Ciproxan intravenous injection 200mg | バイエル薬品 | 6241400A4021 | 1747円/袋 | 処方箋医薬品注) |
| シプロキサン注400mg | Ciproxan intravenous injection 400mg | バイエル薬品 | 6241400A6024 | 1739円/袋 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
成人
<適応菌種>
<適応症>
小児
5. 効能または効果に関連する注意
成人
5.1 本剤の適用は、原則として他の抗菌剤にアレルギーの既往を有する患者、重症あるいは他の抗菌剤を使用しても十分な臨床効果が得られない患者に限定すること。ただし、炭疽及びレジオネラ属による感染症の適応の場合は、この限りではない。
5.2 シプロフロキサシン塩酸塩水和物(経口剤)と異なり、本剤の効能・効果は、敗血症、外傷・熱傷及び手術創等の二次感染、肺炎、腹膜炎、胆嚢炎、胆管炎、炭疽に限定されているので、それ以外の疾患には使用しないこと。
5.3 本剤のメチシリン耐性ブドウ球菌(MRSA)に対する有効性は証明されていないので、MRSAによる感染症が明らかである場合、速やかに抗MRSA作用の強い薬剤を投与すること。
小児
5.4 本剤の適用は、原則として他の抗菌剤にアレルギーの既往を有する患者、重症あるいは他の抗菌剤を使用しても十分な臨床効果が得られない患者に限定すること。ただし、炭疽については、この限りではない。[9.7.2参照]
6. 用法及び用量
成人
通常、シプロフロキサシンとして、1回400mgを1日2回、1時間かけて点滴静注する。患者の状態に応じて1日3回に増量できる。
小児
<一般感染症>
複雑性膀胱炎、腎盂腎炎
通常、シプロフロキサシンとして、1回6〜10mg/kgを1日3回、1時間かけて点滴静注する。ただし、成人における1回量400mgを超えないこととする。
炭疽
通常、シプロフロキサシンとして、1回10mg/kgを1日2回、1時間かけて点滴静注する。ただし、成人における1回量400mgを超えないこととする。
<嚢胞性線維症における緑膿菌による呼吸器感染に伴う症状の改善>
通常、シプロフロキサシンとして、1回10mg/kgを1日3回、1時間かけて点滴静注する。ただし、成人における1回量400mgを超えないこととする。
7. 用法及び用量に関連する注意
<効能共通>
7.1 腎機能が低下していることが多い高齢者あるいは腎機能障害患者・血液透析患者では、腎機能に十分注意し、患者の状態を観察しながら慎重に投与すること。[9.2.1、9.8.2、16.5、16.6.1、16.6.3参照]
(参考)
| クレアチニンクリアランス(Ccr)(mL/min) | 用法・用量 |
| 30≦Ccr≦60 | 1回200mgを12時間ごとに投与 |
| Ccr<30 | 1回200mgを24時間ごとに投与 |
病状により必要と判断された場合には1回量として400mgを投与する。
なお、クレアチニンクリアランス値(mL/min)=[体重(kg)×(140−年齢)]/[72×血清クレアチニン値(mg/dL)]、女性の場合はこれに0.85を乗ずること1)。
なお、クレアチニンクリアランス値(mL/min)=[体重(kg)×(140−年齢)]/[72×血清クレアチニン値(mg/dL)]、女性の場合はこれに0.85を乗ずること1)。
7.2 血液透析中に除去されるシプロフロキサシンは10%程度と大きな影響は受けない。血液透析中の患者への投与に際しては、必要に応じて低用量(200mg)を24時間ごとに投与するなど患者の状態を観察しながら慎重に投与すること。[16.6.1参照]
7.3 症状が緩解した場合には、速やかに経口抗菌剤の投与に切り替えることが望ましい。
<炭疽>
7.4 臨床症状が緩解した場合には、速やかに経口剤投与に切り替え、計60日間投与することを、米国疾病管理センター(CDC)が推奨している。
8. 重要な基本的注意
8.1 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、次の措置をとること。
8.1.1 事前に既往歴等について十分な問診を行うこと。なお、抗生物質等によるアレルギー歴は必ず確認すること。
8.1.2 投与に際しては、必ずショック等に対する救急処置のとれる準備をしておくこと。
8.1.3 投与開始から投与終了後まで、患者を安静の状態に保たせ、十分な観察を行うこと。特に、投与開始直後は注意深く観察すること。
8.2 大動脈瘤、大動脈解離を引き起こすことがあるので、観察を十分に行うとともに、腹部、胸部又は背部に痛み等の症状があらわれた場合には直ちに医師の診察を受けるよう患者に指導すること。[9.1.6、11.1.16参照]
8.3 本剤の使用にあたっては、耐性菌の発現等を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 本人又は両親、兄弟に気管支喘息、発疹、じん麻疹等のアレルギー症状を起こしやすい体質を有する患者
9.1.2 うっ血性心不全、腎不全、ネフローゼ症候群等、ナトリウムの摂取が問題となる患者
本剤には塩化ナトリウムが含まれている。
9.1.3 てんかん等の痙攣性疾患又はこれらの既往歴のある患者
痙攣を起こすことがある。[11.1.6参照]
9.1.4 重症筋無力症患者
症状を悪化させることがある。[11.1.13参照]
9.1.5 QT延長を起こすおそれのある患者
QT延長を起こすことがある。[11.1.15参照]
9.1.6 大動脈瘤又は大動脈解離を合併している患者、大動脈瘤又は大動脈解離の既往、家族歴若しくはリスク因子(マルファン症候群等)を有する患者
9.2 腎機能障害患者
9.5 妊婦
<炭疽以外>
9.5.1 妊婦又は妊娠している可能性のある女性には投与しないこと。[2.5参照]
<炭疽>
9.5.2 妊婦又は妊娠している可能性のある女性には、治療上の有益性を考慮して投与すること。
9.6 授乳婦
授乳しないことが望ましい。母乳中へ移行することが報告されている。
9.7 小児等
<複雑性膀胱炎、腎盂腎炎、嚢胞性線維症、炭疽以外>
9.7.1 投与しないこと。動物実験(幼若イヌ、幼若ラット)で関節毒性が認められている。幼若ラット及び幼若ビーグル犬を用いた反復投与試験(経口)において、関節軟骨のびらん等が認められた。成熟動物(サル)を用いた反復静脈内投与試験においてはいずれの試験でも関節毒性は認められなかった。[2.6参照]
<複雑性膀胱炎、腎盂腎炎、嚢胞性線維症、炭疽>
9.8 高齢者
10. 相互作用
相互作用序文
本剤はチトクロームP4501A2(CYP1A2)を阻害するので、本酵素で代謝される薬剤の代謝を阻害し、血中濃度を上昇させるおそれがある。
薬物代謝酵素用語
CYP1A2
10.1 併用禁忌
| ケトプロフェン(注射剤、坐剤)(カピステン等) [2.2参照] | 痙攣を起こすことがあるので、併用しないこと。 | 併用により、ニューキノロン系抗菌剤のGABAA受容体への阻害作用が増強され、痙攣が誘発されると考えられている。 てんかん等の痙攣性疾患又はこれらの既往歴のある患者、腎障害のある患者では特に注意すること。 |
| チザニジン塩酸塩(テルネリン) [2.3参照] | チザニジンのCmaxが7倍、AUCが10倍それぞれ上昇し、血圧低下、傾眠、めまい等があらわれたとの報告がある。チザニジンの作用を増強させるおそれがあるので、併用しないこと。 | チザニジンの肝での代謝を阻害し、チザニジンの血中濃度を上昇させると考えられている。 |
| ロミタピドメシル酸塩(ジャクスタピッド) [2.4参照] | ロミタピドの血中濃度が著しく上昇するおそれがある。 | ロミタピドの代謝酵素(CYP3A4)が阻害されるおそれがある。 |
10.2 併用注意
| テオフィリン アミノフィリン水和物 | テオフィリンのCmaxが17%、AUCが22%それぞれ上昇したとの報告がある3)。テオフィリンの作用を増強させる可能性があるので、併用する場合にはテオフィリンを減量するなど適切な処置を行うこと。 | テオフィリンの肝での代謝を抑制し、クリアランスを減少させるためと考えられている。肝障害のある患者、高齢者では特に注意すること。 |
| カフェイン デュロキセチン塩酸塩 | これらの薬剤の血中濃度が上昇することがある。 | これらの薬剤の肝での代謝を抑制し、クリアランスを減少させるためと考えられている。 |
| フェニル酢酸系非ステロイド性消炎鎮痛剤 ジクロフェナク、アンフェナク等 プロピオン酸系非ステロイド性消炎鎮痛剤(ただし、ケトプロフェン(注射剤、坐剤)とは併用禁忌) ロキソプロフェン、プラノプロフェン、ザルトプロフェン等 | 痙攣を起こすおそれがある。症状が認められた場合、両剤の投与を中止するなど適切な処置を行うこと。 | 併用により、ニューキノロン系抗菌剤のGABAA受容体への阻害作用が増強され、痙攣が誘発されると考えられている。 てんかん等の痙攣性疾患又はこれらの既往歴のある患者、腎障害のある患者では特に注意すること。 |
| シクロスポリン | 相互に副作用(腎障害等)が増強されるおそれがあるので、頻回に腎機能検査(クレアチニン、BUN等)を行うなど患者の状態を十分に観察すること。 | 発現機序の詳細は不明であるが、相互に肝での代謝を抑制し、一方又は両方の血中濃度が上昇するためと考えられている。肝障害のある患者、高齢者では特に注意すること。 |
| ワルファリン | ワルファリンの作用を増強し、出血、プロトロンビン時間の延長等があらわれることがある。本剤を併用する場合は、プロトロンビン時間国際標準比(INR)値等を測定するなど、観察を十分に行うこと。 | 発現機序の詳細は不明であるが、ワルファリンの肝での代謝を抑制し、クリアランスを減少させるためと考えられている。 |
| スルホニル尿素系血糖降下剤 グリメピリド、グリベンクラミド等 | スルホニル尿素系血糖降下剤の作用を増強し、低血糖があらわれることがある。 | 発現機序の詳細は不明であるが、グリベンクラミドの肝での代謝を阻害するとの報告4)がある。また、膵臓のβ細胞を用いたin vitro試験において、本剤がインスリン分泌作用を促進するとの報告がある。 |
| ロピニロール塩酸塩 | ロピニロールのCmaxが60%、AUCが84%それぞれ上昇したとの報告がある。ロピニロールの投与中に本剤を投与開始又は投与中止する場合には、必要に応じてロピニロールの用量を調節すること。 | 併用により、ロピニロールの肝での代謝が阻害されるためと考えられている。 |
| メトトレキサート | メトトレキサートの血中濃度が上昇し、作用が増強されるおそれがある。併用する場合には患者の状態を十分に観察すること。 | 発現機序の詳細は不明であるが、メトトレキサートの腎尿細管からの排泄が阻害されるためと考えられている。 |
| クラスIA抗不整脈薬 キニジン、プロカインアミド等 クラスIII抗不整脈薬 アミオダロン、ソタロール等 | 本剤を併用した場合、QT延長がみられるおそれがある。 | 併用により、QT延長作用が相加的に増加するおそれがある。 |
| クロザピン オランザピン | 経口剤においてクロザピン及びその代謝物の血中濃度が29%と31%それぞれ上昇したとの報告がある。左記薬剤の投与中に本剤を投与開始又は投与中止する場合には、必要に応じて左記薬剤の用量調節をすること。 | 併用により、左記薬剤の肝での代謝が阻害されるためと考えられている。 |
| シルデナフィルクエン酸塩 | シルデナフィルのCmax及びAUCがそれぞれ約2倍上昇したとの報告がある。 | CYP3A4阻害によりクリアランスが減少するとの報告もあるが、発現機序の詳細は不明である。 |
| フェニトイン | フェニトインの血中濃度が低下したとの報告がある。本剤を併用する場合は、フェニトインの血中濃度を測定するなど、観察を十分に行うこと。 | 機序不明 |
| 副腎皮質ホルモン剤(経口剤、注射剤) プレドニゾロン、ヒドロコルチゾン等 | 腱障害のリスクが増大するとの報告がある。これらの薬剤との併用は、治療上の有益性が危険性を上回る場合のみとすること。 | 機序不明 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
ショック、アナフィラキシー(呼吸困難、浮腫、じん麻疹等)があらわれることがある。
11.1.2 偽膜性大腸炎等の血便を伴う重篤な大腸炎(頻度不明)
腹痛、頻回の下痢があらわれた場合には直ちに投与を中止するなど適切な処置を行うこと。
11.1.3 横紋筋融解症(頻度不明)
筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇を特徴とし、急激な腎機能悪化を伴う横紋筋融解症があらわれることがあるので注意すること。
11.1.4 間質性肺炎(頻度不明)
発熱、咳嗽、呼吸困難、胸部X線異常、好酸球増多等を伴う間質性肺炎があらわれることがあるので、このような症状があらわれた場合には投与を中止し、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.1.5 低血糖(頻度不明)
重篤な低血糖があらわれることがある。高齢者、特にスルホニル尿素系血糖降下剤併用患者であらわれやすい。
11.1.6 痙攣(頻度不明)
特に、腎機能が低下している患者や高齢者であらわれやすい。[9.1.3参照]
11.1.7 骨髄抑制、汎血球減少、無顆粒球症、血小板減少(いずれも頻度不明)
11.1.8 劇症肝炎、肝機能障害、黄疸(いずれも頻度不明)
劇症肝炎、著しいAST、ALT等の上昇を伴う肝機能障害、黄疸があらわれることがある。
11.1.9 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、多形紅斑、急性汎発性発疹性膿疱症(いずれも頻度不明)
11.1.10 急性腎障害、間質性腎炎(いずれも頻度不明)
11.1.11 アキレス腱炎、腱断裂等の腱障害(いずれも頻度不明)
腱周辺の痛み、浮腫、発赤等の症状が認められた場合には投与を中止し、適切な処置を行うこと。なお、外国において、投与終了数ヵ月後にこれらの症状を発現した症例も報告されている。[9.8.1参照]
11.1.12 錯乱、抑うつ等の精神症状(いずれも頻度不明)
11.1.13 重症筋無力症の悪化(頻度不明)[9.1.4参照]
11.1.14 血管炎(頻度不明)
11.1.15 QT延長、心室頻拍(Torsades de pointesを含む)(いずれも頻度不明)[9.1.5参照]
11.2 その他の副作用
| 0.1〜5%未満 | 頻度不明 | |
| 過敏症 | 発疹、そう痒、じん麻疹、発熱、浮腫(末梢、血管、顔面、咽頭) | 光線過敏症、固定薬疹、血清病様反応、発赤(結節性紅斑) |
| 腎臓 | クレアチニン上昇 | 血尿、結晶尿、BUN上昇 |
| 肝臓 | AST上昇、ALT上昇 | Al-P上昇、LDH上昇、γ-GTP上昇 |
| 循環器 | 頻脈、失神、ほてり、低血圧、片頭痛 | |
| 血液 | 好酸球増多、貧血 | 点状出血、プロトロンビン量増加、溶血性貧血、赤血球減少、白血球減少、ヘモグロビン減少、ヘマトクリット減少、血小板増加、白血球増加 |
| 消化器 | 下痢、嘔気、胃不快感 | 腹痛、消化不良、膵炎、食欲不振、腹部膨満感、嘔吐、口内炎 |
| 感覚器 | 眼内異物感 | 味覚異常、無嗅覚、嗅覚錯誤、一過性難聴、耳鳴、視覚異常 |
| 精神神経系 | 頭痛、めまい | 眠気、無力症、不眠症、不安、発汗、悪夢、幻覚、精神病、失調、末梢性ニューロパシー(しびれ感等)、筋緊張亢進、頭蓋内圧亢進、激越、意識障害、振戦 |
| 投与部位 | 注射部位反応(血管痛、静脈炎、紅斑、炎症等) | |
| その他 | 高血糖 | 関節痛、筋肉痛、モニリア症、呼吸困難、胸痛、背部痛、関節障害、筋無力症、CK上昇、倦怠感 |
13. 過量投与
13.1 症状
腎毒性があらわれたとの報告がある。
13.2 処置
腎機能をモニターするとともに、水分及び電解質の補充を行う。シプロフロキサシンは腹膜透析、血液透析では少量(10%程度)しか除去されない。
14. 適用上の注意
14.1 薬剤調製前の注意
保管中に白色の結晶が析出することがあるので、このような場合には温めて結晶を溶解して使用すること。
14.2 薬剤調製時の注意
14.2.1 原則として、点滴静注に際しては、生理食塩液、ブドウ糖注射液又は補液で希釈すること。
14.2.2 注射針はゴム栓の刺針部(中央の凹部)にまっすぐ刺し入れること。また、同一個所に繰り返し刺さないこと。
14.2.3 大気圧で自然に内容液が排出されるため、通気針は不要である。
14.2.4 使用後の残液は使用しないこと。
14.3 薬剤投与時の注意
14.3.1 本剤と配合した時に沈殿、混濁、変色が認められた場合には投与しないこと。特にアルカリ性の溶液と配合しないこと(本剤のpHは3.9〜4.5の範囲である)。配合変化試験において、すべての注射剤が検討されているわけではないが、本剤と配合した直後から24時間後までに、沈殿等が観察された薬剤があるので、配合時には配合変化データを参照すること。
14.3.2 静脈内急速投与により、点滴静注局所の血管痛、静脈炎を起こすことがあるので、これらを予防するために注射部位、注射方法等について十分注意すること。
・30分以内の点滴静注は避けること。
・希釈して緩徐に注入すること。すでに補液等が投与されている場合、側管に連結して投与することができる。
なお、著しい水分摂取制限がかかっている場合等、水分負荷がかけられない場合には希釈せずに投与することができるが、その際はできるだけ太い静脈から投与することが望ましい。
なお、著しい水分摂取制限がかかっている場合等、水分負荷がかけられない場合には希釈せずに投与することができるが、その際はできるだけ太い静脈から投与することが望ましい。
14.3.3 連結管による混合投与の場合は、Y字型連結にして使用すること。
14.3.4 分割投与しないこと。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 大量投与[750mg/回以上(経口剤)]により結晶尿が認められたとの報告がある(外国人データ)。
15.1.2 プロベネシドによる影響
プロベネシドとの併用により、本剤の最高血中濃度は大きく変化しなかったが、t1/2の延長とAUCの増加が認められたとの報告がある(外国人データ)。
15.2 非臨床試験に基づく情報
15.2.1 遺伝毒性については、in vitro試験の一部(マウスリンパ腫細胞を用いた遺伝子突然変異試験、ラット肝初代培養細胞を用いた不定期DNA合成試験、チャイニーズハムスターCHL細胞を用いた染色体異常試験)成績において、陽性を示したとする報告がある。
15.2.2 光遺伝毒性については、ネズミチフス菌TA104を用いた復帰突然変異試験、チャイニーズハムスターV79細胞を用いた染色体異常試験、マウスリンパ腫細胞を用いたコメットアッセイにおいて陽性を示す所見が認められている。
15.2.3 局所刺激性については、ウサギを用いた局所刺激性試験(筋肉内投与)において、軽度の組織障害性が観察されたが、サルにおける4週間反復点滴静脈内投与試験では、投与部位における局所刺激性は認められなかった。
15.2.4 眼毒性については、サルを用いた4、13、26週間反復静脈内投与試験において、いずれの試験でも眼毒性を示唆する所見は認められなかった。ネコを用いた2週間静脈内投与試験において、ERG(網膜電位図)及びVEP(視覚誘発脳波)に関して異常は認められなかった。
15.2.5 腎毒性については、ラット及びサルを用いた反復静脈内投与試験において、それぞれ高用量群[ラット(4週間:80mg/kg/日、26週間:20、40mg/kg/日)、サル(4週間:30mg/kg/日、13週間:18mg/kg/日、26週間:20mg/kg/日、4週間/点滴静脈内投与:20mg/kg)]で尿中に排泄されたシプロフロキサシンが再結晶化したことに起因すると考えられる尿細管変化が認められた。
また、ウサギを用いた反復静脈内投与試験において、30mg/kg/日群で正常ウサギに尿細管拡張が、腎障害ウサギに病理組織学的所見の悪化がみられ、無毒性量は10mg/kg/日であった。
また、ウサギを用いた反復静脈内投与試験において、30mg/kg/日群で正常ウサギに尿細管拡張が、腎障害ウサギに病理組織学的所見の悪化がみられ、無毒性量は10mg/kg/日であった。
15.2.6 光毒性については、マウスに静脈内投与後UVAを照射したが、光毒性は100mg/kg/日においても認められなかった。
15.2.7 ヒスタミン遊離能については、ラット腹腔肥満細胞及びヒト皮膚肥満細胞を用いたin vitro試験5)において、200μg/mL以上の高濃度ではヒスタミン遊離が認められた。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
16.1.2 反復投与
日本人患者に1回400mgを1日2回又は1日3回1時間点滴静注反復投与した場合の投与開始3〜6日目における血中未変化体濃度推移及び薬物動態パラメータは以下のとおりである10)。
| 投与量 | AUCτ,ss(μg・hr/mL) | Cmax,ss(μg/mL) | t1/2,ss※(hr) |
| 400mg 1日2回 | 25.8(23.4)[21] | 8.07(22.5)[22] | 2.44〜8.10[23] |
| 400mg 1日3回 | 22.2(28.8)[8] | 8.14(24.1)[8] | 3.00〜4.54[8] |
16.1.3 経口投与との比較
健康成人男子(20〜22歳)6名を対象に本剤200mgを90分点滴静注により、シプロキサン錠200mg及び300mg(100mg錠2錠または3錠)を経口投与により、クロスオーバー法にてそれぞれ単回投与した。本剤200mg点滴静注時の血中濃度は投与終了時に200mg経口投与時より1.5倍高いピーク値(Cmax)を示し、その後は比較的速やかに低下し、経口投与時と同様の推移で消失した。また、200mg点滴静注時のAUC0-∞は、経口投与時の1.2倍であった。なお、200mg点滴静注時の血中濃度を300mg経口投与時注)と比較したとき、Cmaxは1.2倍、AUCは0.9倍であった。シプロフロキサシンの経口投与時のバイオアベイラビリティは、82.5%であった11)。
| 投与量 | Cmax(μg/mL) | tmax(hr) | t1/2α(hr) | t1/2β(hr) | CLtot(L/hr) | AUC(μg・hr/mL) |
| 300mg経口投与 | 1.71±0.17 | 0.98±0.16 | 0.58±0.14 | 3.40±0.22 | − | 7.31±0.50 |
| 200mg経口投与 | 1.41±0.09 | 0.98±0.13 | 0.61±0.10 | 3.49±0.24 | − | 5.42±0.21 |
| 200mg点滴静注(90分) | 2.06±0.07 | 1.50±0.00 | 0.24±0.05 | 3.89±0.17 | 30.6±1.3 | 6.60±0.27 |
注)経口剤の承認用量は、1回100〜200mgを1日2〜3回。炭疽に対しては1回400mgを1日2回。
16.3 分布
16.4 代謝
健康成人に1回300mgを1時間点滴静注した場合、血中及び尿中代謝物として脱エチレン体(M1)、N-硫酸抱合体(M2)、オキソ体(M3)の3種が検出されている。血中濃度推移から求めた未変化体に対する存在比はそれぞれ1.8%、4.8%、7.3%と低かった7)。
16.5 排泄
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
(1)クレアチニンクリアランス値(Ccr)により腎機能正常例(Ccr>90)(10例)、軽度障害者(61≦Ccr≦90)(11例)、中等度障害者(31≦Ccr≦60)(11例)及び、重度障害者(Ccr≦30)(10例)の4群に分け、1回400mg(重度障害者に対しては300mg)を8〜12時間ごとに本剤を点滴静注にて反復投与したところ、腎機能低下に伴い血中濃度の上昇、半減期の延長及び尿中排泄率の低下が認められている16)(外国人データ)。[7.1、7.2、9.2.1参照]
| クレアチニンクリアランス 投与量・投与間隔 | Cmax(mg/L) 1日目 | AUC(mg・hr/L) 1日目 | AUC0-24c(mg・hr/L) 5日目 | t1/2(hr) 1日目 | CLtot(L/hr/kg) 1日目 | CLr(L/hr/kg) 1日目 |
| Ccr>90a 400mg8時間ごと(10例) | 3.80(14) | 10.2(19) | 32.5(18) | 4.59(16) | 0.45(20) | 0.234(12) |
| 61≦Ccr≦90a 400mg8時間ごと(11例) | 4.59(20)b | 15.4(22)b | 50.4(22)b | 5.23(32) | 0.33(19)b | 0.138(80) |
| 31≦Ccr≦60a 400mg12時間ごと(11例) | 5.35(28)b | 21.5(26)b | 48.3(24)b | 5.72(13)b | 0.23(20)b | 0.087(47)b |
| Ccr≦30a 300mg12時間ごと(10例) | 4.28(21)b | 30.1(28)b | 66.3(29)b | 8.33(30)b | 0.13(26)b | 0.018(86)b |
(2)血液透析を受けている慢性腎障害患者7例を対象として、本剤400mgをクロスオーバー法により、血液透析終了直後及び血液透析開始2時間前にそれぞれ単回点滴静注(1時間)した際の薬物動態パラメータは以下のとおりである。パラメータに両投与時期間で大差は認められず、血液透析により除去されたシプロフロキサシンは10%程度と考えられた17)(外国人データ)。[7.1、7.2、9.2.1参照]
| 投与時期 | Cmax(mg/L) | AUC0-24(mg・hr/L) | AUC(mg・hr/L) | AUCnorm(kg・hr/L) | t1/2(hr) | Vss(L) | CLtot(L/hr) | CLr(L/hr) | CLd(L/hr) |
| 血液透析後 | 7.01(44) | 39.4(41) | 44.7(56) | 8.84(50) | 12.5(68) | 129.2(22) | 8.95(56) | 0.10(169) | 1.18(85) |
| 血液透析2時間前 | 5.71(45) | 34.6(45) | 38.4(55) | 7.65(45) | 11.4(62) | 160.4(27) | 10.4(55) | 0.11(158) | 2.44(37) |
16.6.2 小児等
小児患者を対象とした母集団薬物動態解析の結果、非嚢胞性線維症小児患者(体重30kg、クレアチニンクリアランス100mL/minを想定)におけるクリアランス及び分布容積の母集団平均値はそれぞれ0.60L/h/kg及び2.16L/kgであり、承認用法・用量を投与した際の薬物動態は、小児患者と成人患者とで明らかな差はないことが推定された18)(外国人データ)。
16.6.3 高齢者
高齢者(70〜76歳)に1回200mg1日1回1時間点滴静注(1例)、1回300mg1日2回1時間点滴静注(4例)した場合、健康成人と比較してAUCの増加、CLtotの低下が認められ、またCmaxの増加、Vssの低下が示唆された12)13)。[7.1、9.8.2参照]
| 投与量 | 年齢(歳) | t1/2α(hr) | t1/2β(hr) | Cmax(μg/mL) | Vc(L) | Vss(L) | CLtot(L/hr) | AUC0-∞(μg・hr/mL) |
| 200mg1時間点滴 | 71 | 0.27 | 2.6 | 3.51 | 24.9 | 69.0 | 28.8 | 6.95 |
| 300mg1時間点滴 | 70 | 0.11 | 2.7 | 3.53 | 24.8 | 97.2 | 29.8 | 10.08 |
| 71 | 0.30 | 3.5 | 5.71 | 24.3 | 77.6 | 22.6 | 13.29 | |
| 75 | 0.71 | 3.6 | 3.13 | 73.5 | 108.8 | 24.4 | 12.31 | |
| 76 | 0.47 | 3.5 | 5.16 | 36.6 | 75.4 | 19.5 | 15.37 |
17. 臨床成績
17.1 有効性及び安全性に関する試験
炭疽に対する臨床試験は国内外とも実施されていない。
17.1.1 国内非盲検比較試験、国内一般臨床試験(成人)
1回200mg1日2回あるいは3回、及び1回300mg1日2回投与時の臨床試験(前治療注射剤(第3世代セフェム系、カルバペネム系)無効例※)
| 疾患名 | 有効率 | ||||
| [1]に該当する症例 | [2]に該当する症例 | その他の症例 | 合計 | ||
| 効能・効果にあげた疾患 | 敗血症 | 0/1 | 3/3 | 3/4 | 6/8(75.0) |
| 外傷・熱傷及び手術創等の二次感染 | 9/10(90.0) | 8/8(100) | 31/33(93.9) | 48/51(94.1) | |
| 肺炎 | 4/5 | 5/5 | 100/120(83.3) | 109/130(83.8) | |
| 胆嚢炎、胆管炎 | 3/4 | 0/2 | 11/12(91.7) | 14/18(77.8) | |
| 腹膜炎 | 6/8(75.0) | 2/2 | 13/17(76.5) | 21/27(77.8) | |
| 合計 | 22/28(78.6) | 18/20(90.0) | 158/186(84.9) | 198/234(84.6) | |
首記の適応症に対する本剤の有効率は第3世代セフェム系注射用抗菌剤無効例で78.6%(22/28例)、カルバペネム系注射用抗菌剤無効例で90.0%(18/20例)であった。
起炎菌別有効率ではブドウ球菌属では68.8%(11/16例)、腸球菌属では92.3%(12/13例)、大腸菌では(4/5例)、クレブシエラ属では57.1%(4/7例)、エンテロバクター属では87.5%(7/8例)、緑膿菌では80.8%(21/26例)であった。
起炎菌別有効率ではブドウ球菌属では68.8%(11/16例)、腸球菌属では92.3%(12/13例)、大腸菌では(4/5例)、クレブシエラ属では57.1%(4/7例)、エンテロバクター属では87.5%(7/8例)、緑膿菌では80.8%(21/26例)であった。
細菌性肺炎を対象に本剤1回300mgあるいは対照薬としてセフタジジム水和物1回2g、それぞれ1日2回点滴静注を行った比較試験における有効率は、本剤85.7%(78/91例)、対照薬84.0%(63/75例)であり、臨床効果における同等性(非劣性)が検証された。一方、細菌学的効果が判定できた症例での菌消失率は本剤78.9%(30/38例)、対照薬100%(28/28例)と本剤が有意に劣っていた。起炎菌別にみると、肺炎球菌単独菌感染例で本剤の菌消失率が58.3%(7/12例)と対照薬100%(8/8例)に比較して低値を示した19)。
重症あるいは難治性感染症(内科、泌尿器科及び外科系)患者を対象として本剤200mg1日2〜3回又は300mg1日2回点滴静注した後期第II相試験における複雑性尿路感染症患者での有効率は40.6%(13/32例)と低かった13)。
17.1.2 国内第III相試験(成人)
1回400mg1日2回あるいは3回投与時の臨床試験
重症又は他の抗菌剤で効果が得られない細菌性肺炎又は慢性呼吸器病変の二次感染の入院患者を対象に本剤400mg1日2回あるいは3回点滴静注を行った臨床試験における治癒判定時(最終投与後5〜10日目)の細菌性肺炎での治癒率(「治癒」であった被験者の割合)は70.0%(14/20例)であった。細菌学的効果が判定できた症例での治癒判定時の菌消失率は54.5%(6/11例)であった10)。
副作用(臨床検査値の異常変動を含む)は38例中17例(44.7%)に認められ、主な副作用はALT上昇、AST上昇、肝機能異常、好酸球増多、血管炎、注射部位紅斑及び注射部位反応であり、それぞれ2例(5.3%)に認められた。
副作用(臨床検査値の異常変動を含む)は38例中17例(44.7%)に認められ、主な副作用はALT上昇、AST上昇、肝機能異常、好酸球増多、血管炎、注射部位紅斑及び注射部位反応であり、それぞれ2例(5.3%)に認められた。
17.1.3 海外二重盲検比較試験(小児)
複雑性尿路感染症又は腎盂腎炎の小児患者(1〜17歳)を対象とした無作為化二重盲検並行群間比較試験において、治癒判定時(治療終了後5〜9日目)の臨床効果が「治癒」又は「改善」であった被験者の割合は、シプロフロキサシン注)95.7%(202/211例)、対照薬※192.6%(214/231例)であり、群間差[95%信頼区間]は、3[−1.3、7.3]%で、対照に対する非劣性(非劣性マージン:12%)が検証された。治癒判定時の菌消失率はシプロフロキサシン86%(178/206例)、対照薬81%(181/224例)であった2)。
副作用は335例中53例に認められ、主な副作用は下痢13件(3.9%)、嘔吐9件(2.7%)、消化不良7件(2.1%)等であった。
副作用は335例中53例に認められ、主な副作用は下痢13件(3.9%)、嘔吐9件(2.7%)、消化不良7件(2.1%)等であった。
17.1.4 海外二重盲検比較試験(小児)
嚢胞性線維症の肺感染増悪の小児患者(5〜17歳)を対象とした無作為化二重盲検並行群間比較試験において、投与終了時の臨床効果が「改善」であった被験者の割合は、シプロフロキサシン注)100%(41/41例)、対照薬※2100%(43/43例)であり、投与終了時の1秒量(FEV1)のベースラインからの変化率は、シプロフロキサシン12.3%、対照薬16.4%であった20)。
炭疽に対する臨床試験は国内外とも実施されていない。
副作用は67例中40例に認められ、主な副作用は肝機能検査異常11件(16.4%)、注射部位疼痛10件(14.9%)、注射部位反応10件(14.9%)、発疹7件(10.4%)、静脈炎7件(10.4%)、関節障害5件(7.5%)、嘔吐5件(7.5%)、関節痛4件(6.0%)、好酸球増加症4件(6.0%)等であった。
炭疽に対する臨床試験は国内外とも実施されていない。
副作用は67例中40例に認められ、主な副作用は肝機能検査異常11件(16.4%)、注射部位疼痛10件(14.9%)、注射部位反応10件(14.9%)、発疹7件(10.4%)、静脈炎7件(10.4%)、関節障害5件(7.5%)、嘔吐5件(7.5%)、関節痛4件(6.0%)、好酸球増加症4件(6.0%)等であった。
注)静注剤又は経口剤
※1:セフタジジムとセフィキシム又はトリメトプリム・スルファメトキサゾールとの併用レジメン
※2:トブラマイシンとセフタジジムとの併用レジメン
18. 薬効薬理
18.1 作用機序
細菌のDNAジャイレースに作用し、DNA合成を阻害する。抗菌作用は殺菌的で溶菌作用が認められる。最小発育阻止濃度は最小殺菌濃度とほぼ一致し、細菌の対数増殖期だけでなく休止期にも作用する21)。
18.2 抗菌作用
18.2.1 グラム陽性菌及びグラム陰性菌に対し広い抗菌スペクトルを有し、ブドウ球菌属、腸球菌属、炭疽菌、大腸菌、クレブシエラ属、エンテロバクター属、緑膿菌、レジオネラ属に対して優れた抗菌作用(in vitro)を示す。なお、ブドウ球菌属、腸球菌属、大腸菌、エンテロバクター属(Enterobacter cloacae)及び緑膿菌においては経口剤承認時に比べて感受性の低下傾向が認められている22)23)24)25)26)27)。
18.2.3 黄色ブドウ球菌、大腸菌、肺炎桿菌、緑膿菌のマウス全身感染症モデルに静脈内及び経口投与した試験では、いずれの菌株においても静脈内投与の治療効果は経口投与より優れ、ED50値は約1/14〜1/6倍である28)。
18.2.4 雌雄アカゲザルに炭疽菌芽胞を吸入曝露させた後の肺炭疽に対する発症抑制効果が検討された。同菌株に対するMICは0.08μg/mLであった。吸入曝露24時間後より本剤を30日間経口投与した結果、非治療群(10例中9例死亡:吸入曝露後3〜8日以内)と比較し、本剤投与群(9例中1例死亡:投与終了後6日目)で有意な死亡率の低下が認められた29)。
19. 有効成分に関する理化学的知見
19.1. シプロフロキサシン
20. 取扱い上の注意
20.1 製品の品質を保持するため、ソフトバッグの外袋は使用時まで開封しないこと。
20.2 外袋の内側に内容液の漏出が認められる場合は、無菌性が損なわれている可能性があるので、使用しないこと。
20.3 排出口をシールしているフィルムが万一はがれているときは使用しないこと。
20.4 外袋より取り出した後は、直射日光を避けて保存すること。
22. 包装
<シプロキサン注200mg>
100mL[ソフトバッグ1袋×10]
<シプロキサン注400mg>
200mL[ソフトバッグ1袋×10]
23. 主要文献
- Cockcroft DW,et al., Nephron., 16, 31-41, (1976) »PubMed
- 社内資料:複雑性尿路感染症又は腎盂腎炎の小児患者における二重盲検試験(外国人)(2015年9月24日承認、CTD2.7.6.22)
- 二木芳人他, 基礎と臨床, 20, 8903-8913, (1986)
- Roberge RJ,et al., Ann Emerg Med., 36, 160-163, (2000) »PubMed
- 中川武正他, 炎症, 15, 337-338, (1995) »DOI
- 安永幸二郎他, 基礎と臨床, 31, 2433-2466, (1997)
- 東純一他, 基礎と臨床, 31, 2701-2725, (1997)
- 社内資料:健康成人における薬物動態(外国人300及び400mg)(2015年9月24日承認、CTD2.7.6.1)
- 社内資料:健康成人における薬物動態(外国人200及び400mg)(2015年9月24日承認、CTD2.7.6.2)
- 社内資料:肺炎又は慢性呼吸器病変の二次感染の日本人患者における高用量の非盲検試験(2015年9月24日承認、CTD2.7.6.28)
- 安永幸二郎他, 基礎と臨床, 31, 2503-2512, (1997)
- 原耕平他, 日化療会誌, 45, 923-935, (1997) »DOI
- 小林宏行他, 日化療会誌, 45, 846-871, (1997) »DOI
- 相川直樹他, 日化療会誌, 45, 936-950, (1997) »DOI
- Bergan T, Diag Microbiol Infect Dis., 13, 103-114, (1990) »PubMed
- Shah A,et al., J Antimicrob Chemother., 38, 103-116, (1996) »PubMed
- 社内資料:血液透析患者における薬物動態(外国人)
- 社内資料:小児患者における薬物動態(外国人)
- 原耕平他, 日化療会誌, 45, 901-922, (1997) »DOI
- 社内資料:嚢胞性線維症の小児患者における二重盲検試験(外国人)(2015年9月24日承認、CTD2.7.6.24)
- 山下悟他, Chemotherapy., 33 (S-7), 1-17, (1985) »DOI
- 社内資料:キノロン系抗菌剤Ciprofloxacinに関するin vitro抗菌力
- 社内資料:新キノロン系合成抗菌剤Ciprofloxacinの試験管内抗菌力
- 社内資料:Ciprofloxacinに関する細菌学的評価
- Saito A,et al., J Antimicrob Chemother., 18, 251-260, (1986) »PubMed
- 山口惠三他, Jpn J Antibiotics., 61, 241-268, (2008) »DOI
- Takesue Y,et al., J Infect Chemother., 18, 816-826, (2012) »PubMed
- 西野武志他, Chemotherapy., 42, 140-145, (1996) »PubMed
- Friedlander AM,et al., J Inf Dis., 167, 1239-1243, (1993)
24. 文献請求先及び問い合わせ先
文献請求先
バイエル薬品株式会社
メディカルインフォメーション
〒530-0001
大阪市北区梅田二丁目4番9号
文献請求先
製品情報問い合わせ先
バイエル薬品株式会社
電話:0120-106-398
バイエル医療用医薬品のお問い合わせ先
26. 製造販売業者等
26.1 製造販売元
バイエル薬品株式会社
大阪市北区梅田二丁目4番9号