医薬品情報
| 総称名 | タグリッソ |
|---|---|
| 一般名 | オシメルチニブメシル酸塩 |
| 欧文一般名 | Osimertinib Mesilate |
| 製剤名 | オシメルチニブメシル酸塩錠 |
| 薬効分類名 | 抗悪性腫瘍剤 チロシンキナーゼ阻害剤 |
| 薬効分類番号 | 4291 |
| ATCコード | L01EB04 |
| KEGG DRUG |
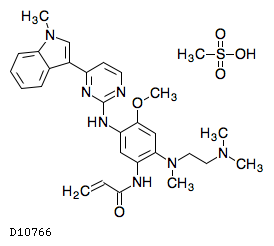
D10766
オシメルチニブメシル酸塩
|
| KEGG DGROUP |
DG03162
EGFR阻害薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年1月 改訂(再審査結果)(第8版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| タグリッソ錠40mg | TAGRISSO Tablets 40mg | アストラゼネカ | 4291045F1027 | 9670円/錠 | 劇薬, 処方箋医薬品注) |
| タグリッソ錠80mg | TAGRISSO Tablets 80mg | アストラゼネカ | 4291045F2023 | 18540.2円/錠 | 劇薬, 処方箋医薬品注) |
1. 警告
1.1 本剤は、緊急時に十分に対応できる医療施設において、がん化学療法に十分な知識・経験を持つ医師のもとで、電子添文を参照して、適切と判断される症例についてのみ投与すること。また、治療開始に先立ち、患者又はその家族に本剤の有効性及び危険性(特に、間質性肺疾患の初期症状、服用中の注意事項、死亡に至った症例があること等に関する情報)、非小細胞肺癌の治療法等を十分説明し、同意を得てから投与すること。
1.2 本剤の投与により間質性肺疾患があらわれ、死亡に至った症例が報告されているので、投与期間中にわたり、初期症状(呼吸困難、咳嗽、発熱等)の確認及び定期的な胸部画像検査の実施等、観察を十分に行うこと。異常が認められた場合には投与を中止し、適切な処置を行うこと。また、特に治療初期は入院又はそれに準ずる管理の下で、間質性肺疾患等の重篤な副作用発現に関する観察を十分に行うこと。[8.1、9.1.1、11.1.1参照]
1.3 本剤投与開始前に、胸部CT検査及び問診を実施し、間質性肺疾患の合併又は既往歴がないことを確認した上で、投与の可否を慎重に判断すること。[9.1.1参照]
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 妊婦又は妊娠している可能性のある女性[9.5参照]
4. 効能または効果
○EGFR遺伝子変異陽性の手術不能又は再発非小細胞肺癌
○EGFR遺伝子変異陽性の非小細胞肺癌における術後補助療法
○EGFR遺伝子変異陽性の切除不能な局所進行の非小細胞肺癌における根治的化学放射線療法後の維持療法
5. 効能または効果に関連する注意
<効能共通>
5.1 EGFR遺伝子変異検査を実施すること。EGFR遺伝子変異検査の実施には、十分な経験を有する病理医又は検査施設において、承認された体外診断用医薬品又は医療機器を用い、EGFR遺伝子変異が確認された患者に投与すること。なお、承認された体外診断用医薬品又は医療機器に関する情報については、以下のウェブサイトから入手可能である:
https://www.pmda.go.jp/review-services/drug-reviews/review-information/cd/0001.html
5.3 本剤の術前補助療法における有効性及び安全性は確立していない。
<EGFR遺伝子変異陽性の手術不能又は再発非小細胞肺癌>
5.4 他のEGFRチロシンキナーゼ阻害剤による治療歴を有し、病勢進行が確認されている患者では、EGFR T790M変異が確認された患者に投与すること。
<EGFR遺伝子変異陽性の非小細胞肺癌における術後補助療法>
5.5 白金系抗悪性腫瘍剤を含む術後補助療法の適応となる場合には、当該治療を終了した患者を対象とすること。
5.6 病理病期IB期(AJCC/UICC 第7版)の患者に対する有効性及び安全性は確立していない。
<EGFR遺伝子変異陽性の切除不能な局所進行の非小細胞肺癌における根治的化学放射線療法後の維持療法>
5.7 根治的化学放射線療法後に病勢進行が認められていない患者を対象とすること。
6. 用法及び用量
通常、成人にはオシメルチニブとして80mgを1日1回経口投与する。ただし、術後補助療法の場合は、投与期間は36カ月間までとする。なお、患者の状態により適宜減量する。
7. 用法及び用量に関連する注意
<効能共通>
7.1 副作用がみられた場合は、症状、重症度等に応じて、以下の基準を考慮して、本剤を休薬、減量又は中止すること。本剤を減量する場合には、40mgを1日1回投与すること。
| 副作用 | 程度 | 処置 |
| 間質性肺疾患/肺臓炎 | − | 本剤の投与を中止する。 |
| 放射線肺臓炎 | Grade1 | 患者の状態に応じて、本剤の投与を継続又は休薬する。 |
| Grade2 | Grade1以下に回復するまで本剤を休薬する。4週間以内にGrade1以下に回復した場合、必要に応じて本剤の減量を考慮し、投与を再開する。4週間以内にGrade1以下に回復しない場合及び再開後に再発した場合は、本剤の投与を中止する。 | |
| Grade3以上 | 本剤の投与を中止する。 | |
| QT間隔延長 | 500msecを超えるQTc値が認められる | 481msec未満又はベースラインに回復するまで本剤を休薬する。481msec未満又はベースラインに回復した後、本剤を減量し、投与を再開する。3週間以内に回復しない場合は本剤の投与を中止すること。 |
| 重篤な不整脈の症状/兆候を伴うQT間隔延長 | 本剤の投与を中止する。 | |
| その他の副作用 | Grade3以上 | Grade2以下に改善するまで本剤を休薬する。Grade2以下に回復した後、必要に応じて本剤の減量を考慮し、投与を再開する。3週間以内にGrade2以下に回復しない場合は本剤の投与を中止すること。 |
<EGFR遺伝子変異陽性の手術不能又は再発非小細胞肺癌>
7.2 本剤を他の抗悪性腫瘍剤と併用する場合、併用する他の抗悪性腫瘍剤は「17.臨床成績」の項の内容を熟知し選択すること。[17.1.4参照]
<EGFR遺伝子変異陽性の非小細胞肺癌における術後補助療法、EGFR遺伝子変異陽性の切除不能な局所進行の非小細胞肺癌における根治的化学放射線療法後の維持療法>
7.3 他の抗悪性腫瘍剤との併用について、有効性及び安全性は確立していない。
8. 重要な基本的注意
8.1 間質性肺疾患、放射線肺臓炎があらわれることがあるので、初期症状(呼吸困難、咳嗽、発熱等)の確認及び定期的な胸部画像検査の実施等、観察を十分に行うこと。必要に応じて、動脈血酸素分圧(PaO2)、動脈血酸素飽和度(SpO2)、肺胞気動脈血酸素分圧較差(A-aDO2)、肺拡散能力(DLco)等の検査を行うこと。また、患者に対して、初期症状があらわれた場合には、速やかに医療機関を受診するよう指導すること。[1.2、9.1.1、9.1.2、11.1.1参照]
8.2 QT間隔延長があらわれることがあるので、本剤投与開始前及び投与中は定期的に心電図検査及び電解質検査(カリウム、マグネシウム、カルシウム等)を行い、患者の状態を十分に観察すること。また、必要に応じて電解質補正を行うこと。[9.1.3、11.1.2参照]
8.3 血小板減少、好中球減少、白血球減少、貧血があらわれることがあるので、本剤投与開始前及び投与中は定期的に血液検査(血球数算定、白血球分画等)を行い、患者の状態を十分に観察すること。[11.1.3参照]
8.4 肝機能障害があらわれることがあるので、本剤投与開始前及び投与中は定期的に肝機能検査を行い、患者の状態を十分に観察すること。[11.1.4参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 間質性肺疾患のある患者又はその既往歴のある患者
9.1.2 放射線肺臓炎のある患者
9.1.3 QT間隔延長のおそれ又はその既往歴のある患者
9.3 肝機能障害患者
9.3.1 重度の肝機能障害(Child-Pugh分類C)のある患者
血漿中濃度が上昇するおそれがある。[16.6.1参照]
9.4 生殖能を有する者
9.4.1 妊娠する可能性のある女性には、本剤投与中及び最終投与後6週間において避妊する必要性及び適切な避妊法について説明すること。[9.5参照]
9.4.2 男性には、本剤投与中及び最終投与後4カ月間においてバリア法(コンドーム)を用いて避妊する必要性について説明すること。
9.5 妊婦
9.6 授乳婦
授乳しないことが望ましい。本剤又は本剤の代謝物がヒトの母乳中に移行するかどうかは不明であるが、動物実験(ラット)で授乳中の母動物へ本剤を投与した際、本剤及び本剤の代謝物が授乳された児に検出され、成長及び生存への悪影響が認められている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
副作用があらわれやすいので、患者の状態を観察しながら慎重に投与すること。一般に高齢者では生理機能が低下していることが多い。
10. 相互作用
相互作用序文
薬物代謝酵素用語
CYP3A
薬物代謝酵素用語
Breast Cancer Resistance Protein(BCRP)
薬物代謝酵素用語
P糖蛋白質(P-gp)
10.2 併用注意
| CYP3A誘導剤 フェニトイン、リファンピシン、カルバマゼピン、セイヨウオトギリソウ(St.John's Wort)等 [16.7.1参照] | 本剤の効果が減弱するおそれがあるので、CYP3A誘導作用のない薬剤への代替を考慮すること。 | 左記薬剤のCYP3A誘導作用により、本剤の代謝が亢進し、血中濃度が低下する可能性がある。 |
| P-gpの基質となる薬剤 フェキソフェナジン、ジゴキシン、ダビガトランエテキシラート、アリスキレン等 [16.7.2参照] | 副作用の発現が増強されるおそれがあるので、患者の状態をよく観察して、副作用の発現に十分注意すること。 | 本剤のP-gp阻害作用により、左記薬剤の血中濃度が増加する可能性がある。 |
| BCRPの基質となる薬剤 ロスバスタチン、サラゾスルファピリジン等 [16.7.3参照] | 副作用の発現が増強されるおそれがあるので、患者の状態をよく観察して、副作用の発現に十分注意すること。 | 本剤のBCRP阻害作用により、左記薬剤の血中濃度が増加する可能性がある。 |
| QT間隔延長を起こすことが知られている薬剤 キニジン、プロカインアミド、オンダンセトロン、クラリスロマイシン等 | QT間隔延長を増強するおそれがある。 | 本剤及びこれらの薬剤はいずれもQT間隔を延長させるおそれがあるため、併用により作用が増強するおそれがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 間質性肺疾患(3.3%、6.3%)注)、放射線肺臓炎(頻度不明、3.5%)注)
11.1.3 血小板減少(9.2%)、好中球減少(8.1%)、白血球減少(10.0%)、貧血(4.6%)[8.3参照]
11.1.4 肝機能障害(8.5%)
ALT、AST、ビリルビン等の上昇を伴う肝機能障害があらわれることがある。[8.4参照]
11.1.5 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(頻度不明)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)、多形紅斑(0.3%)
11.1.6 うっ血性心不全(頻度不明)、左室駆出率低下(頻度不明)
注)発現頻度は、以下の順に記載した。
−臨床試験(AURA3試験、FLAURA試験、ADAURA試験、FLAURA2試験)における本剤単独投与時の併合解析
−根治的化学放射線療法後に本剤を投与した臨床試験(LAURA試験)
11.2 その他の副作用
| 10%以上 | 10%未満1%以上 | 1%未満 | 頻度不明 | |
| 皮膚 | 発疹・ざ瘡等(40.8%)、皮膚乾燥・湿疹等(26.2%)、爪の障害(爪囲炎を含む)(30.6%)、そう痒症(13.6%) | 脱毛、手掌・足底発赤知覚不全症候群、皮膚剥脱、じん麻疹 | 皮膚潰瘍、多毛症、爪痛、皮膚疼痛、皮膚変色、皮膚感染、皮脂欠乏性湿疹、過角化、光線過敏性反応、毛細血管拡張症、蜂巣炎、皮膚反応、黄色板腫 | 毛髪障害、毛質異常、皮膚嚢腫、斑、裂傷、皮膚擦過傷、メラノサイト性母斑、皮膚血管炎 |
| 消化器 | 下痢(38.7%)、口内炎(23.6%) | 嘔吐、食欲減退、便秘、口内乾燥、腹痛、消化不良 | 口唇炎、舌痛、腹部膨満、腹部不快感、胃食道逆流性疾患、嚥下障害、口腔咽頭痛、鼓腸、心窩部不快感、胃腸炎 | 口唇びらん、口腔知覚不全、食道痛、呼気臭、便意切迫、肛門周囲痛、痔出血 |
| 血液 | リンパ球減少症 | 活性化部分トロンボプラスチン時間延長、内出血発生の増加傾向、播種性血管内凝固、血球減少症、脾臓梗塞 | ||
| 神経 | 味覚異常、頭痛 | 末梢性ニューロパチー、末梢性感覚ニューロパチー、脳梗塞、めまい、回転性めまい、異常感覚、感覚鈍麻 | 振戦、体位性めまい、記憶障害、構語障害、知覚過敏 | |
| 眼 | 眼乾燥、結膜炎、霧視 | 眼瞼炎、角膜炎、白内障、流涙増加、眼刺激、羞明、視力低下、視力障害、眼そう痒症、眼精疲労、眼感染 | 黄斑浮腫、網膜出血、夜盲、眼の異物感 | |
| 呼吸器 | 鼻乾燥、鼻出血、咳嗽 | 呼吸困難、気管支炎、肺感染、ウイルス性上気道感染、肺塞栓症、インフルエンザ、鼻漏、鼻の炎症、咽頭炎、気胸、湿性咳嗽、発声障害、鼻炎、咽喉乾燥、喉頭痛、しゃっくり、労作性呼吸困難 | 細菌性肺炎、鼻粘膜障害、咽頭出血、咽頭潰瘍、気縦隔症、胸膜炎 | |
| 循環器 | 駆出率減少 | 非心臓性胸痛、動悸 | 房室ブロック | |
| 腎臓 | クレアチニン増加 | 頻尿、尿路感染、腎機能障害、血尿、排尿困難、膀胱炎 | 腎結石症 | |
| 全身 | 疲労、無力症、末梢性浮腫 | 発熱、四肢膿瘍、顔面浮腫、倦怠感 | 悪寒、ほてり | |
| 筋骨格系 | 筋痙縮、筋肉痛、四肢痛、関節痛 | 背部痛、筋骨格硬直、頚部痛 | 筋骨格痛、足変形、骨盤痛 | |
| 感染症 | 耳感染 | 外耳炎、乳頭炎 | ||
| 代謝及び栄養障害 | 低カリウム血症 | 高カリウム血症、脱水、高血糖、低リン酸血症、高コレステロール血症 | ||
| 精神障害 | うつ病、錯乱状態、幻覚、易刺激性 | |||
| 血管障害 | 深部静脈血栓症、高血圧 | 静脈炎 | ||
| 泌尿器・生殖器 | 外陰腟痛 | |||
| その他 | 体重減少、ALP増加、血中クレアチンホスホキナーゼ増加 | 低アルブミン血症、低カルシウム血症、低ナトリウム血症、アミラーゼ増加 | 高リパーゼ血症、血中コレステロール増加 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することが報告されている。
15. その他の注意
15.1 臨床使用に基づく情報
国内で実施したEGFRチロシンキナーゼ阻害剤に抵抗性のEGFR T790M変異陽性の手術不能又は再発非小細胞肺癌患者を対象とした使用成績調査(全例調査)における多変量解析(主要解析)の結果、間質性肺疾患の病歴、ニボルマブ前治療歴は間質性肺疾患の発現因子となることが示唆されている。
15.2 非臨床試験に基づく情報
15.2.1 ラット及びイヌを用いた反復投与毒性試験において、AUC比較で臨床曝露量未満に相当する用量から消化管(舌を含む)及び皮膚の上皮の萎縮、炎症又は変性、並びに角膜の上皮萎縮、半透明化及び白濁が認められ、角膜の白濁については回復性が確認されていない。
15.2.2 ラット及びイヌを用いた長期の反復投与毒性試験において、AUC比較で臨床曝露量に相当する又は未満に相当する用量から瞼板腺の潰瘍形成、リンパ球浸潤及び導管拡張が認められた。
15.2.3 ラットを用いた104週間がん原性試験において、AUC比較で臨床曝露量の0.2倍に相当する用量で水晶体線維の変性が認められた。また、AUC比較で臨床曝露量に相当する用量で腸間膜リンパ節の血管腫が認められ、雌では血管腫様過形成の発生頻度の上昇が認められた。
15.2.4 ラット及びイヌにおいてAUC比較で臨床曝露量未満に相当する用量で雄性生殖器の変化(精巣の精細管変性、精巣上体の精子減少等)が認められている。また、ラットにおいてAUC比較で臨床曝露量未満に相当する用量で雄受胎能への影響が認められている。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
国際共同第I/II相試験(AURA試験)の第I相部分において、外国人進行非小細胞肺癌患者(11例)に本剤80mgを単回経口投与したとき、オシメルチニブの吸収は緩徐であり、最高血漿中濃度到達時間(tmax)は中央値で約6時間(範囲:2〜24時間)であり、終末相における消失半減期は平均で48.6時間(標準偏差:6.5時間)であった。なお、本剤投与時のオシメルチニブの最高血漿中濃度(Cmax)及び投与後0時間から72時間までの血漿中濃度時間曲線下面積(AUC(0-72))は20〜240mg注)の用量範囲で用量に比例して増加した。外国人進行非小細胞肺癌患者に本剤80mgを単回経口投与したときのオシメルチニブの血漿中濃度推移及び薬物動態パラメータは以下の通りである1)。
注)本剤の承認用法・用量は80mgの1日1回投与である。
図1 外国人進行非小細胞肺癌患者に本剤80mgを単回経口投与したときの血漿中オシメルチニブ濃度推移(算術平均±標準偏差、n=11)
| Cmax(nM) | tmax(h)a | AUC(nM・h)b | t1/2(h)b |
| 247.2±173.6 | 6(2.07〜23.83) | 12170±7340 | 48.6±6.5 |
16.1.2 反復投与
国際共同第I/II相試験(AURA試験)の第II相部分において、日本人進行非小細胞肺癌患者(32例)に本剤80mgを1日1回反復経口投与したとき、オシメルチニブの吸収は緩徐であり、最高血漿中濃度到達時間(tss,max)は中央値で約6時間(範囲:2〜11時間)であった。日本人進行非小細胞肺癌患者に本剤80mgを反復経口投与したときのオシメルチニブの血漿中濃度推移並びにオシメルチニブ及びその活性代謝物(AZ5104及びAZ7550)の薬物動態パラメータは以下の通りである1)。
図2 日本人進行非小細胞肺癌患者に本剤80mgを1日1回反復経口投与したときの投与22日目における血漿中オシメルチニブ濃度推移(算術平均±標準偏差、n=32)
| Css,max(nM) | tss,max(h)a | AUCss(nM・h) | |
| オシメルチニブ | 782.4±333 | 6(2〜11.05) | 14980±6809 |
| AZ5104 | 80.43±46.83 | 6.04(0〜23.93) | 1619±972.3 |
| AZ7550 | 60.75±17.09 | 8(0〜11.95) | 1260±378.5 |
16.2 吸収
16.2.1 バイオアベイラビリティ
健康被験者(10例)に本剤80mgを単回経口投与及び14Cで標識した本剤100μgを単回静脈内投与したとき、オシメルチニブの絶対バイオアベイラビリティは約70%であった2)(外国人データ)。
16.2.2 食事の影響
進行非小細胞肺癌患者(34例)に本剤80mgを高脂肪食摂取後に単回経口投与したとき、オシメルチニブのAUC及びCmaxに食事による影響は認められなかった3)(外国人データ)。
16.3 分布
16.4 代謝
16.5 排泄
健康被験者に14Cで標識した本剤20mgを単回経口投与したとき、84日間までに放射能(投与量の67.8%)は主に糞便中に未変化体又は代謝物として排泄され、尿中排泄率は約14.2%であった。尿中に排泄された未変化体は投与量の2%未満であった5)(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 肝機能障害者
肝機能が正常な進行固形癌患者(10例)、軽度(Child-Pugh分類A)及び中等度(Child-Pugh分類B)の肝機能障害を有する進行固形癌患者(それぞれ7例及び5例)に本剤80mgを単回経口投与したとき、オシメルチニブのCmax及びAUCは軽度肝機能障害者で肝機能正常者のそれぞれ51%(90%信頼区間:37%〜72%)及び63%(90%信頼区間:47%〜85%)、中等度肝機能障害者で肝機能正常者のそれぞれ61%(90%信頼区間:42%〜89%)及び68%(90%信頼区間:50%〜94%)であり、肝機能正常者に比べ軽度及び中等度肝機能障害者においてオシメルチニブの曝露量が高値を示すことはなかった7)(外国人データ)。[9.3.1参照]
16.6.2 腎機能障害者
腎機能が正常(クレアチニンクリアランスが90mL/min以上)な進行固形癌患者(8例)及び重度(クレアチニンクリアランスが30mL/min未満)の腎機能障害を有する進行固形癌患者(7例:透析患者は含まれていない)に本剤80mgを単回経口投与したとき、オシメルチニブのCmax及びAUCは腎機能正常者に比べ重度腎機能障害者においてそれぞれ19%(90%信頼区間:−31%〜107%)及び85%(90%信頼区間:−6%〜264%)高値を示した8)(外国人データ)。
16.7 薬物相互作用
16.7.1 リファンピシン
16.7.2 フェキソフェナジン
16.7.3 ロスバスタチン
16.7.4 その他の薬剤
(1)健康被験者(57例)にオメプラゾールを5日間投与し、胃内pHを上昇させた条件にて、5日目に本剤80mgを併用投与したとき、オシメルチニブのAUC及びCmaxに臨床上問題となる影響は認められなかった3)(外国人データ)。
(2)進行非小細胞肺癌患者(36例)に本剤80mgを強力なCYP3A阻害剤であるイトラコナゾール(200mgを1日2回)と併用投与したとき、オシメルチニブの曝露量に臨床上問題となる影響は認められなかった(Cmaxは20%[90%信頼区間:13%〜27%]低下、AUCは24%[90%信頼区間:15%〜35%]増加)9)(外国人データ)。
(3)進行非小細胞肺癌患者(49例)に本剤80mg/日を反復投与した後、CYP3Aの基質であるシンバスタチン(40mg)を併用投与したとき、シンバスタチンの曝露量に臨床上問題となる影響は認められなかった(AUC及びCmaxはそれぞれ9%[90%信頼区間:−8%〜23%]及び23%[90%信頼区間:6%〜37%]低下)11)(外国人データ)。
16.8 その他
16.8.1 薬物動態とQT間隔との関連性
国際共同第II相試験(AURA2試験)において、本剤を80mgの用量で1日1回反復投与された210例の進行非小細胞肺癌患者において本剤がQT間隔に及ぼす影響を評価した。単回投与時及び反復投与後の定常状態時にデジタルECGを頻回測定し、血漿中未変化体濃度とQT間隔との関連性を評価した。血漿中未変化体濃度とQTc間隔との関係を解析したところ、本剤の投与に起因するQTc間隔の延長は平均で14ms、その90%信頼区間の上限は16msと予測された14)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国際共同第III相試験(AURA3試験)15)
EGFRチロシンキナーゼ阻害剤による治療後に病勢進行したEGFR T790M変異注1)陽性の切除不能な進行・再発の非小細胞肺癌患者注2)419例(本剤群279例、化学療法群140例)(日本人63例[本剤群41例、化学療法群22例])を対象として、本剤80mgと化学療法(ペメトレキセドナトリウム水和物及び白金系抗悪性腫瘍剤の併用投与)の有効性及び安全性を比較する国際共同第III相非盲検無作為化試験が実施された。主要評価項目である主治医判定による無増悪生存期間(中央値[95%信頼区間])の結果は、本剤群で10.1[8.3〜12.3]カ月、化学療法群で4.4[4.2〜5.6]カ月であった(ハザード比[95%信頼区間]:0.30[0.23〜0.41]、p<0.001)(2016年4月15日カットオフデータに基づく集計)。
注1)EGFR遺伝子の活性型変異が腫瘍組織検体で確認され、かつ、EGFRチロシンキナーゼ阻害剤による一次治療後に病勢進行が確認された後に、エクソン20の変異(T790M)が認められた患者が組み入れられた。
注2)非小細胞肺癌のうち、扁平上皮癌が除外基準とされた。
図1 AURA3試験における無増悪生存期間(主治医判定)のKaplan-Meier曲線
安全性評価対象症例279例(日本人41例を含む)中236例(84.6%)に副作用が認められ、主な副作用は、発疹・ざ瘡等87例(31.2%)、下痢86例(30.8%)、爪の障害(爪囲炎を含む)63例(22.6%)、皮膚乾燥・湿疹等53例(19.0%)等であった。また、日本人集団では41例中39例(95.1%)に副作用が認められ、主な副作用は、爪の障害(爪囲炎を含む)20例(48.8%)、下痢14例(34.1%)、発疹・ざ瘡等14例(34.1%)、間質性肺疾患3例(7.3%)等であった。(2016年9月までの集計)[5.2参照]
17.1.2 国際共同第III相試験(FLAURA試験)16)
化学療法歴のないEGFR遺伝子の活性型変異注3)陽性の切除不能な進行・再発の非小細胞肺癌患者注4)556例(本剤群279例、標準的な治療群277例)(日本人120例[本剤群65例、標準的な治療群55例])を対象として、本剤80mgと標準的な治療(ゲフィチニブ又はエルロチニブ塩酸塩)の有効性及び安全性を比較する国際共同第III相二重盲検無作為化試験が実施された。主要評価項目である主治医判定による無増悪生存期間(中央値[95%信頼区間])の結果は、本剤群で18.9[15.2〜21.4]カ月、標準的な治療群で10.2[9.6〜11.1]カ月であった(ハザード比[95%信頼区間]:0.46[0.37〜0.57]、p<0.0001)(2017年6月12日カットオフデータに基づく集計)。
注3)EGFR遺伝子の活性型変異であるエクソン19の欠失(Ex19del)又はエクソン21の変異(L858R)が腫瘍組織検体で確認された患者が組み入れられた。
注4)非小細胞肺癌のうち、腺癌又は腺癌が優勢の混合性の組織型の癌が確認された患者が組み入れられた。
図2 FLAURA試験における無増悪生存期間(主治医判定)のKaplan-Meier曲線
安全性評価対象症例279例(日本人65例を含む)中253例(90.7%)に副作用が認められ、主な副作用は、発疹・ざ瘡等152例(54.5%)、下痢138例(49.5%)、皮膚乾燥・湿疹等93例(33.3%)、爪の障害(爪囲炎を含む)91例(32.6%)等であった。また、日本人集団では65例中64例(98.5%)に副作用が認められ、主な副作用は、発疹・ざ瘡等45例(69.2%)、下痢37例(56.9%)、爪の障害(爪囲炎を含む)35例(53.8%)、間質性肺疾患8例(12.3%)等であった。(効能・効果の一部変更承認時)[5.2参照]
17.1.3 国際共同第III相試験(ADAURA試験)17)
病理病期IB〜IIIA期注5)(本邦では病理病期II〜IIIA期の患者のみが組み入れられた)のEGFR遺伝子変異注3)陽性の非小細胞肺癌の術後患者注6)682例を対象として、本剤80mgとプラセボの有効性及び安全性を比較する国際共同第III相二重盲検無作為化試験が実施された。事前に治験実施計画書に規定されていない時点の解析注7)であるが、主要評価項目であるII〜IIIA期注8)の患者における主治医判定による無病生存期間の結果は、下表のとおりであった。
注5)切除検体の病理診断においてAJCC/UICC病期分類(第7版)に基づくStage IB、Stage II、又はStage IIIAに該当する患者が対象とされた。
注6)白金系抗悪性腫瘍剤を含む術後化学療法歴の有無にかかわらず、非小細胞肺癌のうち、非扁平上皮癌の患者が組み入れられた。
注7)2020年1月17日及び2021年2月1日をデータカットオフとして2回の解析が実施された。
注8)AJCC/UICC病期分類(第7版)に基づくStage II、又はStage IIIAに該当する患者が対象とされた。
| 2020年1月17日データカットオフの解析 | 2021年2月1日データカットオフの解析 | |||
| 本剤群 | プラセボ群 | 本剤群 | プラセボ群 | |
| 症例数(日本人症例数) | 233(46) | 237(53) | 233(46) | 237(53) |
| イベント数 | 26 | 130 | 48 | 154 |
| 無病生存期間(月) (中央値[95%信頼区間]) | 到達せず [38.8、算定不能] | 19.6 [16.6、24.5] | 49.9 [49.5、算定不能] | 21.9 [16.6、27.5] |
| ハザード比a [95%信頼区間] | 0.17[0.12、0.23] | 0.18[0.14、0.25] | ||
図3 ADAURA試験のII〜IIIA期の患者における無病生存期間(主治医判定)のKaplan-Meier曲線(2020年1月17日データカットオフ)
図4 ADAURA試験のII〜IIIA期の患者における無病生存期間(主治医判定)のKaplan-Meier曲線(2021年2月1日データカットオフ)
安全性評価対象症例337例(日本人46例を含む)中308例(91.4%)に副作用が認められ、主な副作用は、下痢135例(40.1%)、爪囲炎83例(24.6%)、皮膚乾燥71例(21.1%)、そう痒症60例(17.8%)、口内炎53例(15.7%)、ざ瘡様皮膚炎35例(10.4%)等であった。また、日本人集団では46例中45例(97.8%)に副作用が認められ、主な副作用は、下痢21例(45.7%)、爪囲炎21例(45.7%)、皮膚乾燥19例(41.3%)、口内炎13例(28.3%)、ざ瘡様皮膚炎12例(26.1%)、間質性肺疾患6例(13.0%)等であった。(2021年2月1日カットオフデータに基づく集計)[5.2参照]
17.1.4 国際共同第III相試験(FLAURA2試験)18)
化学療法歴のないEGFR遺伝子の活性型変異注3)陽性の切除不能な進行・再発の非小細胞肺癌患者注4)557例(本剤併用群279例、本剤単独群278例)(日本人94例[本剤併用群47例、本剤単独群47例])を対象として、本剤80mg及び化学療法(ペメトレキセドナトリウム水和物及び白金系抗悪性腫瘍剤)注9)の併用治療と本剤80mgによる単独治療の有効性及び安全性を比較する国際共同第III相非盲検無作為化試験が実施された。主要評価項目である主治医判定による無増悪生存期間(中央値[95%信頼区間])の結果は、本剤併用群で25.5[24.7〜算出不能]カ月、本剤単独群で16.7[14.1〜21.3]カ月であった(ハザード比[95%信頼区間]:0.62[0.49〜0.79]、p<0.0001)(2023年4月3日カットオフデータに基づく集計)。
図5 FLAURA2試験における無増悪生存期間(主治医判定)のKaplan-Meier曲線(2023年4月3日データカットオフ)
安全性評価対象症例のうち、本剤併用群の276例(日本人47例を含む)中241例(87.3%)に副作用が認められ、主な副作用は、下痢85例(30.8%)、発疹・爪囲炎 各62例(22.5%)、口内炎56例(20.3%)等であった。また、日本人集団では47例中46例(97.9%)に副作用が認められ、主な副作用は、下痢29例(61.7%)、爪囲炎28例(59.6%)、口内炎27例(57.4%)、間質性肺疾患5例(10.6%)等であった。本剤単独群の275例(日本人46例を含む)中241例(87.6%)に副作用が認められ、主な副作用は、下痢94例(34.2%)、爪囲炎71例(25.8%)、皮膚乾燥59例(21.5%)等であった。また、日本人集団では46例中全例に副作用が認められ、主な副作用は、下痢31例(67.4%)、爪囲炎28例(60.9%)、口内炎23例(50.0%)、間質性肺疾患2例(4.3%)等であった(2023年4月3日カットオフデータに基づく集計)。[5.2、7.2参照]
注9)ペメトレキセド500mg/m2及びシスプラチン75mg/m2又はカルボプラチンAUC5mg・min/mL相当量を3週間間隔で4回投与後、ペメトレキセド500mg/m2を3週間間隔で投与した。
17.1.5 国際共同第III相試験(LAURA試験)19)
根治的化学放射線療法注10)後に病勢進行が認められなかった切除不能な局所進行のEGFR遺伝子変異注3)陽性の非小細胞肺癌患者216例(本剤群143例、プラセボ群73例)(日本人30例[本剤群23例、プラセボ群7例])を対象として、化学放射線療法終了後42日以内に本剤80mg又はプラセボを投与した場合の有効性及び安全性を比較する国際共同第III相二重盲検無作為化試験が実施された。主要評価項目である盲検下独立中央判定による無増悪生存期間(中央値[95%信頼区間])の結果は、本剤群で39.13[31.51〜算出不能]カ月、プラセボ群で5.55[3.71〜7.43]カ月であった(ハザード比[95%信頼区間]:0.16[0.10〜0.24]、p<0.001、有意水準[両側]0.05)(2024年1月5日カットオフデータに基づく集計)。
注10)化学放射線療法における化学療法は、白金系抗悪性腫瘍剤と他の抗悪性腫瘍剤(エトポシド、ビンブラスチン、ビノレルビン、パクリタキセル、ドセタキセル、ペメトレキセド又はゲムシタビン[逐次化学放射線療法の場合のみ許容]のうち1剤)との併用投与とし、放射線療法は総線量54〜66Gyの照射とした。同時化学放射線療法の場合は、2サイクル以上の化学療法と放射線療法を同時に受け、かつ無作為化割付け前42日以内に完了することとし、逐次化学放射線療法の場合は、放射線療法前に化学療法を2サイクル以上受け、かつ無作為化割付け前42日以内に完了することとした。
図6 LAURA試験における無増悪生存期間(盲検下独立中央判定)のKaplan-Meier曲線
安全性評価対象症例143例(日本人23例を含む)中115例(80.4%)に副作用が認められ、主な副作用は、下痢30例(21.0%)、発疹29例(20.3%)、爪囲炎21例(14.7%)、皮膚乾燥・そう痒症・白血球数減少各15例(10.5%)、等であった。また、日本人集団では23例中21例(91.3%)に副作用が認められ、主な副作用は、発疹8例(34.8%)、下痢・爪囲炎各7例(30.4%)等であった。(2024年1月5日カットオフデータに基づく集計)[5.2参照]
18. 薬効薬理
18.1 作用機序
本剤は、活性型変異(L858R等)を有するEGFRチロシンキナーゼ並びに活性型変異及びT790M変異を有するEGFRチロシンキナーゼに対して阻害作用を示すことにより、EGFR遺伝子変異を有する腫瘍の増殖を抑制すると考えられている20)。
18.2 抗腫瘍効果
18.2.1 in vitro試験
本剤は、EGFR活性型変異を有する非小細胞肺癌(NSCLC)由来PC9細胞株(Ex19del)、EGFR活性型変異及びT790M変異を有するNSCLC由来H1975(L858R/T790M)及びPC9VanR(Ex19del/T790M)細胞株の増殖を抑制した21)。
18.2.2 in vivo試験
19. 有効成分に関する理化学的知見
19.1. オシメルチニブメシル酸塩
22. 包装
<タグリッソ錠40mg>
28錠[14錠(PTP)×2]
<タグリッソ錠80mg>
14錠[14錠(PTP)×1]
23. 主要文献
- 社内資料:非小細胞肺癌患者を対象とした国際共同第I/II相試験(AURA試験)及び国際共同第II相試験(AURA2試験)で認められた体内動態, (2015)
- Vishwanathan K,et al., Clin Pharmacol Drug Dev., 8 (2), 198-207, (2019) »PubMed
- Vishwanathan K,et al., J Clin Pharmacol., 58 (4), 474-484, (2018) »PubMed
- 社内資料:オシメルチニブのヒト血漿蛋白結合率, (2016)
- Dickinson PA,et al., Drug Metab Dispos, 44 (8), 1201-1212, (2016) »PubMed
- 社内資料:ヒトに[14C]-オシメルチニブを投与したマスバランス試験(2016年3月28日承認、CTD2.7.2.2.2.1.3), (2015)
- Grande E,et al., J Pharmacol Exp Ther, 369 (2), 291-299, (2019) »PubMed
- Vishwanathan K,et al., Pharmacol Res Perspect., 8 (4), e00613, (2020), (DOI:10.1002/prp2.613) »PubMed
- Vishwanathan K,et al., Br J Clin Pharmacol., 84 (6), 1156-1169, (2018) »PubMed
- Calvo E,et al., J Clin Pharmacol., 59 (8), 1099-1109, (2019) »PubMed
- Harvey RD,et al., Br J Clin Pharmacol., 84 (12), 2877-2888, (2018) »PubMed
- 社内資料:CYPに対する誘導作用[in vitro試験](2016年3月28日承認、CTD2.6.4.7.5), (2014)
- 社内資料:P-gp及びBCRPの関与[in vitro試験](2016年3月28日承認、CTD2.6.4.7.6.1), (2013)
- 社内資料:血漿中濃度とQT間隔との関連性(2016年3月28日承認、CTD2.7.2.3.5.2.3), (2015)
- Mok TS,et al., N Engl J Med., 376 (7), 629-640, (2017) »PubMed
- Soria JC,et al., N Engl J Med., 378 (2), 113-125, (2018) »PubMed
- Wu YL,et al., N Engl J Med., 383 (18), 1711-1723, (2020) »PubMed
- Planchard D,et al., N Engl J Med., 389 (21), 1935-1948, (2023) »PubMed
- Lu S,et al., N Engl J Med., 391 (7), 585-597, (2024) »PubMed
- Cross DA,et al., Cancer Discov., 4 (9), 1046-1061, (2014) »PubMed
- 社内資料:In vitroにおける細胞増殖抑制作用(2016年3月28日承認、CTD2.6.2.2.1.6), (2014)
- 社内資料:EGFR依存性腫瘍異種移植モデルにおける抗腫瘍作用(2016年3月28日承認、CTD2.6.2.2.2.1), (2013〜2014)
- 社内資料:EGFRm/T790M変異を有するトランスジェニックモデルにおける抗腫瘍作用(2016年3月28日承認、CTD2.6.2.2.2.5), (2012)
- 社内資料:脳転移異種移植モデルにおける抗腫瘍作用(2016年3月28日承認、CTD2.6.2.2.2.6), (2014)
- Nanjo S,et al., Oncotarget., 7 (4), 3847-3856, (2016) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
アストラゼネカ株式会社
メディカルインフォメーションセンター
〒530-0011
大阪市北区大深町3番1号
電話:0120-189-115
製品情報問い合わせ先
アストラゼネカ株式会社
メディカルインフォメーションセンター
〒530-0011
大阪市北区大深町3番1号
電話:0120-189-115
26. 製造販売業者等
26.1 製造販売元
アストラゼネカ株式会社
大阪市北区大深町3番1号