医薬品情報
| 総称名 | ラパリムス |
|---|---|
| 一般名 | シロリムス |
| 欧文一般名 | Sirolimus |
| 製剤名 | シロリムス外用ゲル剤 |
| 薬効分類名 | 結節性硬化症に伴う皮膚病変治療剤(mTOR阻害剤) |
| 薬効分類番号 | 4291 |
| ATCコード | L01EG04 L04AH01 |
| KEGG DRUG |
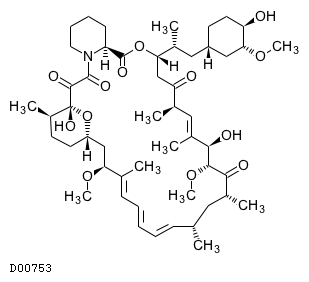
D00753
シロリムス
|
| KEGG DGROUP |
DG01597
mTOR阻害薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2022年3月 改訂(第2版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ラパリムスゲル0.2% | Rapalimus Gel 0.2% | ノーベルファーマ | 4291700Q1028 | 3926.4円/g | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
本剤の成分又はシロリムス誘導体に対し過敏症の既往歴のある患者
4. 効能または効果
結節性硬化症に伴う皮膚病変
5. 効能または効果に関連する注意
白斑、シャグリンパッチ及び爪線維腫に対する本剤の有効性は確認されていない。
6. 用法及び用量
通常、1日2回、患部に適量を塗布する。
7. 用法及び用量に関連する注意
7.1 1日あたりの最大塗布量については、以下を目安にすること。
| 年齢(体表面積)区分 | 1日最大塗布量 |
| 5歳以下(0.8m2未満) | 0.4g |
| 6〜11歳(0.8m2以上1.3m2未満) | 0.6g |
| 12歳以上(1.3m2以上) | 0.8g |
7.2 治療開始12週以内に症状の改善が認められない場合には本剤の必要性を検討し、漫然と投与を継続しないこと。
8. 重要な基本的注意
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性に対しては、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.7 小児等
3歳未満の幼児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
10. 相互作用
10.2 併用注意
| PUVA療法等の紫外線療法 [8参照] | 光線過敏症が発現するおそれがある。 | 本剤の使用により光感受性が増強されるおそれがある。 |
11. 副作用
11.2 その他の副作用
| 10%以上 | 10%未満 | 頻度不明 | |
| 感染症 | 結膜炎、毛包炎、せつ、口腔ヘルペス | ||
| 代謝・栄養 | 高トリグリセリド血症 | ||
| 神経系 | 錯感覚 | ||
| 眼 | 眼瞼紅斑、眼刺激、眼充血 | ||
| 血管障害 | ほてり | ||
| 呼吸器 | 鼻部不快感 | ||
| 胃腸障害 | 急性膵炎、口内炎 | ||
| 皮膚・皮下組織 | 皮膚乾燥(30.4%)、ざ瘡(10.1%) | 皮膚嚢腫、皮膚炎、ざ瘡様皮膚炎、接触皮膚炎、湿疹、紅斑、そう痒症、発疹、そう痒性皮疹、脂漏性皮膚炎、皮膚刺激、蕁麻疹、乾皮症、皮脂欠乏症、皮膚出血 | |
| 腎・尿路 | 蛋白尿 | ||
| 生殖器 | 精子数減少 | ||
| 全身・投与局所 | 適用部位刺激感(27.0%) | 異常感、適用部位異常感覚、適用部位腫脹、適用部位出血 | 適用部位疼痛 |
| 臨床検査 | 血小板数増加 | ||
| 傷害・処置 | 皮膚擦過傷 |
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 皮膚以外の部位(粘膜等)には使用しないこと。また、眼の周囲に使用する場合には眼に入らないように注意すること。
14.1.2 創傷、皮膚感染症又は湿疹・皮膚炎等がみられる部位は避けて塗布すること。
15. その他の注意
15.2 非臨床試験に基づく情報
モルモットの皮膚光感作性試験において、光線過敏様皮膚反応を示すとの報告がある1)。[8参照]
16. 薬物動態
16.1 血中濃度
(1)12週間投与
日本人結節性硬化症患者30例(成人17例、小児13例)において、本剤を1日2回12週間顔面又は頭部の皮膚病変に塗布し、投与開始から4週後及び12週後に血中シロリムス濃度を測定したところ、以下のとおりであった2)。
| 測定時期 | 対象集団 | 測定例数 | 検出例数 | 血中シロリムス濃度(ng/mL) 平均値±S.D.* |
| 4週後 | 成人 | 17 | 15 | 0.24±0.08 |
| 小児 | 13 | 12 | 0.19±0.07 | |
| 12週後 | 成人 | 17 | 11 | 0.27±0.12 |
| 小児 | 13 | 10 | 0.21±0.09 |
(2)52週間投与
シロリムス経口剤が併用されていない日本人結節性硬化症患者93例(成人43例、小児50例)において、本剤を1日2回顔面又は頭部の皮膚病変に塗布し、投与開始から52週後まで血中シロリムス濃度を測定したところ、以下のとおりであった3)。
| 測定時期 | 対象集団 | 測定例数 | 検出例数 | 血中シロリムス濃度(ng/mL) 平均値±S.D.* |
| 12週後 | 成人 | 40 | 31 | 0.44±0.64 |
| 小児 | 48 | 37 | 0.27±0.21 | |
| 26週後 | 成人 | 38 | 28 | 0.25±0.21 |
| 小児 | 49 | 35 | 0.28±0.29 | |
| 39週後 | 成人 | 39 | 25 | 0.24±0.16 |
| 小児 | 49 | 35 | 0.28±0.30 | |
| 52週後 | 成人 | 38 | 17 | 0.29±0.15 |
| 小児 | 49 | 29 | 0.25±0.14 |
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験
結節性硬化症患者62例(成人35例、小児27例)を対象としたプラセボ対照二重盲検試験において、本剤又はプラセボを1日2回、12週間顔面又は頭部の皮膚病変に塗布した。投与量は病変部50cm2(両頬の面積に相当)あたり0.125gを目安とし、年齢に応じて1日あたり、5歳以下:0.4g、6〜11歳:0.6g、12歳以上:0.8gを上限とした。また、各年齢区分の標準的な体格(体表面積)から大きく逸脱する場合は、体表面積に応じて、体表面積0.8m2未満:0.4g、0.8m2以上1.3m2未満:0.6g、1.3m2以上:0.8gを最大塗布量とした。主要評価項目である12週後の血管線維腫の改善度(中央写真判定)の分布は表のとおりであり、プラセボ群と比較して本剤群で有意な改善が認められた(p<0.001:有意水準両側5%、Wilcoxon順位和検定)。
| 群 (例数) | 改善度 例数(%) | ||||||
| 著明改善 | 改善 | やや改善 | 不変 | やや悪化 | 悪化 | 評価不能 | |
| 本剤 (30例) | 5(16.7) | 13(43.3) | 11(36.7) | 1(3.3) | 0 | 0 | 0 |
| プラセボ (32例) | 0 | 0 | 5(15.6) | 26(81.3) | 0 | 0 | 1(3.1) |
副作用の発現率は本剤群で73.3%(22/30例、39件)であった。本剤群の主な副作用(5%以上)は適用部位刺激感36.7%(11/30例)、皮膚乾燥36.7%(11/30例)、そう痒症16.7%(5/30例)、ざ瘡6.7%(2/30例)であった2)。
17.1.2 国内長期投与試験
結節性硬化症患者94例(成人44例、小児50例)を対象とした、長期投与における安全性及び有効性を検討する非盲検、非対照試験において、本剤を1日2回顔面又は頭部の皮膚病変に塗布し、52週までの有効性を評価した。投与量は病変部50cm2(両頬の面積に相当)あたり0.125gを目安とし、下表に示す年齢区分に応じた1日あたりの最大塗布量を超えない範囲で塗布した。ただし、各年齢区分の標準的な体格(体表面積)から大きく逸脱する被験者については、体表面積区分に応じて塗布量及び処方本数の上限値を規定した。
| 年齢(体表面積)区分 | 1日最大塗布量 | 1ヵ月あたりの処方本数の上限 |
| 5歳以下(0.8m2未満) | 0.4g | 10gチューブ2本 |
| 6〜11歳(0.8m2以上1.3m2未満) | 0.6g | 10gチューブ2本 |
| 12歳以上(1.3m2以上) | 0.8g | 10gチューブ3本 |
血管線維腫の改善度(中央写真判定)の分布は表のとおりである。
| 評価時期 | 例数 | 著明改善 | 改善 | やや改善 | 不変 | やや悪化 | 悪化 | 評価不能 | 改善率a) |
| 52週 | 65 | 13(20.0) | 36(55.4) | 15(23.1) | 1(1.5) | 0(0.0) | 0(0.0) | 0(0.0) | 49(75.4) |
「有害事象に伴う中止がない症例」の割合(95%信頼区間)は97.9%(91.8〜99.5%)であった。「中止に至った有害事象」の発現率は全体で2.1%(2/94例)、成人で2.3%(1/44例)、小児で2.0%(1/50例)であった。2例とも投与開始後1週以内に認められ、成人の1例で眼刺激及び紅斑が各1件、小児の1例で接触皮膚炎が1件発現し、いずれも本剤との因果関係が認められ、軽度であった。
副作用の発現率は全体で72.3%(68/94例、143件)であった。主な副作用(5%以上)は適用部位刺激感(28.7%)、皮膚乾燥(25.5%)、ざ瘡(12.8%)、そう痒症(8.5%)、眼刺激(7.4%)、ざ瘡様皮膚炎及び紅斑(6.4%)、接触皮膚炎(5.3%)であった3)。
副作用の発現率は全体で72.3%(68/94例、143件)であった。主な副作用(5%以上)は適用部位刺激感(28.7%)、皮膚乾燥(25.5%)、ざ瘡(12.8%)、そう痒症(8.5%)、眼刺激(7.4%)、ざ瘡様皮膚炎及び紅斑(6.4%)、接触皮膚炎(5.3%)であった3)。
18. 薬効薬理
18.1 腫瘍増殖抑制作用
ヌードマウスの結節性硬化症モデルにおいてシロリムスを経皮投与(軟膏剤を局所塗布)したとき、シロリムスは腫瘍増殖抑制作用を示すことが報告されている4)。
19. 有効成分に関する理化学的知見
19.1. シロリムス
20. 取扱い上の注意
火気に近づけないこと。
21. 承認条件
21.1 医薬品リスク管理計画を策定の上、適切に実施すること。
22. 包装
10g[10g(チューブ)×1]
23. 主要文献
- 社内資料:シロリムス外用剤のモルモットにおける皮膚光感作性試験(2018年3月23日承認、申請資料概要4.2.3.7-3)
- Wataya-Kaneda M,et al., JAMA Dermatol, 154 (7), 781-8, (2018) »PubMed
- 社内資料:国内長期投与試験(2018年3月23日承認、申請資料概要5.3.5.2)
- Rauktys A.et al., BMC Dermatology, 8, 1-9, (2008)
24. 文献請求先及び問い合わせ先
文献請求先
ノーベルファーマ株式会社
カスタマーセンター
〒104-0033
東京都中央区新川1-17-24
電話:フリーダイヤル:0120-003-140
製品情報問い合わせ先
ノーベルファーマ株式会社
カスタマーセンター
〒104-0033
東京都中央区新川1-17-24
電話:フリーダイヤル:0120-003-140
26. 製造販売業者等
26.1 製造販売元
ノーベルファーマ株式会社
東京都中央区新川1-17-24