医薬品情報
| 総称名 | ジェミーナ |
|---|---|
| 一般名 | レボノルゲストレル エチニルエストラジオール |
| 欧文一般名 | Levonorgestrel Ethinylestradiol |
| 製剤名 | レボノルゲストレル・エチニルエストラジオール配合製剤 |
| 薬効分類名 | 月経困難症治療剤 |
| 薬効分類番号 | 2482 |
| KEGG DRUG |
D04482
エチニルエストラジオール・レボノルゲストレル
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年11月 改訂(承認条件の項削除)(第5版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ジェミーナ配合錠 | Jemina tablets | ノーベルファーマ | 2482012F1025 | 273.9円/錠 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分に対し過敏性素因のある患者
2.4 血栓性静脈炎、肺塞栓症、脳血管障害、冠動脈疾患又はその既往歴のある患者[血液凝固能が亢進され、これらの症状が増悪することがある。][11.1.1参照]
2.6 前兆(閃輝暗点、星型閃光等)を伴う片頭痛の患者[前兆を伴う片頭痛の患者は前兆を伴わない患者に比べ脳血管障害(脳卒中等)が発生しやすくなるとの報告がある。][11.1.1参照]
2.7 肺高血圧症又は心房細動を合併する心臓弁膜症の患者、亜急性細菌性心内膜炎の既往歴のある心臓弁膜症の患者[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。][9.1.9、11.1.1参照]
2.8 血管病変を伴う糖尿病患者(糖尿病性腎症、糖尿病性網膜症等)[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。][11.1.1参照]
2.9 血栓性素因のある患者[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。][11.1.1参照]
2.10 抗リン脂質抗体症候群の患者[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。][11.1.1参照]
2.12 重篤な肝障害のある患者[9.3.1参照]
2.13 肝腫瘍のある患者[症状が増悪することがある。]
2.14 脂質代謝異常のある患者[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。また、脂質代謝に影響を及ぼす可能性があるため、症状が増悪することがある。][11.1.1参照]
2.16 耳硬化症の患者[症状が増悪することがある。]
2.17 妊娠中に黄疸、持続性そう痒症又は妊娠ヘルペスの既往歴のある患者[症状が再発するおそれがある。]
2.19 授乳婦[9.6参照]
2.20 骨成長が終了していない可能性がある患者[骨端の早期閉鎖を来すおそれがある。]
4. 効能または効果
○月経困難症
○生殖補助医療における調節卵巣刺激の開始時期の調整
5. 効能または効果に関連する注意
<生殖補助医療における調節卵巣刺激の開始時期の調整>
妊娠率や生産率の報告を踏まえると、本剤を含む低用量卵胞ホルモン・黄体ホルモン配合剤で調節卵巣刺激の開始時期の調整を行った場合は、開始時期の調整を行わない場合と比べて、妊娠率や生産率が低下する可能性があるので、このことを患者に説明した上で、本剤の投与の要否は、患者ごとに治療上の必要性を考慮して慎重に判断すること。[15.1.6参照]
6. 用法及び用量
<月経困難症>
下記のいずれかを選択する。
・1日1錠を毎日一定の時刻に21日間連続経口投与し、その後7日間休薬する。以上28日間を1周期とし、出血が終わっているか続いているかにかかわらず、29日目から次の周期を開始し、以後同様に繰り返す。
・1日1錠を毎日一定の時刻に77日間連続経口投与し、その後7日間休薬する。以上84日間を1周期とし、出血が終わっているか続いているかにかかわらず、85日目から次の周期を開始し、以後同様に繰り返す。
<生殖補助医療における調節卵巣刺激の開始時期の調整>
1日1錠を毎日一定の時刻に、通常、14〜28日間連続経口投与する。
7. 用法及び用量に関連する注意
<効能共通>
7.1 毎日一定の時刻に服用させること。
7.2 本剤の服用にあたっては飲み忘れ等がないよう服用方法を十分指導すること。
7.3 万一前日の飲み忘れに気付いた場合、直ちに前日の飲み忘れた錠剤を服用し、当日の錠剤も通常の服薬時刻に服用する。2日以上服薬を忘れた場合は、気付いた時点で前日分の1錠を服用し、当日の錠剤も通常の服薬時刻に服用し、その後は当初の服薬スケジュールとおり服用を継続すること。
<月経困難症>
7.4 初めて服用させる場合、原則として月経第1〜5日目に服用を開始させること。
8. 重要な基本的注意
<効能共通>
8.1 本剤を避妊目的で使用しないこと。
8.2 本剤の服用により、年齢、喫煙、肥満、家族歴等のリスク因子の有無にかかわらず血栓症があらわれることがあるので、次のような症状があらわれた場合は直ちに投与を中止し、適切な処置を行うこと。
緊急対応を要する血栓症の主な症状
下肢の急激な疼痛・腫脹、突然の息切れ、胸痛、激しい頭痛、四肢の脱力・麻痺、構語障害、急性視力障害等
患者に対しても、このような症状があらわれた場合は、直ちに服用を中止し、救急医療機関を受診するよう説明すること。[11.1.1参照]
8.3 本剤の服用中に、血栓症が疑われる症状があらわれた場合は、投与を中止するなど適切な処置を行うこと。[11.1.1参照]
血栓症が疑われる症状
下肢の疼痛・腫脹・しびれ・発赤・熱感、頭痛、嘔気・嘔吐等
8.4 血栓症のリスクが高まる状態(体を動かせない状態、顕著な血圧上昇、脱水等)が認められる場合は、投与を中止するなど適切な処置を行うこと。[11.1.1参照]
8.5 患者には、投与開始時及び継続時に以下について説明すること。[11.1.1参照]
・血栓症は生命に関わる経過をたどることがあること。
・血栓症が疑われる症状があらわれた場合や、血栓症のリスクが高まる状態になった場合は、症状・状態が軽度であっても直ちに服用を中止し医師等に相談すること。
・血栓症を疑って他の医療機関を受診する際は、本剤の使用を医師に告知し、本剤による血栓症を念頭においた診察を受けられるようにすること。
8.8 本剤は黄体ホルモンと卵胞ホルモンの配合剤であることから、黄体ホルモン又は卵胞ホルモンを含有する薬剤(経口避妊薬等)を使用している場合は、本剤の投与開始前に中止させること。また、本剤投与中にこれらの薬剤を使用しないよう患者に指導すること。
<月経困難症>
8.9 本剤の投与に際しては、患者の病歴調査及び検診が必要である。この検診には、血圧測定、乳房・腹部の検査及び臨床検査が含まれる。本剤投与中は6ヵ月毎の検診を行い、1年に1回以上、子宮・卵巣を中心とした骨盤内臓器の検査を行うこと。また、1年に1回、子宮頸部の細胞診の実施を考慮すること。[2.2、2.3、9.1.1参照]
8.11 本剤投与中の器質的疾患を伴う月経困難症患者では、不正性器出血の発現に注意するとともに定期的に内診及び超音波検査等を実施して、器質的疾患の増悪の有無を確認すること。特に、子宮内膜症性卵巣嚢胞(卵巣チョコレート嚢胞)は、自然経過において悪性化することを示唆する報告があるので、画像診断や腫瘍マーカー等の検査も行うこと。本剤投与中に腫瘤が増大するなど器質的疾患の増悪が認められる場合は、他の治療法も勘案したうえで投与継続の可否を判断すること。[2.2、2.3参照]
8.12 本剤投与中は経過を十分に観察し、期待する効果が得られない場合には漫然と投与を継続せず、他の適切な治療を考慮すること。
8.14 本剤投与により希発月経等の月経異常や不正性器出血がみられる。患者にはあらかじめ十分に説明し、通常の月経に比べて出血量が多く持続日数が長い場合あるいは月経の発来がない場合には、医師へ相談するよう指導すること。出血が続く患者には必要に応じて血液検査等を実施し、異常が認められた場合には鉄剤の投与又は本剤の投与中止など適切な処置を行うこと。
8.15 服用中に激しい下痢、嘔吐が続いた場合には本剤の吸収不良をきたすことがあり、妊娠する可能性が高くなるので注意すること。
<生殖補助医療における調節卵巣刺激の開始時期の調整>
8.16 本剤は、不妊治療に十分な知識と経験のある医師のもとで使用すること。本剤投与により予想されるリスク及び注意すべき症状について、あらかじめ患者に説明を行うこと。
8.17 服用中に激しい下痢、嘔吐が続いた場合には本剤の吸収不良を来すことがあり、予定した時期に消退出血が発来しない可能性があるので、医師に相談すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 子宮筋腫のある患者
定期的に内診や画像診断等の検査を行うなど慎重に投与すること。筋腫の腫大を促すことがある。[8.9参照]
9.1.2 40歳以上の患者(ただし、1日15本以上の喫煙者には投与しないこと)
9.1.3 乳癌の既往歴のある患者
乳癌が再発するおそれがある。[8.10参照]
9.1.4 乳癌の家族歴又は乳房に結節のある患者
定期的に乳房検診を行うなど慎重に投与すること。エストロゲン投与と乳癌発生との因果関係についてその関連性を示唆する報告もある。[8.10参照]
9.1.5 喫煙者(ただし、35歳以上で1日15本以上の喫煙者には投与しないこと)
9.1.6 肥満の患者
血栓症等の心血管系の障害が発生しやすくなるとの報告がある。[11.1.1参照]
9.1.7 血栓症の家族歴を持つ患者
血栓症等の心血管系の障害が発生しやすくなるとの報告がある。[11.1.1参照]
9.1.8 前兆を伴わない片頭痛の患者
脳血管障害(脳卒中等)が発生しやすくなるとの報告がある。[11.1.1参照]
9.1.9 心臓弁膜症の患者(ただし、肺高血圧症又は心房細動を合併する心臓弁膜症の患者、亜急性細菌性心内膜炎の既往歴のある心臓弁膜症の患者には投与しないこと)
9.1.10 軽度の高血圧(妊娠中の高血圧の既往も含む)のある患者
9.1.11 耐糖能の低下している患者(糖尿病患者及び耐糖能異常の患者)
十分コントロールを行いながら投与すること。耐糖能が低下することがある。
9.1.12 ポルフィリン症の患者
症状が増悪することがある。
9.1.13 心疾患又はその既往歴のある患者
ナトリウム又は体液の貯留により症状が増悪することがある。
9.1.14 てんかん患者
症状が増悪することがある。
9.1.15 テタニーのある患者
症状が増悪することがある。
9.2 腎機能障害患者
9.2.1 腎疾患又はその既往歴のある患者
ナトリウム又は体液の貯留により症状が増悪することがある。
9.3 肝機能障害患者
9.3.1 重篤な肝障害のある患者
投与しないこと。代謝能が低下しており肝臓への負担が増加するため、症状が増悪することがある。[2.12参照]
9.3.2 肝障害のある患者(重篤な肝障害の患者を除く)
代謝能が低下しており肝臓への負担が増加するため、症状が増悪することがある。
9.4 生殖能を有する者
<月経困難症(用法及び用量共通)>
9.4.3 妊娠を希望する場合には、本剤の服用を中止後に月経周期が回復するまで避妊させることが望ましい。
<月経困難症(21日投与7日休薬の用法及び用量)>
9.5 妊婦
9.5.2 卵胞ホルモン剤を妊娠動物(マウス)に投与した場合、児の成長後腟上皮及び子宮内膜の悪性変性を示唆する結果が報告されている。また、新生児(マウス)に投与した場合、児の成長後腟上皮の悪性変性を認めたとの報告がある。
9.6 授乳婦
投与しないこと。母乳の量的質的低下が起こることがある。また、母乳中への移行、児において黄疸、乳房腫大が起こるとの報告がある。[2.19参照]
9.7 小児等
小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
10. 相互作用
10.2 併用注意
| 副腎皮質ホルモン プレドニゾロン等 三環系抗うつ剤 イミプラミン等 セレギリン塩酸塩 シクロスポリン テオフィリン オメプラゾール | これらの薬剤の作用が増強するおそれがある。 | 本剤はこれらの薬剤の代謝を抑制すると考えられる。 |
| チザニジン | これらの薬剤の作用が増強するおそれがある。 | 本剤は肝の薬物代謝酵素(CYP1A2)を阻害し、この薬剤の代謝を抑制すると考えられる。 |
| リファンピシン リファブチン | 本剤の効果の減弱化及び不正性器出血の発現率が増大するおそれがある。 | これらの薬剤は肝の薬物代謝酵素(CYP3A4等)を誘導し、本剤の代謝を促進すると考えられる。 |
| バルビツール酸系製剤 フェノバルビタール等 ヒダントイン系製剤 フェニトインナトリウム等 カルバマゼピン ボセンタン モダフィニル トピラマート | 本剤の効果の減弱化及び不正性器出血の発現率が増大するおそれがある。 | これらの薬剤は肝の薬物代謝酵素を誘導し、本剤の代謝を促進すると考えられる。 |
| テトラサイクリン系抗生物質 テトラサイクリン等 ペニシリン系抗生物質 アンピシリン等 | 本剤の効果の減弱化及び不正性器出血の発現率が増大するおそれがある。 | これらの薬剤は腸内細菌叢を変化させ、本剤の腸肝循環による再吸収を抑制すると考えられる。 |
| テルビナフィン塩酸塩 | 黄体ホルモン・卵胞ホルモン配合剤との併用で、月経異常があらわれたとの報告がある。 | 機序不明 |
| Gn-RH誘導体 ブセレリン酢酸塩等 | これらの薬剤の作用を減弱するおそれがある。 | これらの薬剤は性ホルモンの分泌を低下することにより薬効を示すため、性ホルモンである本剤の投与によってこれらの薬剤の効果を減弱する可能性が考えられる。 |
| 血糖降下剤 インスリン製剤 スルフォニル尿素系製剤 スルフォンアミド系製剤 ビグアナイド系製剤等 | 血糖降下剤の作用が減弱するおそれがある。血糖値その他患者の状態を十分観察し、血糖降下剤の用量を調節するなど注意する。 | 本剤は耐糖能を低下させ、血糖降下剤の作用を減弱させると考えられる。 |
| ラモトリギン モルヒネ サリチル酸 | これらの薬剤の血中濃度が低下するおそれがある。 | 本剤はこれらの薬剤のグルクロン酸抱合を促進すると考えられる。 |
| HIVプロテアーゼ阻害剤 ネルフィナビルメシル酸塩 ホスアンプレナビル(リトナビル併用時) | エチニルエストラジオールの血中濃度が低下するおそれがある。 | 機序不明 |
| HIVプロテアーゼ阻害剤 リトナビル ダルナビル(リトナビル併用時) | エチニルエストラジオールの血中濃度が低下するおそれがある。 | リトナビルは薬物代謝酵素を誘導し、本剤の代謝を促進すると考えられる。 |
| HIVプロテアーゼ阻害剤 ロピナビル・リトナビル配合剤 | エチニルエストラジオールの血中濃度が低下するおそれがある。 | この薬剤は薬物代謝酵素を誘導し、本剤の代謝を促進すると考えられる。 |
| 非ヌクレオシド系逆転写酵素阻害剤 ネビラピン | エチニルエストラジオールの血中濃度が低下するおそれがある。 | 機序不明 |
| 非ヌクレオシド系逆転写酵素阻害剤 エファビレンツ | レボノルゲストレルの血中濃度が低下するおそれがある。 | 機序不明 |
| HIVプロテアーゼ阻害剤 アタザナビル | 本剤の血中濃度が上昇するおそれがある。 | 本剤の代謝酵素(CYP3A4)を阻害すると考えられる。 |
| 非ヌクレオシド系逆転写酵素阻害剤 エトラビリン | 本剤の血中濃度が上昇するおそれがある。 | この薬剤は本剤の代謝酵素(CYP2C9)を阻害すると考えられる。 |
| アプレピタント ホスアプレピタント | 本剤の効果が減弱されるおそれがある。 | 機序は解明されていないが、これらの薬剤との併用により本剤の代謝が亢進すると考えられる。 |
| フルコナゾール | 本剤の血中濃度が上昇するおそれがある。 | フルコナゾールは本剤の代謝酵素(CYP3A4)を阻害すると考えられる。 |
| ボリコナゾール | 本剤の血中濃度が上昇するおそれがある。 ボリコナゾールの血中濃度が上昇するおそれがある。 | ボリコナゾールは本剤の代謝酵素(CYP3A4)を阻害すると考えられる。 本剤がボリコナゾールの代謝酵素(CYP2C19)を阻害すると考えられる。 |
| アセトアミノフェン | 本剤の血中濃度が上昇するおそれがある。 アセトアミノフェンの血中濃度が低下するおそれがある。 | アセトアミノフェンはエチニルエストラジオールの硫酸抱合を阻害すると考えられる。 本剤が肝におけるアセトアミノフェンのグルクロン酸抱合を促進すると考えられる。 |
| ルフィナミド | 本剤の効果が減弱化するおそれがある。 | 機序不明 |
| セイヨウオトギリソウ(St.John's Wort、セント・ジョーンズ・ワート)含有食品 | 本剤の効果の減弱化及び不正性器出血の発現率が増大するおそれがあるので、本剤投与時はセイヨウオトギリソウ含有食品を摂取しないよう注意すること。 | この食品は肝の薬物代謝酵素を誘導し、本剤の代謝を促進すると考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 血栓症(四肢、肺、心、脳、網膜等)(頻度不明)
11.2 その他の副作用
| 5%以上 | 0.1〜5%未満 | 頻度不明 | |
| 過敏症 | 発疹 | ||
| 血液 | 貧血、鉄欠乏性貧血 | ||
| 内分泌代謝 | 浮腫、体重増加 | ||
| 精神神経 | 頭痛(11.2%) | 不快気分、浮動性めまい、体位性めまい、感覚鈍麻、傾眠、回転性めまい、倦怠感 | 神経過敏、抑うつ |
| 眼 | 閃輝暗点 | 網膜血流障害による視力障害 | |
| 循環器 | 動悸、静脈瘤、ほてり、末梢性浮腫、血圧上昇 | ||
| 消化器 | 悪心(10.4%) | 食欲亢進、食欲減退、腹部不快感、腹部膨満、腹痛、上腹部痛、便秘、下痢、痔核、胃炎、嘔吐、口渇 | 口内炎 |
| 肝臓 | 肝機能異常、黄疸 | ||
| 皮膚 | ざ瘡 | 色素沈着注) | |
| 筋・骨格 | 背部痛、四肢痛 | 肩こり | |
| 卵巣 | 卵巣嚢胞 | ||
| 子宮 | 下腹部痛(20.3%)、無月経(10.4%)、月経過多(21.6%)、不正子宮出血(72.9%)、希発月経(44.6%) | 子宮平滑筋腫、月経困難症、過少月経、頻発月経、月経前症候群、腟分泌物 | 経血量変化 |
| 乳房 | 乳房硬結、乳房痛、乳汁漏出症、乳房不快感 | 乳房腫大、乳汁分泌、乳房萎縮 | |
| 臨床検査 | ALT増加、AST増加、血中クレアチニン増加、血中フィブリノゲン増加、血中鉄減少、血中LDH増加、血中トリグリセリド増加、フィブリンDダイマー増加、γ-GTP増加、ヘマトクリット減少、ヘモグロビン減少、プラスミノーゲン減少、プラスミノーゲン増加、プロテインC減少、プロトロンビン時間延長、赤血球数減少、アンチトロンビンIII減少、プロテインS減少、血小板数増加 | 総コレステロール上昇 | |
| その他 | 突発性難聴、呼吸困難、腋窩痛 | カンジダ腟炎、熱感、冷感、代償性鼻出血 |
12. 臨床検査結果に及ぼす影響
含有するエチニルエストラジオールの作用による血清蛋白(コルチコイド結合性グロブリン、サイロキシン結合性グロブリン等)の増加により、総コルチゾール、総T3、総T4の上昇がみられることがある。また、これらの遊離型は変化しないとされている。これら検査値の判定に際しては注意すること。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 外国の疫学調査の結果、静脈血栓症のリスクは、経口避妊薬を服用している女性は服用していない女性に比し、3.25〜4.0倍高くなるとの報告がある。
また、静脈血栓症のリスクは経口避妊薬服用開始の最初の1年間において最も高くなるとの報告がある。
さらに、外国での大規模市販後調査の結果、初めて経口避妊薬の服用を開始した時だけでなく、4週間以上の中断後に服用を再開した時又は4週間以上の中断後に別の経口避妊薬へ切り替えた時にも静脈血栓症のリスクが上昇し、そのリスクは服用開始後3ヵ月間が特に高いとの報告がある。
また、静脈血栓症のリスクは経口避妊薬服用開始の最初の1年間において最も高くなるとの報告がある。
さらに、外国での大規模市販後調査の結果、初めて経口避妊薬の服用を開始した時だけでなく、4週間以上の中断後に服用を再開した時又は4週間以上の中断後に別の経口避妊薬へ切り替えた時にも静脈血栓症のリスクが上昇し、そのリスクは服用開始後3ヵ月間が特に高いとの報告がある。
15.1.2 外国での疫学調査の結果、経口避妊薬の服用により乳癌及び子宮頸癌になる可能性が高くなるとの報告がある。
15.1.3 外国で、経口避妊薬を2年以上服用した場合、良性肝腫瘍が10万人当たり3.4人発生するとの報告がある。
また、腫瘍の破裂により腹腔内出血を起こす可能性がある。一方、悪性肝腫瘍(肝癌)の発生率は極めて低く、100万人当たり1人に満たない。
また、腫瘍の破裂により腹腔内出血を起こす可能性がある。一方、悪性肝腫瘍(肝癌)の発生率は極めて低く、100万人当たり1人に満たない。
15.1.4 外国で、経口避妊薬の服用により全身性エリテマトーデス(SLE)の悪化、アナフィラキシー、溶血性尿毒症症候群(HUS)があらわれたとの報告がある。
15.1.5 外国で、経口避妊薬の服用による角膜厚の変化等によりコンタクトレンズがうまく調整されないため、視力・視野の変化、装用時の不快感等がみられたとの報告がある。
15.1.6 調節卵巣刺激の前周期に低用量卵胞ホルモン・黄体ホルモン配合剤を投与した場合の生産率及び継続妊娠率は、投与しなかった場合と比較して低かったとの報告がある1)。[5.参照]
16. 薬物動態
16.1 血中濃度
健康成人女性13例への本剤(レボノルゲストレル0.09mg、エチニルエストラジオール0.02mg)21日間反復経口投与時の薬物動態パラメータは、以下のとおりであった2)。
| AUC0-24(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | t1/2(hr) | |
| レボノルゲストレル | 67.0±29.6 | 5.3±1.8 | 1.3±0.4 | 28.4±7.0 |
| エチニルエストラジオール | 0.603±0.241 | 0.067±0.032 | 1.6±0.8 | 14.3±3.4 |
16.4 代謝
16.5 排泄
17. 臨床成績
17.1 有効性及び安全性に関する試験
<月経困難症>
17.1.1 国内第III相試験
月経困難症患者(21日投与7日休薬群:16〜50歳、平均32.1歳、77日投与7日休薬群:17〜48歳、平均31.6歳、プラセボ群:18〜47歳、平均33.1歳)を対象としたプラセボ対照比較試験において、月経困難症スコア合計注1)の投与前から3周期(1〜3周期の平均)までの変化量は、21日投与7日休薬群及び77日投与7日休薬群のいずれもプラセボ群と比較して有意差が認められた。また、月経困難症に対する効果は投与52週まで持続することが確認された6)。
| 1〜3周期変化量注2),注3) | 群間差注2),注3) | P値注3),注4) | |
| 21日投与7日休薬群(n=81) | −1.8±0.12 | −0.9±0.16 | <0.001 |
| 77日投与7日休薬群(n=86) | −3.1±0.12 | −2.2±0.16 | <0.001 |
| プラセボ群(n=78) | −0.9±0.13 | − | − |
注1)月経困難症スコア合計(月経困難症の程度+鎮痛薬の使用)
| 程度 | 内容 | スコア | |
| 月経困難症の程度 | なし | なし | 0 |
| 軽度 | 仕事(学業・家事)に若干の支障あり | 1 | |
| 中等度 | 横になって休憩したくなるほど仕事(学業・家事)への支障をきたす | 2 | |
| 重度 | 1日以上寝込み、仕事(学業・家事)ができない | 3 | |
| 鎮痛薬の使用 | なし | なし | 0 |
| 軽度 | 直前(あるいは現在)の月経期間中に、鎮痛薬を1日使用した | 1 | |
| 中等度 | 直前(あるいは現在)の月経期間中に、鎮痛薬を2日使用した | 2 | |
| 重度 | 直前(あるいは現在)の月経期間中に、鎮痛薬を3日以上使用した | 3 |
注2)最小二乗平均値±標準誤差
注3)投与群と観察周期の交互作用を固定効果、被験者を変量効果とし、相関構造にCompound Symmetryを仮定した混合効果モデル
注4)シミュレーション法により検定の多重性を調整
副作用(臨床検査値異常を含む)の発現頻度は、88.8%(214/241例)であった。
21日投与7日休薬群(プラセボからの切り替え症例を含む)における副作用の発現頻度は83.2%(129/155例)であった。主な副作用(10%以上)は、不正子宮出血67.7%(105例)、希発月経27.1%(42例)、月経過多18.7%(29例)、下腹部痛14.2%(22例)であった。77日投与7日休薬群における副作用の発現頻度は98.8%(85/86例)であった。主な副作用(10%以上)は、不正子宮出血95.3%(82例)、希発月経86.0%(74例)、月経過多32.6%(28例)、無月経31.4%(27例)、下腹部痛31.4%(27例)、頭痛12.8%(11例)、悪心11.6%(10例)であった6)。
18. 薬効薬理
18.1 作用機序
<月経困難症>
18.1.1 本剤は、排卵抑制作用及び子宮内膜増殖抑制作用により、プロスタグランジンの産生を抑制し、子宮平滑筋収縮等による疼痛を緩和すると考えられる。
<生殖補助医療における調節卵巣刺激の開始時期の調整>
18.1.2 本剤を一定期間投与し、内因性の卵胞ホルモン及び黄体ホルモンの分泌を抑制した上で、本剤の有効成分である合成卵胞ホルモンと合成黄体ホルモンの血中濃度を一定期間維持し、本剤の中止によりそれらの血中濃度を急激に低下させることで子宮内膜がはく落し、生殖補助医療における調節卵巣刺激の開始時期を規定する消退出血が生じる。
18.2 排卵抑制作用
健康成人女性(13例)に本剤を1日1回1錠21日間投与した時、エストラジオール及びプロゲステロンの分泌抑制が認められた2)。
18.3 子宮内膜増殖抑制作用
国内第III相試験において、本剤21日投与7日休薬群及び77日投与7日休薬群のいずれもプラセボ群と比較して子宮内膜の厚さの有意な菲薄化が認められた6)。
19. 有効成分に関する理化学的知見
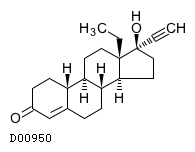
19.1. レボノルゲストレル
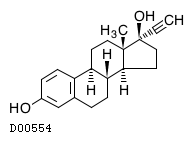
19.2. エチニルエストラジオール
20. 取扱い上の注意
アルミピロー包装開封後は、湿気を避けて遮光して保存すること。
22. 包装
63錠[21錠(PTP)×3](脱酸素剤入り)
84錠[28錠(PTP)×3](脱酸素剤入り)
23. 主要文献
- Farquhar C,et al., Oral contraceptive pill, progestogen or oestrogen pretreatment for ovarian stimulation protocols for women undergoing assisted reproductive techniques., 5, (2017), (Cochrane Database Syst Rev)
- 社内資料:健康成人女性への反復経口投与試験(2018年7月2日承認、申請資料概要2.7.2.2)
- Sisenwine SF,et al., Drug Metab.Dispos., 3, 180-188, (1975) »PubMed
- Orme ML'E,et al., Clin.Pharmacokinet., 8, 95-136, (1983)
- Speck U,et al., Contraception., 14, 151-163, (1976) »PubMed
- 社内資料:第III相長期投与試験−無作為化プラセボ対照二重盲検比較試験(2018年7月2日承認、申請資料概要2.7.6.2)
24. 文献請求先及び問い合わせ先
文献請求先
ノーベルファーマ株式会社
カスタマーセンター
〒104-0033
東京都中央区新川1-17-24
電話:フリーダイヤル:0120-003-140
あすか製薬株式会社
くすり相談室
〒108-8532
東京都港区芝浦二丁目5番1号
電話:0120-848-339
FAX:03-5484-8358
製品情報問い合わせ先
ノーベルファーマ株式会社
カスタマーセンター
〒104-0033
東京都中央区新川1-17-24
電話:フリーダイヤル:0120-003-140
あすか製薬株式会社
くすり相談室
〒108-8532
東京都港区芝浦二丁目5番1号
電話:0120-848-339
FAX:03-5484-8358
25. 保険給付上の注意
本剤が避妊の目的で処方された場合には、保険給付の対象とはしないこと。
26. 製造販売業者等
26.1 製造販売元
ノーベルファーマ株式会社
東京都中央区新川1-17-24
26.2 提携
あすか製薬株式会社
東京都港区芝浦二丁目5番1号