医薬品情報
| 総称名 | クロベタゾールプロピオン酸エステル |
|---|---|
| 一般名 | クロベタゾールプロピオン酸エステル |
| 欧文一般名 | Clobetasol Propionate |
| 製剤名 | クロベタゾールプロピオン酸エステル軟膏 |
| 薬効分類名 | 副腎皮質ホルモン外用剤 |
| 薬効分類番号 | 2646 |
| ATCコード | D07AD01 |
| KEGG DRUG |
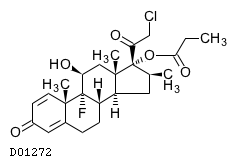
D01272
クロベタゾールプロピオン酸エステル
|
| KEGG DGROUP |
DG01955
副腎皮質ステロイド
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年6月 改訂(第2版)

|
2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| クロベタゾールプロピオン酸エステル軟膏0.05%「イワキ」 (後発品) | Clobetasol Propionate Ointment 0.05%"IWAKI" | 岩城製薬 | 2646713M1217 | 11.7円/g | 劇薬 |
2. 禁忌
次の患者には投与しないこと
2.1 細菌・真菌・スピロヘータ・ウイルス皮膚感染症及び動物性皮膚疾患(疥癬・けじらみ等)[感染を悪化させるおそれがある。]
2.2 本剤の成分に対して過敏症の既往歴のある患者
2.3 鼓膜に穿孔のある湿疹性外耳道炎[穿孔部位の治癒が遅れるおそれがある。また、感染のおそれがある。]
2.4 潰瘍(ベーチェット病は除く)、第2度深在性以上の熱傷・凍傷[皮膚の再生が抑制され、治癒が著しく遅れるおそれがある。]
4. 効能または効果
○湿疹・皮膚炎群(進行性指掌角皮症、ビダール苔癬、日光皮膚炎を含む)
○痒疹群(蕁麻疹様苔癬、ストロフルス、固定蕁麻疹を含む)
○乾癬
○虫さされ
○薬疹・中毒疹
○扁平紅色苔癬
○紅皮症
○肥厚性瘢痕・ケロイド
○肉芽腫症(サルコイドーシス、環状肉芽腫)
○アミロイド苔癬
○天疱瘡群
○類天疱瘡(ジューリング疱疹状皮膚炎を含む)
○悪性リンパ腫(菌状息肉症を含む)
○円形脱毛症(悪性を含む)
5. 効能または効果に関連する注意
皮膚感染を伴う湿疹・皮膚炎には使用しないことを原則とするが、やむを得ず使用する必要がある場合には、あらかじめ適切な抗菌剤(全身適用)、抗真菌剤による治療を行うか、又はこれらとの併用を考慮すること。
6. 用法及び用量
通常1日1〜数回適量を塗布する。なお、症状により適宜増減する。
8. 重要な基本的注意
8.1 皮膚萎縮、ステロイド潮紅などの局所的副作用が発現しやすいので、特に顔面、頸、陰部、間擦部位の皮疹への使用には、適応症、症状の程度を十分考慮すること。
8.2 大量又は長期にわたる広範囲の使用(特に密封法(ODT))により、副腎皮質ステロイド剤を全身投与した場合と同様な症状があらわれることがあるので、特別な場合を除き長期大量使用や密封法(ODT)を極力避けること。[9.5、9.7、9.8、11.1参照]
8.3 本剤の使用により症状の改善がみられない場合又は症状の悪化をみる場合は使用を中止すること。
8.4 症状改善後は、速やかに他のより緩和な局所療法に転換すること。
9. 特定の背景を有する患者に関する注意
9.5 妊婦
9.7 小児等
長期使用又は密封法(ODT)は避けること。発育障害を来すおそれがある。また、おむつは密封法(ODT)と同様の作用があるので注意すること。[8.2参照]
9.8 高齢者
大量又は長期にわたる広範囲の密封法(ODT)等の使用に際しては特に注意すること。一般に、副作用があらわれやすい。[8.2参照]
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には使用を中止するなど適切な処置を行うこと。
眼圧亢進、緑内障、白内障(いずれも頻度不明)
眼瞼皮膚への使用に際し、あらわれることがある。大量又は長期にわたる広範囲の使用、密封法(ODT)により緑内障、白内障等の症状があらわれることがある。[8.2参照]
11.2 その他の副作用
| 頻度不明 | |
| 皮膚の感染症注1) | 真菌症(カンジダ症、白癬等)、細菌感染症(伝染性膿痂疹、毛のう炎等)、ウイルス感染症 |
| 過敏症注2) | 紅斑、発疹、蕁麻疹、そう痒、皮膚灼熱感、接触性皮膚炎 |
| その他の皮膚症状 | ステロイド皮膚注3)(皮膚萎縮、毛細血管拡張、紫斑)、色素脱失注3)、酒さ様皮膚炎・口囲皮膚炎注3)(ほほ、口囲等に潮紅、丘疹、膿疱、毛細血管拡張)、多毛注3)、ステロイドざ瘡、魚鱗癬様皮膚変化、一過性の刺激感、乾燥 |
| その他 | 下垂体・副腎皮質系機能抑制注4)、中心性漿液性網脈絡膜症 |
14. 適用上の注意
14.1 薬剤交付時の注意
患者に治療以外の目的(化粧下、ひげそり後など)には使用しないよう注意すること。
14.2 薬剤投与時の注意
眼科用として使用しないこと。
15. その他の注意
15.1 臨床使用に基づく情報
乾癬患者に長期大量使用した場合、治療中あるいは治療中止後、乾癬性紅皮症、膿疱性乾癬等がみられたとの報告がある2)。
16. 薬物動態
16.2 吸収
切除目的の腋臭症患者の腋窩皮膚に3H-クロベタゾールプロピオン酸エステル0.05%含有クリームを塗布(密封法(ODT))した後、オートラジオグラフィー法で表皮への取り込みを経時的に観察した結果、塗布後30分で既に表皮に取り込まれ、塗布後5時間で定常状態となり、この状態は塗布後24時間まで持続した。また外用剤除去24時間後も表皮内に貯留していた3)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<虫さされ、薬疹・中毒疹、ジベルばら色粃糠疹、慢性円板状エリテマトーデス、扁平紅色苔癬、紅皮症、肥厚性瘢痕・ケロイド、肉芽腫症(サルコイドーシス、環状肉芽腫)、アミロイド苔癬、天疱瘡群、類天疱瘡(ジューリング疱疹状皮膚炎を含む)、悪性リンパ腫(菌状息肉症を含む)、円形脱毛症(悪性を含む)>
17.1.1 国内第III相試験
難治性慢性皮膚疾患等のいずれかを有する患者284例に対する非盲検試験において、クロベタゾールプロピオン酸エステルを1日1〜数回患部に塗布した時の有効率は下表のとおりであった4)。
| 疾患名 | 使用期間(日) | 有効率% (有効症例率/症例数) |
| 虫さされ | 2〜24 | 100.0(20/20) |
| 薬疹・中毒疹 | 100.0(21/21) | |
| ジベルばら色粃糠疹 | 100.0(20/20) | |
| 慢性円板状エリテマトーデス | 14〜56 | 95.2(20/21) |
| 扁平紅色苔癬 | 95.8(23/24) | |
| 紅皮症 | 96.7(29/30) | |
| 肥厚性瘢痕・ケロイド | 65.3(32/49) | |
| 肉芽腫症 (サルコイドーシス、環状肉芽腫) | 81.3(13/16) | |
| アミロイド苔癬 | 93.8(15/16) | |
| 天疱瘡群 | 100.0(14/14) | |
| 類天疱瘡 (ジューリング疱疹状皮膚炎を含む) | 92.3(12/13) | |
| 悪性リンパ腫 (菌状息肉症を含む) | 71.4(10/14) | |
| 円形脱毛症 (悪性を含む) | 21〜63 | 73.1(19/26) |
副作用発現頻度は、13.0%(37/284例)であった。主な副作用は、皮膚萎縮11件、毛細血管拡張8件、毛包炎・せつ10件、ざ瘡様疹11件であった。
18. 薬効薬理
18.1 作用機序
クロベタゾールプロピオン酸エステルは合成コルチコステロイドの一種であり、炎症性サイトカイン産生の抑制及びアラキドン酸代謝の阻害等のメカニズムを介して抗炎症作用を示すと考えられる。
18.2 血管収縮作用
18.2.1 血管収縮試験
クロベタゾールプロピオン酸エステルはMcKenzieらの方法による健康成人皮膚における血管収縮試験(皮膚蒼白度を指標)においてフルオシノロンアセトニドの約18.7倍、ベタメタゾン吉草酸エステルの約5.2倍の血管収縮作用を示した5)。
18.2.2 生物学的同等性試験
クロベタゾールプロピオン酸エステル軟膏0.05%「イワキ」とデルモベート軟膏0.05%を、それぞれ健康成人男子28名に単回経皮投与し、皮膚毛細血管収縮試験を行い、皮膚毛細血管収縮反応により生じた皮膚蒼白化の程度を判定し、統計解析をした結果、両剤の生物学的同等性が確認された6)。
2時間塗布後の血管収縮反応の陽性率(%)
| 製剤\製剤除去後経過時間(hr) | 2 | 4 | 6 | 24 |
| クロベタゾールプロピオン酸エステル軟膏0.05%「イワキ」 | 17.9 | 14.3 | 7.1 | 0 |
| デルモベート軟膏0.05% | 17.9 | 14.3 | 3.6 | 0 |
皮膚毛細血管収縮反応の陽性率等は、被験者の選択、血管収縮反応の測定回数・時間等の試験条件によって異なる可能性がある。
4時間塗布後の血管収縮反応の陽性率(%)
| 製剤\製剤除去後経過時間(hr) | 2 | 4 | 6 | 24 |
| クロベタゾールプロピオン酸エステル軟膏0.05%「イワキ」 | 46.4 | 28.6 | 3.6 | 0 |
| デルモベート軟膏0.05% | 42.9 | 32.1 | 3.6 | 0 |
皮膚毛細血管収縮反応の陽性率等は、被験者の選択、血管収縮反応の測定回数・時間等の試験条件によって異なる可能性がある。
18.3 肉芽腫抑制作用
クロベタゾールプロピオン酸エステルは副腎摘出ラットにおける綿球肉芽腫抑制試験においてヒドロコルチゾンの112.5倍、ベタメタゾン吉草酸エステルの約2.4倍の肉芽腫抑制作用を示した7)。
18.4 浮腫抑制作用
クロベタゾールプロピオン酸エステルはラットにおけるホルマリン浮腫及びカラゲニン浮腫抑制試験においてヒドロコルチゾンの約36〜161倍、ベタメタゾン吉草酸エステルの約2〜4倍の浮腫抑制作用を示した7)。
18.5 皮膚局所への影響
クロベタゾールプロピオン酸エステル0.05%含有軟膏のラットにおける塗布部位の皮膚萎縮に及ぼす影響は、0.025%フルオシノロンアセトニドより軽度であった8)。
18.6 全身への影響
クロベタゾールプロピオン酸エステル0.05%含有軟膏を成長期のラットの背部皮膚に塗布した結果、胸腺萎縮作用及び体重増加抑制に及ぼす影響は0.025%フルオシノロンアセトニドより軽度であった8)。
19. 有効成分に関する理化学的知見
19.1. クロベタゾールプロピオン酸エステル
22. 包装
10本[5g(チューブ)×10]
50本[5g(チューブ)×50]
50本[10g(チューブ)×50]
500g[ボトル]
23. 主要文献
- 倉本昌明ほか, 基礎と臨床, 9, 3259-3283, (1975)
- Tan RS-H, Proc R Soc Med., 67, 719-720, (1974)
- 竹田勇士ほか, 西日本皮膚科, 37, 796-801, (1975) »DOI
- Clobetasol 17-Propionate外用剤難治性皮膚疾患研究班, 西日本皮膚科, 44, 677-689, (1982) »DOI
- Munro DD,et al., Br Med J., 3, 626-628, (1975) »PubMed
- 岩城製薬株式会社 社内資料(生物学的同等性試験)
- 中村悦郎ほか, 共立薬科大学研究年報, 19, 13-25, (1974)
- 武田克之ほか, 西日本皮膚科, 39, 775-784, (1977) »DOI
24. 文献請求先及び問い合わせ先
文献請求先
岩城製薬株式会社
マーケティング部 学術グループ
〒103-8434
東京都中央区日本橋本町4-8-2
電話:03-6626-6251
FAX:03-6626-6261
製品情報問い合わせ先
岩城製薬株式会社
マーケティング部 学術グループ
〒103-8434
東京都中央区日本橋本町4-8-2
電話:03-6626-6251
FAX:03-6626-6261
26. 製造販売業者等
26.1 製造販売元
岩城製薬株式会社
東京都中央区日本橋本町4-8-2