医薬品情報
| 総称名 | オキシコドン |
|---|---|
| 一般名 | オキシコドン塩酸塩水和物 |
| 欧文一般名 | Oxycodone Hydrochloride Hydrate |
| 製剤名 | オキシコドン塩酸塩水和物錠 |
| 薬効分類名 | がん疼痛治療剤 |
| 薬効分類番号 | 8119 |
| ATCコード | N02AA05 |
| KEGG DRUG |
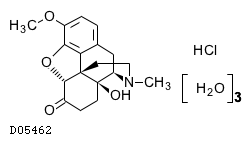
D05462
オキシコドン塩酸塩水和物
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年4月 改訂(第4版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| オキシコドン錠2.5mgNX「第一三共」 (後発品) | OXYCODONE TABLETS NX"DAIICHI SANKYO" | 第一三共 | 8119002F5024 | 46.5円/錠 | 劇薬, 麻薬, 処方箋医薬品注) |
| オキシコドン錠5mgNX「第一三共」 (後発品) | OXYCODONE TABLETS NX"DAIICHI SANKYO" | 第一三共 | 8119002F6020 | 84.7円/錠 | 劇薬, 麻薬, 処方箋医薬品注) |
| オキシコドン錠10mgNX「第一三共」 (後発品) | OXYCODONE TABLETS NX"DAIICHI SANKYO" | 第一三共 | 8119002F7027 | 154円/錠 | 劇薬, 麻薬, 処方箋医薬品注) |
| オキシコドン錠20mgNX「第一三共」 (後発品) | OXYCODONE TABLETS NX"DAIICHI SANKYO" | 第一三共 | 8119002F8023 | 300.9円/錠 | 劇薬, 麻薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 重篤な呼吸抑制のある患者、重篤な慢性閉塞性肺疾患の患者[呼吸抑制を増強する。][11.1.3参照]
2.2 気管支喘息発作中の患者[呼吸を抑制し、気道分泌を妨げる。]
2.3 慢性肺疾患に続発する心不全の患者[呼吸抑制や循環不全を増強する。][9.1.2参照]
2.4 痙攣状態(てんかん重積症、破傷風、ストリキニーネ中毒)にある患者[脊髄の刺激効果があらわれる。][9.1.14参照]
2.5 麻痺性イレウスの患者[消化管運動を抑制する。][11.1.6参照]
2.6 急性アルコール中毒の患者[呼吸抑制を増強する。]
2.7 本剤の成分(オキシコドン、ナロキソン等)及びアヘンアルカロイドに対し過敏症の患者
2.8 出血性大腸炎の患者[腸管出血性大腸菌(O157等)や赤痢菌等の重篤な細菌性下痢のある患者では、症状の悪化、治療期間の延長を来すおそれがある。][9.1.1参照]
2.9 ナルメフェン塩酸塩水和物を投与中又は投与中止後1週間以内の患者[10.1参照]
4. 効能または効果
中等度から高度の疼痛を伴う各種癌における鎮痛
6. 用法及び用量
通常、成人にはオキシコドン塩酸塩(無水物)として1日10〜80mgを4回に分割経口投与する。
なお、症状に応じて適宜増減する。
なお、症状に応じて適宜増減する。
7. 用法及び用量に関連する注意
<臨時追加投与(レスキュー薬の投与)として本剤を使用する場合>
7.1 疼痛が増強した場合や鎮痛効果が得られている患者で突発性の疼痛が発現した場合は、直ちに本剤の臨時追加投与を行い鎮痛を図ること。本剤の1回量は定時投与中のオキシコドン塩酸塩経口製剤の1日量の1/8〜1/4を経口投与すること。
<定時投与時>
7.2 本剤の1日量を4分割して使用する場合には、6時間ごとの定時に経口投与すること。
7.2.1 初回投与
本剤の投与開始前のオピオイド鎮痛薬による治療の有無を考慮して初回投与量を設定することとし、既に治療されている場合にはその投与量及び鎮痛効果の持続を考慮して副作用の発現に注意しながら適宜投与量を調節すること。
(1)オピオイド鎮痛薬を使用していない患者には、疼痛の程度に応じてオキシコドン塩酸塩として10〜20mgを1日投与量とすることが望ましい。
(2)モルヒネ製剤の経口投与を本剤に変更する場合には、モルヒネ製剤1日投与量の2/3量を1日投与量の目安とすることが望ましい。
(3)経皮フェンタニル貼付剤から本剤へ変更する場合には、経皮フェンタニル貼付剤剥離後にフェンタニルの血中濃度が50%に減少するまで17時間以上かかることから、剥離直後の本剤の使用は避け、本剤の使用を開始するまでに、フェンタニルの血中濃度が適切な濃度に低下するまでの時間をあけるとともに、本剤の低用量から投与することを考慮すること。
7.2.2 増量
本剤投与開始後は患者の状態を観察し、適切な鎮痛効果が得られ副作用が最小となるよう用量調整を行うこと。2.5mgから5mgへの増量の場合を除き増量の目安は、使用量の25〜50%増とする。[8.4参照]
7.2.3 減量
7.2.4 投与の中止
8. 重要な基本的注意
8.1 連用により薬物依存を生じることがあるので、観察を十分に行い、慎重に投与すること。[11.1.2参照]
8.2 眠気、眩暈が起こることがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械の操作に従事させないように注意すること。
8.3 本剤を投与する場合には、便秘に対する対策として緩下剤、嘔気・嘔吐に対する対策として制吐剤の併用を、また、鎮痛効果が得られている患者で通常とは異なる強い眠気がある場合には、過量投与の可能性を念頭において本剤の減量を考慮するなど、本剤投与時の副作用に十分注意すること。[13.1、13.2参照]
8.4 本剤を増量する場合には、副作用に十分注意すること。[7.2.2参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 細菌性下痢のある患者
治療上やむを得ないと判断される場合を除き、投与しないこと。治療期間の延長を来すおそれがある。[2.8参照]
9.1.2 心機能障害あるいは低血圧のある患者
循環不全を増強するおそれがある。[2.3参照]
9.1.3 呼吸機能障害のある患者
呼吸抑制を増強するおそれがある。[11.1.3参照]
9.1.4 脳に器質的障害のある患者
呼吸抑制や頭蓋内圧の上昇を起こすおそれがある。
9.1.5 ショック状態にある患者
循環不全や呼吸抑制を増強するおそれがある。[11.1.1参照]
9.1.6 代謝性アシドーシスのある患者
呼吸抑制を起こしたときアシドーシスを増悪させるおそれがある。
9.1.7 甲状腺機能低下症(粘液水腫等)の患者
呼吸抑制や昏睡を起こすおそれがある。
9.1.8 副腎皮質機能低下症(アジソン病等)の患者
呼吸抑制作用に対し、感受性が高くなっている。
9.1.9 薬物・アルコール依存又はその既往歴のある患者
依存性を生じやすい。[9.1.10参照]
9.1.10 薬物、アルコール等による精神障害のある患者
症状が増悪するおそれがある。[9.1.9参照]
9.1.11 衰弱者
呼吸抑制作用に対し、感受性が高くなっている。
9.1.12 前立腺肥大による排尿障害、尿道狭窄、尿路手術術後の患者
排尿障害を増悪することがある。
9.1.13 器質的幽門狭窄又は最近消化管手術を行った患者
消化管運動を抑制する。
9.1.14 痙攣の既往歴のある患者
痙攣を誘発するおそれがある。[2.4参照]
9.1.15 胆嚢障害、胆石症又は膵炎の患者
オッジ筋を収縮させ症状が増悪することがある。
9.1.16 重篤な炎症性腸疾患のある患者
連用した場合、巨大結腸症を起こすおそれがある。
9.2 腎機能障害患者
排泄が遅延し副作用があらわれるおそれがある。[16.6.1参照]
9.3 肝機能障害患者
代謝が遅延し副作用があらわれるおそれがある。[16.6.2参照]
9.5 妊婦
9.5.1 妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。オキシコドンでは催奇形作用は認められていないが、類薬のモルヒネの動物試験(マウス、ラット)で催奇形作用が報告されている。
9.5.2 分娩前に投与した場合、出産後新生児に退薬症候(多動、神経過敏、不眠、振戦等)があらわれることがある。
9.5.3 分娩時の投与により、新生児に呼吸抑制があらわれることがある。
9.6 授乳婦
本剤投与中は授乳を避けさせること。ヒト母乳中へ移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら、慎重に投与すること。一般に生理機能が低下しており、特に呼吸抑制の感受性が高い。
10. 相互作用
相互作用序文
本剤は、主として薬物代謝酵素CYP3A4及び一部CYP2D6で代謝される。[16.4参照]
薬物代謝酵素用語
CYP3A4
薬物代謝酵素用語
CYP2D6
10.1 併用禁忌
| ナルメフェン塩酸塩水和物 セリンクロ [2.9参照] | 本剤の鎮痛作用を減弱させることがある。また、退薬症候を起こすことがある。 | μオピオイド受容体拮抗作用により、本剤の作用が競合的に阻害される。 |
10.2 併用注意
| 中枢神経抑制剤 フェノチアジン誘導体、バルビツール酸誘導体等 吸入麻酔剤 MAO阻害剤 三環系抗うつ剤 β遮断剤 アルコール | 臨床症状:呼吸抑制、低血圧及び顕著な鎮静又は昏睡が起こることがある。 措置方法:減量するなど慎重に投与すること。 | 相加的に中枢神経抑制作用を増強させる。 |
| クマリン系抗凝血剤 ワルファリンカリウム | クマリン系抗凝血剤の作用が増強されることがあるので投与量を調節するなど慎重に投与すること。 | 機序は不明である。 |
| 抗コリン作用を有する薬剤 フェノチアジン系薬剤、三環系抗うつ剤等 | 臨床症状:麻痺性イレウスに至る重篤な便秘又は尿貯留が起こることがある。 | 相加的に抗コリン作用を増強させる。 |
| ブプレノルフィン、ペンタゾシン等 | 本剤の鎮痛作用を減弱させることがある。また、退薬症候を起こすことがある。 | ブプレノルフィン、ペンタゾシン等は本剤の作用するμ受容体の部分アゴニストである。 |
| CYP3A4阻害作用を有する薬剤 ボリコナゾール、イトラコナゾール、フルコナゾール、リトナビル、クラリスロマイシン等 [16.7.1-16.7.3参照] | 本剤の血中濃度が上昇し、副作用が発現するおそれがあるので、観察を十分に行い、慎重に投与すること。 | CYP3A4を介する本剤の代謝が阻害される。 |
| CYP3A4誘導作用を有する薬剤 リファンピシン、カルバマゼピン、フェニトイン等 [16.7.4参照] | 本剤の血中濃度が低下し、作用が減弱する可能性がある。なお、これらの薬剤の中止後に、本剤の血中濃度が上昇し、副作用が発現するおそれがあるので、観察を十分に行い、慎重に投与すること。 | CYP3A4を介する本剤の代謝が促進される。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
顔面蒼白、血圧低下、呼吸困難、頻脈、全身発赤、血管浮腫、蕁麻疹等の症状があらわれた場合には投与を中止し、適切な処置を行うこと。[9.1.5参照]
11.1.2 依存性(頻度不明)
11.1.3 呼吸抑制(頻度不明)
11.1.4 錯乱(頻度不明)、譫妄(2%未満)
11.1.5 無気肺、気管支痙攣、喉頭浮腫(いずれも頻度不明)
11.1.6 麻痺性イレウス、中毒性巨大結腸(いずれも頻度不明)
炎症性腸疾患の患者に投与した場合、中毒性巨大結腸があらわれるとの報告がある。[2.5参照]
11.1.7 肝機能障害(頻度不明)
AST、ALT、Al-P等の著しい上昇を伴う肝機能障害があらわれることがある。
11.2 その他の副作用
| 5%以上 | 5%未満 | 頻度不明 | |
| 過敏症 | 発疹、蕁麻疹 | ||
| 循環器 | 低血圧 | 不整脈、血圧変動、起立性低血圧、失神 | |
| 精神神経系 | 眠気(16.9%)、傾眠、眩暈 | 頭痛・頭重感、不眠 | 発汗、幻覚、意識障害、しびれ、筋れん縮、焦燥、不安、異夢、悪夢、興奮、視調節障害、縮瞳、神経過敏、感覚異常、痙攣、振戦、筋緊張亢進、健忘、抑うつ、感情不安定、多幸感、思考異常、構語障害、痛覚過敏注)、アロディニア |
| 消化器 | 便秘(26.8%)、嘔気(16.9%)、嘔吐 | 下痢、食欲不振、胃不快感、口渇 | 腹痛、おくび、鼓腸、味覚異常、嚥下障害、オッジ筋の機能不全 |
| その他 | そう痒感、発熱、倦怠感、血管拡張(顔面潮紅、熱感)、呼吸困難 | 悪寒、頭蓋内圧の亢進、脱力感、胸部圧迫感、排尿障害、尿閉、脱水、無月経、性欲減退、勃起障害、浮腫、皮膚乾燥 |
13. 過量投与
14. 適用上の注意
14.1 薬剤投与時の注意
本剤を注射しないこと。本剤には水に不溶性である添加剤が含まれており、肺塞栓、血管閉塞、潰瘍、膿瘍を引き起こすなど、重度で致死的な事態を生じることがある。また、本剤には乱用防止を目的として麻薬拮抗剤ナロキソンを添加している。本剤を注射するとオキシコドンの作用が拮抗され、麻薬依存患者では退薬症候を誘発するおそれがある。
14.2 薬剤交付時の注意
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
がん疼痛患者を対象に、オキシコドン塩酸塩散2.5mg、5mgを食後単回経口投与したときの、オキシコドン及びノルオキシコドンの薬物動態パラメータを次の表に示す1)。
| 投与量(mg) | 例数 | Cmax(ng/mL) | Tmax(hr) | AUC0-6(ng・hr/mL) | t1/2(hr) | |
| 2.5 | オキシコドン | 18 | 6.80±1.89 | 1.9±1.4 | 28.3±6.4 | 6.0±3.9 |
| ノルオキシコドン | 2.32±1.18 | 2.1±1.4 | 9.59±5.26 | − | ||
| 5 | オキシコドン | 16a) | 13.7±4.8 | 1.7±1.3 | 53.2±20.0 | 4.5±2.3 |
| ノルオキシコドン | 5.28±1.91 | 1.8±1.2 | 23.8±9.5 | − |
16.1.2 生物学的同等性試験
オキシコドン錠5mgNX「第一三共」とオキノーム散(それぞれオキシコドン塩酸塩として5mg)を、クロスオーバー法により健康成人男性23例に空腹時単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された。なお、血漿中ナロキソン濃度は、測定されたすべての時点で定量下限未満であった2)。
単回経口投与時の血漿中オキシコドン濃度推移
| n | AUC0-24hr(ng・hr/mL) | Cmax(ng/mL) | Tmaxa)(hr) | t1/2(hr) | |
| オキシコドン錠5mgNX「第一三共」 | 23 | 60.7±15.0 | 13.3±3.64 | 0.75(0.50〜1.50) | 3.92±0.453 |
| オキノーム散(即放性散剤、5mg) | 23 | 57.9±14.4 | 12.5±2.34 | 1.00(0.50〜4.00) | 3.90±0.369 |
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.2 吸収
16.2.1 バイオアベイラビリティ
16.2.2 食事の影響
健康成人22例においてオキシコドン塩酸塩内用液剤20mgを単回経口投与したときの食事の影響について評価したところ、空腹時に比べ高脂肪食摂取後でCmaxは約80%に低下し、AUCは約1.2倍に増大した5)(外国人データ)。
16.3 分布
16.3.1 血清蛋白結合率
限外ろ過法を用いて測定したヒト血清蛋白結合率は45.0〜45.8%であり、主としてアルブミンと結合する6)(in vitro)。
16.3.2 母乳中への移行
オキシコドン塩酸塩とアセトアミノフェンの合剤を授乳婦6例に経口投与したとき、母乳への移行が認められ、そのときの投与0.25〜12時間後におけるオキシコドン塩酸塩濃度の乳汁/血漿中濃度の平均比率は3.4であった7)(外国人データ)。
16.4 代謝
16.5 排泄
健康成人9例にオキシコドン塩酸塩0.28mg/kgを経口投与したとき、投与後24時間までの尿中に投与量の5.5±2.5%(平均値±標準偏差)が未変化体として、また、2.3±5.5%がオキシコドンの抱合体として排泄された。また、尿中にはノルオキシコドンとオキシモルフォン抱合体も排泄された3)(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
16.6.2 肝機能障害患者
16.6.3 高齢者
健康高齢者(65〜79歳)、健康非高齢者(21〜45歳)各14例にオキシコドン塩酸塩徐放錠20mgを空腹時単回経口投与したとき、薬物動態に関しては高齢者と非高齢者との間に差は認められなかった11)(外国人データ)。
16.6.4 男女差
健康成人男女各14例にオキシコドン塩酸塩徐放錠20mgを空腹時単回経口投与したとき、女性では、Cmax並びにAUCが、いずれも男性より約1.4倍高かった11)(外国人データ)。
16.7 薬物相互作用
16.7.1 ボリコナゾール(100〜200mg/日、経口投与)とオキシコドン塩酸塩(24〜48mg/日、持続皮下投与)を4日間併用した症例(1例)の定常状態時におけるオキシコドンの血漿中濃度は、測定した全症例の平均の3.57倍であった12)(国内におけるオキシコドン注射剤の臨床試験成績)。
また、ボリコナゾール〔400mg/日(2日目のみ600mg/日)〕の経口投与中にオキシコドン塩酸塩(10mg)を単回経口投与した場合、オキシコドンのCmaxが1.72倍、AUCが3.61倍上昇したとの報告がある13)(外国人データ)。[10.2参照]
また、ボリコナゾール〔400mg/日(2日目のみ600mg/日)〕の経口投与中にオキシコドン塩酸塩(10mg)を単回経口投与した場合、オキシコドンのCmaxが1.72倍、AUCが3.61倍上昇したとの報告がある13)(外国人データ)。[10.2参照]
16.7.2 リトナビル(600mg/日)の経口投与中にオキシコドン塩酸塩(10mg)を単回経口投与した場合、オキシコドンのCmaxが1.74倍、AUCが2.95倍上昇したとの報告がある14)(外国人データ)。[10.2参照]
16.8 その他
オキシコドン錠2.5mgNX「第一三共」、オキシコドン錠10mgNX「第一三共」、オキシコドン錠20mgNX「第一三共」は、「含量が異なる経口固形製剤の生物学的同等性試験ガイドライン」に基づき、オキシコドン錠5mgNX「第一三共」を標準製剤としたとき、溶出挙動が等しく、生物学的に同等とみなされた17)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
オキシコドン塩酸塩水和物の承認時における一般臨床試験での中等度から高度のがん疼痛を有する患者に対する臨床試験成績の概要を以下に示す。
17.1.1 国内第III相試験(オープンラベル試験)
(1)疼痛コントロール達成率
オキシコドン塩酸塩水和物投与による疼痛コントロール達成状況を評価したところ、90%以上の疼痛コントロール達成率が得られた1)。
| 治療開始前のオピオイド系鎮痛剤の使用状況 | 疼痛コントロール達成例数/評価対象例数 | 疼痛コントロール達成率(%) |
| あり | 39/43 | 90.7 |
| なし | 22/23 | 95.7 |
| 合計 | 61/66 | 92.4 |
(2)疼痛強度評点
オキシコドン塩酸塩水和物投与開始24時間後及びオキシコドン塩酸塩水和物投与終了時の疼痛強度は、オキシコドン塩酸塩水和物投与前に比べて有意に改善していた。なお、疼痛強度の評価は患者自身による4段階評価(評点:0=なし「痛くない」、1=軽度「少し痛い」、2=中等度「痛い」、3=高度「非常に痛い」)で行った1)。
| 観察時期 | 評価症例数 | 疼痛強度評点(平均値±標準偏差) | p値a) |
| 投与前 | 66 | 1.4±0.8 | − |
| 投与開始24時間後 | 65 | 1.0±0.7 | <0.0001 |
| 投与終了時 | 61 | 0.8±0.4 | <0.0001 |
(3)副作用発現頻度は63.4%(45/71例)であった。主な副作用は、便秘26.8%(19/71例)、眠気、嘔気各16.9%(12/71例)であった1)。
17.1.2 国内第III相試験(臨時追加投与)
オキシコドン塩酸塩水和物徐放錠の定時投与時に発現する突発性疼痛に対して、オキシコドン塩酸塩水和物を臨時追加投与したところ、投与1時間後の疼痛強度(CAT)はオキシコドン塩酸塩水和物投与前に比べて有意に軽減した。また、投与1時間後の鎮痛効果についても有効率注1)は80%であった。
鎮痛効果の発現注2)は投与15分以内から認められ、30分以内に85%の患者において効果が認められた。
副作用発現頻度は83.7%(41/49例)であった。主な副作用は、便秘40.8%(20/49例)、嘔気36.7%(18/49例)、眠気24.5%(12/49例)、嘔吐20.4%(10/49例)、食欲不振14.3%(7/49例)、傾眠12.2%(6/49例)、めまい10.2%(5/49例)であった18)。
鎮痛効果の発現注2)は投与15分以内から認められ、30分以内に85%の患者において効果が認められた。
副作用発現頻度は83.7%(41/49例)であった。主な副作用は、便秘40.8%(20/49例)、嘔気36.7%(18/49例)、眠気24.5%(12/49例)、嘔吐20.4%(10/49例)、食欲不振14.3%(7/49例)、傾眠12.2%(6/49例)、めまい10.2%(5/49例)であった18)。
注1)患者自身による本剤投与1時間後の鎮痛評価(1:「よく効いた」、2:「効いた」、3:「少し効いた」、4:「効かなかった」)のうち、「よく効いた」、「効いた」の占める割合
注2)患者が鎮痛効果があらわれ始めたと感じた時間
18. 薬効薬理
18.1 作用機序
モルヒネと同様にμオピオイド受容体を介して鎮痛作用を示すものと考えられる。
18.2 薬理作用
鎮痛作用についてモルヒネ硫酸塩を対照薬として検討した。
マウスのHot plate法、Tail pressure法、酢酸ライジング法及びラットのTail flick法(いずれも経口投与)を用いて検討した結果、オキシコドン塩酸塩はモルヒネ硫酸塩よりED50値で3〜6倍、効力比で3〜5倍強い鎮痛作用を示した19)。
マウスのHot plate法、Tail pressure法、酢酸ライジング法及びラットのTail flick法(いずれも経口投与)を用いて検討した結果、オキシコドン塩酸塩はモルヒネ硫酸塩よりED50値で3〜6倍、効力比で3〜5倍強い鎮痛作用を示した19)。
| 試験法 | 動物種 | ED50(95%信頼限界)mg/kg | |
| オキシコドン塩酸塩 | モルヒネ硫酸塩 | ||
| Hot plate法 | マウス | 3.2(0.9-5.3) | 15.6(8.6-21.9) |
| Tail pressure法 | マウス | 3.5(2.7-4.5) | 8.9(4.8-12.7) |
| 酢酸ライジング法 | マウス | 2.3(1.6-4.0) | 7.0(4.6-15.6) |
| Tail flick法 | ラット | 3.8(1.8-5.5) | 21.6(19.2-24.2) |
19. 有効成分に関する理化学的知見
19.1. オキシコドン塩酸塩水和物
20. 取扱い上の注意
<2.5mg錠>
錠剤表面に使用色素による赤色又は黒色の斑点がみられることがある。
<5mg錠>
錠剤表面に使用色素による黄色の斑点がみられることがある。
<20mg錠>
錠剤表面に使用色素による赤色の斑点がみられることがある。
22. 包装
<オキシコドン錠2.5mgNX「第一三共」>
(PTP、乾燥剤入り) 20錠(10錠×2) 100錠(10錠×10)
<オキシコドン錠5mgNX「第一三共」>
(PTP、乾燥剤入り) 20錠(10錠×2) 100錠(10錠×10)
<オキシコドン錠10mgNX「第一三共」>
(PTP、乾燥剤入り) 20錠(10錠×2) 100錠(10錠×10)
<オキシコドン錠20mgNX「第一三共」>
(PTP、乾燥剤入り) 20錠(10錠×2) 100錠(10錠×10)
23. 主要文献
- 国内オープンラベル試験(オキノーム散:2006年10月20日承認、CTD2.7.6.7)
- 社内資料:健康成人を対象としたオキシコドン錠5mgNX「第一三共」と標準製剤の生物学的同等性試験
- Poyhia R,et al., Br J Clin Pharmacol., 33 (6), 617-621, (1992) »PubMed
- Leow KP,et al., Clin Pharmacol Ther., 52 (5), 487-495, (1992) »PubMed
- 食事の影響試験(オキシコンチン錠:2003年4月16日承認、申請資料概要ヘ.3.(1)4))
- Leow KP,et al., Ther Drug Monit., 15 (5), 440-447, (1993) »PubMed
- Marx CM,et al., Drug Intell Clin Pharm., 20, 474, (1986)
- Lalovic B,et al., Drug Metab Dispos., 32 (4), 447-454, (2004) »PubMed
- 腎機能障害者における薬物動態(オキシコンチン錠:2003年4月16日承認、申請資料概要ヘ.3.(1)6))
- 肝機能障害者における薬物動態(オキシコンチン錠:2003年4月16日承認、申請資料概要ヘ.3.(1)7))
- 高齢者における薬物動態(オキシコンチン錠:2003年4月16日承認、申請資料概要ヘ.3.(1)5))
- 国内第III相試験、有効性及び安全性の概要(オキファスト注:2012年1月18日承認、CTD2.5.5.5)
- Hagelberg NM,et al., Eur J Clin Pharmacol., 65 (3), 263-271, (2009) »PubMed
- Nieminen TH,et al., Eur J Clin Pharmacol., 66 (10), 977-985, (2010) »PubMed
- Liukas A,et al., J Clin Psychopharmacol., 31 (3), 302-308, (2011) »PubMed
- Nieminen TH,et al., Anesthesiology, 110 (6), 1371-1378, (2009) »PubMed
- 社内資料:オキシコドン錠NXの溶出性に関する資料
- 継続投与試験(オキノーム散:2006年10月20日承認、CTD2.7.6.8)
- マウス、ラットにおける鎮痛作用(オキシコンチン錠:2003年4月16日承認、申請資料概要ホ.1.(1))
24. 文献請求先及び問い合わせ先
文献請求先
第一三共株式会社
製品情報センター
〒103-8426
東京都中央区日本橋本町3-5-1
電話:0120-065-132(がん・医療用麻薬専用)
製品情報問い合わせ先
第一三共株式会社
製品情報センター
〒103-8426
東京都中央区日本橋本町3-5-1
電話:0120-065-132(がん・医療用麻薬専用)
25. 保険給付上の注意
本剤は厚生労働省告示第75号(平成24年3月5日付)に基づき、1回30日分を限度として投薬する。
26. 製造販売業者等
26.1 製造販売元
第一三共株式会社
東京都中央区日本橋本町3-5-1