医薬品情報
| 総称名 | フェノテロール臭化水素酸塩 |
|---|---|
| 一般名 | フェノテロール臭化水素酸塩 |
| 欧文一般名 | Fenoterol Hydrobromide |
| 製剤名 | シロップ用フェノテロール臭化水素酸塩 |
| 薬効分類名 | 気管支拡張剤 |
| 薬効分類番号 | 2252 |
| ATCコード | R03AC04 R03CC04 |
| KEGG DRUG |
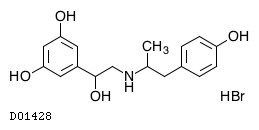
D01428
フェノテロール臭化水素酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2023年11月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 12.臨床検査結果に及ぼす影響 16.薬物動態 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| フェノテロール臭化水素酸塩DS小児用0.5%「タカタ」 (後発品) | Fenoterol Hydrobromide Dry syrup "TAKATA" for Pediatric | 高田製薬 | 2252006R2057 | 22.7円/g | 劇薬 |
2. 禁忌
次の患者には投与しないこと
2.1 カテコールアミン(エピネフリン、イソプロテレノール等)を投与中の患者[10.1参照]
2.2 本剤の成分に対して過敏症の既往歴のある患者
4. 効能または効果
6. 用法及び用量
通常幼小児に対し、1日0.075g/kg(フェノテロール臭化水素酸塩として0.375mg/kg)を3回に分け、用時溶解して経口投与する。なお、年齢、症状により適宜増減するが、標準投与量は通常、
0.5〜1歳未満 0.3〜0.6g(フェノテロール臭化水素酸塩として1.5〜3.0mg)
1〜3歳未満 0.6〜0.9g(フェノテロール臭化水素酸塩として3.0〜4.5mg)
3〜5歳未満 0.9〜1.5g(フェノテロール臭化水素酸塩として4.5〜7.5mg)
を1日量とし、1日3回に分け、用時溶解して経口投与する。
0.5〜1歳未満 0.3〜0.6g(フェノテロール臭化水素酸塩として1.5〜3.0mg)
1〜3歳未満 0.6〜0.9g(フェノテロール臭化水素酸塩として3.0〜4.5mg)
3〜5歳未満 0.9〜1.5g(フェノテロール臭化水素酸塩として4.5〜7.5mg)
を1日量とし、1日3回に分け、用時溶解して経口投与する。
8. 重要な基本的注意
8.1 用法用量どおり正しく使用しても効果が認められない場合は、本剤が適当でないと考えられるので、投与を中止すること。また、経過の観察を十分に行うこと。
8.2 過度に使用を続けた場合、不整脈、場合により心停止を起こすおそれがあるので、使用が過度にならないように注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 甲状腺機能亢進症の患者
症状を悪化させるおそれがある。
9.1.2 高血圧症の患者
血圧が上昇することがある。
9.1.3 心疾患のある患者
動悸、不整脈等があらわれることがある。
9.1.4 糖尿病の患者
症状を悪化させるおそれがある。
9.1.5 低酸素血症の患者
血清カリウム値をモニターすることが望ましい。低酸素血症は血清カリウム値の低下が心リズムに及ぼす作用を増強することがある。[11.1.1参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
動物実験(ラット)で胎児骨格異常の出現頻度の増加が報告されている。
動物実験(ラット)で胎児骨格異常の出現頻度の増加が報告されている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
動物実験(ウサギ)で乳汁中へ移行することが報告されている。
動物実験(ウサギ)で乳汁中へ移行することが報告されている。
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下している。
10. 相互作用
10.1 併用禁忌
| カテコールアミン(エピネフリン、イソプロテレノール等) エピネフリン製剤(エピネフリン、ボスミン注、ノルエピネフリン) イソプロテレノール製剤(アスプール液、メジヘラー・イソ) [2.1参照] | 不整脈、場合によっては心停止を起こすおそれがある。 | エピネフリン、イソプロテレノール等のカテコールアミン併用により、アドレナリン作動性神経刺激の増大が起きる。 そのため不整脈を起こすことが考えられる。 |
10.2 併用注意
| キサンチン誘導体 テオフィリン アミノフィリン ステロイド剤 ベタメタゾン プレドニゾロン コハク酸ヒドロコルチゾンナトリウム 利尿剤 フロセミド [11.1.1参照] | 血清カリウム値の低下作用を増強することがある。 血清カリウム値のモニターを行う。 | キサンチン誘導体はアドレナリン作動性神経刺激を増大させるため、血清カリウム値の低下を増強することが考えられる。 ステロイド剤及び利尿剤は尿細管でのカリウム排泄促進作用があるため、血清カリウム値の低下が増強することが考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 重篤な血清カリウム値の低下(頻度不明)
11.2 その他の副作用
| 0.1%以上 | 頻度不明 | |
| 循環器 | 動悸(0.2%) | 顔のほてり、頻脈、胸痛 |
| 精神神経系 | 頭痛(0.2%) | 振戦 |
| 消化器 | 口渇(0.2%)、嘔気(0.2%)、嘔吐(0.2%) | 腹痛、食欲不振、胃部不快感、便秘 |
| 過敏症 | 発疹、そう痒症、じん麻疹 | |
| その他 | 倦怠感、手指腫脹感 |
12. 臨床検査結果に及ぼす影響
本剤はアレルゲンによる皮膚反応に抑制的に作用する場合があるので、注意すること。
16. 薬物動態
16.1 血中濃度
16.1.1 生物学的同等性試験
フェノテロール臭化水素酸塩DS小児用0.5%「タカタ」とベロテックシロップ0.05%をクロスオーバー法により、健康成人男子16名にそれぞれフェノテロール臭化水素酸塩として7.5mgを空腹時に単回経口投与し、投与前、投与後0.5、1、2、3、4、5、6、9、12及び24時間に前腕静脈から採血した。液体クロマトグラフィーにより測定したフェノテロール臭化水素酸塩の血漿中濃度の推移及びパラメータは次のとおりであり、AUC及びCmaxについて統計的評価を行った結果、両剤の生物学的同等性が確認された1)。
図16-1 血漿中濃度
| 判定パラメータ | 参考パラメータ | |||
| AUCt(ng・hr/mL) | Cmax(ng/mL) | tmax(hr) | t1/2(hr) | |
| フェノテロール臭化水素酸塩DS小児用0.5%「タカタ」 | 289.23±30.01 | 44.88±5.63 | 2.2±0.4 | 4.4±1.0 |
| ベロテックシロップ0.05% | 284.11±24.99 | 49.32±5.72 | 2.7±0.3 | 3.8±0.8 |
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
18. 薬効薬理
18.1 作用機序
フェノテロールの薬効薬理作用の主体は、β2アドレナリン受容体刺激による気管支平滑筋弛緩作用(気管支拡張作用)である2)。
19. 有効成分に関する理化学的知見
19.1. フェノテロール臭化水素酸塩
20. 取扱い上の注意
20.1 開封後は遮光し、湿気を避けて保存すること。
20.2 溶解後はできるだけ速やかに使用すること。
22. 包装
100g[プラスチック瓶、バラ、乾燥剤入り]
500g[プラスチック瓶、バラ、乾燥剤入り]
23. 主要文献
- 社内資料:生物学的同等性試験(フェノテロール臭化水素酸塩DS小児用0.5%「タカタ」)
- 柳川孝生他, 応用薬理, 20, 415-424, (1980)
24. 文献請求先及び問い合わせ先
文献請求先
高田製薬株式会社
文献請求窓口
〒336-8666
さいたま市南区沼影1丁目11番1号
電話:0120-989-813
FAX:048-816-4183
製品情報問い合わせ先
高田製薬株式会社
文献請求窓口
〒336-8666
さいたま市南区沼影1丁目11番1号
電話:0120-989-813
FAX:048-816-4183
26. 製造販売業者等
26.1 製造販売元
高田製薬株式会社
さいたま市西区宮前町203番地1