医薬品情報
| 総称名 | カボメティクス |
|---|---|
| 一般名 | カボザンチニブリンゴ酸塩 |
| 欧文一般名 | Cabozantinib Malate |
| 製剤名 | カボザンチニブリンゴ酸塩錠 |
| 薬効分類名 | 抗悪性腫瘍剤 キナーゼ阻害剤 |
| 薬効分類番号 | 4291 |
| ATCコード | L01EX07 |
| KEGG DRUG |
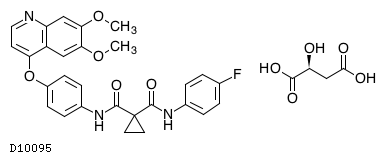
D10095
カボザンチニブリンゴ酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年2月 改訂(第7版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| カボメティクス錠20mg | CABOMETYX tablets 20mg | 武田薬品工業 | 4291064F1020 | 8007.6円/錠 | 劇薬, 処方箋医薬品注) |
| カボメティクス錠60mg | CABOMETYX tablets 60mg | 武田薬品工業 | 4291064F2026 | 22333円/錠 | 劇薬, 処方箋医薬品注) |
1. 警告
本剤を投与する場合には、緊急時に十分対応できる医療機関において、がん化学療法に十分な知識及び経験を持つ医師のもとで、本剤が適切と判断される症例についてのみ投与すること。また、治療開始に先立ち、患者又は患者の家族に有効性及び危険性を十分説明し、同意を得てから投与すること。
2. 禁忌
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
5. 効能または効果に関連する注意
<根治切除不能又は転移性の腎細胞癌>
5.1 本剤の術後補助療法における有効性及び安全性は確立していない。
<がん化学療法後に増悪した切除不能な肝細胞癌>
6. 用法及び用量
カボメティクス錠20mg
| 販売名 | 効能又は効果 | 用法及び用量 |
| カボメティクス錠20mg | 根治切除不能又は転移性の腎細胞癌 | 通常、成人にはカボザンチニブとして1日1回60mgを空腹時に経口投与する。なお、患者の状態により適宜減量する。 ニボルマブ(遺伝子組換え)と併用する場合は、通常、成人にはカボザンチニブとして1日1回40mgを空腹時に経口投与する。なお、患者の状態により適宜減量する。 |
| がん化学療法後に増悪した切除不能な肝細胞癌 | 通常、成人にはカボザンチニブとして1日1回60mgを空腹時に経口投与する。なお、患者の状態により適宜減量する。 |
カボメティクス錠60mg
| 販売名 | 効能又は効果 | 用法及び用量 |
| カボメティクス錠60mg | 根治切除不能又は転移性の腎細胞癌 がん化学療法後に増悪した切除不能な肝細胞癌 | 通常、成人にはカボザンチニブとして1日1回60mgを空腹時に経口投与する。なお、患者の状態により適宜減量する。 |
7. 用法及び用量に関連する注意
カボメティクス錠20mg
<効能共通>
7.1 食後に本剤を投与した場合、Cmax及びAUCが増加するとの報告がある。食事の影響を避けるため、食事の1時間前から食後2時間までの間の服用は避けること。[16.2.1参照]
7.2 副作用が発現した場合には、以下の基準を考慮して、本剤を休薬、減量又は中止すること。
| 減量レベル | 投与量 | |
| 本剤単独投与の場合 | ニボルマブ(遺伝子組換え)と併用する場合 | |
| 通常投与量 | 60mg/日 | 40mg/日 |
| 1段階減量 | 40mg/日 | 20mg/日 |
| 2段階減量 | 20mg/日 | 20mg/日を隔日投与 |
| 中止 | 20mg/日で忍容不能な場合、投与を中止する。 | 20mg/日の隔日投与で忍容不能な場合、投与を中止する。 |
| 副作用 | 程度注) | 処置 |
| ニボルマブ(遺伝子組換え)との併用投与下の肝機能障害 | ALT若しくはASTが基準値上限の3倍超5倍以下に増加、又は総ビリルビンが基準値上限の1.5倍超3倍以下の場合 | 管理困難で忍容不能な場合は、Grade1以下に回復するまで1段階ずつ減量又は休薬する。 休薬後に投与を再開する際には、1段階減量した用量から開始する(休薬前の用量まで再増量不可)。 |
| ALT又はASTが基準値上限の5倍超8倍以下に増加し、かつ総ビリルビンが基準値上限の2倍以下の場合 | Grade1以下に回復するまで休薬する。投与を再開する際には、1段階減量した用量から開始する(休薬前の用量まで再増量不可)。 | |
| ALT若しくはASTが基準値上限の8倍超、又はALT若しくはASTが基準値上限の3倍超、かつ総ビリルビンが基準値上限の2倍超の場合 | 投与を中止する。 | |
| 上記以外の副作用 | Grade2の場合 | 管理困難で忍容不能な場合は、Grade1以下に回復するまで1段階ずつ減量又は休薬する。休薬後に投与を再開する際には、1段階減量した用量から開始する(単独投与の場合は休薬前の用量まで再増量可)。 |
| Grade3の場合 | Grade1以下に回復するまで1段階ずつ減量又は休薬する。休薬後に投与を再開する際には、1段階減量した用量から開始する(単独投与の場合は休薬前の用量まで再増量可)。 | |
| Grade4の場合 | Grade1以下に回復するまで休薬する。投与を再開する際には、1段階減量した用量から開始する(休薬前の用量まで再増量不可)。 |
7.3 20mg錠と60mg錠の生物学的同等性は示されていないため、60mgを投与する際には20mg錠を使用しないこと。
<がん化学療法後に増悪した切除不能な肝細胞癌>
7.4 他の抗悪性腫瘍剤との併用について、有効性及び安全性は確立していない。
カボメティクス錠60mg
<効能共通>
7.1 食後に本剤を投与した場合、Cmax及びAUCが増加するとの報告がある。食事の影響を避けるため、食事の1時間前から食後2時間までの間の服用は避けること。[16.2.1参照]
7.2 副作用が発現した場合には、以下の基準を考慮して、本剤を休薬、減量又は中止すること。
| 減量レベル | 投与量 |
| 本剤単独投与の場合 | |
| 通常投与量 | 60mg/日 |
| 1段階減量 | 40mg/日 |
| 2段階減量 | 20mg/日 |
| 中止 | 20mg/日で忍容不能な場合、投与を中止する。 |
| 程度注) | 処置 |
| Grade2の場合 | 管理困難で忍容不能な場合は、Grade1以下に回復するまで1段階ずつ減量又は休薬する。休薬後に投与を再開する際には、1段階減量した用量から開始する(単独投与の場合は休薬前の用量まで再増量可)。 |
| Grade3の場合 | Grade1以下に回復するまで1段階ずつ減量又は休薬する。休薬後に投与を再開する際には、1段階減量した用量から開始する(単独投与の場合は休薬前の用量まで再増量可)。 |
| Grade4の場合 | Grade1以下に回復するまで休薬する。投与を再開する際には、1段階減量した用量から開始する(休薬前の用量まで再増量不可)。 |
7.3 20mg錠と60mg錠の生物学的同等性は示されていないため、60mgを投与する際には20mg錠を使用しないこと。
<がん化学療法後に増悪した切除不能な肝細胞癌>
7.4 他の抗悪性腫瘍剤との併用について、有効性及び安全性は確立していない。
8. 重要な基本的注意
8.2 蛋白尿があらわれることがあるので、本剤の投与開始前及び投与期間中は定期的に尿蛋白を観察すること。[11.1.8参照]
8.3 肝不全、肝機能障害があらわれることがあるので、本剤の投与開始前及び投与期間中は定期的に肝機能検査を行うこと。なお、主に肝細胞癌患者において肝性脳症が報告されているので、意識障害等の臨床症状を十分に観察すること。[11.1.9参照]
8.4 血清アミラーゼ、血清リパーゼの上昇があらわれることがあるので、本剤の投与開始前及び投与期間中は定期的に膵酵素を含む検査を行うこと。[11.1.7参照]
8.5 創傷治癒を遅らせる可能性があるので、外科的処置が予定されている場合には、外科的処置の前に本剤の投与を中断すること。外科的処置後の投与再開は、患者の状態に応じて判断すること。[9.1.6、11.1.15参照]
8.6 顎骨壊死があらわれることがある。報告された症例の多くが抜歯等の顎骨に対する侵襲的な歯科処置や局所感染に関連して発現している。本剤の投与開始前は口腔内の管理状態を確認し、必要に応じて患者に対して適切な歯科検査を受け、侵襲的な歯科処置をできる限り済ませておくよう指導すること。本剤投与中に歯科処置が必要になった場合には、できる限り非侵襲的な歯科処置を受けるよう指導すること。また、口腔内を清潔に保つこと、定期的な歯科検査を受けること、歯科受診時に本剤の使用を歯科医師に告知して侵襲的な歯科処置はできる限り避けることなどを患者に十分説明し、異常が認められた場合には、直ちに歯科・口腔外科を受診するよう指導すること。[11.1.6参照]
8.7 骨髄抑制があらわれることがあるので、本剤の投与開始前及び投与期間中は定期的に血液学的検査を行うなど、患者の状態を十分に観察すること。[11.1.10参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 高血圧の患者
9.1.2 消化管等腹腔内の炎症を合併している患者、消化管に腫瘍の浸潤を認める患者
消化管穿孔、瘻孔のおそれがある。[11.1.1参照]
9.1.3 血栓塞栓症又はその既往のある患者
血栓塞栓症が悪化又は再発するおそれがある。[11.1.3参照]
9.1.4 脳転移を有する患者
脳出血のおそれがある。[11.1.2参照]
9.1.5 肺転移を有する患者
肺出血のおそれがある。[11.1.2参照]
9.1.6 外科処置後、創傷外科的処置後、創傷が治癒していない患者
9.3 肝機能障害患者
減量を考慮するとともに、患者の状態をより慎重に観察し、副作用の発現に十分注意すること。血中濃度が上昇し、副作用が強くあらわれるおそれがある。重度肝機能障害患者(Child-Pugh分類C)を対象とした臨床試験は実施していない。[16.6.2参照]
9.4 生殖能を有する者
妊娠可能な女性に対しては、本剤投与中及び投与終了後一定期間は適切な避妊を行うよう指導すること。[9.5参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
胚・胎児発生毒性試験において、ラットでは最大臨床用量(60mg/日)におけるカボザンチニブの曝露量(AUC)の0.5倍の曝露量で着床後胚死亡率の増加が認められている。また、ヒトでの相当量は不明であるが、胎児の外表異常(浮腫、口蓋裂、口唇裂、曲尾/痕跡尾、皮膚形成不全)が認められている。ウサギでは、最大臨床用量(60mg/日)におけるカボザンチニブの曝露量(AUC)の0.1倍の曝露量で胎児の内臓異常(肺中葉の矮小化又は欠損、脾臓の小型化)が認められている。[9.4参照]
胚・胎児発生毒性試験において、ラットでは最大臨床用量(60mg/日)におけるカボザンチニブの曝露量(AUC)の0.5倍の曝露量で着床後胚死亡率の増加が認められている。また、ヒトでの相当量は不明であるが、胎児の外表異常(浮腫、口蓋裂、口唇裂、曲尾/痕跡尾、皮膚形成不全)が認められている。ウサギでは、最大臨床用量(60mg/日)におけるカボザンチニブの曝露量(AUC)の0.1倍の曝露量で胎児の内臓異常(肺中葉の矮小化又は欠損、脾臓の小型化)が認められている。[9.4参照]
9.6 授乳婦
授乳しないことが望ましい。ラットの出生前及び出生後の生殖毒性試験で授乳期に本剤を母動物に投与したとき、出生児の血漿中に本剤が検出されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
10. 相互作用
相互作用序文
本剤は、主に薬物代謝酵素CYP3A4で代謝される。
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| CYP3A阻害剤 リトナビル イトラコナゾール クラリスロマイシン等 グレープフルーツ(ジュース) [16.7.1参照] | 本剤の副作用が増強されるおそれがあるので、本剤の減量を考慮するとともに、患者の状態を慎重に観察し、副作用の発現に十分注意すること。 | 左記薬剤等との併用により本剤の代謝が阻害され、本剤の血中濃度が上昇するおそれがある。 |
| CYP3A誘導剤 リファンピシン デキサメタゾン カルバマゼピン 等 セイヨウオトギリソウ(St.John's Wort、セント・ジョーンズ・ワート)含有食品 [16.7.2参照] | 本剤の効果が減弱するおそれがあるので、CYP3A誘導作用のない薬剤への代替を考慮すること。 | 左記薬剤等との併用により本剤の代謝が促進され、本剤の血中濃度が低下するおそれがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 消化管穿孔(0.9%)、瘻孔(0.7%)[9.1.2参照]
11.1.2 出血(7.7%)
11.1.3 血栓塞栓症(4.1%)
肺塞栓症(1.7%)、深部静脈血栓症(0.7%)、虚血性脳卒中(0.2%)等の血栓塞栓症があらわれることがある。[9.1.3参照]
11.1.4 高血圧(32.6%)
11.1.5 可逆性後白質脳症症候群(頻度不明)
痙攣、頭痛、錯乱、視覚障害、皮質盲等が認められた場合には投与を中止し、血圧のコントロールを含め、適切な処置を行うこと。
11.1.6 顎骨壊死(0.2%)[8.6参照]
11.1.7 膵炎(0.6%)[8.4参照]
11.1.8 腎障害(13.6%)
急性腎障害(1.3%)、蛋白尿(8.7%)等の腎障害があらわれることがある。[8.2参照]
11.1.9 肝不全(0.1%)、肝機能障害(34.8%)
肝不全、AST、ALT等の上昇を伴う肝機能障害、肝性脳症(0.7%)、胆汁うっ滞性肝炎(0.1%)等があらわれることがある。[8.3参照]
11.1.10 骨髄抑制
貧血(9.2%)、好中球減少(8.1%)、血小板減少(13.3%)、リンパ球減少(2.5%)等の骨髄抑制があらわれることがある。[8.7参照]
11.1.11 虚血性心疾患(0.1%)、不整脈(1.3%)、心不全(0.2%)
11.1.12 横紋筋融解症(0.2%)
筋肉痛、脱力感、CK上昇、血中及び尿中ミオグロビン上昇等が認められた場合には、投与を中止すること。また、横紋筋融解症による急性腎障害の発症に注意すること。
11.1.13 間質性肺疾患(1.4%)
11.1.14 手足症候群(44.3%)
11.1.15 創傷治癒遅延(0.6%)
11.1.16 重度の下痢(8.7%)
11.1.17 動脈解離(頻度不明)
大動脈解離を含む動脈解離があらわれることがある1)。
11.2 その他の副作用
| 10%以上 | 1〜10%未満 | 1%未満 | |
| 消化器 | 下痢(57.2%)、食欲減退、悪心、口内炎、嘔吐、腹痛 | 消化不良、便秘 | 舌痛 |
| 皮膚 | 発疹 | 皮膚乾燥、脱毛、ざ瘡様皮膚炎、毛髪変色、紅斑、過角化 | 皮膚血管炎 |
| その他 | 疲労、味覚異常、体重減少、甲状腺機能低下症、発声障害、粘膜の炎症、無力症 | 浮動性めまい、頭痛、筋痙縮、四肢痛、関節痛、脱水、末梢性ニューロパチー、嚥下障害、低マグネシウム血症、低リン酸血症、低カリウム血症、低カルシウム血症、低アルブミン血症、アミラーゼ上昇、リパーゼ上昇 | 膿瘍 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.2 非臨床試験に基づく情報
15.2.1 ラット2年間経口投与がん原性試験では、最大臨床用量(60mg/日)におけるカボザンチニブの曝露量(AUC)の0.08倍の曝露量で副腎髄質褐色細胞腫の発現頻度の上昇が認められた。
15.2.2 反復投与毒性試験(マウス、ラット及びイヌ)では、生殖器組織への影響が認められており、ラットの受胎能試験では、最大臨床用量(60mg/日)におけるカボザンチニブの曝露量(AUC)の1.4倍(雄)又は0.5倍(雌)の曝露量で受胎能の低下が認められている。
16. 薬物動態
16.1 血中濃度
16.1.1 単回及び反復投与
日本人固形癌患者に本剤40mg及び60mgを1日1回反復経口投与したときのカボザンチニブの薬物動態パラメータ及び血漿中濃度推移は以下のとおりであった。また、本剤60mgを1日1回反復経口投与した際の投与19日目におけるカボザンチニブの蓄積率の幾何平均値は5.07であった2)。
| 用量(mg) | Day | N | tmax(時間) | Cmax(ng/mL) | AUC24h(h*ng/mL) |
| 40 | 1 | 3 | 4(2,4) | 251(8.3) | 4158(17.6) |
| 19 | 3 | 2(2,2) | 1327(36.8) | 20031(25.7) | |
| 60 | 1 | 26 | 4(1,24) | 459(39.2) | 7002(26.2) |
| 19 | 26 | 2(0,24) | 1969(28.6) | 35494(33.3) |
血漿中濃度−時間プロファイル
16.2 吸収
16.2.1 食事の影響
16.3 分布
16.3.1 蛋白結合率
16.4 代謝
16.4.1 薬物代謝
16.5 排泄
16.5.1 排泄率
健康成人8例に14C標識したカボザンチニブ140mg注)を単回経口投与したとき、投与48日後までに総投与放射能の約81%が回収された(糞中54%、尿中27%)8)(外国人データ)。
注)本剤の承認用量は、単独投与の場合は1回60mg、ニボルマブ(遺伝子組換え)との併用投与の場合は1回40mgである。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
本剤(カプセル剤)60mgを軽度腎機能障害患者〔eGFR(mL/min/1.73m2)が60以上89以下〕10例又は中等度腎機能障害患者〔eGFR(mL/min/1.73m2)が30以上59以下〕10例に投与したとき、腎機能正常被験者10例と比較して、Cmaxの幾何平均値はそれぞれ19%及び3%増加し、AUCinfの幾何平均値はそれぞれ30%及び6%増加した。なお、重度腎機能障害患者〔eGFR(mL/min/1.73m2)が29以下〕に与える影響については検討していない9)(外国人データ)。
16.6.2 肝機能障害患者
16.7 薬物相互作用
16.7.1 ケトコナゾール
16.7.2 リファンピシン
16.7.3 その他
癌患者32例を対象に本剤(カプセル剤)140mg注)を1日1回21日間反復経口投与時にロシグリタゾン4mgを併用投与したとき、ロシグリタゾンのCmax及びAUCinfに対する影響は認められなかった10)(外国人データ)。
健康成人22例を対象にプロトンポンプ阻害剤であるエソメプラゾール40mgを1日1回6日間反復経口投与時に本剤100mg注)を併用投与したとき、カボザンチニブのCmax及びAUCinfに対する影響は認められなかった10)(外国人データ)。
in vitro試験において、CYP3A4の誘導作用及びP-糖蛋白質に対する阻害作用(IC50:7.0μmol/L)が認められた11)。
注)本剤の承認用量は、単独投与の場合は1回60mg、ニボルマブ(遺伝子組換え)との併用投与の場合は1回40mgである。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<根治切除不能又は転移性の腎細胞癌>
17.1.1 国内第II相試験(Cabozantinib-2001試験)
血管新生阻害剤(スニチニブ、パゾパニブ等)による治療後に増悪した、根治切除不能又は転移性の淡明細胞型腎細胞癌患者(35例)を対象として、本剤60mgを1日1回投与した結果注1)、主要評価項目である奏効率(完全奏効又は部分奏効)は20%(90%CI:9.783〜34.305)であった12)。
本剤の投与を受けた安全性評価対象35例のうち、34例(97%)に副作用が認められた。主な副作用は、手掌・足底発赤知覚不全症候群63%(22例)、下痢54%(19例)、高血圧、蛋白尿〔以上40%(それぞれ14例)〕、肝機能異常、口内炎〔以上34%(それぞれ12例)〕、味覚異常31%(11例)、AST増加、食欲減退〔以上26%(それぞれ9例〕及びALT増加20%(7例)であった。[5.2参照]
本剤の投与を受けた安全性評価対象35例のうち、34例(97%)に副作用が認められた。主な副作用は、手掌・足底発赤知覚不全症候群63%(22例)、下痢54%(19例)、高血圧、蛋白尿〔以上40%(それぞれ14例)〕、肝機能異常、口内炎〔以上34%(それぞれ12例)〕、味覚異常31%(11例)、AST増加、食欲減退〔以上26%(それぞれ9例〕及びALT増加20%(7例)であった。[5.2参照]
注1)データカットオフ日:2018年10月23日
17.1.2 海外第III相試験(METEOR試験)
血管新生阻害剤(スニチニブ、パゾパニブ等)による治療後に増悪した、根治切除不能又は転移性の淡明細胞型腎細胞癌患者(658例)を対象として、本剤60mg(330例)とエベロリムス10mg(328例)を1日1回投与した無作為化比較試験の結果、主要評価項目である無増悪生存期間(PFS)中央値は本剤群で7.4ヵ月、エベロリムス群で3.8ヵ月であり、層別因子で調整したハザード比(HR)は0.59〔95%CI:0.46〜0.76、両側p<0.001(層別ログランク検定)〕であった注2)13)。
Kaplan-Meier無増悪生存曲線(独立画像評価委員会判定、有効性解析対象集団)
本剤群の安全性評価対象331例のうち、322例(97%)に副作用が認められた。本剤群の主な副作用は、下痢70%(231例)、疲労53%(174例)、悪心45%(149例)、手掌・足底発赤知覚不全症候群43%(142例)、食欲減退40%(134例)、高血圧33%(109例)、体重減少27%(90例)、嘔吐24%(79例)、味覚異常23%(76例)、甲状腺機能低下症21%(68例)及び口内炎20%(67例)であった注3)。[5.2参照]
注2)データカットオフ日:2015年5月22日
注3)データカットオフ日:2016年10月2日
17.1.3 海外第II相試験(CABOSUN試験)
化学療法歴のない、根治切除不能又は転移性の淡明細胞型腎細胞癌患者(157例)を対象として、本剤(79例、1日1回60mg投与)とスニチニブ(78例、1日1回50mg4週間投与2週間休薬)の無作為化比較試験の結果、主要評価項目であるPFS中央値は本剤群で8.2ヵ月、スニチニブ群で5.6ヵ月であり、HRは0.66〔95%CI:0.46〜0.95、片側p=0.012(層別ログランク検定)〕であった注4)14)15)。
Kaplan-Meier無増悪生存曲線(治験責任医師判定、ITT集団)
本剤群で安全性評価対象78例のうち、74例(95%)に副作用が認められた。本剤群の主な副作用は、下痢72%(56例)、疲労62%(48例)、AST増加60%(47例)、高血圧56%(44例)、ALT増加54%(42例)、食欲減退45%(35例)、手掌・足底発赤知覚不全症候群42%(33例)、味覚異常41%(32例)、血小板数減少、口内炎〔以上37%(それぞれ29例)〕、悪心、体重減少〔以上31%(それぞれ24例)〕、貧血29%(23例)、消化不良、低リン酸血症〔以上23%(それぞれ18例)〕、甲状腺機能低下症22%(17例)及び血中クレアチニン増加、発声障害、低マグネシウム血症〔以上21%(それぞれ16例)〕であった注5)。[5.2参照]
注4)データカットオフ日:2016年4月11日
注5)データカットオフ日:2016年9月15日
17.1.4 国際共同第III相試験(CA2099ER試験)
化学療法歴のない、根治切除不能又は転移性の淡明細胞型腎細胞癌患者651例(日本人患者46例を含む)を対象とした、本剤(1日1回40mg投与)及びニボルマブ(240mgを2週間間隔投与)の併用投与(323例)とスニチニブ単独投与(1日1回50mgを4週間投与後2週間休薬、328例)の無作為化比較試験の結果注6)、主要評価項目であるPFS中央値は、本剤とニボルマブの併用群で16.6ヵ月、スニチニブ群で8.3ヵ月であり、層別因子で調整したHRは0.51〔95%CI:0.41〜0.64、両側p<0.0001(層別ログランク検定)〕であった16)。
Kaplan-Meier無増悪生存曲線(独立画像評価委員会判定、ITT集団)
本剤とニボルマブ併用群で安全性評価対象320例(日本人患者22例を含む)のうち、309例(97%)に副作用が認められた。本剤とニボルマブ併用群の主な副作用は、下痢57%(182例)、手掌・足底発赤知覚不全症候群38%(122例)、甲状腺機能低下症33%(107例)、高血圧30%(97例)、疲労27%(86例)、ALT増加25%(80例)、AST増加23%(75例)、味覚不全22%(69例)、悪心21%(68例)及び食欲減退20%(65例)であった。[5.2参照]
注6)データカットオフ日:2020年2月12日
<がん化学療法後に増悪した切除不能な肝細胞癌>
17.1.5 国内第II相試験(Cabozantinib-2003試験)
全身化学療法歴を有するChild-Pugh分類Aの切除不能な肝細胞癌患者注7)(34例)を対象として、本剤60mgを1日1回投与した結果注8)、ソラフェニブによる治療歴を有する患者(20例)における主要評価項目である24週時の無増悪生存率は、59.8%(90%CI:36.1〜77.2)であった17)。
本剤の投与を受けた安全性評価対象34例のうち、全例(100%)に副作用が認められた。主な副作用は、手掌・足底発赤知覚不全症候群76%(26例)、下痢56%(19例)、高血圧47%(16例)、食欲減退44%(15例)、血小板数減少38%(13例)、AST増加35%(12例)、ALT増加、甲状腺機能低下症〔以上29%(それぞれ10例)〕、発声障害、倦怠感〔以上24%(それぞれ8例)〕、味覚異常、疲労、好中球数減少、蛋白尿、発疹〔以上21%(それぞれ7例)〕であった。[5.5参照]
注7)局所療法(経皮的エタノール注入療法、ラジオ波焼灼療法、マイクロ波凝固療法、肝動脈塞栓療法/肝動脈化学塞栓療法、放射線療法等)の適応となる患者は除外された。
注8)データカットオフ日:2019年7月23日
17.1.6 海外第III相試験(CELESTIAL試験)
ソラフェニブによる治療歴を有し、全身化学療法後に増悪したChild-Pugh分類Aの切除不能な肝細胞癌患者注9)(707例)を対象として、本剤60mg(470例)とプラセボ(237例)を1日1回投与した無作為化比較試験の結果注10)、主要評価項目である全生存期間の中央値は、本剤群で10.2ヵ月、プラセボ群で8.0ヵ月であり、層別因子で調整したHRは0.76〔95%CI:0.63〜0.92、両側p=0.0049(層別ログランク検定)〕であった18)。
Kaplan-Meier全生存曲線(ITT集団)
本剤群の安全性評価対象467例のうち、439例(94%)に副作用が認められた。本剤群の主な副作用は、下痢、手掌・足底発赤知覚不全症候群〔以上46%(それぞれ216例)〕、疲労38%(178例)、食欲減退37%(174例)、高血圧27%(128例)及び悪心25%(115例)であった。[5.5参照]
注9)局所療法(経皮的エタノール注入療法、ラジオ波焼灼療法、マイクロ波凝固療法、肝動脈塞栓療法/肝動脈化学塞栓療法、放射線療法等)の適応となる患者は除外された。
注10)データカットオフ日:2017年6月1日
18. 薬効薬理
18.1 作用機序
カボザンチニブは、血管内皮細胞増殖因子受容体2(VEGFR2)、肝細胞増殖因子受容体(MET)、AXL等のキナーゼに対する阻害作用を有する低分子化合物である。カボザンチニブは、VEGFR2等を介したシグナル伝達を阻害することにより、腫瘍増殖抑制作用を示すと考えられている19)。
19. 有効成分に関する理化学的知見
19.1. カボザンチニブリンゴ酸塩
21. 承認条件
医薬品リスク管理計画を策定の上、適切に実施すること。
22. 包装
<カボメティクス錠20mg>
PTP 30錠(10錠×3)
<カボメティクス錠60mg>
PTP 10錠(10錠×1)
23. 主要文献
- NDBを用いた調査結果の概要(VEGF/VEGFR阻害作用を有する薬剤の動脈解離に関するリスク評価), (https://www.pmda.go.jp/files/000266521.pdf)
- カボザンチニブリンゴ酸塩の国内第I相試験成績(2020年3月25日承認、CTD 2.7.2.2)
- Nguyen L et al., J Clin Pharmacol., 55 (11), 1293-1302, (2015)
- カボザンチニブリンゴ酸塩の非臨床薬物動態試験成績(血漿蛋白結合率)(2020年3月25日承認、CTD 2.6.4.4)
- カボザンチニブリンゴ酸塩の腎機能障害患者における薬物動態試験成績(2020年3月25日承認、CTD 2.7.2.2)
- カボザンチニブリンゴ酸塩の肝機能障害患者における薬物動態試験成績(2020年3月25日承認、CTD 2.7.2.2)
- カボザンチニブリンゴ酸塩の非臨床薬物動態試験成績(代謝、in vitro)(2020年3月25日承認、CTD 2.6.4.5)
- Lacy S.et al., Drug Metab Dispos., 43 (8), 1190-1207, (2015)
- Nguyen L.et al., J Clin Pharmacol., 56 (9), 1130-1140, (2016)
- Nguyen L.et al., J Clin Pharmacol., 55 (9), 1012-1023, (2015)
- カボザンチニブリンゴ酸塩の非臨床薬物動態試験成績(薬物間相互作用、in vitro)(2020年3月25日承認、CTD 2.6.4.7)
- カボザンチニブリンゴ酸塩の国内第II相試験成績[1](2020年3月25日承認、CTD 2.7.3.3、2.7.4.1、2.7.6.14)
- カボザンチニブリンゴ酸塩の海外第III相試験成績[1](2020年3月25日承認、CTD 2.7.3.3、2.7.4.1、2.7.6.12)
- カボザンチニブリンゴ酸塩の海外第II相試験成績(2020年3月25日承認、CTD 2.7.3.3、2.7.4.1、2.7.6.13)
- Choueiri TK et al., J Clin Oncol., 35 (6), 591-597, (2017)
- カボザンチニブリンゴ酸塩の国際共同第III相試験成績(社内資料)
- カボザンチニブリンゴ酸塩の国内第II相試験成績[2](社内資料)
- カボザンチニブリンゴ酸塩の海外第III相試験成績[2](社内資料)
- カボザンチニブリンゴ酸塩の薬効薬理試験成績(2020年3月25日承認、CTD 2.6.2.2)
24. 文献請求先及び問い合わせ先
文献請求先
武田薬品工業株式会社
くすり相談室
〒103-8668
東京都中央区日本橋本町二丁目1番1号
電話:フリーダイヤル 0120-566-587 受付時間 9:00〜17:30(土日祝日・弊社休業日を除く)
製品情報問い合わせ先
武田薬品工業株式会社
くすり相談室
〒103-8668
東京都中央区日本橋本町二丁目1番1号
電話:フリーダイヤル 0120-566-587 受付時間 9:00〜17:30(土日祝日・弊社休業日を除く)
26. 製造販売業者等
26.1 製造販売元
武田薬品工業株式会社
〒540-8645
大阪市中央区道修町四丁目1番1号
26.2 提携
Exelixis,Inc.
1851 Harbor Bay Parkway,Alameda,CA 94502 USA