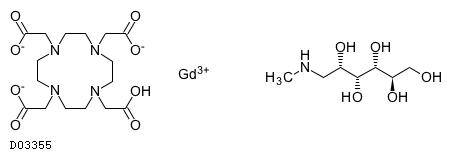医薬品情報
| 総称名 | ガドテル酸メグルミン |
|---|---|
| 一般名 | ガドテル酸メグルミン |
| 欧文一般名 | meglumine gadoterate |
| 製剤名 | ガドテル酸メグルミン注射液 |
| 薬効分類名 | 環状型MRI用造影剤 |
| 薬効分類番号 | 7290 |
| ATCコード | V08CA02 |
| KEGG DRUG |
D03355
ガドテル酸メグルミン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年1月 改訂(第1版)

|
1.警告 2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 11.副作用 12.臨床検査結果に及ぼす影響 14.適用上の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ガドテル酸メグルミン静注38%シリンジ10mL「GE」 (後発品) | GADOTERATE MEGLUMINE inj.38% Syringe | GEヘルスケアファーマ | 7290411G1049 | 1969円/筒 | 処方箋医薬品注) |
| ガドテル酸メグルミン静注38%シリンジ11mL「GE」 (後発品) | GADOTERATE MEGLUMINE inj.38% Syringe | GEヘルスケアファーマ | 7290411G4030 | 2230円/筒 | 処方箋医薬品注) |
| ガドテル酸メグルミン静注38%シリンジ13mL「GE」 (後発品) | GADOTERATE MEGLUMINE inj.38% Syringe | GEヘルスケアファーマ | 7290411G5036 | 2407円/筒 | 処方箋医薬品注) |
| ガドテル酸メグルミン静注38%シリンジ15mL「GE」 (後発品) | GADOTERATE MEGLUMINE inj.38% Syringe | GEヘルスケアファーマ | 7290411G2045 | 2707円/筒 | 処方箋医薬品注) |
| ガドテル酸メグルミン静注38%シリンジ20mL「GE」 (後発品) | GADOTERATE MEGLUMINE inj.38% Syringe | GEヘルスケアファーマ | 7290411G3041 | 3280円/筒 | 処方箋医薬品注) |
1. 警告
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分又はガドリニウム造影剤に対し過敏症の既往歴のある患者
4. 効能または効果
磁気共鳴コンピューター断層撮影における下記造影
脳・脊髄造影
躯幹部・四肢造影
5. 効能または効果に関連する注意
ガドリニウム造影剤を複数回投与した患者において、非造影T1強調MR画像上、小脳歯状核、淡蒼球等に高信号が認められたとの報告や脳の剖検組織からガドリニウムが検出されたとの報告があるので、ガドリニウム造影剤を用いた検査の必要性を慎重に判断すること。
6. 用法及び用量
通常、成人には本剤0.2mL/kgを静脈内注射する。腎臓を対象とする場合は、0.1mL/kgを静脈内注射するが、必要に応じて、0.2mL/kgまで増量することができる。
8. 重要な基本的注意
8.2 ショック、アナフィラキシー等が発現することがあるので、本剤の投与に際しては必ず救急処置の準備を行うこと。
また、類薬において投与開始より1時間〜数日後にも遅発性副作用(発熱、発疹、悪心、血圧低下、呼吸困難等)があらわれるとの報告があるので、投与後も患者の状態を十分に観察すること。患者に対して、上記の症状があらわれた場合には速やかに主治医等に連絡するよう指導するなど適切な対応をとること。[11.1.1参照]
また、類薬において投与開始より1時間〜数日後にも遅発性副作用(発熱、発疹、悪心、血圧低下、呼吸困難等)があらわれるとの報告があるので、投与後も患者の状態を十分に観察すること。患者に対して、上記の症状があらわれた場合には速やかに主治医等に連絡するよう指導するなど適切な対応をとること。[11.1.1参照]
8.3 通常、コントラストは本剤投与直後から約45分後まで持続する。追加投与によって有効性が向上するとは限らないので追加投与しないこと。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 一般状態の極度に悪い患者
診断上やむを得ないと判断される場合を除き、投与しないこと。
9.1.2 気管支喘息のある患者
9.1.3 アレルギー性鼻炎、発疹、蕁麻疹等を起こしやすいアレルギー体質を有する患者[8.1参照]
9.1.4 両親、兄弟に気管支喘息、アレルギー性鼻炎、発疹、蕁麻疹等を起こしやすいアレルギー体質を有する患者[8.1参照]
9.1.5 薬物過敏症の既往歴のある患者[8.1参照]
9.1.6 既往歴を含めて、痙攣、てんかん及びその素質のある患者
類薬で痙攣が報告されている。
9.2 腎機能障害患者
9.2.1 重篤な腎障害のある患者
9.2.2 長期透析が行われている終末期腎障害、eGFR(estimated glomerular filtration rate:推算糸球体ろ過値)が30mL/min/1.73m2未満の慢性腎障害、急性腎障害の患者(重篤な腎障害のある患者を除く)
9.2.3 腎機能障害のある患者又は腎機能が低下しているおそれのある患者(重篤な腎障害のある患者を除く)
9.3 肝機能障害患者
9.3.1 重篤な肝障害のある患者
診断上やむを得ないと判断される場合を除き、投与しないこと。肝機能に影響を及ぼすおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、診断上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
診断上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物試験(ヤギ静脈内投与)で乳汁中に移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を十分に観察しながら慎重に投与すること。本剤は主として腎臓から排泄されるが、腎機能が低下していることが多いため、高い血中濃度を維持するおそれがある。
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
11.1.2 腎性全身性線維症(Nephrogenic Systemic Fibrosis、NSF)(頻度不明)
11.2 その他の副作用
| 0.1〜0.5%未満 | 頻度不明 | |
| 過敏症 | 発疹、そう痒症 | 顔面浮腫、血管浮腫、潮紅、紅斑、眼瞼浮腫、蕁麻疹 |
| 循環器 | 血圧上昇、血圧低下 | |
| 呼吸器 | 呼吸困難、口腔咽頭不快感、鼻閉、咳嗽、くしゃみ | |
| 消化器 | 悪心、嘔吐 | |
| 精神神経系 | 頭痛 | 浮動性めまい |
| 眼 | 眼の異物感 | 眼充血、眼そう痒症 |
| その他 | 熱感、味覚異常、胸部不快感 | 感覚鈍麻、冷感、多汗症、異常感 |
12. 臨床検査結果に及ぼす影響
本剤は血清鉄の測定値に影響を与えることがある。
14. 適用上の注意
14.1 薬剤投与時の注意
14.1.1 髄腔内投与は行わないこと。[1.1参照]
14.1.2 注射に際しては血管外に漏出しないよう十分注意する。血管外に漏出した場合には、注射部疼痛や腫脹があらわれることがある。
14.2 薬剤投与後の注意
1回の検査にのみ使用し、余剰の溶液は廃棄すること。
16. 薬物動態
16.1 血中濃度
健康成人男性各5例に、ガドテル酸メグルミン0.1mL/kg(0.05mmol/kg)、0.2mL/kg(0.10mmol/kg)を静脈内投与したところ、血中からの分布相半減期及び消失相半減期はそれぞれ5.0〜5.9分、72.0〜72.6分であった1)。
血漿中Gd濃度の推移
| 投与量 | ||
| 0.05mmol/kg | 0.10mmol/kg | |
| t1/2α(min) | 5.0±1.2 | 5.9±3.2 |
| t1/2β(hr) | 1.20±0.19 | 1.21±0.16 |
| AUC0-∞(nmol・hr/mL) | 530.2±97.9 | 994.8±105.7 |
16.5 排泄
健康成人男性各5例にガドテル酸メグルミン0.1mL/kg(0.05mmol/kg)、0.2mL/kg(0.10mmol/kg)を静脈内単回投与したところ、6時間後までに投与量の89%以上が、24時間後までに95%以上が尿中に排泄された。HPLC法を用いた尿中代謝物の分析において未変化体のみが検出されたことから、ガドテル酸メグルミンは静脈内投与後に代謝されず未変化体のまま尿中に排泄されることが示唆された1)。
尿中累積排泄率
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験
(1)比較臨床試験
第II相臨床試験2)で臨床至適投与量として妥当とされた0.1mmol/kg投与におけるガドテル酸メグルミンの造影効果、安全性及び臨床的有用性を客観的に検討することを目的とした3)。なお、腎臓を撮像部位とした場合の用量は、比較対照薬の許可用量である0.05mmol/kgとした。ガドテル酸メグルミン投与群の総合的有効性における解析対象146例の有効率は92.5%であった。また、腎臓を撮像部位とした場合の有効率は100%であった。
ガドテル酸メグルミン投与群の概括安全度の解析対象152例において、2例(1.3%)に3件の副作用が発現した。内訳は嘔気、発疹、そう痒感が各1件認められたがいずれも軽度であった。臨床検査値の異常変動は、ガドテル酸メグルミン投与群では血清鉄9例など16例(21件)に認められた。
ガドテル酸メグルミン投与群の概括安全度の解析対象152例において、2例(1.3%)に3件の副作用が発現した。内訳は嘔気、発疹、そう痒感が各1件認められたがいずれも軽度であった。臨床検査値の異常変動は、ガドテル酸メグルミン投与群では血清鉄9例など16例(21件)に認められた。
| 領域 | 投与群 | 計 | 著効 | 有効 | やや有効 | 無効 | 判定不能 | 有効率※1(%) (補正値)※2 | |
| 全解析対象 | 脳・脊髄 | ガドテル酸メグルミン群 | 38 | 16 | 18 | 4 | 0 | 0 | 89.5 |
| 心臓・胸部 | ガドテル酸メグルミン群 | 32 | 10 | 17 | 4 | 1 | 0 | 84.4 | |
| 腹部・四肢 | ガドテル酸メグルミン群 | 76 | 47 | 27 | 2 | 0 | 0 | 97.4 | |
| 合計 | ガドテル酸メグルミン群 | 146 | 73 | 62 | 10 | 1 | 0 | 92.5 (92.4) | |
| ※3 | 合計 | ガドテル酸メグルミン群 | 135 | 68 | 58 | 8 | 1 | 0 | 93.3 (93.3) |
| ※4 | 合計 | ガドテル酸メグルミン群 | 130 | 62 | 57 | 10 | 1 | 0 | 91.5 (91.5) |
| ※5 | 合計 | ガドテル酸メグルミン群 | 122 | 58 | 55 | 8 | 1 | 0 | 92.6 (92.6) |
(2)一般臨床試験
第II相臨床試験2)で臨床至適投与量として妥当とされた0.1mmol/kg投与におけるガドテル酸メグルミンの造影効果、安全性及び臨床的有用性をさらに多くの対象で検討することを目的とした4)5)6)7)8)9)10)11)12)13)14)15)16)17)18)19)20)21)22)。424例を対象として、T1強調画像もしくはDynamic撮影においてガドテル酸メグルミン0.1mmol/kgを投与した。総合的有効性における解析対象例数402例において、有効率は88.8%であった。概括安全度の解析対象例数402例において、5例(1.2%)9件に副作用が発現した。内訳は頭痛、熱感、発疹各2件、眼の異物感、嘔気、嘔吐が各1件であった。いずれも軽度で、投薬により消失した頭痛1例を除いて、処置なく自然回復した。臨床検査値の異常変動は、24例31項目に認められ、血清鉄11件、フェリチン1件等であり、臨床的に特に問題はなかった。
18. 薬効薬理
18.1 測定法
本剤はその構造にキレート化したGdイオンを有しており常磁性を示す。MRI検査において本剤を投与すると、Gdイオンの強い磁気モーメントにより組織中の水プロトンの緩和時間が短縮し、MR画像上で組織及び病変部のコントラスト増強効果が得られる。
19. 有効成分に関する理化学的知見
19.1. ガドテル酸メグルミン
22. 包装
ガドテル酸メグルミン静注38%シリンジ10mL「GE」
10本
ガドテル酸メグルミン静注38%シリンジ11mL「GE」
10本
ガドテル酸メグルミン静注38%シリンジ13mL「GE」
10本
ガドテル酸メグルミン静注38%シリンジ15mL「GE」
10本
ガドテル酸メグルミン静注38%シリンジ20mL「GE」
10本
23. 主要文献
- 松山真記子ほか, 診療と新薬, 31 (3), 513-521, (1994)
- 谷本伸弘ほか, 診療と新薬, 33 (4), 571-590, (1996)
- 谷本伸弘ほか, 診療と新薬, 33 (9), 1367-1389, (1996)
- 秋葉英成ほか, 診療と新薬, 33 (4), 591-601, (1996)
- 伊藤直記ほか, 診療と新薬, 33 (4), 715-726, (1996)
- 信澤宏ほか, 診療と新薬, 33 (4), 695-704, (1996)
- 堀地悌ほか, 診療と新薬, 33 (4), 603-613, (1996)
- 深津博ほか, 診療と新薬, 33 (4), 615-624, (1996)
- 河村泰孝ほか, 診療と新薬, 33 (4), 625-635, (1996)
- 板金宏ほか, 診療と新薬, 33 (4), 657-665, (1996)
- 北野悟ほか, 診療と新薬, 33 (4), 763-770, (1996)
- 杉原修司ほか, 診療と新薬, 33 (4), 677-686, (1996)
- 興梠征典ほか, 診療と新薬, 33 (4), 637-648, (1996)
- 村上卓道ほか, 診療と新薬, 33 (4), 727-741, (1996)
- 瀬尾善宣ほか, 診療と新薬, 33 (4), 649-655, (1996)
- 五味達哉ほか, 診療と新薬, 33 (4), 771-775, (1996)
- 白川久美子ほか, 診療と新薬, 33 (4), 687-694, (1996)
- 伊藤亨ほか, 診療と新薬, 33 (4), 705-714, (1996)
- 揖靖ほか, 診療と新薬, 33 (4), 777-784, (1996)
- 三木均ほか, 診療と新薬, 33 (4), 743-756, (1996)
- 廣橋伸治ほか, 診療と新薬, 33 (4), 757-761, (1996)
- 蒲田敏文ほか, 診療と新薬, 33 (4), 667-676, (1996)
24. 文献請求先及び問い合わせ先
文献請求先
GEヘルスケアファーマ株式会社
メディカルインフォメーションセンター
〒108-0074
東京都港区高輪4-10-18
電話:0120-241-454
製品情報問い合わせ先
GEヘルスケアファーマ株式会社
メディカルインフォメーションセンター
〒108-0074
東京都港区高輪4-10-18
電話:0120-241-454
26. 製造販売業者等
26.1 製造販売元
GEヘルスケアファーマ株式会社
東京都港区高輪4-10-18