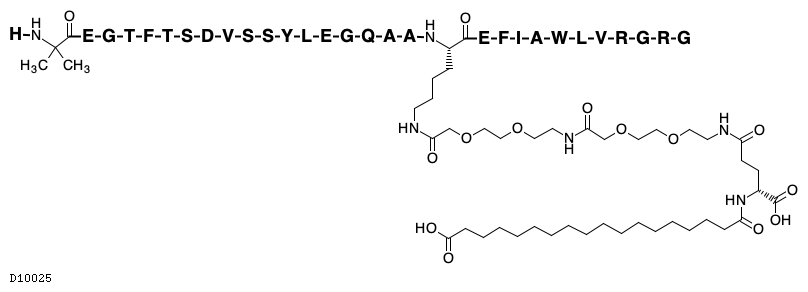医薬品情報
| 総称名 | リベルサス |
|---|---|
| 一般名 | セマグルチド(遺伝子組換え) |
| 欧文一般名 | Semaglutide(Genetical Recombination) |
| 製剤名 | セマグルチド(遺伝子組換え) |
| 薬効分類名 | 2型糖尿病治療剤 経口GLP-1受容体作動薬 |
| 薬効分類番号 | 2499 |
| ATCコード | A10BJ06 |
| KEGG DRUG |
D10025
セマグルチド
|
| KEGG DGROUP |
DG01493
GLP-1受容体作動薬
DG02044
血糖降下薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年7月 改訂(第5版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| リベルサス錠3mg | Rybelsus tablets | ノボノルディスクファーマ | 2499014F1021 | 143.1円/錠 | 劇薬, 処方箋医薬品注) |
| リベルサス錠7mg | Rybelsus tablets | ノボノルディスクファーマ | 2499014F2028 | 333.8円/錠 | 劇薬, 処方箋医薬品注) |
| リベルサス錠14mg | Rybelsus tablets | ノボノルディスクファーマ | 2499014F3024 | 500.7円/錠 | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 糖尿病性ケトアシドーシス、糖尿病性昏睡又は前昏睡、1型糖尿病の患者[インスリン製剤による速やかな治療が必須となるので、本剤を投与すべきでない。]
2.3 重症感染症、手術等の緊急の場合[インスリン製剤による血糖管理が望まれるので、本剤の投与は適さない。]
4. 効能または効果
5. 効能または効果に関連する注意
本剤の適用は、あらかじめ糖尿病治療の基本である食事療法、運動療法を十分に行ったうえで効果が不十分な場合に限り考慮すること。
6. 用法及び用量
通常、成人には、セマグルチド(遺伝子組換え)として1日1回7mgを維持用量とし経口投与する。ただし、1日1回3mgから開始し、4週間以上投与した後、1日1回7mgに増量する。なお、患者の状態に応じて適宜増減するが、1日1回7mgを4週間以上投与しても効果不十分な場合には、1日1回14mgに増量することができる。
7. 用法及び用量に関連する注意
7.1 本剤の吸収は胃の内容物により低下することから、本剤は、1日のうちの最初の食事又は飲水の前に、空腹の状態でコップ約半分の水(約120mL以下)とともに3mg錠、7mg錠又は14mg錠を1錠服用すること。また、服用時及び服用後少なくとも30分は、飲食及び他の薬剤の経口摂取を避けること。分割・粉砕及びかみ砕いて服用してはならない。[16.2.1-16.2.3参照]
7.2 本剤14mgを投与する際には、本剤の7mg錠を2錠投与することは避けること。[16.2.1参照]
7.3 投与を忘れた場合はその日は投与せず、翌日投与すること。
8. 重要な基本的注意
8.1 投与する場合には、血糖、尿糖を定期的に検査し、薬剤の効果を確かめ、3〜4ヵ月間投与して効果が不十分な場合には、より適切と考えられる治療への変更を考慮すること。
8.2 本剤の消失半減期は長く、本剤中止後も効果が持続する可能性があるため、血糖値の変動や副作用予防、副作用発現時の処置について十分留意すること。[16.1参照]
8.4 低血糖症状を起こすことがあるので、高所作業、自動車の運転等に従事している患者に投与するときには注意すること。[11.1.1参照]
8.5 急激な血糖コントロールの改善に伴い、糖尿病網膜症の顕在化又は増悪があらわれることがあるので、注意すること。
8.8 下痢、嘔吐から脱水を続発し、急性腎障害に至るおそれがあるので、患者の状態に注意すること。
8.9 本剤投与中は、甲状腺関連の症候の有無を確認し、異常が認められた場合には、専門医を受診するよう指導すること。[15.2.1参照]
8.10 胆石症、胆嚢炎、胆管炎又は胆汁うっ滞性黄疸が発現するおそれがあるので、腹痛等の腹部症状がみられた場合には、必要に応じて画像検査等による原因精査を考慮するなど、適切に対応すること。[11.1.3参照]
8.11 本剤はセマグルチド(遺伝子組換え)を含有しているため、ウゴービ等他のセマグルチド(遺伝子組換え)含有製剤と併用しないこと。
8.12 本剤とDPP-4阻害剤はいずれもGLP-1受容体を介した血糖降下作用を有している。両剤を併用した際の臨床試験成績はなく、有効性及び安全性は確認されていない。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.2 重度胃不全麻痺等、重度の胃腸障害のある患者
十分な使用経験がなく、胃腸障害の症状が悪化するおそれがある。
9.1.3 低血糖を起こすおそれがある以下の患者又は状態
9.1.4 胃摘出術を受けた患者
他剤での治療を考慮すること。本剤は主に胃において吸収されるため、有効性が減弱する可能性がある。[16.2.1参照]
9.1.5 腹部手術の既往又はイレウスの既往のある患者
腸閉塞を含むイレウスを起こすおそれがある。[11.1.4参照]
9.4 生殖能を有する者
2ヵ月以内に妊娠を予定する女性には本剤を投与せず、インスリンを使用すること。[9.5参照]
9.5 妊婦
9.6 授乳婦
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。一般に生理機能が低下していることが多い。[16.6.3参照]
10. 相互作用
10.2 併用注意
| 糖尿病用薬 ビグアナイド系薬剤 スルホニルウレア剤 速効型インスリン分泌促進剤 α-グルコシダーゼ阻害剤 チアゾリジン系薬剤 DPP-4阻害剤 SGLT2阻害剤 インスリン製剤 等 [11.1.1参照] | 低血糖症の発現に注意すること。特に、インスリン製剤又はスルホニルウレア剤と併用する場合、低血糖のリスクが増加するおそれがあるため、必要に応じ、これらの薬剤の減量を検討すること。 | 血糖降下作用が増強される。 |
| レボチロキシン製剤 [16.7参照] | 本剤との併用時に、レボチロキシン単回併用後のチロキシン総曝露量(AUC、内因性値で補正)が33%増大したとの報告がある。 併用時には甲状腺パラメータのモニタリングを検討すること。 | レボチロキシンの曝露量の増加は、セマグルチドによる胃内容排出の遅延によると考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 低血糖(頻度不明)
11.1.2 急性膵炎(0.1%)
11.1.3 胆嚢炎、胆管炎、胆汁うっ滞性黄疸(いずれも頻度不明)[8.10参照]
11.1.4 イレウス(頻度不明)
腸閉塞を含むイレウスを起こすおそれがある。高度の便秘、腹部膨満、持続する腹痛、嘔吐等の異常が認められた場合には投与を中止し、適切な処置を行うこと。[9.1.5参照]
11.2 その他の副作用
| 5%以上 | 1〜5%未満 | 0.5〜1%未満 | 頻度不明 | |
| 免疫系障害 | 過敏症(発疹、じん麻疹等) | |||
| 代謝及び栄養障害 | 食欲減退 | |||
| 神経系障害 | 頭痛 | 浮動性めまい、味覚異常 | ||
| 眼障害 | 糖尿病網膜症 | |||
| 心臓障害 | 心拍数増加注1 | |||
| 胃腸障害 | 悪心、下痢 | 便秘、嘔吐、腹部不快感、腹痛、消化不良、上腹部痛、腹部膨満、胃食道逆流性疾患 | 鼓腸、胃炎、おくび | 胃排出遅延 |
| 肝胆道系障害 | 胆石症 | |||
| 全身障害及び投与部位状態 | 疲労、無力症 | |||
| 臨床検査注2 | リパーゼ増加 | 体重減少、血中クレアチンホスホキナーゼ増加、アミラーゼ増加 |
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
14.1.2 本剤は吸湿性が強いため、服用直前にPTPシートから取り出して服用するよう指導すること。
14.1.3 本剤は吸湿性が強く、PTPシートで防湿しているため、原則としてミシン目以外の場所で切り離さないこと。やむを得ず切り離す場合には、PTPシートのポケット部分を破損しないようにすること。
15. その他の注意
15.2 非臨床試験に基づく情報
15.2.1 マウス及びラットを用いたセマグルチドのがん原性試験
15.2.2 サルカプロザートナトリウムの非臨床評価
本剤は胃で崩壊・吸収される。吸収は錠剤表面の周辺部に限定される。サルカプロザートナトリウムによる局所でのpH緩衝作用により、セマグルチドの急速な酵素的分解を防ぐことができる8)。
マウス、ラット及びサルにおける反復投与毒性試験において、最大臨床用量でのCmax(非結合型)の276倍を超える用量を投与した場合に、嗜眠、呼吸異常、運動失調、異常姿勢、活動性の低下、身体緊張の低下、反射の低下等の一般状態変化又は死亡が認められている9)。
授乳ラットでサルカプロザートナトリウム又は代謝物の乳汁への移行が報告されている10)。
ラットでサルカプロザートナトリウムの胎盤通過性が認められ、胎児組織に達することが報告されている10)。ラットにおける生殖発生毒性試験からは、新生児の発達に対する影響は認められていない9)。[9.5、9.6参照]
マウス、ラット及びサルにおける反復投与毒性試験において、最大臨床用量でのCmax(非結合型)の276倍を超える用量を投与した場合に、嗜眠、呼吸異常、運動失調、異常姿勢、活動性の低下、身体緊張の低下、反射の低下等の一般状態変化又は死亡が認められている9)。
授乳ラットでサルカプロザートナトリウム又は代謝物の乳汁への移行が報告されている10)。
ラットでサルカプロザートナトリウムの胎盤通過性が認められ、胎児組織に達することが報告されている10)。ラットにおける生殖発生毒性試験からは、新生児の発達に対する影響は認められていない9)。[9.5、9.6参照]
16. 薬物動態
16.1 血中濃度
反復経口投与後の薬物動態
日本人健康男性被験者(17例)を対象に、1日1回本剤各用量を6時間以上絶食及び2時間以上絶飲後120mLの水で28日間反復投与(投与後30分間絶食)したときのセマグルチドの曝露量(幾何平均)は、以下のとおりであった11)。
| 用量 | Cmax(nmol/L) | AUC0-24h(nmol・h/L) | tmax(h) | t1/2(h) |
| 10mg | 19.05(62.07) | 374.03(59.17) | 1.0[0.5,2.0] | − |
| 20mg | 34.74(46.26) | 675.94(43.84) | 1.0[0.5,6.0] | − |
| 40mg | 61.56(38.52) | 1234.37(36.99) | 1.0[0.0,6.0] | 161.11(9.91) |
日本人健康男性被験者における定常状態での平均セマグルチド濃度の推移
2型糖尿病患者2431例(うち日本人531例)を対象とした母集団薬物動態解析の結果、日本人被験者における本剤3mg、7mg及び14mgの1日1回経口投与後の定常状態の平均セマグルチド濃度は、それぞれ約3.6nmol/L、約8.4nmol/L及び約16.7nmol/Lと推定された。[8.2参照]
16.2 吸収
16.2.1 バイオアベイラビリティ
16.2.2 食事の影響
健康被験者を対象に、1日1回本剤5mgを5日間投与後に本剤10mgを5日間反復経口投与したときのセマグルチドの曝露量は絶食下投与では以下のとおりであった。一方、食後投与した26例中14例ではいずれの時点でも定量下限を超える濃度は認められなかった12)(外国人データ)。[7.1参照]
| 投与群 | 飲水量(mL) | 投与後絶食時間(min) | 例数 | Cmax(nmol/L) | AUC0-24h(nmol・h/L) | tmax(h) |
| 6時間絶食 | 120 | 30 | 26 | 15.53±6.46 | 296.90±124.51 | 1.00[0.50,4.00] |
| 10時間絶食 | 240 | 240 | 26 | 29.18±28.69 | 554.50±546.71 | 1.75[0.50,6.02] |
16.2.3 絶食時間及び飲水量の影響
健康男性被験者を対象に、1日1回本剤10mgを10日間反復経口投与したときのセマグルチドの曝露量は投与後絶食時間、飲水量別では以下のとおりであった13)(外国人データ)。[7.1参照]
| 飲水量(mL) | 投与後絶食時間(min) | 例数 | Cmax(nmol/L) | AUC0-24h(nmol・h/L) | tmax(h) |
| 50 | 15 | 20 | 12.6±10.74a) | 254.9±227.98a) | 0.5[0.5,3.0]b) |
| 30 | 20 | 21.3±10.43 | 422.0±220.57 | 1.0[0.5,4.0] | |
| 60 | 20 | 21.8±11.70b) | 439.6±243.87b) | 1.5[0.5,4.0]b) | |
| 120 | 19 | 33.4±16.87b) | 685.9±333.89b) | 2.3[0.5,12.0]b) | |
| 120 | 15 | 19 | 11.2±7.28 | 221.7±140.06 | 0.5[0.5,6.1] |
| 30 | 20 | 16.8±5.84 | 338.5±114.95 | 1.0[0.5,12.0] | |
| 60 | 20 | 32.5±29.07a) | 634.9±517.68a) | 1.5[0.5,6.0]a) | |
| 120 | 20 | 32.9±15.15b) | 668.6±333.13b) | 2.0[1.0,4.0]b) |
健康男性被験者を対象に、本剤10mgを単回経口投与(投与後4時間絶食、投与2時間後に水200mLを飲水)したときのセマグルチドの曝露量は、飲水量別では以下のとおりであった14)(外国人データ)。
| 飲水量(mL) | 例数 | Cmax(nmol/L) | AUC0-24h(nmol・h/L) | tmax(h) |
| 50 | 24 | 10.5±6.8 | 171.8±114.8 | 1.5[0.5,3.0] |
| 240 | 26 | 7.9±8.0 | 129.3±142.0 | 1.5[0.5,4.0]a) |
16.3 分布
16.4 代謝
3Hでラベル化したセマグルチド0.5mgを健康男性被験者7例に単回皮下投与した結果、セマグルチドはペプチド骨格のタンパク質分解及び脂肪酸側鎖のβ酸化により代謝されると推定された(外国人データ)17)。
16.5 排泄
3Hでラベル化したセマグルチド0.5mgを健康男性被験者7例に単回皮下投与した結果、最大56日までの総投与放射能に対する尿中及び糞中の放射能排泄率は53.0%及び18.6%であった。総投与放射能のうち、セマグルチド未変化体の尿中放射能排泄率は3.12%であった(外国人データ)17)。
また、セマグルチドは、ヒトトランスポーター(P-gp、BCRP、OATP1B1、OATP1B3、OAT1、OAT3及びOCT2)に対して臨床上問題となる阻害作用を示さなかった20)(外国人データ、in vitro試験)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害被験者
腎機能障害の程度の異なる被験者(クレアチニンクリアランス(Ccr)による分類)における本剤10日間経口投与後(本剤5mgを5日間投与後に本剤10mgを5日間投与)の薬物動態を、腎機能が正常な被験者(Ccr90mL/min以上)と比較検討した結果を以下に示す21)(外国人データ)。
| 腎機能 | AUC0-24h | Cmax |
| 比の推定値[90%信頼区間] | 比の推定値[90%信頼区間] | |
| 軽度/正常(軽度:Ccr60〜89mL/min) | 1.37[0.91;2.06] | 1.39[0.93;2.06] |
| 中等度/正常(中等度:Ccr30〜59mL/min) | 1.13[0.69;1.84] | 1.20[0.75;1.93] |
| 重度/正常(重度:Ccr15〜29mL/min) | 0.61[0.42;0.88] | 0.61[0.42;0.87] |
| 末期/正常(末期:血液透析を必要とする被験者) | 1.02[0.59;1.79] | 1.06[0.61;1.84] |
16.6.2 肝機能障害被験者
肝機能障害の程度の異なる被験者(Child-Pugh scoresに基づく分類)における本剤10日間経口投与後(本剤5mgを5日間投与後に本剤10mgを5日間投与)の薬物動態を、肝機能が正常な被験者と比較検討した結果を以下に示す22)(外国人データ)。
| 肝機能 | AUC0-24h | Cmax |
| 比の推定値[90%信頼区間] | 比の推定値[90%信頼区間] | |
| 軽度/正常(軽度:Child-Pugh分類A) | 0.91[0.60;1.40] | 0.92[0.60;1.40] |
| 中等度/正常(中等度:Child-Pugh分類B) | 0.87[0.57;1.31] | 0.85[0.55;1.30] |
| 重度/正常(重度:Child-Pugh分類C) | 0.90[0.61;1.32] | 0.88[0.61;1.28] |
16.6.3 高齢者
2型糖尿病患者2431例(うち日本人531例)を対象とした母集団薬物動態解析の結果、65歳未満に対する65歳以上〜75歳未満及び75歳以上の定常状態の平均血漿中セマグルチド濃度の比と90%信頼区間は0.95[0.89;1.01]及び1.02[0.90;1.17]と推定された。[9.8参照]
16.7 薬物相互作用
本剤の併用投与による、リシノプリル、ワルファリン、メトホルミン、ジゴキシン、経口避妊薬(エチニルエストラジオール及びレボノルゲストレル)、フロセミド、ロスバスタチンのAUC及びCmaxへの臨床的に問題となる影響はみられなかった。本剤の併用投与時、レボチロキシンの単回投与後にチロキシン(内因性値で補正)のAUCの増大がみられた(33%)が、Cmaxへの影響はみられなかった。
セマグルチドのAUC及びCmaxに、オメプラゾールとの併用による臨床的に問題となる影響はみられなかった(外国人データ)。[10.2参照]
セマグルチドのAUC及びCmaxに、オメプラゾールとの併用による臨床的に問題となる影響はみられなかった(外国人データ)。[10.2参照]
| 被相互作用薬a,b | N | AUCc比e[90%信頼区間] | Cmaxd比e[90%信頼区間] |
| リシノプリル(20mg) | 46 | 1.07[0.99;1.15] | 0.96[0.88;1.06] |
| S-ワルファリン(25mg) | 46 | 1.08[1.04;1.12] | 0.88[0.83;0.94] |
| R-ワルファリン(25mg) | 46 | 1.11[1.06;1.15] | 0.91[0.86;0.96] |
| メトホルミン(850mg) | 31 | 1.32[1.23;1.43] | 0.98[0.90;1.06] |
| ジゴキシン(500μg) | 31 | 1.03[0.96;1.11] | 0.98[0.89;1.09] |
| エチニルエストラジオール(0.03mg) | 25 | 1.06[1.01;1.10] | 0.97[0.90;1.05] |
| レボノルゲストレル(0.15mg) | 25 | 1.06[0.97;1.17] | 0.95[0.87;1.05] |
| フロセミド(40mg) | 39 | 1.28[1.16;1.42] | 0.66[0.53;0.82] |
| ロスバスタチン(20mg) | 33 | 1.41[1.24;1.60] | 1.10[0.94;1.28] |
| レボチロキシン(600μg)f | 43 | 1.33[1.25;1.42] | 0.88[0.81;0.94] |
| 被相互作用薬a,b | N | AUC0-24h比c[95%信頼区間] | Cmax比c[95%信頼区間] |
| 本剤(10mg) | 26/27 | 1.13[0.84;1.53] | 1.16[0.85;1.57] |
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 単独療法:プラセボ対照二重盲検、実薬対照非盲検比較試験(第II/III相国内試験)
経口糖尿病薬の単独療法又は食事療法及び運動療法で血糖コントロールが不十分な日本人2型糖尿病患者243例を対象に無作為割り付けを行い、本剤3mg、本剤7mg、本剤14mgの1日1回経口投与、リラグルチド0.9mgの1日1回皮下投与又はプラセボの1日1回経口投与を52週間実施した(本剤3mg群:49例、本剤7mg群:49例、本剤14mg群:48例、リラグルチド0.9mg群:48例、プラセボ群:49例)。経口糖尿病薬の単独療法を実施していた被験者は、経口糖尿病薬のウォッシュアウト後に本剤の投与を開始した。本剤は1日1回3mgで投与を開始した。用量漸増は4週間ごととし、7mg及び14mgの用量にはそれぞれ投与開始から4週後及び8週後に到達するよう設定した。本剤は、空腹状態でその日の最初の食事の30分以上前に、コップ半分以下の水と共に経口投与した。
26週におけるHbA1cの結果を下表に示す。
26週におけるHbA1cの結果を下表に示す。
| HbA1c(%) | 本剤3mg | 本剤7mg | 本剤14mg | リラグルチド0.9mg | プラセボ |
| ベースラインa | 8.1±0.8(49) | 8.3±1.0(49) | 8.0±0.9(48) | 8.3±0.8(48) | 8.3±1.1(49) |
| 26週までの変化量a | −1.1±0.8(43) | −1.7±0.8(45) | −1.7±0.8(44) | −1.4±1.1(45) | −0.2±0.7(41) |
| 群差(本剤−リラグルチド0.9mg)b[95%信頼区間] | 0.3[−0.0;0.6] | −0.1[−0.4;0.2] | −0.3[−0.6;−0.0] | − | − |
| 群差(本剤−プラセボ)b[95%信頼区間] | −1.1[−1.4;−0.8] | −1.5[−1.7;−1.2] | −1.7[−2.0;−1.4] | − | − |
52週において、HbA1cのベースラインからの変化量(平均±標準偏差)は、本剤3mg群で−1.0±0.9%、本剤7mg群で−1.4±0.9%、本剤14mg群で−1.5±0.8%、リラグルチド0.9mg群で−1.3±1.0%及びプラセボ群で0.1±0.7%であった。リラグルチド0.9mg群との群差の推定値は、本剤3mg群で0.2%(95%信頼区間:−0.1;0.6)、本剤7mg群で−0.2%(95%信頼区間:−0.5;0.2)及び本剤14mg群で−0.4%(95%信頼区間:−0.8;0.0)であった。プラセボとの群差の推定値は、本剤3mgで−1.3%(95%信頼区間:−1.7;−0.9)、本剤7mgで−1.7%(95%信頼区間:−2.1;−1.3)及び本剤14mgで−1.9%(95%信頼区間:−2.3;−1.5)であった。
ベースラインから26週までの体重の変化量(平均±標準偏差)は、本剤3mg群で−0.4±1.9kg(ベースラインの平均:71.4kg)、本剤7mg群で−1.2±1.9kg(ベースラインの平均:71.3kg)、本剤14mg群で−2.4±3.0kg(ベースラインの平均:68.0kg)、リラグルチド0.9mg群で0.1±1.6kg(ベースラインの平均:74.7kg)及びプラセボ群で−1.1±1.6kg(ベースラインの平均:70.3kg)であった。ベースラインから52週までの体重の変化量(平均±標準偏差)は、本剤3mg群で0.0±2.4kg、本剤7mg群で−0.8±2.1kg、本剤14mg群で−2.9±3.9kg、リラグルチド0.9mg群で0.5±2.0kg及びプラセボ群で−1.0±1.7kgであった。
重大な低血糖は報告されなかった。重大な又は血糖値確定(56mg/dL未満)症候性低血糖注)は本剤の各用量群及びプラセボ群では認められなかったが、リラグルチド0.9mg群では2例2件報告された28)。[11.1.1参照]
注)重大な低血糖(米国糖尿病学会分類による)又は低血糖症状を伴う血糖値(血漿)が56mg/dL未満の低血糖。
17.1.2 単独療法:プラセボ対照二重盲検比較試験(第III相国際共同試験)
食事療法及び運動療法で血糖コントロールが不十分な2型糖尿病患者703例を対象に無作為割り付けを行い、二重盲検下で本剤3mg、本剤7mg、本剤14mgの1日1回経口投与又はプラセボの1日1回経口投与を26週間実施した(本剤3mg群:175例(日本人:29例)、本剤7mg群:175例(日本人:29例)、本剤14mg群:175例(日本人:28例)、プラセボ群:178例(日本人:30例))。本剤は1日1回3mgで投与を開始した。用量漸増は4週間ごととし、7mg及び14mgの用量にはそれぞれ投与開始から4週後及び8週後に到達するよう設定した。本剤は、空腹状態でその日の最初の食事の30分以上前に、コップ半分以下の水と共に経口投与した。主要評価項目であるHbA1cのベースラインから26週までの変化量に関して、本剤単独療法のすべての用量でプラセボに対する優越性が検証された(p<0.0001)。
| HbA1c(%) | 本剤3mg | 本剤7mg | 本剤14mg | プラセボ |
| ベースラインa | 7.9±0.7(175) | 8.0±0.6(175) | 8.0±0.7(175) | 7.9±0.7(178) |
| 26週までの変化量a | −0.9±1.2(167) | −1.3±1.0(160) | −1.5±1.0(160) | −0.3±1.2(168) |
| 群差(本剤−プラセボ)b[95%信頼区間] | −0.6[−0.8;−0.4] | −0.9[−1.1;−0.6] | −1.1[−1.3;−0.9] | − |
ベースラインから26週までの体重の変化量(平均±標準偏差)は、本剤3mg群で−1.5±3.3kg(ベースラインの平均:86.9kg)、本剤7mg群で−2.6±4.1kg(ベースラインの平均:89.0kg)、本剤14mg群で−4.0±4.2kg(ベースラインの平均:88.1kg)及びプラセボ群で−1.4±3.5kg(ベースラインの平均:88.6kg)であった。
17.1.3 併用療法:メトホルミンのみ又はメトホルミンとスルホニルウレア剤の両剤との併用、実薬対照二重盲検比較試験(第III相国際共同試験)
2型糖尿病患者1864例を対象に無作為割り付けを行い、メトホルミンのみ又はメトホルミンとスルホニルウレア剤の両剤による併用療法に追加して、二重盲検下で本剤3mg、本剤7mg又は本剤14mgの1日1回経口投与、あるいはシタグリプチン100mgの1日1回経口投与を78週間実施した(本剤3mg群:466例(日本人:52例)、本剤7mg群:466例(日本人:52例)、本剤14mg群:465例(日本人:51例)、シタグリプチン100mg群:467例(日本人:52例))。本剤は1日1回3mgで投与を開始した。用量漸増は4週間ごととし、7mg及び14mgの用量にはそれぞれ投与開始から4週後及び8週後に到達するよう設定した。本剤は、空腹状態でその日の最初の食事の30分以上前に、コップ半分以下の水と共に経口投与した。
主要評価項目であるHbA1cのベースラインから26週までの変化量に関して、本剤7mg及び本剤14mgのシタグリプチン100mgに対する非劣性が検証された(非劣性マージン:0.3%)。本剤3mgのシタグリプチン100mgに対する非劣性は示されなかった(下表参照)。
主要評価項目であるHbA1cのベースラインから26週までの変化量に関して、本剤7mg及び本剤14mgのシタグリプチン100mgに対する非劣性が検証された(非劣性マージン:0.3%)。本剤3mgのシタグリプチン100mgに対する非劣性は示されなかった(下表参照)。
| HbA1c(%) | 本剤3mg | 本剤7mg | 本剤14mg | シタグリプチン100mg |
| ベースラインa | 8.3±1.0(466) | 8.4±1.0(465) | 8.3±0.9(465) | 8.3±0.9(467) |
| 26週までの変化量a | −0.6±1.0(435) | −1.1±1.1(438) | −1.3±1.0(436) | −0.8±0.9(446) |
| 群差(本剤−シタグリプチン100mg)b[95%信頼区間] | 0.2[0.1;0.3] | −0.2[−0.4;−0.1] | −0.5[−0.6;−0.4] | − |
78週における日本人でのメトホルミン単剤との併用結果を下表に示す。
| HbA1c(%) | 本剤3mg | 本剤7mg | 本剤14mg | シタグリプチン100mg |
| ベースラインa | 8.0±1.0(40) | 8.2±0.9(39) | 8.1±0.8(38) | 8.0±0.8(40) |
| 78週までの変化量a | −0.7±0.9(38) | −1.2±1.1(39) | −1.5±0.9(37) | −0.8±0.9(39) |
| 群差(本剤−シタグリプチン100mg)b[95%信頼区間] | 0.1[−0.2;0.5] | −0.2[−0.6;0.1] | −0.6[−1.0;−0.2] | − |
17.1.4 併用療法:メトホルミンのみ又はメトホルミンとSGLT2阻害剤の両剤との併用、実薬及びプラセボ対照二重盲検比較試験(第III相国際共同試験)
2型糖尿病患者711例を対象に無作為割り付けを行い、メトホルミンのみ又はメトホルミンとSGLT2阻害剤の両剤との併用療法に追加して、ダブルダミー法による二重盲検下で本剤14mgの1日1回経口投与、リラグルチド1.8mgの1日1回皮下投与あるいはプラセボの1日1回投与を52週間実施した(本剤14mg群:285例(日本人:31例)、リラグルチド1.8mg群:284例(日本人:29例)、プラセボ群:142例(日本人:15例))。本剤は1日1回3mgで投与を開始した。用量漸増は4週間ごととし、14mgの用量には投与開始から8週後に到達するよう設定した。本剤は、空腹状態でその日の最初の食事の30分以上前に、コップ半分以下の水と共に経口投与した。
主要評価項目であるHbA1cのベースラインから26週までの変化量に関して、本剤14mgのプラセボに対する優越性(p<0.0001)及びリラグルチド1.8mgに対する非劣性(非劣性マージン:0.4%)が検証された。
主要評価項目であるHbA1cのベースラインから26週までの変化量に関して、本剤14mgのプラセボに対する優越性(p<0.0001)及びリラグルチド1.8mgに対する非劣性(非劣性マージン:0.4%)が検証された。
| HbA1c(%) | 本剤14mg | リラグルチド1.8mg | プラセボ |
| ベースラインa | 8.0±0.7(285) | 8.0±0.7(284) | 7.9±0.7(142) |
| 26週までの変化量a | −1.2±0.9(278) | −1.1±0.9(272) | −0.1±0.7(134) |
| 群差(本剤−リラグルチド1.8mg)b[95%信頼区間] | −0.1[−0.3;0.0] | − | − |
| 群差(本剤−プラセボ)b[95%信頼区間] | −1.1[−1.2;−0.9] | − | − |
17.1.5 併用療法:インスリンとの併用又はインスリンとメトホルミンとの併用、プラセボ対照二重盲検比較試験(第III相国際共同試験)
メトホルミン併用又は非併用下でのインスリンによる治療(Basalインスリン、混合インスリン又はBasal-Bolus療法)で血糖コントロールが不十分な2型糖尿病患者731例を対象に無作為割り付けを行い、二重盲検下で経口投与による本剤3mg、本剤7mg又は本剤14mgの1日1回あるいはプラセボの1日1回の追加投与を52週間実施した(本剤3mg群:184例(日本人:49例)、本剤7mg群:182例(日本人:48例)、本剤14mg群:181例(日本人:47例)、プラセボ群:184例(日本人:50例))。本剤は1日1回3mgで投与を開始した。用量漸増は4週間ごととし、7mg及び14mgの用量にはそれぞれ投与開始から4週後及び8週後に到達するよう設定した。本剤は、空腹状態でその日の最初の食事の30分以上前に、コップ半分以下の水と共に経口投与した。なお、低血糖のリスクを低減するために併用投与開始時のインスリン用量を20%減量した。
主要評価項目であるHbA1cのベースラインから26週までの変化量に関して、本剤のいずれの用量でもプラセボに対する優越性が検証された(p<0.0001)。
主要評価項目であるHbA1cのベースラインから26週までの変化量に関して、本剤のいずれの用量でもプラセボに対する優越性が検証された(p<0.0001)。
| HbA1c(%) | 本剤3mg | 本剤7mg | 本剤14mg | プラセボ |
| ベースラインa | 8.2±0.7(184) | 8.2±0.7(182) | 8.2±0.7(181) | 8.2±0.7(184) |
| 26週までの変化量a | −0.5±1.0(176) | −1.0±1.1(174) | −1.3±1.1(173) | −0.1±0.9(176) |
| 群差(本剤−プラセボ)b[95%信頼区間] | −0.5[−0.7;−0.3] | −0.9[−1.1;−0.7] | −1.2[−1.4;−1.0] | − |
52週において、HbA1cのベースラインからの変化量(平均±標準偏差)は、本剤3mg群で−0.6±1.0%、本剤7mg群で−0.9±1.1%、本剤14mg群で−1.2±1.0%及びプラセボ群で−0.2±0.8%であった。
17.1.6 非盲検長期(52週間)有効性及び安全性試験(第III相国内試験)
日本人2型糖尿病患者458例を対象に無作為割り付けを行い、経口糖尿病薬単剤(スルホニルウレア剤、速効型インスリン分泌促進剤、α-グルコシダーゼ阻害剤、チアゾリジン系薬剤又はSGLT2阻害剤のいずれか)に追加して、本剤3mg、本剤7mg又は本剤14mgの1日1回経口投与あるいはデュラグルチド0.75mgの週1回皮下投与を52週間実施した(本剤3mg群:131例、本剤7mg群:132例、本剤14mg群:130例、デュラグルチド0.75mg群:65例)。本剤は1日1回3mgで投与を開始した。用量漸増は4週間ごととし、7mg及び14mgの用量にはそれぞれ投与開始から4週後及び8週後に到達するよう設定した。本剤は、空腹状態でその日の最初の食事の30分以上前に、コップ半分以下の水と共に経口投与した。
52週において、HbA1cのベースラインからの変化量注)(平均±標準偏差)は、本剤3mg群で−0.8±1.0%(ベースラインの平均:8.2±0.9%)、本剤7mg群で−1.4±1.0%(ベースラインの平均:8.3±0.9%)、本剤14mg群で−1.8±1.0%(ベースラインの平均:8.4±1.0%)及びデュラグルチド0.75mg群で−1.4±0.9%(ベースラインの平均:8.4±0.9%)であった。
ベースラインから52週までの体重の変化量注)(平均±標準偏差)は、本剤3mg群で0.0±2.4kg(ベースラインの平均:71.5kg)、本剤7mg群で−0.9±3.4kg(ベースラインの平均:72.7kg)、本剤14mg群で−1.7±3.5kg(ベースラインの平均:72.6kg)及びデュラグルチド0.75mg群で1.0±2.7kg(ベースラインの平均:71.2kg)であった。
ベースラインから52週までの体重の変化量注)(平均±標準偏差)は、本剤3mg群で0.0±2.4kg(ベースラインの平均:71.5kg)、本剤7mg群で−0.9±3.4kg(ベースラインの平均:72.7kg)、本剤14mg群で−1.7±3.5kg(ベースラインの平均:72.6kg)及びデュラグルチド0.75mg群で1.0±2.7kg(ベースラインの平均:71.2kg)であった。
注)治験薬投与の早期中止または追加の糖尿病薬の使用の有無に関わらず、得られた観測値に基づく。
52週における併用薬別のHbA1cの結果を下表に示す。
| HbA1c(%) | ベースライン | 52週までの変化量 |
| 本剤3mg | ||
| スルホニルウレア剤 | 8.5±1.0(42) | −0.7±1.2(42) |
| 速効型インスリン分泌促進剤 | 8.1±0.5(22) | −0.7±1.0(21) |
| α-グルコシダーゼ阻害剤 | 8.0±0.8(22) | −1.1±0.8(21) |
| チアゾリジン系薬剤 | 8.3±0.9(23) | −1.1±0.8(20) |
| SGLT2阻害剤 | 8.2±1.0(22) | −0.8±1.0(22) |
| 本剤7mg | ||
| スルホニルウレア剤 | 8.3±0.9(42) | −1.3±1.1(40) |
| 速効型インスリン分泌促進剤 | 8.5±1.0(22) | −1.6±0.9(21) |
| α-グルコシダーゼ阻害剤 | 8.2±1.1(22) | −1.6±1.2(22) |
| チアゾリジン系薬剤 | 8.4±1.0(23) | −1.5±1.3(23) |
| SGLT2阻害剤 | 8.3±0.7(23) | −1.4±0.6(23) |
| 本剤14mg | ||
| スルホニルウレア剤 | 8.7±1.1(42) | −1.9±1.1(41) |
| 速効型インスリン分泌促進剤 | 8.5±0.9(22) | −1.7±1.1(21) |
| α-グルコシダーゼ阻害剤 | 8.4±1.0(22) | −1.8±1.1(21) |
| チアゾリジン系薬剤 | 8.2±1.0(22) | −1.7±1.0(22) |
| SGLT2阻害剤 | 8.3±0.8(22) | −1.7±0.7(22) |
18. 薬効薬理
18.1 作用機序
本剤はヒトGLP-1アナログであり、内因性GLP-1が標的とするGLP-1受容体と選択的に結合し、cAMP放出量を増加させるGLP-1受容体作動薬として作用する。
本剤はアルブミンと結合して代謝による分解の遅延及び腎クリアランスの低下を示すと考えられており、またアミノ酸置換によりDPP-4による分解に対して抵抗性を示すことにより、作用が持続する。
18.2 薬理作用
ヒトでの薬力学的作用の評価は、特記する場合を除き、すべて皮下投与用セマグルチド1.0mgの週1回12週間(用量漸増期間を含む)皮下投与後の定常状態において行われた。
18.2.1 血糖降下作用
セマグルチドの皮下投与により、糖尿病db/dbマウス(1日1回28日間反復投与)で溶媒対照群と比較し血糖値が低下した34)。
外国人2型糖尿病患者において、セマグルチドの皮下投与によりグルコース濃度依存的にインスリン分泌が促進及びグルカゴン分泌が抑制され、血中グルコース濃度はプラセボと比較して低下した35)。
外国人2型糖尿病患者にセマグルチド1.0mgを週1回13週間(用量漸増期間を含む)皮下投与した結果、最終投与後1週間における空腹時血糖値はプラセボと比較して低く、血糖降下作用は1週間後においても持続していた36)。
18.2.2 グルコース応答性インスリン分泌
外国人2型糖尿病患者にセマグルチドを皮下投与した結果、静脈内グルコース急速注入後のインスリンの第1相分泌(グルコース投与直後から10分後)及び第2相分泌(グルコース投与10分後から120分後)反応は、プラセボと比較して増加した35)。
18.2.3 グルカゴン分泌
外国人2型糖尿病患者において、セマグルチドの皮下投与により、プラセボと比較して空腹時グルカゴン濃度及び食後のグルカゴン分泌反応が低下した35)。
18.2.4 胃内容排出
外国人肥満被験者において、パラセタモール(アセトアミノフェン)の血中濃度プロファイルに基づくCmax及びAUC0-1hを指標として検討した結果、セマグルチドの皮下投与により食後早期の胃内容排出が遅延した39)。
19. 有効成分に関する理化学的知見
19.1. セマグルチド(遺伝子組換え)
20. 取扱い上の注意
本剤は吸湿性が強く、光に不安定なため、PTPシートの状態で保存すること。
21. 承認条件
医薬品リスク管理計画を策定の上、適切に実施すること。
22. 包装
<リベルサス錠3mg>
100錠[10錠(PTP)×10]
<リベルサス錠7mg>
100錠[10錠(PTP)×10]
<リベルサス錠14mg>
100錠[10錠(PTP)×10]
23. 主要文献
- 社内資料:ラットを用いた受胎能及びEFD試験(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.6.6.1)
- 社内資料:ウサギを用いたEFD試験(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.6.6.2)
- 社内資料:カニクイザルを用いたEFD試験(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.6.6.3)
- 社内資料:カニクイザルを用いたEFD及びPPND試験(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.6.6.3)
- 社内資料:健康授乳婦を対象とした薬物動態試験(第1相臨床試験:NN9924-4669)
- 社内資料:ラットを用いた104週間反復皮下投与がん原性試験(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.6.5)
- 社内資料:マウスを用いた104週間反復皮下投与がん原性試験(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.6.5)
- Buckley S.T.,et al., Sci Transl Med., 10 (467), eaar7047, (2018) »PubMed
- 社内資料:サルカプロザートナトリウムの毒性試験(2020年6月29日承認,CTD2.4.5.4)
- 社内資料:サルカプロザートナトリウムの薬物動態試験(2020年6月29日承認,CTD2.4.5.3)
- 社内資料:第I相臨床試験(NN9924-4140)(2020年6月29日承認,CTD2.7.2.3)
- 社内資料:第I相臨床試験(NN9924-4154)(2020年6月29日承認,CTD2.7.2.3)
- 社内資料:第I相臨床試験(NN9924-3794)(2020年6月29日承認,CTD2.7.2.3)
- 社内資料:第I相臨床試験(NN9924-3957)(2020年6月29日承認,CTD2.7.2.3)
- Marbury T.C.,et al., Clin Pharmacokinet., 56 (11), 1381-90, (2017) »PubMed
- Jensen L.,et al., Diabetes Obes Metab., 20 (4), 998-1005, (2018) »PubMed
- Jensen L.,et al., Eur J Pharm Sci, 104, 31-41, (2017) »PubMed
- 社内資料:酵素誘導(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.4.7)
- 社内資料:酵素阻害(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.4.7)
- 社内資料:トランスポーター阻害(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.4.7)
- Granhall C.,et al., Clin Pharmacokinet., 57 (12), 1571-80, (2018) »PubMed
- Baekdal T.A.,et al., J Clin Pharmacol., 58 (10), 1314-23, (2018) »PubMed
- Baekdal T.A.,et al., Clin Pharmacokinet., 58 (9), 1193-203, (2019) »PubMed
- 社内資料:第I相臨床試験(NN9924-4249)(2020年6月29日承認,CTD2.7.2.3)
- 社内資料:第I相臨床試験(NN9924-4250)(2020年6月29日承認,CTD2.7.2.3)
- 社内資料:第I相臨床試験(NN9924-4279)(2020年6月29日承認,CTD2.7.2.3)
- Baekdal T.A.,et al., Expert Opin Drug Metab Toxicol., 14 (8), 869-77, (2018) »PubMed
- Yamada Y.,et al., Lancet Diabetes Endocrinol., 8 (5), 377-91, (2020) »PubMed
- Aroda V.R.,et al., Diabetes Care., 42 (9), 1724-32, (2019) »PubMed
- Rosenstock J.,et al., JAMA., 321 (15), 1466-80, (2019) »PubMed
- Pratley R.,et al., Lancet., 394 (10192), 39-50, (2019) »PubMed
- Zinman B.,et al., Diabetes Care., 42 (12), 2262-71, (2019) »PubMed
- Yabe D.,et al., Lancet Diabetes Endocrinol., 8 (5), 392-406, (2020) »PubMed
- 社内資料:db/dbマウスにおける体重、摂餌量、血糖及びβ細胞容積ならびに機能への影響(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.2.2.2.3)
- Kapitza C.,et al., Diabetologia, 60 (8), 1390-9, (2017) »PubMed
- 社内資料:第I相臨床試験(NN9535-3684)(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.5.3.4)
- 社内資料:摘出灌流ラット膵臓からのインスリン分泌(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.2.2.1.2)
- 社内資料:ミニブタのインスリン分泌に及ぼす薬理作用持続時間の検討(オゼンピック皮下注2mg:2018年3月23日承認,CTD2.6.2.2.2.4)
- Blundell J.,et al., Diabetes Obes Metab., 19 (9), 1242-51, (2017) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
ノボノルディスクファーマ株式会社
ノボケア相談室
〒100-0005
東京都千代田区丸の内2-1-1
電話:0120-180363(フリーダイアル)
MSD株式会社
MSDカスタマーサポートセンター
〒102-8667
東京都千代田区九段北1-13-12
電話:0120-024961(フリーダイアル)
製品情報問い合わせ先
ノボノルディスクファーマ株式会社
ノボケア相談室
〒100-0005
東京都千代田区丸の内2-1-1
電話:0120-180363(フリーダイアル)
MSD株式会社
MSDカスタマーサポートセンター
〒102-8667
東京都千代田区九段北1-13-12
電話:0120-024961(フリーダイアル)
26. 製造販売業者等
26.1 製造販売元
26.2 販売提携
MSD株式会社
東京都千代田区九段北1-13-12