医薬品情報
| 総称名 | スピロペント |
|---|---|
| 一般名 | クレンブテロール塩酸塩 |
| 欧文一般名 | Clenbuterol Hydrochloride |
| 製剤名 | クレンブテロール塩酸塩製剤 |
| 薬効分類名 | 持続性気管支拡張剤 腹圧性尿失禁治療剤 |
| 薬効分類番号 | 2259 2590 |
| ATCコード | R03AC14 R03CC13 |
| KEGG DRUG |
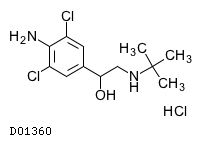
D01360
クレンブテロール塩酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年3月 改訂(第2版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| スピロペント錠10μg | Spiropent Tablet 10μg | 帝人ファーマ | 2259006F1080 | 6.3円/錠 |
2. 禁忌
次の患者には投与しないこと
2.1 下部尿路が閉塞している患者[下部尿路の閉塞を増悪させるおそれがある。]
2.2 本剤に対して過敏症の既往歴のある患者
4. 効能または効果
5. 効能または効果に関連する注意
<気管支喘息>
5.1 気管支喘息治療における長期管理の基本は、吸入ステロイド剤等の抗炎症剤の使用であり、吸入ステロイド剤等により症状の改善が得られない場合、あるいは患者の重症度から吸入ステロイド剤等との併用による治療が適切と判断された場合にのみ、本剤と吸入ステロイド剤等を併用して使用すること。
<腹圧性尿失禁>
5.2 本剤は、腹圧性以外の原因による尿失禁には使用しないこと。
6. 用法及び用量
<気管支喘息、慢性気管支炎、肺気腫、急性気管支炎>
通常、成人には1回クレンブテロール塩酸塩として20μgを1日2回、朝及び就寝前に経口投与する。
頓用として、通常、成人には1回クレンブテロール塩酸塩として20μgを経口投与する。
なお、年齢、症状により適宜増減する。
頓用として、通常、成人には1回クレンブテロール塩酸塩として20μgを経口投与する。
なお、年齢、症状により適宜増減する。
5歳以上の小児には、1回クレンブテロール塩酸塩として0.3μg/kgを1日2回、朝及び就寝前に経口投与する。
頓用として、5歳以上の小児には通常、1回クレンブテロール塩酸塩として0.3μg/kgを経口投与する。
なお、年齢、症状により適宜増減する。
頓用として、5歳以上の小児には通常、1回クレンブテロール塩酸塩として0.3μg/kgを経口投与する。
なお、年齢、症状により適宜増減する。
本剤の頓用を反復しなければならない場合には、早急に医師の指示を受けさせること。
<腹圧性尿失禁>
通常、成人には1回クレンブテロール塩酸塩として20μgを1日2回、朝及び夕に経口投与する。
なお、年齢、症状により適宜増減する。ただし、60μg/日を上限とする。
なお、年齢、症状により適宜増減する。ただし、60μg/日を上限とする。
7. 用法及び用量に関連する注意
高齢者においては、低用量(例えば1回10μgを1日2回)から用いるなど慎重に投与すること。[9.8参照]
8. 重要な基本的注意
<効能共通>
8.1 用法及び用量通り正しく使用しても効果が認められない場合は、本剤が適当でないと考えられるので、投与を中止すること。小児に投与する場合には、使用法を正しく指導し、経過の観察を十分に行うこと。
8.2 過度に使用を続けた場合、不整脈、場合によっては心停止を起こすおそれがあるので、使用が過度にならないように注意すること。[9.1.3参照]
<気管支喘息、慢性気管支炎、肺気腫>
8.3 本剤の投与期間中に発現する急性増悪に対しては、短時間作動型吸入β2刺激剤等の他の適切な薬剤を使用するよう患者、保護者又はそれに代わり得る適切な者に注意を与えること。
また、その薬剤の使用量が増加したり、あるいは効果が十分でなくなってきた場合には、疾患の管理が十分でないことが考えられるので、可及的速やかに医療機関を受診し治療を受けるよう患者、保護者又はそれに代わり得る適切な者に注意を与えること。
また、その薬剤の使用量が増加したり、あるいは効果が十分でなくなってきた場合には、疾患の管理が十分でないことが考えられるので、可及的速やかに医療機関を受診し治療を受けるよう患者、保護者又はそれに代わり得る適切な者に注意を与えること。
<気管支喘息>
8.4 本剤は吸入ステロイド剤等の抗炎症剤の代替薬ではないため、患者が本剤の使用により症状改善を感じた場合であっても、医師の指示なく吸入ステロイド剤等を減量又は中止し、本剤を単独で用いることのないよう、患者、保護者又はそれに代わり得る適切な者に注意を与えること。
8.5 本剤の投与期間中に発現する急性増悪に対して、短時間作動型吸入β2刺激剤等の薬剤の使用量が増加したり、あるいは効果が十分でなくなってきた場合には、患者の生命が脅かされる可能性があるので、患者の症状に応じて吸入ステロイド剤等の増量等の抗炎症療法の強化を行うこと。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 甲状腺機能亢進症の患者
症状が増悪するおそれがある。
9.1.2 高血圧症の患者
血圧が上昇することがある。
9.1.3 心疾患のある患者
動悸、不整脈等があらわれることがある。[8.2参照]
9.1.4 糖尿病の患者
症状が増悪するおそれがある。
9.1.5 低酸素血症の患者
血清カリウム値をモニターすることが望ましい。低酸素血症は血清カリウム値の低下が心リズムに及ぼす作用を増強することがある。[11.1.1参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。動物実験(ラット)で、妊娠後期に投与すると子宮筋の収縮を抑制して分娩遅延をおこすこと及び胎盤通過性を有することが報告されている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物実験(ラット)で、乳汁への移行性を有することが報告されている。
9.7 小児等
低出生体重児、新生児、乳児又は4歳以下の幼児を対象とした臨床試験は実施していない。
9.8 高齢者
一般に生理機能が低下している。[7.参照]
10. 相互作用
10.2 併用注意
| カテコールアミン製剤 アドレナリン イソプロテレノール等 | 不整脈、場合によっては心停止を起こすおそれがある。副作用の発現に注意し、異常が認められた場合には減量又は投与を中止するなど適切な処置を行うこと。 | カテコールアミン製剤の併用によりアドレナリン作動性神経刺激の増大が起こる。 |
| キサンチン誘導体 テオフィリン アミノフィリン水和物 ジプロフィリン等 ステロイド剤 ベタメタゾン プレドニゾロン ヒドロコルチゾンコハク酸エステルナトリウム等 利尿剤 フロセミド等 [11.1.1参照] | 血清カリウム値が低下し、低カリウム血症による不整脈を起こすおそれがある。副作用の発現に注意し、異常が認められた場合には減量又は投与を中止するなど適切な処置を行うこと。 | キサンチン誘導体はアドレナリン作動性神経刺激による血清カリウム値の低下を増強することが考えられる。ステロイド剤及び利尿剤は尿細管でのカリウム排泄促進作用があるため、血清カリウム値の低下を増強することが考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 重篤な血清カリウム値の低下(頻度不明)
11.2 その他の副作用
| 5%以上 | 0.1〜5%未満 | 0.1%未満 | |
| 過敏症 | 発疹 | そう痒 | |
| 精神神経系 | 振戦 | 筋痙直、頭痛 | 四肢しびれ感、興奮、不眠、めまい、眠気 |
| 循環器 | 動悸 | 頻脈、不整脈、血圧上昇 | |
| 消化器 | 嘔気 | 食欲不振、腹痛、下痢、便秘、口渇、胸やけ | |
| 肝臓 | AST上昇、ALT上昇 | ||
| 泌尿器 | 排尿障害 | ||
| その他 | 全身倦怠感、浮腫、ほてり |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
抗コリン作用、カルシウム拮抗作用を有する排尿障害治療薬との併用は使用経験が少ない。
16. 薬物動態
16.1 血中濃度
16.4 代謝
健康成人男子にクレンブテロール塩酸塩錠を40μg注)経口投与したとき、血漿中ではほとんど未変化体として存在した3)。
16.5 排泄
健康成人男子にクレンブテロール塩酸塩錠を20、40及び80μg注)経口投与したとき、いずれの用量においても、投与後72時間までに未変化体が18〜22%尿中に排泄された1)。
注)本剤の承認された成人の1回用量は、クレンブテロール塩酸塩として20μgである。
17. 臨床成績
17.1 有効性及び安全性に関する試験
18. 薬効薬理
18.1 作用機序
18.2 気管支拡張作用
18.3 気管支拡張作用持続性
イヌ及びモルモットで検討したクレンブテロール塩酸塩の気管支拡張作用持続時間は、イソプロテレノール、クロルプレナリン及びサルブタモールより長いことが確認されている8)。
18.4 末梢気道拡張作用
イヌを用いたtantalum bronchogramによる試験で、クレンブテロール塩酸塩は細い気管支に対しイソプロテレノールより強い拡張作用を示した10)。
18.5 β2受容体への選択性
モルモットを用い、β1受容体を含む標本(心房、回腸)とβ2受容体を含む標本(気管、子宮、血管)への選択性を検討したところ、クレンブテロール塩酸塩はイソプロテレノールより優れたβ2選択性を示した14)。
18.6 抗アレルギー作用
18.7 気道分泌系に対する作用
ラットの気道を用いた試験でクレンブテロール塩酸塩は、気道線毛運動並びに粘液輸送速度を亢進することが認められている18)。
18.8 気道過敏性亢進抑制及び気道上皮傷害抑制作用
イヌのインフルエンザCウイルス感染モデルにおいて、クレンブテロール塩酸塩は気道過敏性亢進及び気道上皮傷害を抑制することが認められている19)。
18.9 膀胱内圧低下作用
麻酔ラットを用いた膀胱内圧測定試験で、クレンブテロール塩酸塩は静脈内投与により膀胱の内圧低下を示した11)。
18.10 膀胱平滑筋弛緩作用
ウサギの膀胱を用いた試験で、クレンブテロール塩酸塩は膀胱平滑筋の静止張力に対してイソプロテレノールより強い弛緩作用を示した12)。
18.11 外尿道括約筋に対する作用
ウサギの尿道周囲に介在する外尿道括約筋を用いた試験で、クレンブテロール塩酸塩は経壁電気刺激による収縮をイソプロテレノールより強く増強することが認められている13)。
19. 有効成分に関する理化学的知見
19.1. クレンブテロール塩酸塩
22. 包装
PTP
100錠(10錠×10)、500錠(10錠×50)、1000錠(10錠×100)
23. 主要文献
- Yamamoto I,et al., J Pharmacobio-Dyn., 8 (5), 385-91, (1985) »PubMed
- 関野久之, 関野病院報告(未発表)顆粒と錠の生物学的同等性試験, (1995)
- Zimmer A,et al., Arzneim-Forsch., 26 (7), 1446-50, (1976)
- 濱田朝夫ほか, 臨床と研究, 62 (3), 957-72, (1985)
- 滝島 任ほか, 薬理と治療, 12 (8), 3627-40, (1984)
- 高橋昭三ほか, 臨床医薬, 8 (5), 1149-64, (1992)
- 島崎 淳ほか, 泌尿器外科, 2 (11), 1179-98, (1989)
- 宮田 健ほか, 日本薬理学雑誌, 74 (5), 573-88, (1978) »DOI
- Kato H,et al., Arzneim-Forsch., 35 (7), 1037-41, (1985) »PubMed
- 一ノ瀬正和ほか, 呼吸, 3 (6), 838-40, (1984)
- 鈴木敦子ほか, 自律神経, 26 (4), 380-7, (1989) »DOI
- 岸本 直ほか, J Smooth Muscle Res., 25 (1), 13-25, (1989) »DOI
- 岸本 直ほか, Tohoku J Exp Med., 165 (3), 243-5, (1991) »DOI
- O'Donnell SR., Arch Int Pharmacodyn Ther., 224, 190-8, (1976) »PubMed
- 小森谷恵司ほか, 応用薬理, 28 (4), 615-21, (1984)
- 山崎 登ほか, Gen Pharmacol., 15 (4), 345-8, (1984) »PubMed
- 佐藤博史ほか, アレルギーの臨床, 4 (9), 736-41, (1984)
- Iravani J,et al., Arzneim-Forsch., 24 (6), 849-55, (1974) »PubMed
- 門田孝志ほか, 呼吸, 11 (1), 66-75, (1992)
24. 文献請求先及び問い合わせ先
文献請求先
帝人ファーマ株式会社
メディカル情報グループ
〒100-8585
東京都千代田区霞が関3丁目2番1号
電話:フリーダイヤル 0120-189-315
製品情報問い合わせ先
帝人ファーマ株式会社
メディカル情報グループ
〒100-8585
東京都千代田区霞が関3丁目2番1号
電話:フリーダイヤル 0120-189-315
26. 製造販売業者等
26.1 製造販売元
帝人ファーマ株式会社
東京都千代田区霞が関3丁目2番1号