医薬品情報
| 総称名 | イトラコナゾール |
|---|---|
| 一般名 | イトラコナゾール |
| 欧文一般名 | Itraconazole |
| 製剤名 | イトラコナゾール内用液 |
| 薬効分類名 | 経口抗真菌剤 |
| 薬効分類番号 | 6290 |
| ATCコード | J02AC02 |
| KEGG DRUG |
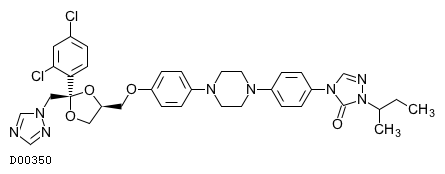
D00350
イトラコナゾール
|
| KEGG DGROUP |
DG01523
トリアゾール系抗真菌薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年5月 改訂(第6版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| イトラコナゾール内用液1%「VTRS」 (後発品) | ITRACONAZOLE Oral Solution | ヴィアトリス・ヘルスケア | 6290004S1044 | 49.5円/mL | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 ピモジド、キニジン、ベプリジル、トリアゾラム、シンバスタチン、アゼルニジピン、アゼルニジピン・オルメサルタン メドキソミル、ニソルジピン、エルゴタミン・カフェイン・イソプロピルアンチピリン、ジヒドロエルゴタミン、エルゴメトリン、メチルエルゴメトリン、バルデナフィル、エプレレノン、ブロナンセリン、シルデナフィル(レバチオ)、タダラフィル(アドシルカ)、スボレキサント、イブルチニブ、チカグレロル、ロミタピド、イバブラジン、ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期)、ルラシドン塩酸塩、アナモレリン塩酸塩、フィネレノン、ボクロスポリン、イサブコナゾニウム硫酸塩、アリスキレン、ダビガトラン、リバーロキサバンを投与中の患者[10.1参照]
2.5 妊婦又は妊娠している可能性のある女性[9.5参照]
4. 効能または効果
○真菌感染症
[適応菌種]
[適応症]
○好中球減少が予測される血液悪性腫瘍又は造血幹細胞移植患者における深在性真菌症の予防
5. 効能または効果に関連する注意
<好中球減少が予測される血液悪性腫瘍又は造血幹細胞移植患者における深在性真菌症の予防>
5.1 好中球数が500/mm3未満に減少することが予測される場合に本剤を投与すること。
<食道カンジダ症>
5.2 食道カンジダ症を疑う場合は、内視鏡検査を実施するなど確定診断後に本剤を投与すること。
6. 用法及び用量
<真菌感染症>
・真菌血症、呼吸器真菌症、消化器真菌症、尿路真菌症、真菌髄膜炎、ブラストミセス症、ヒストプラスマ症
通常、成人には20mL(イトラコナゾールとして200mg)を1日1回空腹時に経口投与する。なお、年齢、症状により適宜増減する。ただし、1回量の最大は20mL、1日量の最大は40mLとする。
・口腔咽頭カンジダ症、食道カンジダ症
通常、成人には20mL(イトラコナゾールとして200mg)を1日1回空腹時に経口投与する。
<好中球減少が予測される血液悪性腫瘍又は造血幹細胞移植患者における深在性真菌症の予防>
通常、成人には20mL(イトラコナゾールとして200mg)を1日1回空腹時に経口投与する。なお、患者の状態などにより適宜増減する。ただし、1回量の最大は20mL、1日量の最大は40mLとする。
7. 用法及び用量に関連する注意
<真菌感染症>
7.1 ブラストミセス症、ヒストプラスマ症
ブラストミセス症及びヒストプラスマ症の初期治療又は重症の患者に対しては、本剤で治療を開始しないこと。
7.2 口腔咽頭カンジダ症
服薬の際、数秒間口に含み、口腔内に薬剤をゆきわたらせた後に嚥下すること。なお、本剤は、主として消化管から吸収され作用を発現する。
<好中球減少が予測される血液悪性腫瘍又は造血幹細胞移植患者における深在性真菌症の予防>
7.3 好中球数が1,000/mm3以上に回復する、又は免疫抑制剤の投与終了など、適切な時期に投与を終了すること。
<効能共通>
7.5 本剤はイトリゾールカプセル50と生物学的に同等ではなく、バイオアベイラビリティが向上しているため、本剤からイトリゾールカプセル50への切り替えについては、イトラコナゾールの血中濃度が低下することがあるので、本剤の添加剤であるヒドロキシプロピル-β-シクロデキストリンに起因する胃腸障害(下痢、軟便等)及び腎機能障害による異常を認めた場合などを除き、原則として切り替えを行わないこと。[16.2.1参照]
7.6 国内において、内用液としては400mg/日を超える用量での有効性及び安全性は十分に検討されていないことから、400mg/日を超えて使用しないこと。
8. 重要な基本的注意
8.1 本剤の投与に際しては、肝疾患の既往歴、薬物過敏症、アレルギー既往歴等について十分な問診を行い、これらの現症又は既往歴のある患者については、投与中止又は慎重投与について考慮すること。[2.3、2.4、9.1.1、9.3.1、9.3.3参照]
8.2 本剤の高用量又は長期にわたる使用の場合には、血液検査、腎機能検査等を定期的に行うことが望ましい。
8.3 肝障害、胆汁うっ滞、黄疸があらわれることがあるので、定期的に肝機能検査を行うことが望ましい。[11.1.3参照]
8.4 本剤とワルファリンとの併用において、ワルファリンの作用が増強し、著しいINR上昇を来した症例が報告されている。本剤投与開始にあたっては、あらかじめワルファリン服用の有無を確認し、ワルファリンと併用する場合は、プロトロンビン時間測定及びトロンボテストの回数を増やすなど慎重に投与すること。[10.2参照]
8.5 本剤はイトリゾールカプセル50と生物学的に同等ではなく、バイオアベイラビリティが向上しているため、イトリゾールカプセル50から本剤に切り替える際には、イトラコナゾールの血中濃度(AUC、Cmax)の上昇による副作用の発現に注意すること。[16.2.1参照]
8.6 添加剤であるヒドロキシプロピル-β-シクロデキストリンに起因する胃腸障害(下痢、軟便等)があらわれることがあるので、観察を十分に行い、異常が認められた場合には適切な処置を行うこと。
8.7 添加剤であるヒドロキシプロピル-β-シクロデキストリンは浸透圧性腎症を引き起こす可能性があることが知られているため、高用量又は長期にわたる使用の場合には、血清クレアチニン値を測定するなど観察を十分に行い、腎機能障害がみられた場合には他の抗真菌剤への切り替えも考慮すること。[15.2.2参照]
8.8 本剤で効果が認められない場合は、漫然と投与を継続しないこと。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.2 うっ血性心不全又はその既往歴のある患者
うっ血性心不全の悪化又は再発を来すおそれがある。虚血性心疾患、基礎心疾患(弁膜症等)、慢性閉塞性肺疾患、腎不全、その他の浮腫性疾患等うっ血性心不全を起こすおそれのある患者に対して本剤を投与する場合には、その危険性について十分に説明するとともに、下肢浮腫、呼吸困難等の異常が認められた場合には投与を中止するなど適切な処置を行うこと。[11.1.2参照]
9.2 腎機能障害患者
9.2.1 腎機能障害のある患者で、コルヒチンを投与中の患者
9.2.2 腎機能障害のある患者(コルヒチンを投与中の患者を除く)
本剤及び代謝物等の排泄が遅延し、副作用があらわれやすくなるおそれがある。
9.3 肝機能障害患者
9.3.1 重篤な肝疾患の現症、既往歴のある患者
9.3.2 肝機能障害のある患者で、コルヒチンを投与中の患者
9.3.3 肝機能障害のある患者(コルヒチンを投与中の患者又は重篤な肝疾患のある患者を除く)
9.4 生殖能を有する者
妊娠する可能性のある女性には、本剤投与中及び投与終了後一定期間は、適切な避妊を行うよう指導すること。
9.5 妊婦
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒトで母乳中へ移行することが報告されている2)。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
消化器症状等副作用があらわれた場合は減量又は休薬するなど慎重に投与すること。高齢者では生理機能が低下していることが多く、副作用があらわれやすい。
10. 相互作用
相互作用序文
本剤は、主に肝チトクロームP450 3A4(CYP3A4)によって代謝される。また、本剤は、CYP3A4及びP糖蛋白に対して阻害作用を示す。他の薬剤との相互作用はすべての薬剤との組み合わせについて検討されているわけではなく、下表における併用薬剤は包括的なものではない。そのため、他剤による治療中に新たに本剤を併用したり、本剤による治療中に新たに他の薬剤を併用する場合には、併用薬剤の添付文書情報(代謝経路、相互作用経路、潜在的リスク及び併用時の具体的な対処方法等)を確認するとともに患者の状態を十分に観察し、慎重に投与すること。また、本剤空腹時投与のバイオアベイラビリティは、同用量のイトラコナゾールカプセル剤食直後投与時に比べて高くなると考えられるので、カプセル剤と同用量の本剤を投与する場合には薬物相互作用の増強の可能性を考慮し、慎重に投与すること。本剤投与終了後の血漿中薬物濃度は、本剤の投与量及び投与期間に応じて徐々に低下するため、本剤によって代謝が影響される薬剤の投与開始に際しては患者の状態を十分に観察し、慎重に投与すること。[16.2.1参照]
薬物代謝酵素用語
CYP3A4
薬物代謝酵素用語
P糖蛋白
10.1 併用禁忌
| ピモジド キニジン3)4) ベプリジル5) ベプリコール [2.1参照] | これらの薬剤の血中濃度上昇により、QT延長が発現する可能性がある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| トリアゾラム6) ハルシオン [2.1参照] | トリアゾラムの血中濃度上昇、作用の増強、作用時間の延長があらわれることがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| シンバスタチン7) リポバス [2.1参照] | シンバスタチンの血中濃度上昇により、横紋筋融解症があらわれやすくなる。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| アゼルニジピン カルブロック アゼルニジピン・オルメサルタン メドキソミル レザルタス配合錠 ニソルジピン8) [2.1参照] | これらの薬剤の血中濃度を上昇させることがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| エルゴタミン・カフェイン・イソプロピルアンチピリン クリアミン配合錠 ジヒドロエルゴタミン エルゴメトリン メチルエルゴメトリン パルタンM [2.1参照] | これらの薬剤の血中濃度上昇により、血管攣縮等の副作用が発現するおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| バルデナフィル レビトラ [2.1参照] | バルデナフィルのAUCが増加しCmaxが上昇するとの報告がある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| エプレレノン9) セララ [2.1参照] | エプレレノンの血中濃度を上昇させるおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ブロナンセリン ロナセン [2.1参照] | ブロナンセリンの血中濃度が上昇し、作用が増強するおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| シルデナフィル10) レバチオ [2.1参照] | シルデナフィルの血中濃度を上昇させるおそれがある(シルデナフィルとリトナビルの併用により、シルデナフィルのCmax及びAUCがそれぞれ3.9倍及び10.5倍に増加したとの報告がある)。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| タダラフィル アドシルカ [2.1参照] | タダラフィルの血中濃度を上昇させるおそれがある(タダラフィルとケトコナゾールの併用により、タダラフィルのAUC及びCmaxがそれぞれ312%及び22%増加したとの報告がある)。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| スボレキサント ベルソムラ [2.1参照] | スボレキサントの作用を著しく増強させるおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| イブルチニブ イムブルビカ [2.1参照] | イブルチニブの血中濃度が上昇し、副作用が増強されるおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| チカグレロル ブリリンタ [2.1参照] | チカグレロルの血中濃度が上昇し、出血の危険性が増大するおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ロミタピド ジャクスタピッド [2.1参照] | ロミタピドの血中濃度が著しく上昇するおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| イバブラジン コララン [2.1参照] | イバブラジンの血中濃度が上昇し、過度の徐脈があらわれることがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期) ベネクレクスタ [2.1参照] | ベネトクラクスの血中濃度が上昇し、腫瘍崩壊症候群の発現が増強する可能性がある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ルラシドン塩酸塩 ラツーダ [2.1参照] | ルラシドン塩酸塩の血中濃度が上昇し、作用が増強するおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| アナモレリン塩酸塩 エドルミズ [2.1参照] | アナモレリン塩酸塩の血中濃度が上昇し、副作用の発現が増強するおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| フィネレノン ケレンディア [2.1参照] | フィネレノンの血中濃度が著しく上昇するおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ボクロスポリン ルプキネス [2.1参照] | ボクロスポリンの血中濃度が上昇し、作用が増強するおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| イサブコナゾニウム硫酸塩 クレセンバ [2.1参照] | イサブコナゾールの血中濃度が上昇し、作用が増強するおそれがある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| アリスキレン11) ラジレス [2.1参照] | イトラコナゾールカプセルの併用投与(空腹時)により、アリスキレンのCmax及びAUCがそれぞれ約5.8倍及び約6.5倍に上昇したとの報告がある。 | 本剤のP糖蛋白阻害作用により、アリスキレンの排泄が阻害されると考えられる。 |
| ダビガトラン プラザキサ [2.1参照] | ダビガトランの血中濃度が上昇し、出血の危険性が増大することがある。 | 本剤のP糖蛋白阻害作用により、ダビガトランの排泄が阻害されると考えられる。 |
| リバーロキサバン イグザレルト [2.1参照] | リバーロキサバンの血中濃度が上昇し、出血の危険性が増大するおそれがある(リバーロキサバンとケトコナゾールの併用により、リバーロキサバンのAUC及びCmaxがそれぞれ158%及び72%増加したとの報告がある)。 | 本剤のCYP3A4及びP糖蛋白阻害作用により、リバーロキサバンの代謝及び排泄が阻害され、抗凝固作用が増強されると考えられる。 |
10.2 併用注意
| アトルバスタチン12) | アトルバスタチンの血中濃度を上昇させることがあり、横紋筋融解症があらわれやすくなる。必要に応じてアトルバスタチンの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ビンカアルカロイド系 抗悪性腫瘍剤 ビンクリスチン13) ビンブラスチン等 | これらの薬剤の血中濃度を上昇させることがあり、ビンカアルカロイド系抗悪性腫瘍剤の副作用が増強されることがある。必要に応じてこれらの薬剤の投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| メチルプレドニゾロン14) デキサメタゾン15) ブデソニド16) | これらの薬剤の血中濃度を上昇させることがあり、これらの薬剤の副作用が増強されることがある。必要に応じてこれらの薬剤の投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| コルヒチン [2.2、9.2.1、9.3.2参照] | コルヒチンの血中濃度を上昇させることがあり、コルヒチンの作用が増強されることがある。必要に応じてコルヒチンの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ジソピラミド | ジソピラミドの血中濃度上昇により、QT延長が発現する可能性がある。必要に応じてジソピラミドの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ベンゾジアゼピン系薬剤 ミダゾラム17) ブロチゾラム アルプラゾラム18) | これらの薬剤の血中濃度を上昇させることがある。必要に応じてこれらの薬剤の投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| 抗精神病薬 ハロペリドール アリピプラゾール19) ペロスピロン20) クエチアピン | これらの薬剤の血中濃度を上昇させることがある。必要に応じてこれらの薬剤の投与量を減量するなど用量に注意すること。 ・本剤とアリピプラゾールの併用により、アリピプラゾールのCmax、AUC、t1/2がそれぞれ19.4%、48.0%、18.6%増加したとの報告がある。 ・本剤とペロスピロンの併用により、ペロスピロンのCmax及びAUCがそれぞれ5.7倍及び6.8倍増加したとの報告がある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| 免疫抑制剤 シクロスポリン タクロリムス水和物 | これらの薬剤の血中濃度を上昇させることがある。必要に応じてこれらの薬剤の投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| 抗悪性腫瘍剤 ドセタキセル水和物21) エベロリムス テムシロリムス ゲフィチニブ ダサチニブ エルロチニブ ラパチニブ ボルテゾミブ イマチニブ スニチニブ ボスチニブ カバジタキセル セリチニブ クリゾチニブ シロリムス(錠) パノビノスタット ポナチニブ ルキソリチニブ アパルタミド トレチノイン (カプセル) ペミガチニブ エヌトレクチニブ | これらの薬剤の血中濃度を上昇させることがある。必要に応じてこれらの薬剤の投与量を減量するなど用量に注意すること。 ・クリゾチニブ反復投与時に本剤を併用投与したとき、クリゾチニブの定常状態におけるAUCtau及びCmaxは単独投与と比べそれぞれ57%及び33%増加した。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| オピオイド系鎮痛剤 フェンタニル オキシコドン22) メサドン | これらの薬剤の血中濃度を上昇させることがある。必要に応じてこれらの薬剤の投与量を減量するなど用量に注意すること。 ・本剤とオキシコドンの併用により、オキシコドンのクリアランスが32%減少し、AUCが51%増加したとの報告がある(オキシコドン注射剤)。また、オキシコドンのAUCが144%上昇したとの報告がある(オキシコドン経口剤)。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ブプレノルフィン セレギリン ガランタミン トルバプタン エレトリプタン サルメテロール シクレソニド フルチカゾン アプレピタント イミダフェナシン23) ソリフェナシン トルテロジン シロスタゾール シナカルセト エバスチン ダルナビル マラビロク オキシブチニン ドンペリドン シロドシン キニーネ ゾピクロン グアンファシン ジエノゲスト | これらの薬剤の血中濃度を上昇させることがある。必要に応じてこれらの薬剤の投与量を減量するなど用量に注意すること。 ・トルバプタンとの併用が避けられない場合は、トルバプタンの減量あるいは、低用量から開始するなど用量に注意すること。 ・本剤とイミダフェナシンの併用により、イミダフェナシンのCmax及びAUCがそれぞれ1.32倍及び1.78倍増加したとの報告がある。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| シルデナフィル バイアグラ | シルデナフィルとエリスロマイシンの併用によりシルデナフィルのCmax、AUCの増加が認められたとの報告がある。必要に応じてシルデナフィルの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| タダラフィル シアリス ザルティア | タダラフィルの血中濃度を上昇させるおそれがある(タダラフィルとケトコナゾールの併用により、タダラフィルのAUC及びCmaxがそれぞれ312%及び22%増加したとの報告がある)。必要に応じてタダラフィルの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ワルファリン24) [8.4参照] | ワルファリンの作用が増強し、著しいINR上昇があらわれることがある。必要に応じてワルファリンの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| アキシチニブ | アキシチニブの血中濃度が上昇し、副作用の発現頻度及び重症度が増加するおそれがある。やむを得ず併用する際にはアキシチニブの減量を考慮するとともに、患者の状態を慎重に観察し、副作用発現に十分注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| フェソテロジン | 活性代謝物5-HMTの血漿中濃度の上昇に伴い効果や副作用の増強が予想される。必要に応じてフェソテロジンの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ボセンタン | ボセンタンの血中濃度が上昇し、ボセンタンの副作用が発現しやすくなるおそれがある。必要に応じてボセンタンの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| アルテメテル・ルメファントリン | アルテメテル及びルメファントリンの血中濃度が上昇し、QT延長が起こるおそれがある。必要に応じてアルテメテル・ルメファントリンの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| デソゲストレル・エチニルエストラジオール | これらの薬剤の血中濃度を上昇させることがある。必要に応じてデソゲストレル・エチニルエストラジオールの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の維持投与期、急性骨髄性白血病) | ベネトクラクスの血中濃度が上昇し、副作用が増強する可能性があるので、ベネトクラクスを減量するとともに患者の状態を慎重に観察すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。 |
| ジヒドロピリジン系Ca拮抗剤 ニフェジピン25) ニルバジピン フェロジピン26)等 ベラパミル27) | これらの薬剤の血中濃度を上昇させることがある。また、心機能が低下する可能性がある。必要に応じてこれらの薬剤の投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4に対する阻害作用により、これらの薬剤の代謝が阻害される。また、両剤の心抑制作用が増強する可能性がある。 |
| イリノテカン | イリノテカンの活性代謝物の血中濃度が上昇することがある。必要に応じてイリノテカンの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4阻害作用により、イリノテカンの活性代謝物の無毒化が阻害されると考えられる。 |
| バルベナジン | バルベナジン及び活性代謝物の血漿中濃度が上昇するおそれがある。バルベナジンの作用が増強することで副作用があらわれるおそれがあるため、観察を十分に行うこと。本剤を併用する場合にはバルベナジンの増量はしないこと。 | 本剤のCYP3A阻害作用により、バルベナジン及び活性代謝物の代謝が阻害されると考えられる。 |
| ニロチニブ | ニロチニブの血中濃度が上昇し、QT延長があらわれることがある。必要に応じてニロチニブの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4及びP糖蛋白阻害作用により、ニロチニブの代謝及び排泄が阻害されると考えられる。 |
| アピキサバン | アピキサバンの血中濃度を上昇させることがある。必要に応じてアピキサバンの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4及びP糖蛋白阻害作用により、アピキサバンの代謝及び排泄が阻害されると考えられる。 |
| エドキサバン | エドキサバンの血中濃度を上昇させ、出血の危険性を増大させるおそれがある。必要に応じてエドキサバンの投与量を減量するなど用量に注意すること。 | 本剤のP糖蛋白阻害作用により、エドキサバンのバイオアベイラビリティを上昇させると考えられる。 |
| タラゾパリブ | タラゾパリブの副作用が増強されるおそれがあるので、本剤との併用は可能な限り避けること。やむを得ず併用する場合には、患者の状態を慎重に観察し、副作用の発現に十分注意すること。 | 本剤のP糖蛋白阻害作用により、タラゾパリブの血中濃度が上昇する可能性がある。 |
| ジゴキシン28) ブスルファン29) | これらの薬剤の血中濃度を上昇させることがある。 本剤とブスルファンの併用により、ブスルファンのクリアランスが20%減少したとの報告がある。必要に応じてこれらの薬剤の投与量を減量するなど用量に注意すること。 | 機序不明 |
| ロペラミド | ロペラミドの血中濃度が上昇することがある。必要に応じてロペラミドの投与量を減量するなど用量に注意すること。 | 本剤のCYP3A4及びP糖蛋白阻害作用により、ロペラミドの代謝及び排泄が阻害されると考えられる。 |
| クラリスロマイシン30) リトナビル ホスアンプレナビル/リトナビル エリスロマイシン シプロフロキサシン31) | 本剤の血中濃度が上昇することがある。 本剤とシプロフロキサシンの併用により、イトラコナゾールのCmax及びAUCがそれぞれ53.13%及び82.46%増加したとの報告がある。必要に応じて本剤の投与量を減量するなど用量に注意すること。 | これらの薬剤のCYP3A4に対する阻害作用により、本剤の代謝が阻害される。 |
| ダルナビル/リトナビル | 本剤又はダルナビルの血中濃度が上昇する可能性がある(ダルナビル/リトナビルとケトコナゾールの併用により、ダルナビルとケトコナゾールの血中濃度の上昇が認められたとの報告がある)。必要に応じて本剤又はこれらの薬剤の投与量を調節するなど用量に注意すること。 | 本剤及びこれらの薬剤のCYP3A4に対する阻害作用により、血中濃度の変化が起こる場合がある。 |
| エルビテグラビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミドフマル酸塩 エルビテグラビル・コビシスタット・エムトリシタビン・テノホビル ジソプロキシルフマル酸塩 | 本剤、エルビテグラビル及びコビシスタットの血中濃度が上昇する可能性がある。必要に応じて本剤又はこれらの薬剤の投与量を調節するなど用量に注意すること。 | 本剤及びコビシスタットのCYP3A等阻害作用により、相互に代謝が阻害される。 |
| ダルナビル エタノール付加物・コビシスタット | 本剤、ダルナビル又はコビシスタットの血中濃度が上昇する可能性がある。必要に応じて本剤又はダルナビル エタノール付加物・コビシスタットの投与量を調節するなど用量に注意すること。 | 本剤とダルナビル及びコビシスタットのCYP3A阻害作用により、相互に代謝が阻害される。 |
| ダルナビル エタノール付加物・コビシスタット・エムトリシタビン・テノホビル アラフェナミドフマル酸塩 | 本剤、ダルナビル、コビシスタット又はテノホビル アラフェナミドの血中濃度が上昇する可能性がある。必要に応じて本剤又はダルナビル エタノール付加物・コビシスタット・エムトリシタビン・テノホビル アラフェナミドフマル酸塩の投与量を調節するなど用量に注意すること。 | 本剤とダルナビル、コビシスタット及びテノホビル アラフェナミドのCYP3A及びP糖蛋白阻害作用により、相互に代謝が阻害される。 |
| カルバマゼピン32)33) エトラビリン リファブチン [7.4参照] | 本剤の血中濃度が低下することがある。また、これらの薬剤の血中濃度が上昇する可能性がある。必要に応じて本剤又はこれらの薬剤の投与量を調節するなど用量に注意すること。 | これらの薬剤の肝薬物代謝酵素誘導により、本剤の肝代謝が促進される。また、本剤のCYP3A4に対する阻害作用によりこれらの薬剤の代謝が阻害される。 |
| リファンピシン フェニトイン イソニアジド34) フェノバルビタール エファビレンツ ネビラピン35) [7.4参照] | 本剤の血中濃度が低下することがある。 本剤とネビラピンの併用により、本剤のCmax、AUC及びt1/2がそれぞれ38%、61%及び31%減少したとの報告がある。必要に応じて本剤の投与量、両剤の投与間隔を調節するなど注意すること。 | これらの薬剤の肝薬物代謝酵素誘導により、本剤の肝代謝が促進される。 |
| メロキシカム36) | 本剤とメロキシカムの併用により、メロキシカムのCmax及びAUCがそれぞれ64%及び37%減少したとの報告がある。必要に応じてメロキシカムの投与量を調節するなど用量に注意すること。 | 本剤がメロキシカムの消化管からの吸収を抑制すると考えられる。 |
| リオシグアト | リオシグアトの血中濃度を上昇させるおそれがある(リオシグアトとケトコナゾールの併用により、リオシグアトのAUC及びCmaxがそれぞれ150%及び46%増加、また、消失半減期が延長したとの報告がある)。本剤との併用が必要な場合は、患者の状態に注意し、必要に応じてリオシグアトの減量を考慮すること。 | 本剤のCYP1A1及びCYP3A4阻害作用により、リオシグアトのクリアランスが低下することが考えられる。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック(頻度不明)、アナフィラキシー(頻度不明)
チアノーゼ、冷汗、血圧低下、呼吸困難、胸内苦悶等があらわれた場合には投与を中止し、適切な処置を行うこと。
11.1.2 うっ血性心不全(1.7%)、肺水腫(頻度不明)
下肢浮腫、呼吸困難等の症状に注意すること。[9.1.2参照]
11.1.3 肝障害(10.0%)、胆汁うっ滞(0.6%)、黄疸(頻度不明)
11.1.4 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(頻度不明)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)、急性汎発性発疹性膿疱症(頻度不明)、剥脱性皮膚炎(頻度不明)、多形紅斑(頻度不明)
11.1.5 間質性肺炎(頻度不明)
咳嗽、呼吸困難、発熱、肺音の異常(捻髪音)等が認められた場合には、速やかに胸部X線、胸部CT、血清マーカー等の検査を実施し、本剤の投与を中止するとともに、適切な処置を行うこと。
11.1.6 低カリウム血症(12.2%)[8.9参照]
11.1.7 偽アルドステロン症(頻度不明)
低カリウム血症、血圧上昇、ナトリウム・体液の貯留、浮腫、体重増加等があらわれることがある。[8.9参照]
発現頻度は、深在性真菌症及び真菌感染が疑われる発熱性好中球減少症患者注)を対象とし、イトラコナゾール注射剤最短3日間から最長2週間投与後、本剤最大200mgを1日2回最長12週間投与した臨床試験(JK1211-JPN-07)の安全性解析対象集団を含む
注)真菌感染が疑われる発熱性好中球減少症は国内承認外
11.2 その他の副作用
| 5%以上 | 5%未満 | 頻度不明 | |
| 感染症 | 鼻炎 | ||
| 過敏症 | 血管浮腫 | ||
| 代謝・栄養 | 高トリグリセリド血症 | ||
| 循環器 | 血圧上昇、不整脈、心電図異常、高血圧、狭心症発作、徐脈 | 動悸、心室性期外収縮、房室ブロック、血管障害、頻脈、低血圧 | |
| 消化器 | 下痢・軟便(26.1%)、悪心 | 腹部不快感、食欲不振、嘔吐、腹痛、腹部膨満、便秘、上腹部痛、消化不良、口内炎、口腔内痛、胃炎、歯周炎 | 舌炎、おくび、腹部腰背部痛、胃十二指腸潰瘍、食道炎 |
| 肝臓 | 肝機能異常、高ビリルビン血症、γ-GTP増加、ALT増加、AST増加、ALP増加、LDH増加 | LAP増加 | |
| 呼吸器 | 咳嗽、発声障害、咽喉頭疼痛 | 呼吸困難 | |
| 皮膚 | 発疹、そう痒症、蕁麻疹 | 紅斑、脱毛、湿疹、光線過敏性反応、白血球破砕性血管炎、紅斑性発疹、皮膚乾燥、皮膚腫脹、多汗症、皮膚障害 | |
| 精神神経系 | めまい、感覚鈍麻、頭痛、不眠 | 味覚異常、傾眠、振戦、倦怠感、末梢神経障害、錯感覚、肩こり、眠気、不安、失神、うつ病、錯乱状態 | |
| 腎臓 | 腎機能検査値異常(尿中β2ミクログロブリン増加、β-NアセチルDグルコサミニダーゼ増加、尿中α1ミクログロブリン増加、尿検査異常) | 腎障害、腎尿細管障害、蛋白尿、尿量減少、血尿 | 頻尿、尿失禁、BUN上昇、尿検査異常、尿円柱 |
| 生殖器 | 月経異常、勃起不全 | ||
| 血液 | 白血球減少、血小板減少、貧血、好酸球増多、白血球増多 | 好中球減少、赤血球数減少、ヘマトクリット減少、ヘモグロビン減少、顆粒球減少 | |
| その他 | 末梢性浮腫、浮腫、潮紅、ほてり、高血糖、視覚障害(霧視、複視を含む)、体重増加 | 発熱、異常感、無力症、顔面浮腫、血清病、筋痛、関節痛、耳鳴、難聴、胸痛、悪寒、筋硬直、腫脹、自傷、脱水、多汗症 | |
| 臨床検査 | 血中コレステロール減少、CRP増加、CK増加、血中ナトリウム減少、血中リン増加 | 血清尿酸上昇、血清カリウム上昇、血中アミラーゼ増加、総蛋白増加、総コレステロール増加、尿糖陽性 |
13. 過量投与
本剤は血液透析によって除去できない。
14. 適用上の注意
14.1 薬剤交付時の注意
本剤は個々の患者の投与期間に基づいた必要量を交付し、計量カップを用い、正確に本剤1回服用量を量り取って服用するよう患者に指導すること。また、飲み忘れ等による服薬期間後の残薬については、服用しないよう指導すること。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 類似化合物(ミコナゾール)では血糖降下剤との併用により、著しい血糖低下が認められたとの報告がある。
15.2 非臨床試験に基づく情報
15.2.1 ヒドロキシプロピル-β-シクロデキストリンの混餌投与によるラットがん原性試験において、膵臓腫瘍及び大腸腫瘍の発生率増加が認められた。しかしながら、膵臓腫瘍はラットのみに種特異的に生じる所見であり、大腸腫瘍は大量(ヒトの約15倍)のヒドロキシプロピル-β-シクロデキストリンを長期間経口投与したことで生じた所見であり、他の難吸収性多糖類の長期間大量経口投与でも同様に生じる所見である39)。
15.2.2 ラット及びイヌの3ヵ月静脈内投与試験において、添加剤のヒドロキシプロピル-β-シクロデキストリンは、腎機能には影響を与えないが、腎臓及び膀胱において、高張な物質を排泄する過程で生じる適応性変化と考えられる浸透圧性腎症がみられている。この所見は3ヵ月の休薬後も軽度に残存していたものの、回復性が認められた。また、同様の所見がラット及びイヌの12ヵ月経口投与試験においても認められた。[8.7参照]
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人男性を対象に、イトラコナゾール内用液をイトラコナゾールとして100及び200mgを空腹時に単回経口投与したとき、血漿中未変化体及び主活性代謝物ヒドロキシイトラコナゾールの薬物動態パラメータは以下のとおりであった40)。
| 用量 | 対象 | Cmax(ng/mL) | Tmax(hr) | AUC(ng・hr/mL) | t1/2(hr) |
| 100mg(n=6) | 未変化体 | 309.9±43.8 | 1.8±0.4 | 2,842.7±703.3 | 24.1±9.6 |
| 主活性代謝物 | 539.5±67.5 | 2.5±0.8 | 7,055.1±1,718.2 | 7.7±1.8 | |
| 200mg(n=6) | 未変化体 | 688.3±163.8 | 2.2±0.4 | 7,914.3±1,874.7 | 26.3±5.2 |
| 主活性代謝物 | 1,002.3±203.1 | 3.0±1.1 | 19,073.7±3,732.6 | 8.3±1.4 |
16.1.2 反復投与
(1)健康成人男性を対象に、イトラコナゾール内用液をイトラコナゾールとして100mg及び200mgを空腹時に1日1回、12日間反復経口投与したとき、各投与群における未変化体及びヒドロキシイトラコナゾールはいずれも投与期間中に定常状態に達した。また、最終投与後の未変化体及びヒドロキシイトラコナゾールのCmaxは、ほぼ投与量に比例して増加したが、最終投与後の未変化体及びヒドロキシイトラコナゾールのt1/2は単回投与時よりも延長した。また、AUC(0→24)は用量比を上回る増加(2.5倍及び2.3倍)を示し、肝代謝の飽和に起因すると考えられる非線形性が認められた41)。
| 用量 | 対象 | 投与日 | Cmax(ng/mL) | Tmax(hr) | AUC(0→24)(ng・hr/mL) | t1/2(hr) |
| 100mg(n=7) | 未変化体 | 1日目 | 296.5±67.8 | 1.7±0.5 | 2,004.9±456.0 | − |
| 最終日 | 1,028.0±98.8 | 1.9±0.7 | 12,248.3±2,076.0 | 28.1±10.4 | ||
| 主活性代謝物 | 1日目 | 511.5±45.5 | 2.1±0.4 | 6,267.0±1,162.7 | − | |
| 最終日 | 1,298.1±186.1 | 3.6±0.5 | 25,998.9±4,665.1 | 19.0±8.2 | ||
| 200mg(n=7) | 未変化体 | 1日目 | 738.0±174.4 | 1.7±0.8 | 4,932.0±1,069.3 | − |
| 最終日 | 2,503.7±537.1 | 2.1±1.1 | 31,169.1±7,527.8 | 39.0±5.6 | ||
| 主活性代謝物 | 1日目 | 914.8±102.0 | 2.6±1.0 | 13,359.0±2,358.0 | − | |
| 最終日 | 2,851.7±692.6 | 3.0±1.0 | 59,652.5±14,939.6 | 37.6±12.1 |
(2)日本人患者(深在性真菌症患者及び真菌感染が疑われる発熱性好中球減少症患者注1))を対象にイトラコナゾール内用液をイトラコナゾールとして200mg 1日1回投与したとき、血漿中未変化体のトラフ濃度(推定値の平均値)は日本人患者にイトラコナゾール内用液をイトラコナゾールとして2.5mg/kg 1日2回投与注2)したときと比べ低値を示したが、その分布範囲に大きな差はなく、外国人の重度好中球減少症を有する血液悪性疾患患者を対象にイトラコナゾール内用液をイトラコナゾールとして2.5mg/kg 1日2回投与したときの血漿中未変化体のトラフ濃度(実測値)と同程度又は高値を示すと考えられた42)。
注1)真菌感染が疑われる発熱性好中球減少症は国内承認外
注2)本剤の承認された用法及び用量は、「通常、成人には20mL(イトラコナゾールとして200mg)を1日1回空腹時に経口投与する。なお、年齢、症状により適宜増減する。ただし、1回量の最大は20mL、1日量の最大は40mLとする。」である。
16.1.3 生物学的同等性試験
イトラコナゾール内用液1%「VTRS」とイトリゾール内用液1%を、クロスオーバー法によりそれぞれ20mL(イトラコナゾールとして200mg)健康成人男子に絶食時単回経口投与して血漿中イトラコナゾール濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された43)。
| 判定パラメータ | 参考パラメータ | |||
| AUCt(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | T1/2(hr) | |
| イトラコナゾール内用液1%「VTRS」 | 9537.08±2893.35 | 1017.73±395.85 | 1.9±0.5 | 24.20±4.97 |
| イトリゾール内用液1% | 9110.00±3257.85 | 1036.96±344.57 | 1.7±0.6 | 25.20±6.03 |
血漿中イトラコナゾールの濃度推移
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.2 吸収
16.2.1 製剤間のバイオアベイラビリティ
健康成人男性を対象に、イトラコナゾール内用液(空腹時)又はイトラコナゾールカプセル剤(食直後)をイトラコナゾールとして100及び200mgを単回経口投与した試験の成績を比較した結果、イトラコナゾール内用液のバイオアベイラビリティはイトラコナゾールカプセル剤と比べ高値を示した40)44)45)。[7.5、8.5、10.参照]
| パラメータ | 対象 | 100mg | 200mg | ||
| イトラコナゾール内用液(n=6) | イトラコナゾールカプセル剤(n=5) | イトラコナゾール内用液(n=6) | イトラコナゾールカプセル剤(n=5) | ||
| Cmax(ng/mL) | 未変化体 | 309.9±43.8 | 132.2±80.7 | 688.3±163.8 | 215.6±58.1 |
| 主活性代謝物 | 539.5±67.5 | 267.4±71.4 | 1,002.3±203.1 | 678.6±62.4 | |
| Tmax(hr) | 未変化体 | 1.8±0.4 | 4.8±1.8 | 2.2±0.4 | 4.4±0.9 |
| 主活性代謝物 | 2.5±0.8 | 6.0±1.4 | 3.0±1.1 | 5.2±1.8 | |
| AUC(ng・hr/mL) | 未変化体 | 2,842.7±703.3 | 2,221±1,141 | 7,914.3±1,874.7 | 4,142±1,272 |
| 主活性代謝物 | 7,055.1±1,718.2 | 6,772±3,221 | 19,073.7±3,732.6 | 15,028±2,524 | |
| t1/2(hr) | 未変化体 | 24.1±9.6 | 24.9±7.7 | 26.3±5.2 | 27.9±9.9 |
| 主活性代謝物 | 7.7±1.8 | 17.4±11.2 | 8.3±1.4 | 9.5±2.1 | |
16.2.2 食事の影響
イトラコナゾール内用液を空腹時に単回経口投与したとき、食直後投与よりも未変化体及びヒドロキシイトラコナゾールのTmaxの短縮(約0.5倍)、Cmaxの上昇(1.7倍及び1.6倍)及びAUCの増加(1.1倍及び1.2倍)が認められた40)。
16.3 分布
16.3.1 体組織への分布
イトラコナゾール200mg経口投与後の肺、腎、肝、皮膚等の組織内濃度は血漿中濃度よりも高かった46)(外国人データ)。
16.3.2 乳汁移行性
健康女性のデータでは、授乳婦にイトラコナゾール1回200mgを1日2回経口投与したとき、乳汁中に未変化体が検出された2)。
16.3.3 血漿蛋白結合率
99.8%47)(in vitro、平衡透析法)
16.4 代謝
ヒトにイトラコナゾールを経口投与したとき、肝臓で主に代謝され、主な代謝物はヒドロキシイトラコナゾールである48)。
初回通過効果
あり49)
代謝物の活性の有無
ヒドロキシイトラコナゾール(主活性代謝物)は、未変化体と比較してほぼ同等の抗真菌活性を示す50)。
代謝酵素(チトクロームP450)の分子種
CYP3A448)
16.5 排泄
16.8 その他
17. 臨床成績
17.1 有効性及び安全性に関する試験
<真菌感染症(口腔咽頭カンジダ症)>
17.1.1 国内第III相試験(JK1211-JPN-06)
<真菌感染症(食道カンジダ症)>
17.1.2 海外第III相試験(ITR-USA-12)
<真菌感染症>
17.1.3 国内第III相試験(JK1211-JPN-07)
<好中球減少が予測される血液悪性腫瘍又は造血幹細胞移植患者における深在性真菌症の予防>
17.1.4 海外第III試験(ITR-ITA-18)
好中球減少を伴う血液悪性疾患患者を対象とし、イトラコナゾール内用液2.5mg/kgを1日2回最長8週間投与※したときの予防効果をプラセボと比較したときの真菌感染症発症率は以下のとおりであった53)54)。
| 真菌感染症の発症 | イトラコナゾール群(n=201) | プラセボ群(n=204) | p値注) | |
| 深在性真菌症(確定診断例+疑診例)+表在性真菌症 | 48(23.9%) | 68(33.3%) | 0.035 | |
| 深在性真菌症:確定診断例 | 5(2.5%) | 9(4.4%) | 0.291 | |
| 深在性真菌症:疑診例 | 43(21.4%) | 59(28.9%) | 0.081 | |
| 表在性真菌症 | 0(0%) | 0(0%) | − | |
副作用の主なものは下痢、嘔吐、悪心であった53)。
17.1.5 海外第III試験(ITR-INT-54)
好中球減少を伴う血液悪性疾患患者を対象とし、イトラコナゾール内用液2.5mg/kgを1日2回最長8週間投与※したときの予防効果をアムホテリシンBカプセルと比較したときの真菌感染症発症率は以下のとおりであった37)55)。
| 真菌感染症の発症 | イトラコナゾール群(n=281) | アムホテリシンB群(n=276) | p値注1) | |
| 侵襲性アスペルギルス症 | 5(1.8%) | 9(3.3%) | 0.264 | |
| 深在性真菌症(確定診断例注2)+疑診例)+表在性真菌症 | 93(33.1%) | 106(38.4%) | 0.191 | |
| 深在性真菌症:確定診断例注2) | 8(2.8%) | 13(4.7%) | 0.248 | |
| 深在性真菌症:疑診例 | 83(29.5%) | 80(29.0%) | 0.886 | |
| 表在性真菌症 | 2(0.7%) | 13(4.7%) | 0.004 | |
※本剤の承認された用法及び用量は、「通常、成人には20mL(イトラコナゾールとして200mg)を1日1回空腹時に経口投与する。なお、患者の状態などにより適宜増減する。ただし、1回量の最大は20mL、1日量の最大は40mLとする。」である。
主な有害事象は下痢、悪心、嘔吐であった37)。
18. 薬効薬理
18.1 作用機序
真菌のチトクロームP450に特異的に作用して、真菌の細胞膜の主要構成脂質であるエルゴステロールの生合成を阻害する。イトラコナゾールは哺乳類由来のチトクロームP450には影響が少なかった56)。
18.2 抗真菌作用
19. 有効成分に関する理化学的知見
19.1. イトラコナゾール
20. 取扱い上の注意
小児の手の届かない所に保管すること。
22. 包装
140mL[瓶]
23. 主要文献
- イトラコナゾールの催奇形性試験(ラット)(イトリゾール内用液1%:2006.7.26承認、CTD2.6.6.6)
- イトラコナゾールのヒト乳汁中への排泄(イトリゾール内用液1%:2006.7.26承認、CTD2.6.4.6)
- Cruccu V,et al., Clin Ter., 146, 383-389, (1995) »PubMed
- Kaukonen KM,et al., Clin Pharmacol Ther., 62, 510-517, (1997) »PubMed
- Gopaul VS,et al., Drug Metab Rev., 36 (Suppl.1), 208, (2004)
- Varhe A,et al., Clin Pharmacol Ther., 56, 601-607, (1994) »PubMed
- Horn M, Arch Dermatol., 132, 1254, (1996) »PubMed
- Heinig R,et al., Eur J Clin Pharmacol., 55, 57-60, (1999) »PubMed
- Cook CS,et al., Xenobiotica., 34, 215-228, (2004) »PubMed
- Muirhead GJ,et al., Br J Clin Pharmacol., 50, 99-107, (2000) »PubMed
- Tapaninen T,et al., J Clin Pharmacol., 51, 359-367, (2011) »PubMed
- Kantola T,et al., Clin Pharmacol Ther., 64, 58-65, (1998) »PubMed
- Boehme A,et al., Onkologie., 17 (Suppl.2), 13, (1994)
- Linthoudt H,et al., J Heart Lung Transplant., 15, 1165, (1996) »PubMed
- Varis T,et al., Clin Pharmacol Ther., 68, 487-494, (2000) »PubMed
- Raaska K,et al., Clin Pharmacol Ther., 72, 362-369, (2002) »PubMed
- Olkkola K,et al., Clin Pharmacol Ther., 55, 481-485, (1994) »PubMed
- Yasui N,et al., Psychopharmacology., 139, 269-273, (1998) »PubMed
- Kubo M,et al., Drug Metab Pharmacokinet., 20, 55-64, (2005) »PubMed
- Masui T,et al., Ther Drug Monit., 28, 73-75, (2006) »PubMed
- Royer I,et al., Cancer Res., 56, 58-65, (1996) »PubMed
- Saari TI,et al., Eur J Clin Pharmacol., 66, 387-397, (2010) »PubMed
- Ohno T,et al., J Clin Pharmacol., 48, 330-334, (2008) »PubMed
- Yeh J,et al., Br Med J., 301, 669, (1990)
- Tailor S,et al., Arch Dermatol., 132, 350-352, (1996) »PubMed
- Neuvonen P,et al., J Am Acad Dermatol., 33, 134-135, (1995) »PubMed
- Kroemer HK,et al., Arch Pharmacol., 348, 332-337, (1993)
- Sachs M,et al., Clin Infect Dis., 16, 400-403, (1993) »PubMed
- Buggia I,et al., Anticancer Res., 16, 2083-2088, (1996) »PubMed
- Hardin TC,et al., Pharmacother., 17, 195, (1997)
- Sriwiriyajan S,et al., Biopharm Drug Dispos., 32, 168-174, (2011) »PubMed
- Bonay M,et al., Drug Safety., 9, 309-311, (1993) »PubMed
- Spina E,et al., Ther Drug Monit., 19, 535-538, (1997) »PubMed
- Pilheu JA,et al., Medicina., 49, 43-47, (1989) »PubMed
- Jaruratanasirikul S,et al., Eur J Clin Pharmacol., 63, 451-456, (2007) »PubMed
- Hynninen VV,et al., Antimicrob Agents Chemother., 53, 587-592, (2009) »PubMed
- Harousseau JL,et al., Antimicrob Agents Chemother., 44, 1887-1893, (2000) »PubMed
- Glasmacher A,et al., Mycoses., 42, 591-600, (1999) »PubMed
- ヒドロキシプロピル-β-シクロデキストリンのがん原性試験(イトリゾール内用液1%:2006.7.26承認、CTD2.6.6.8)
- 丁宗鉄ほか, 日本化学療法学会雑誌, 54 (Suppl.1), 6-17, (2006)
- イトラコナゾール内用液の国内第I相試験(イトリゾール内用液1%:2006.7.26承認、CTD2.7.2.2)
- イトラコナゾール内用液単独投与における薬物動態の検討(イトリゾール内用液1%:2011.9.26承認、CTD2.7.2.3.2)
- 社内資料:生物学的同等性試験(イトラコナゾール内用液1%「VTRS」)
- 小口勝司ほか, 基礎と臨床, 25, 397-407, (1991)
- 山口英世ほか, 日本化学療法学会雑誌, 54 (Suppl.1), 18-31, (2006)
- L.Willems,et al., J Clin Pharm Ther., 26, 159-169, (2001)
- イトラコナゾールの蛋白結合率の検討(イトリゾール内用液1%:2006.7.26承認、CTD2.6.4.4)
- 薬物動態試験(イトリゾール内用液1%:2006.7.26承認、CTD2.4.3)
- 第十八改正 日本薬局方解説書, C-625-633, (2021), (廣川書店)
- 三上襄ほか, Chemotherapy., 42, 290-296, (1994) »DOI
- Wilcox CM,et al., J Infect Dis., 176, 227-232, (1997) »PubMed
- イトラコナゾール内用液の国内第III相試験(イトリゾール内用液1%:2011.9.26承認、CTD2.7.6.1)
- Menichetti F,et al., Clin Infect Dis., 28, 250-255, (1999) »PubMed
- イトラコナゾール内用液の海外第III相試験(イトリゾール内用液1%:2011.9.26承認、CTD2.7.6.3)
- イトラコナゾール内用液の海外臨床第III相試験(イトリゾール内用液1%:2011.9.26承認、CTD2.7.6.4)
- Vanden Bossche H,et al., Mycoses., 32 (Suppl.1), 35-52, (1989)
- 平谷民雄ほか, Jpn J Antibiotics., 44, 580-587, (1991) »DOI
- 内田勝久ほか, Jpn J Antibiotics., 44, 562-570, (1991) »DOI
- Van Cutsem J, Mycoses., 32 (Suppl.1), 7-13, (1989)
- Van Cutsem J,et al., Rev Infect Dis., 9 (Suppl.1), 15-32, (1987)
- Uchida K,et al., Microbiol Immunol., 50, 679-685, (2006) »PubMed
- Ishibashi H,et al., J Antimicrob Chemother., 59, 317-320, (2007) »PubMed
- Van Cutsem J, Mycoses., 32 (Suppl.1), 14-34, (1989)
- 内田勝久ほか, Jpn J Antibiotics., 44, 588-599, (1991) »DOI
24. 文献請求先及び問い合わせ先
文献請求先
ヴィアトリス製薬合同会社
メディカルインフォメーション部
〒106-0041
東京都港区麻布台一丁目3番1号
電話:フリーダイヤル 0120-419-043
製品情報問い合わせ先
ヴィアトリス製薬合同会社
メディカルインフォメーション部
〒106-0041
東京都港区麻布台一丁目3番1号
電話:フリーダイヤル 0120-419-043
26. 製造販売業者等
26.1 製造販売元
ヴィアトリス・ヘルスケア合同会社
東京都港区麻布台一丁目3番1号
26.2 販売元
ヴィアトリス製薬合同会社
東京都港区麻布台一丁目3番1号
その他の説明
使用方法
この容器は、誤用を防ぐために安全キャップになっております。
また、使用後に薬液が固まって、再度キャップが開けにくくなることがあります。
また、使用後に薬液が固まって、再度キャップが開けにくくなることがあります。
開け方
手のひらで、キャップを上から押さえたまま(操作[1])反時計回りに回して(操作[2])キャップを外します。
閉め方
必ず瓶口の周辺に付いた薬液を紙タオルなどできれいにふきとり、キャップが止まるまで時計回りに回して閉めます。