医薬品情報
| 総称名 | エルロチニブ |
|---|---|
| 一般名 | エルロチニブ塩酸塩 |
| 欧文一般名 | Erlotinib Hydrochloride |
| 製剤名 | エルロチニブ塩酸塩錠 |
| 薬効分類名 | 抗悪性腫瘍剤 上皮増殖因子受容体(EGFR)チロシンキナーゼ阻害剤 |
| 薬効分類番号 | 4291 |
| ATCコード | L01EB02 |
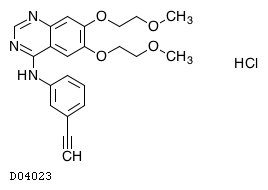
| KEGG DRUG |
D04023
エルロチニブ塩酸塩
|
| KEGG DGROUP |
DG03162
EGFR阻害薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年12月 改訂(第2版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| エルロチニブ錠25mg「NK」 (後発品) | Erlotinib Tablets 25mg「NK」 | 日本化薬 | 4291016F1039 | 438.4円/錠 | 劇薬, 処方箋医薬品注) |
| エルロチニブ錠100mg「NK」 (後発品) | Erlotinib Tablets 100mg「NK」 | 日本化薬 | 4291016F2035 | 1469.5円/錠 | 劇薬, 処方箋医薬品注) |
1. 警告
1.1 本剤は、緊急時に十分に対応できる医療施設において、がん化学療法に十分な知識・経験を持つ医師のもとで、電子添文を参照して、適切と判断される症例についてのみ投与すること。適応患者の選択にあたっては、本剤及び併用薬剤の電子添文を参照して十分に注意すること。また、治療開始に先立ち、患者又はその家族に本剤の有効性及び危険性(特に、間質性肺疾患の初期症状、服用中の注意事項、死亡に至った症例があること等に関する情報)、非小細胞肺癌、膵癌の治療法等について十分に説明し、同意を得てから投与すること。[8.1参照]
1.2 本剤の投与により間質性肺疾患があらわれることがあるので、初期症状(息切れ、呼吸困難、咳嗽、発熱等)の確認及び胸部X線検査の実施等、観察を十分に行うこと。異常が認められた場合には投与を中止し、適切な処置を行うこと。また、国内臨床試験において、間質性肺疾患により死亡に至った症例があることから、治療初期は入院又はそれに準ずる管理の下で、間質性肺疾患等の重篤な副作用発現に関する観察を十分に行うこと。[8.3、9.1.2、9.1.3、11.1.1、15.1.1参照]
1.3 膵癌を対象とした本剤とゲムシタビンとの併用療法の国内臨床試験における間質性肺疾患の発現率(8.5%)、特定使用成績調査における間質性肺疾患の発現率(6.2%)は、海外第III相試験(3.5%)や、非小細胞肺癌を対象とした本剤単独療法の国内臨床試験(5.3%)及び二次治療以降の特定使用成績調査(全例調査)(4.3%)と比べて高いこと等から、膵癌に使用する場合には、「17.臨床成績」の項の国内臨床試験における対象患者を参照して、本剤の有効性及び危険性を十分に理解した上で、投与の可否を慎重に判断するとともに、以下の点も注意すること。[8.3、9.1.2、9.1.3、11.1.1、15.1.1参照]
1.3.1 本剤投与開始前に、胸部CT検査及び問診を実施し、間質性肺疾患の合併又は既往歴がないことを確認した上で、投与の可否を慎重に判断すること。
1.3.2 本剤投与開始後は、胸部CT検査及び胸部X線検査をそれぞれ定期的に実施し、肺の異常所見の有無を十分に観察すること。
2. 禁忌
次の患者には投与しないこと
本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
5. 効能または効果に関連する注意
<効能共通>
5.1 非小細胞肺癌及び膵癌に対する術後補助化学療法として本剤を使用した場合の有効性及び安全性は確立していない。
<非小細胞肺癌>
5.2 EGFR遺伝子変異陽性の切除不能な再発・進行性で、がん化学療法未治療の非小細胞肺癌の場合には、臨床試験に組み入れられた患者の遺伝子変異の種類等について、「17.臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。
<治癒切除不能な膵癌>
5.3 「17.臨床成績」の項の内容を熟知し、国内臨床試験に組み入れられた患者背景や本剤の有効性及び安全性を十分に理解した上で適応患者の選択を慎重に行うこと。
6. 用法及び用量
<非小細胞肺癌>
通常、成人にはエルロチニブとして150mgを食事の1時間以上前又は食後2時間以降に1日1回経口投与する。なお、患者の状態により適宜減量する。
<治癒切除不能な膵癌>
ゲムシタビンとの併用において、通常、成人にはエルロチニブとして100mgを食事の1時間以上前又は食後2時間以降に1日1回経口投与する。なお、患者の状態により適宜減量する。
7. 用法及び用量に関連する注意
<効能共通>
7.1 副作用の発現により用量を変更する場合には、50mgずつ減量すること。
7.2 高脂肪、高カロリーの食後に本剤を投与した場合、AUCが増加するとの報告がある。食事の影響を避けるため食事の1時間前から食後2時間までの間の服用は避けること。[16.2.2参照]
<非小細胞肺癌>
<治癒切除不能な膵癌>
7.4 本剤をゲムシタビン以外の抗悪性腫瘍剤との併用で使用した場合や本剤を化学放射線療法として使用した場合の有効性及び安全性は確立していない。
7.5 「17.臨床成績」の項の内容を十分に理解した上で本剤を使用すること。
7.6 国内第II相臨床試験(JO20302/JO21097試験)の基準を目安として、休薬、減量又は中止を考慮すること。
| 副作用 | Grade注1) | 休薬基準注2) | 投与再開時の用量注3)注4) |
| 間質性肺疾患 | Gradeは問わない | 疑われる症状が発現した場合には、直ちに休薬、その後CT検査を含めた適切な検査を実施し、医学的に間質性肺疾患と判断した場合には投与中止 | 医学的に間質性肺疾患と判断されなかった場合には、同一用量で投与再開 |
| 角膜炎 | 2 | 2週間以上継続する場合はGrade 1以下になるまで休薬 | 同一用量で再開。ただし、主治医判断で50mgに減量して再開可能。 |
| 3 | Grade 1以下になるまで休薬 | 50mgで再開 | |
| 下痢 | 2 | その症状が忍容できない場合はGrade 1以下に回復するまで休薬 | 同一用量で再開。ただし、主治医判断で50mgに減量して再開可能。 |
| 3 | Grade 1以下になるまで休薬 | 50mgで再開 | |
| 発疹(ざ瘡/ざ瘡様) | 2 | その症状が忍容できない場合はGrade 1以下に回復するまで休薬 | 同一用量で再開。ただし、主治医判断で50mgに減量して再開可能。 |
| 3 | Grade 1以下になるまで休薬。ただし、主治医が継続投与可能と判断した場合は同一用量で投与可能。 | 50mgで再開 | |
| AST又はALT | 3 | Grade 2以下になるまで休薬 | 50mgで再開 |
| 上記以外の非血液毒性 | 2 | 4週間以上継続した場合はGrade 1以下になるまで休薬。ただし、主治医が継続投与可能と判断した場合は同一用量で投与可能。 | 50mgで再開 |
| 3 | Grade 1以下になるまで休薬。ただし、主治医が継続投与可能と判断した場合は同一用量で投与可能。 | 50mgで再開 | |
| 全ての非血液毒性注5) | 4 | 投与の中止 | − |
| 血液毒性 | 4 | Grade 2以下になるまで休薬 | 同一用量で再開 |
8. 重要な基本的注意
<効能共通>
8.1 本剤を投与するにあたっては、本剤の副作用について患者に十分に説明すること。[1.1参照]
8.2 本剤の投与により、間質性肺疾患、発疹、下痢、角膜穿孔、角膜潰瘍等の副作用があらわれることがある。これらの発現又は症状の増悪が疑われた場合には、速やかに医療機関を受診するよう患者を指導すること。
8.3 本剤の投与により間質性肺疾患があらわれることがあるので、初期症状(息切れ、呼吸困難、咳嗽、発熱等の有無)を十分に観察し、胸部X線検査を行うこと。また、必要に応じて胸部CT検査、動脈血酸素分圧(PaO2)、動脈血酸素飽和度(SpO2)、肺胞気動脈血酸素分圧較差(A-aDO2)、肺拡散能力(DLCO)等の検査を行うこと。[1.2、1.3、9.1.2、9.1.3、11.1.1、15.1.1参照]
8.5 重度の皮膚障害があらわれることがあるので、必要に応じて皮膚科を受診するよう患者に指導すること。[11.1.5参照]
<治癒切除不能な膵癌>
8.6 ゲムシタビンとの併用により、骨髄抑制等の副作用が高頻度に発現するため、投与中は定期的に臨床検査を行い、異常が認められた場合には適切な処置を行うこと。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 消化管潰瘍、腸管憩室のある患者又はその既往歴のある患者
9.1.2 肺感染症等のある患者又はその既往歴のある患者
9.1.3 間質性肺疾患のある患者又はその既往歴のある患者
9.3 肝機能障害患者
9.4 生殖能を有する者
妊娠する可能性のある女性には、本剤投与中及び最終投与後2週間において避妊する必要性及び適切な避妊法について説明すること。[9.5参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。やむを得ず投与する場合は、本剤投与による胎児へのリスク、妊娠中断の危険性について患者に十分説明すること。妊婦における使用経験はない。また、動物実験では、流産(ウサギ)、胚致死及び生存胎児数減少(ウサギ、ラット)が報告されている。また、胎児中(ラット)に移行することが報告されている。[9.4参照]
9.6 授乳婦
授乳しないことが望ましい。ヒトでの乳汁移行に関するデータはないが、動物実験(ラット)で乳汁中に移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。一般に生理機能が低下していることが多い。
10. 相互作用
相互作用序文
薬物代謝酵素用語
CYP
薬物代謝酵素用語
CYP3A4
薬物代謝酵素用語
CYP1A2
薬物代謝酵素用語
UGT1A1
10.2 併用注意
| CYP3A4阻害剤 ケトコナゾール イトラコナゾール クラリスロマイシン テリスロマイシン インジナビル ネルフィナビル リトナビル サキナビル 等 グレープフルーツジュース | ケトコナゾールと本剤を併用すると、エルロチニブのAUC(中央値)が86%、Cmax(中央値)が69%上昇した。 | CYP3A4阻害剤との併用により、エルロチニブの代謝が阻害され血漿中濃度が増加する可能性がある。 |
| CYP3A4誘導剤 リファンピシン フェニトイン カルバマゼピン フェノバルビタール セイヨウオトギリソウ(セント・ジョーンズ・ワート)含有食品 等 | リファンピシンと本剤を併用すると、エルロチニブのAUC(中央値)が69%低下した。 | CYP3A4誘導剤等との併用により、エルロチニブの代謝が亢進し血漿中濃度が低下する可能性がある。 |
| 塩酸シプロフロキサシン | 塩酸シプロフロキサシンと本剤を併用すると、エルロチニブのAUC(幾何平均値)が39%、Cmax(幾何平均値)が17%上昇した。 | CYP1A2及びCYP3A4を阻害する薬剤との併用により、エルロチニブの代謝が阻害され血漿中濃度が増加する可能性がある。 |
| プロトンポンプ阻害剤 オメプラゾール 等 | オメプラゾールと本剤を併用すると、エルロチニブのAUC(幾何平均値)が46%低下した。 | 持続的な胃内pHの上昇により、本剤の溶解度が低下し吸収が低下する可能性がある。 |
| H2受容体拮抗剤 ラニチジン 等 | ラニチジンと本剤を併用すると、エルロチニブのAUC(幾何平均値)が33%低下した。 | 胃内pHの上昇により、本剤の溶解度が低下し吸収が低下する可能性がある。 |
| 抗凝血薬 ワルファリン 等 | INR増加や胃腸出血等があらわれたとの報告がある。本剤とワルファリンを併用中の患者では、定期的に血液凝固能検査(プロトロンビン時間又はINR等)を行うこと。 | 機序不明 |
| タバコ(喫煙) | 喫煙によりエルロチニブのAUC(平均値)が64%低下した。 | 喫煙によるCYP1A2の誘導により、エルロチニブの代謝が亢進し血漿中濃度が低下する可能性がある。 |
11. 副作用
11.1 重大な副作用
注1)注2)
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 間質性肺疾患(4.4%、6.4%)
11.1.2 肝炎(0.1%未満、頻度不明)、肝不全(0.1%未満、頻度不明)、肝機能障害(1.6%、4.6%)
11.1.3 重度の下痢(1.1%、0.7%)
重度の下痢、悪心、嘔吐、食欲不振により脱水症状をきたし、腎不全に至った症例が報告されている。必要に応じて電解質や腎機能検査を行い、患者状態により止瀉薬(ロペラミド等)の投与、補液等の適切な処置を行うとともに、本剤の減量又は休薬を考慮すること。
11.1.4 急性腎障害(0.1%未満、0.2%)
急性腎障害等の重篤な腎機能障害があらわれることがある。
11.1.5 重度の皮膚障害
ざ瘡様皮疹等の発疹(6.3%、4.1%)、爪囲炎等の爪の障害(0.8%、0.9%)、皮膚乾燥・皮膚亀裂(0.3%、0.2%)、皮膚潰瘍(0.2%、頻度不明)、そう痒症(0.1%、0.1%)等があらわれることがある。また、重度の皮膚障害発現後に、蜂巣炎、敗血症等の感染症を合併した症例も報告されている。[8.5参照]
11.1.6 皮膚粘膜眼症候群(Stevens-Johnson症候群)(0.1%未満、頻度不明)、中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(頻度不明、頻度不明)、多形紅斑(0.1%未満、0.2%)
皮膚粘膜眼症候群、中毒性表皮壊死融解症、多形紅斑等の重篤な水疱性・剥脱性の皮膚障害があらわれることがある。
11.1.7 消化管穿孔(0.1%未満、0.2%)、消化管潰瘍(0.4%、0.7%)、消化管出血(0.3%、1.4%)
11.1.8 角膜穿孔(0.1%未満、頻度不明)、角膜潰瘍(0.1%未満、0.1%)
眼痛等の異常が認められた場合には本剤の投与を中止するなど、適切な処置を行うこと。[15.2.2参照]
注1)非小細胞肺癌における頻度はEGFR遺伝子変異陽性例の国内第II相臨床試験(一次化学療法)、国内第I相臨床試験、国内第I相継続試験及び国内第II相臨床試験(二次治療以降)、特定使用成績調査(全例調査)(二次治療以降)に基づき記載した。治癒切除不能な膵癌における頻度は、国内第II相臨床試験、特定使用成績調査に基づき記載した。
注2)「重大な副作用」の発現頻度は、非小細胞肺癌、治癒切除不能な膵癌の順に記載した。
11.2 その他の副作用
| 5%以上 | 1%以上5%未満 | 1%未満 | 頻度不明 | |
| 皮膚注3) | ざ瘡様皮疹等の発疹(61.6%)、皮膚乾燥・皮膚亀裂(9.3%)、爪囲炎等の爪の障害(8.8%) | そう痒症、紅斑 | 皮膚剥脱、脱毛、皮膚潰瘍、皮下出血、皮膚色素沈着、皮膚血管炎(IgA血管炎等)、光線過敏症 | 男性型多毛症 |
| 眼注4) | 結膜炎 | 眼乾燥、角膜炎、眼瞼炎、睫毛/眉毛の異常、眼そう痒症、角膜びらん、眼脂、霧視、流涙増加、ぶどう膜炎 | ||
| 肝臓 | ビリルビン上昇、ALT上昇、AST上昇 | Al-P上昇、LDH上昇、γ-GTP上昇 | ||
| 腎臓 | クレアチニン上昇、BUN上昇、血尿、尿沈渣異常 | |||
| 血液 | 貧血 | 血小板減少、白血球増加、白血球減少、好中球減少、リンパ球減少、好中球増加、INR上昇 | ||
| 消化器 | 下痢(22.8%)、口内炎(9.6%)、食欲不振(7.0%) | 悪心、嘔吐、口唇炎、腹痛、便秘 | 胃炎、口内乾燥、消化不良、腸炎、アミラーゼ増加、食道炎 | |
| 呼吸器 | 鼻出血、呼吸困難、咳嗽、喀血、口腔咽頭痛 | |||
| 精神神経系 | 味覚異常 | 不眠症、頭痛、浮動性めまい、末梢性ニューロパチー、意識障害 | ||
| その他 | 感染症(皮膚感染、肺感染、上気道感染等)、倦怠感、発熱、疲労 | 電解質異常、体重減少、血中アルブミン減少、CRP上昇、浮腫、血圧上昇、筋肉痛、筋痙縮・筋痙攣、血糖値上昇、総蛋白減少、脱水、血栓・塞栓 |
| 5%以上 | 1%以上5%未満 | 1%未満 | 頻度不明 | |
| 皮膚注3) | ざ瘡様皮疹等の発疹(65.3%)、爪囲炎等の爪の障害(11.6%)、皮膚乾燥・皮膚亀裂(10.8%)、そう痒症(8.5%)、脱毛(5.9%) | 手足症候群、皮膚色素沈着、皮膚剥脱 | 紅斑 | 男性型多毛症、光線過敏症、皮膚血管炎(IgA血管炎等) |
| 眼注4) | 角膜炎、結膜炎、眼乾燥、眼脂、霧視、眼瞼炎、睫毛/眉毛の異常 | ぶどう膜炎 | ||
| 肝臓 | ALT上昇(9.3%)、AST上昇(8.4%) | γ-GTP上昇、Al-P上昇、ビリルビン上昇、LDH上昇 | ||
| 腎臓 | 血尿、尿中蛋白陽性、クレアチニン上昇、BUN上昇 | |||
| 血液 | 血小板減少(17.8%)、白血球減少(17.2%)、貧血(17.0%)、好中球減少(16.2%) | リンパ球減少、血小板増加、単球減少、好酸球減少 | 白血球増加 | |
| 消化器 | 食欲不振(20.9%)、下痢(20.9%)、口内炎(14.1%)、悪心(13.5%)、便秘(6.6%)、嘔吐(5.8%) | 血中アミラーゼ増加、口唇炎、腹痛 | 腹部膨満、口内乾燥、食道炎、腸炎、胃炎、消化不良 | |
| 呼吸器 | 鼻出血、咳嗽 | 呼吸困難 | ||
| 精神神経系 | 味覚異常(8.2%) | 不眠症 | 浮動性めまい、末梢性ニューロパチー、うつ病、頭痛 | |
| その他 | 疲労(11.7%)、発熱(8.1%)、血中アルブミン減少(5.6%)、倦怠感(5.5%)、体重減少(5.4%)、感染症(皮膚感染、肺感染、上気道感染等)(5.1%) | 電解質異常、CRP上昇、総蛋白減少、血糖値上昇、浮腫、血圧上昇 | KL-6増加、血中コレステロール減少、悪寒 |
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 国内で実施した非小細胞肺癌を対象とした特定使用成績調査(全例調査)における多変量解析の結果、喫煙歴有、全身状態不良(ECOG Performance Status:2-4)、間質性肺疾患の合併又は既往、肺感染症の合併又は既往、肺気腫又は慢性閉塞性肺疾患の合併又は既往が間質性肺疾患発現・増悪の危険因子として検出された(2013年2月集計時)。また、間質性肺疾患が発現した患者集団を対象とした多変量解析の結果、全身状態不良(ECOG Performance Status:2-4)、正常肺占有率の低値、蜂巣肺の併存が間質性肺疾患の予後不良因子(転帰死亡)として検出された(2015年9月集計時)。国内で実施した膵癌を対象とした特定使用成績調査(全例調査)における多変量解析の結果、肺疾患の合併又は既往、原疾患の転移臓器数が間質性肺疾患発現・増悪の危険因子として検出された(2014年8月集計時)。[1.2、1.3、8.3、9.1.2、9.1.3、11.1.1参照]
15.1.2 海外において、EGFR遺伝子変異の有無を問わず実施した化学療法未治療の進行性非小細胞肺癌患者を対象とした2つの第III相臨床試験が実施され、プラチナ製剤を含む化学療法(ゲムシタビン/シスプラチン、及びパクリタキセル/カルボプラチン)と本剤の同時併用にて臨床的な有用性は示されなかったとの報告がある(外国人データ)。[7.3参照]
15.2 非臨床試験に基づく情報
15.2.1 ヒト肝ミクロソーム及びヒト遺伝子組換え型のUGT1A1を用いた試験においてビリルビンのグルクロン酸抱合の阻害が認められていることから、Gilbert症候群等のグルクロン酸抱合異常又はUGT1A1発現量が低下している患者では、血清ビリルビン濃度が上昇するおそれがある。また、消失過程で主にUGT1A1によるグルクロン酸抱合を受けるイリノテカン塩酸塩水和物等の薬物との相互作用の可能性がある。[10.参照]
15.2.2 イヌを用いた反復経口投与毒性試験において、高用量の50mg/kg/日群で角膜の異常(浮腫、混濁、潰瘍、穿孔)が認められている。[11.1.8参照]
15.2.3 ラット又はイヌを用いた反復経口投与毒性試験において皮膚(毛包の変性及び炎症:ラット、発赤及び脱毛:イヌ)、肝臓(肝細胞壊死:ラット)、消化管(下痢:イヌ)、腎臓(腎乳頭壊死及び尿細管拡張:ラット及びイヌ)及び卵巣(萎縮:ラット)への影響が報告されている。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与及び反復投与
固形癌患者15例にエルロチニブとして50、100又は150mg注4)を単回経口投与し、引き続き3日目から23日目まで50、100又は150mg注4)を1日1回の用量で反復経口投与を実施した時の薬物動態パラメータを単回投与の結果と併せて表に示した。単回投与時の薬物動態パラメータから、エルロチニブの体内動態には線形性が認められた1)。
| AUC0-24h(hr・ng/mL) | Cmax(ng/mL) | Tmax(hr) | t1/2(hr) | ||
| 50mg/日注4) | 1日目注1) | 3266(54) | 194(44) | 5.0(72) | 14.8(71) |
| 23日目注1) | 15844(50) | 820(42) | 4.3(114) | 23.6(67) | |
| 100mg/日 | 1日目注2) | 7705(46) | 571(47) | 6.0(150) | 18.0(62) |
| 23日目注3) | 14623(48) | 1023(31) | 3.0(67) | 15.6(56) | |
| 150mg/日 | 1日目注2) | 12845(29) | 958(48) | 6.0(149) | 25.9(36) |
| 23日目注2) | 42679(48) | 2384(39) | 1.8(22) | 27.2(33) | |
16.1.2 母集団薬物動態解析の成績
海外において591例の固形癌患者にエルロチニブを投与したときの母集団薬物動態解析の結果では、クリアランスについて人種、性別は影響を及ぼす因子ではなかった2)(外国人データ)。
16.1.3 生物学的同等性試験
健康成人男性15名にエルロチニブ錠25mg「NK」とタルセバ錠25mgを、2剤2期クロスオーバー試験法によりそれぞれ1錠(エルロチニブとして25mg)空腹時単回経口投与して血漿中濃度を測定した。多重性を調整した中間解析を行った結果、AUCt、Cmaxから算出した検定統計量が、中間解析時の有意水準に対応する棄却限界値を上回ったことから、両剤の生物学的同等性が確認された3)。
| 判定パラメータ | 参考パラメータ | |||
| AUCt(ng・hr/mL) | Cmax(ng/mL) | Tmax(hr) | t1/2(hr) | |
| エルロチニブ錠25mg「NK」 | 4110±1320 | 329±90 | 2.53±1.06 | 9.54±4.76 |
| タルセバ錠25mg | 4190±1310 | 354±87 | 2.80±1.01 | 9.76±5.69 |
血漿中濃度並びにAUCt、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.2 吸収
16.3 分布
エルロチニブは血漿中のアルブミン及びα1-酸性糖蛋白と結合する。ヒトにおける血漿蛋白結合率は、3.8μg/mLの濃度において約95%であった。また、ワルファリン及びプロプラノロールの共存によっても結合率の変化は認められなかった6)(in vitro)。
エルロチニブの血球移行率の計算値は、ヘマトクリットが0.48の時34.2%であった6)(in vitro)。
白色系ラットにおける、14C-エルロチニブ経口投与後の放射能は、各組織に比較的速やかに分布したが、脳への移行は少なかった。最高濃度到達後の組織中の放射能は速やかに消失し、投与後72時間ではほとんどの組織において定量限界以下となった。有色系ラットにおける14C-エルロチニブ経口投与後の放射能分布は白色系ラットに類似したが、メラニン色素を含む組織(ブドウ膜系、有色皮膚)において放射能が高かった7)。
16.4 代謝
16.5 排泄
健康成人4人に14C-エルロチニブ100mg注4)を単回経口投与後264時間(11日間)で、投与放射能のうち約91%が回収され、尿中に8%、糞中に83%の放射能が排泄された。また、尿及び糞中に排泄されたエルロチニブは投与量の2%未満であった9)(外国人データ)。
注4)承認された用法・用量は、非小細胞肺癌ではエルロチニブとして150mgを1日1回、膵癌では100mgを1日1回である。
16.8 その他
エルロチニブ錠100mg「NK」は、「含量が異なる経口固形製剤の生物学的同等性試験ガイドライン(令和2年3月19日薬食審査発0319第1号 別紙2)」に基づき、エルロチニブ錠150mg「NK」注5)を標準製剤とした溶出試験の結果、溶出挙動は同等と判定され、生物学的に同等とみなされた11)。
注5)生物学的同等性試験でタルセバ錠150mgとの同等性が確認された。
17. 臨床成績
17.1 有効性及び安全性に関する試験
<がん化学療法未治療の非小細胞肺癌>
17.1.1 国内第II相試験
化学療法未治療のEGFR遺伝子変異(Exon19の欠失変異又はExon21のL858R変異)を有する進行又は再発の非小細胞肺癌を対象としたエルロチニブ単独療法の国内第II相臨床試験(JO22903)における有効性評価対象例102例の成績を以下に示す。
| 項目注1) | JO22903(102例) |
| 無増悪生存期間中央値 (95%信頼区間) | 11.8ヵ月 (9.7ヵ月-推定不能) |
| 奏効率注2) | 78.4%(80/102例) |
| 病勢コントロール率注3) | 95.1%(97/102例) |
| 奏効期間中央値 (95%信頼区間) | 11.1ヵ月 (9.4ヵ月-推定不能) |
注1)カットオフ日:2011年9月1日
注2)RECIST(Ver.1.0)ガイドラインによる判定(CR+PR)
注3)RECIST(Ver.1.0)ガイドラインによる判定(CR+PR+SD)
安全性評価対象例103例中103例(100%)に副作用が認められた。主な副作用は、発疹85例(82.5%)、下痢82例(79.6%)、皮膚乾燥79例(76.7%)、爪囲炎68例(66.0%)、そう痒症66例(64.1%)、口内炎64例(62.1%)等であった。
17.1.2 海外第III相試験
化学療法未治療のEGFR遺伝子変異(Exon19の欠失変異又はExon21のL858R変異)を有する進行又は再発の非小細胞肺癌を対象にエルロチニブ投与群と化学療法注4)群を比較した第III相臨床試験(ML20650)における有効性評価対象例153例の成績を以下に示す12)(外国人データ)。
| 項目注5) | エルロチニブ投与群 | 化学療法群 | HR(ハザード比)注6) [95%信頼区間] | p値 |
| 無増悪生存期間 (中央値) | 9.4ヵ月 (77例) | 5.2ヵ月 (76例) | 0.42 [0.27-0.64] | <0.0001注7) |
| 奏効率注2) | 54.5% (42/77例) | 10.5% (8/76例) | − | <0.0001注8) |
注4)化学療法:シスプラチン+ドセタキセル又はシスプラチン+ゲムシタビン(シスプラチンをカルボプラチンへ変更しても良い。)
注5)カットオフ日:2010年8月2日
注6)層化調整しないCox回帰モデルにおけるハザード比
注7)非層別Log-rank検定
注8)カイ2乗検定
無増悪生存期間のKaplan-Meier曲線
エルロチニブ投与群の安全性評価対象例75例中69例(92.0%)に副作用が認められた。主な副作用は、下痢43例(57.3%)、発疹37例(49.3%)等であった。
17.1.3 国際共同第Ib/III相試験(RELAY試験)
化学療法歴のないEGFR遺伝子変異(Exon19の欠失変異又はExon21のL858R変異)陽性の進行・再発の非小細胞肺癌患者449例(日本人症例211例を含む)を対象に、ラムシルマブ+エルロチニブとプラセボ+エルロチニブとを比較する無作為化二重盲検プラセボ対照試験(第III相パート)を実施した。ラムシルマブ10mg/kg又はプラセボ(2週間に1回)とエルロチニブ150mg(1日1回)を病態の悪化等が認められるまで投与を継続した。主要評価項目である無増悪生存期間において有意な延長を認めた。1年無増悪生存率はラムシルマブ+エルロチニブ投与群で71.9%(95%信頼区間65.1〜77.6)、プラセボ+エルロチニブ投与群で50.7%(95%信頼区間43.7〜57.3)であった13)。
| ラムシルマブ+エルロチニブ投与群 | プラセボ+エルロチニブ投与群 | |
| 症例数 | 224 | 225 |
| イベント発現例数 | 122 | 158 |
| 無増悪生存期間中央値(月) (95%信頼区間) | 19.35 (15.38-21.55) | 12.39 (10.97-13.50) |
| ハザード比 (95%信頼区間) | 0.591(0.461-0.760) P<0.0001 | |
無増悪生存期間のKaplan-Meier曲線(RELAY試験)
エルロチニブとラムシルマブが併用投与された221例(日本人症例105例を含む)において発現した主な有害事象は、感染症(80.5%)、下痢(70.1%)、高血圧(45.2%)、口内炎(41.6%)、蛋白尿(34.4%)等であった。[7.3参照]
<がん化学療法施行後に増悪した非小細胞肺癌>
17.1.4 国内第II相試験
少なくとも前化学療法1レジメンが無効であった非小細胞肺癌を対象としたエルロチニブ単独療法の国内第II相臨床試験(JO16565)における有効性評価対象例60例の成績を以下に示す14)。
| 項目 | JO16565(60例) |
| 奏効率注2) | 28.3%(17/60例) |
| 病勢コントロール率注3) | 50.0%(30/60例) |
| 奏効期間中央値 (95%信頼区間) | 278日 (203日-422日) |
| 無増悪期間中央値 (95%信頼区間) | 77日 (55日-166日) |
安全性評価対象例62例中62例(100.0%)に副作用が認められた。主な副作用は、発疹61例(98.4%)、皮膚乾燥50例(80.6%)、下痢46例(74.2%)、そう痒症45例(72.6%)等であった。
17.1.5 国内第II相試験
少なくとも前化学療法1レジメンが無効であった非小細胞肺癌を対象としたエルロチニブ単独療法の国内第II相臨床試験(JO18396)における有効性評価対象例46例の成績を以下に示す15)。
| 項目 | JO18396(46例) |
| 奏効率注2) | 28.3%(13/46例) |
| 病勢コントロール率注3) | 47.8%(22/46例) |
| 奏効期間中央値 (95%信頼区間) | 推定不能 |
| 無増悪期間中央値 (95%信頼区間) | 75日 (56日-推定不能) |
安全性評価対象例46例中46例(100.0%)に副作用が認められた。主な副作用は、発疹45例(97.8%)、下痢31例(67.4%)、そう痒症30例(65.2%)、皮膚乾燥27例(58.7%)等であった16)。
17.1.6 海外第III相試験
少なくとも前化学療法1レジメンが無効であった非小細胞肺癌731例を対象にエルロチニブ投与群とプラセボ投与群を比較した無作為化二重盲検第III相臨床試験(BR.21)の成績を以下に示す17)(外国人データ)。
| 項目 | エルロチニブ投与群 | プラセボ投与群 | HR(ハザード比)注9) [95%信頼区間] | p値注10) |
| 全生存期間 (中央値) | 6.67ヵ月 (488例) | 4.70ヵ月 (243例) | 0.73 [0.60-0.87] | 0.001 |
| 1年生存率 | 31.2% (488例) | 21.5% (243例) | − | − |
| 無増悪生存期間 (中央値) | 9.71週 (488例) | 8.00週 (243例) | 0.61 [0.51-0.73] | <0.001 |
| 奏効率注2) | 8.9% (38/427例) | 0.9% (2/211例) | − | − |
| 奏効期間 (中央値) | 34.3週 (38例) | − | − | − |
EGFR蛋白発現状況に関する全生存期間の部分集団解析の結果は、EGFR蛋白発現陽性(エルロチニブ群117例、プラセボ群68例)HR=0.68(95%信頼区間;0.49-0.94)、EGFR蛋白発現陰性(エルロチニブ群93例、プラセボ群48例)HR=0.93(95%信頼区間;0.63-1.36)、EGFR蛋白発現不明(エルロチニブ群278例、プラセボ群127例)HR=0.77(95%信頼区間;0.61-0.98)であった。
エルロチニブ投与群の安全性評価対象例485例中481例(99%)に有害事象が認められた。主な有害事象は、ざ瘡様皮疹等の発疹366例(75%)、下痢261例(54%)、食欲不振、疲労各250例(52%)等であった18)。
<治癒切除不能な膵癌>
17.1.7 国内第II相試験
切除不能膵癌を対象とした、エルロチニブとゲムシタビンとの併用療法の国内第II相臨床試験(JO20302/JO21097)における有効性評価対象例106例の成績を以下に示す19)。なお、本試験ではECOG Performance Status(PS):0-2の患者(実際に投与された患者のPSは0、1であった)、間質性肺疾患の合併又は既往歴のない患者を対象とした。
| 項目 | JO20302/JO21097注11) |
| 全生存期間中央値 (95%信頼区間) | 9.23ヵ月 (8.31ヵ月-10.78ヵ月) |
| 無増悪生存期間中央値 (95%信頼区間) | 3.48ヵ月 (2.63ヵ月-3.78ヵ月) |
| 奏効率注2) | 20.3%(13/64例) |
安全性評価対象例106例中、105例(99.1%)に副作用が認められた。主な副作用は、ざ瘡様皮疹等の発疹99例(93.4%)、貧血86例(81.1%)、白血球減少85例(80.2%)、血小板減少、食欲不振各77例(72.6%)、好中球減少74例(69.8%)等であった。
17.1.8 海外第III相試験
切除不能な局所進行又は転移性膵癌569例(登録患者数)を対象にエルロチニブ(100mg投与群261例、150mg投与群24例)又はプラセボ(284例)をゲムシタビン(GEM)と併用した無作為化二重盲検第III相臨床試験(PA.3)の成績を以下に示す20)(外国人データ)。なお、本試験におけるGEMの第一サイクルの投与スケジュールは国内で承認されている用法・用量及び国内第II相臨床試験(JO20302/JO21097)の用法・用量とは異なり、最初の8週間は7週投与、1週休薬であった。
| 項目 | エルロチニブ+GEM群 | プラセボ+GEM群 | HR(ハザード比)注13) [95%信頼区間] | p値注14) |
| 全生存期間中央値 | 6.37ヵ月 (285例) | 5.91ヵ月 (284例) | 0.79 [0.66-0.95] | 0.011 |
| 無増悪生存期間中央値 | 3.75ヵ月 (285例) | 3.55ヵ月 (284例) | 0.77 [0.64-0.92] | 0.004 |
| 奏効率注2) | 8.6% (23/268例) | 8.0% (21/262例) | − | 0.875 |
エルロチニブ100mg投与群の安全性評価対象例259例中256例(99%)に有害事象が認められた。主な有害事象は、疲労188例(73%)、発疹180例(69%)、悪心155例(60%)、食欲不振134例(52%)等であった21)。
18. 薬効薬理
18.1 作用機序
エルロチニブは上皮増殖因子受容体チロシンキナーゼ(EGFR-TK)を選択的に阻害した。IC50は精製全長型EGFR-TKに対し2nMであり、組換え型EGFR細胞内ドメインのチロシンキナーゼに対し1nMであった。一方、他のチロシンキナーゼ、c-src及びv-ablに対する阻害活性は全長型EGFR-TKの1/1000以下であり、ヒトインスリン受容体及びI型インスリン様増殖因子受容体の細胞内ドメインのキナーゼに対する阻害活性は細胞内EGFR-TKの1/10000以下であった。また、エルロチニブによる細胞周期のG1期停止及びアポトーシス誘導作用が確認された22)。
エルロチニブはEGFRチロシンリン酸化の阻害を介し、細胞増殖の抑制及びアポトーシスの誘導に基づき腫瘍増殖を抑制すると推察される。
エルロチニブはEGFRチロシンリン酸化の阻害を介し、細胞増殖の抑制及びアポトーシスの誘導に基づき腫瘍増殖を抑制すると推察される。
18.2 抗腫瘍効果
19. 有効成分に関する理化学的知見
19.1. エルロチニブ塩酸塩
22. 包装
<エルロチニブ錠25mg「NK」>
10錠(PTP10錠×1)
<エルロチニブ錠100mg「NK」>
10錠(PTP10錠×1)
23. 主要文献
- 固形癌患者に対する第I相臨床試験(JO16564)(タルセバ錠:2007年10月19日承認、申請資料概要2.7.2.2.3.1)
- 患者の母集団薬物動態解析(タルセバ錠:2007年10月19日承認、申請資料概要2.5.3.5、2.7.2.2.3.7、2.7.2.3.2.5)
- 社内資料:生物学的同等性試験(25mg)
- 健康成人を対象としたバイオアベイラビリティ及び生物学的同等性試験(タルセバ錠:2007年10月19日承認、申請資料概要2.7.1.2.1)
- 健康成人を対象とした薬物動態に及ぼす食事の影響(タルセバ錠:2007年10月19日承認、申請資料概要2.7.1.2.2)
- 蛋白結合のin vitro評価(タルセバ錠:2007年10月19日承認、申請資料概要2.7.2.2.1.2)
- ラットにおける組織内分布試験(タルセバ錠:2007年10月19日承認、申請資料概要2.6.4.4.1)
- ヒト生体試料を使ったエルロチニブの代謝解明(タルセバ錠:2007年10月19日承認、申請資料概要2.7.2.2.1.1)
- 健康成人を対象とした代謝及び排泄を検討する試験(タルセバ錠:2007年10月19日承認、申請資料概要2.7.2.2.2.1)
- 主要代謝物の血漿中濃度(タルセバ錠:2007年10月19日承認、申請資料概要2.5.3.1-2)
- 社内資料:生物学的同等性試験(100mg)
- 海外第III相臨床試験(ML20650:EURTAC)(タルセバ錠:2013年6月14日承認、審査報告書)
- Nakagawa K,et al., Lancet Oncol., 20 (12), 1655-1669, (2019) »PubMed
- Kubota K,et al., J Thorac Oncol., 3 (12), 1439-1445, (2008) »PubMed
- 進行性/転移性/再発性非小細胞肺癌に対する国内第II相臨床試験(JO18396)の有効性(タルセバ錠:2007年10月19日承認、申請資料概要2.5.4.3、2.5.4.4)
- 進行性/転移性/再発性非小細胞肺癌に対する国内第II相臨床試験(JO18396)の安全性(タルセバ錠:2007年10月19日承認、申請資料概要2.5.5.2)
- 標準療法無効の進行性/転移性非小細胞肺癌に対する海外第III相臨床試験(BR.21)の有効性(タルセバ錠:2007年10月19日承認、申請資料概要2.7.3.3)
- 標準療法無効の進行性/転移性非小細胞肺癌に対する海外第III相臨床試験(BR.21)の安全性(タルセバ錠:2007年10月19日承認、申請資料概要2.7.4.2.1.1.1)
- Okusaka T,et al., Cancer Sci., 102 (2), 425-431, (2011) »PubMed
- 切除不能な局所進行又は転移性膵癌に対するゲムシタビン併用の海外第III相臨床試験(PA.3)(タルセバ錠:2011年7月1日承認、申請資料概要2.5.4.1)
- 海外臨床試験(PA.3)の有害事象(タルセバ錠:2011年7月1日承認、申請資料概要2.7.4.2.1.1.1)
- Moyer JD,et al., Cancer Res., 57 (21), 4838-4848, (1997) »PubMed
- Pollack VA,et al., J Pharmacol Exp Ther., 291 (2), 739-748, (1999) »PubMed
- Higgins B,et al., Anticancer Drugs., 15 (5), 503-512, (2004) »PubMed
- Furugaki K,et al., Oncol Lett., 1 (2), 231-235, (2010) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
日本化薬株式会社
医薬品情報センター
〒100-0005
東京都千代田区丸の内二丁目1番1号
電話:0120-505-282
製品情報問い合わせ先
日本化薬株式会社
医薬品情報センター
〒100-0005
東京都千代田区丸の内二丁目1番1号
電話:0120-505-282
26. 製造販売業者等
26.1 製造販売元
日本化薬株式会社
東京都千代田区丸の内二丁目1番1号