医薬品情報
| 総称名 | リブテンシティ |
|---|---|
| 一般名 | マリバビル |
| 欧文一般名 | Maribavir |
| 製剤名 | マリバビル錠 |
| 薬効分類名 | 抗サイトメガロウイルス化学療法剤 |
| 薬効分類番号 | 6250 |
| ATCコード | J05AX10 |
| KEGG DRUG |
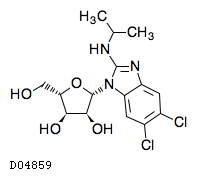
D04859
マリバビル
|
| KEGG DGROUP |
DG01937
抗サイトメガロウイルス薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年9月 改訂(第3版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| リブテンシティ錠200mg | LIVTENCITY tablets 200mg | 武田薬品工業 | 6250055F1027 | 37536.2円/錠 | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
臓器移植(造血幹細胞移植も含む)における既存の抗サイトメガロウイルス療法に難治性のサイトメガロウイルス感染症
5. 効能または効果に関連する注意
5.2 中枢神経系のサイトメガロウイルス感染症及びサイトメガロウイルス網膜炎に対する有効性及び安全性は検討していない。非臨床試験の結果から、本剤は血液脳関門を透過し得るが、中枢神経系への通過量は低いと考えられる1)。
6. 用法及び用量
通常、成人にはマリバビルとして1回400mgを1日2回経口投与する。
7. 用法及び用量に関連する注意
強い又は中程度のCYP3A4誘導剤(リファンピシン及びセイヨウオトギリソウ含有食品を除く)と本剤との併用は避け、代替薬への変更を考慮すること。併用が避けられない場合は、マリバビルとして1回1,200mgまでの増量(1日2回経口投与)を考慮すること。[10.2参照]
8. 重要な基本的注意
本剤による治療中及び治療後に薬剤耐性によるウイルス学的失敗が認められる可能性があるため、サイトメガロウイルスDNA量又はサイトメガロウイルス抗原陽性細胞数等をモニタリングすること。治療に反応しない場合は本剤に対する耐性発現の可能性を考慮し、投与継続の可否を検討すること。本剤に対する耐性を示すウイルス由来のプロテインキナーゼ(UL97)変異がガンシクロビル及びバルガンシクロビルに対する交差耐性をもたらす可能性がある。[18.2.3参照]
9. 特定の背景を有する患者に関する注意
9.3 肝機能障害患者
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないことが望ましい。ラットを用いた受胎能及び胚・胎児発生試験において、本剤の臨床用量における曝露量未満の曝露量で、生存胎児数の減少、早期吸収胚数の増加及び着床後胚死亡の増加が認められている2)。
9.6 授乳婦
授乳しないことが望ましい。マリバビル又はその代謝物のヒトでの乳汁移行性は不明である。ラットを用いた出生前及び出生後の発生毒性試験において、本剤の臨床用量における曝露量未満と推定される曝露量で、母動物の一般毒性発現に伴う出生児の生存率の低下及び身体的発達遅延を伴う体重増加抑制が認められている2)。
9.7 小児等
小児等を対象とした臨床試験成績は得られていない。
10. 相互作用
相互作用序文
本剤は、主に薬物代謝酵素CYP3A4で代謝される。また、本剤はCYP3A4、P-糖蛋白(P-gp)及び乳癌耐性蛋白(BCRP)の阻害作用を有する。
薬物代謝酵素用語
CYP3A4
薬物代謝酵素用語
P-糖蛋白(P-gp)
薬物代謝酵素用語
乳癌耐性蛋白(BCRP)
10.1 併用禁忌
| ガンシクロビル(デノシン) バルガンシクロビル(バリキサ) [2.2、18.2.1参照] | 併用により、これらの薬剤の抗ウイルス作用が阻害されるおそれがある。 | 本剤は、これらの薬剤の活性化又はリン酸化に必要なウイルス由来のUL97を阻害する。 |
| リファンピシン(リファジン) セイヨウオトギリソウ(St.John's Wort、セント・ジョーンズ・ワート)含有食品 [2.3、16.7.2参照] | 本剤とリファンピシンを併用投与したとき、本剤の単独投与時と比較して、本剤のAUCは40%、Cmaxは61%に減少した。 これらの薬剤又は食品との併用により、本剤の血漿中濃度が大きく減少し、本剤の有効性が減弱するおそれがある。 | これらの薬剤又は食品は、本剤の代謝酵素であるCYP3A4を誘導する。 |
10.2 併用注意
| タクロリムス シクロスポリン エベロリムス シロリムス [16.7.2参照] | 本剤とタクロリムスを併用投与したとき、タクロリムスの単独投与時と比較して、タクロリムスのAUCは151%、Cmaxは138%に増加した。 これらの薬剤との併用により、これらの薬剤の血漿中濃度が増加するおそれがあるため、これらの薬剤の血漿中濃度を頻回に(特に本剤投与開始後及び本剤投与中止後に)モニタリングし、必要に応じてこれらの薬剤の用量を調節すること。 | 本剤は、これらの薬剤の代謝及び排泄に必要なCYP3A4及びP-gpを阻害する。 |
| 強い又は中程度のCYP3A4誘導剤 フェニトイン フェノバルビタール カルバマゼピン エファビレンツ リファブチン等 [7.参照] | これらの薬剤との併用により、本剤の血漿中濃度が減少し、本剤の有効性が減弱するおそれがあるため、併用は避け、代替薬への変更を考慮すること。併用が避けられない場合は、本剤の増量を考慮すること。 | これらの薬剤は、本剤の代謝酵素であるCYP3A4を誘導する。 |
| ロスバスタチン | 併用により、ロスバスタチンの血漿中濃度が増加するおそれがあるため、ロスバスタチン関連事象(特にミオパチー及び横紋筋融解症)の発現を注意深く観察すること。 | 本剤は、ロスバスタチンの排泄に必要なBCRPを阻害する。 |
| ジゴキシン [16.7.2参照] | 本剤とジゴキシンを併用投与したとき、ジゴキシンの単独投与時と比較して、ジゴキシンのAUCは121%、Cmaxは125%に増加した。 併用により、ジゴキシンの血漿中濃度が増加するおそれがあるため、ジゴキシンの血漿中濃度をモニタリングし、必要に応じてジゴキシンの用量を減量すること。 | 本剤は、ジゴキシンの排泄に必要なP-gpを阻害する。 |
| サラゾスルファピリジン | 併用により、サラゾスルファピリジンの血漿中濃度が増加するおそれがある。 | 本剤は、サラゾスルファピリジンの排泄に必要なBCRPを阻害する。 |
11. 副作用
11.2 その他の副作用
| 10%以上 | 1%以上10%未満 | |
| 神経系障害 | 味覚障害 | 頭痛 |
| 胃腸障害 | 悪心、嘔吐、下痢 | 上腹部痛 |
| 全身障害 | 疲労 | 食欲不振 |
| 臨床検査 | 免疫抑制剤濃度増加、体重増加 |
15. その他の注意
15.2 非臨床試験に基づく情報
マウスを用いた2年間がん原性試験において、臨床曝露量の約4.0倍の曝露量に相当する用量で、雄マウスの複数の組織に血管腫及び血管肉腫の発生増加が報告されている2)。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人(12例)にマリバビルとして400mgを空腹時に単回経口投与したときの血漿中濃度推移及び薬物動態パラメータは以下のとおりであった3)。
血漿中濃度推移(平均値±標準偏差)
| 投与量 | Cmax(μg/mL) | AUClast(h*μg/mL) | Tmax(h) | t1/2z(h) |
| 400mg | 17.4(27.4) | 92.3(35.3) | 1.25[0.500,4.00] | 5.48(32.91) |
16.1.2 反復投与
日本人の造血幹細胞移植又は固形臓器移植患者[サイトメガロウイルス(CMV)感染/感染症]にマリバビルとして400mgを1日2回反復経口投与したときの定常状態における薬物動態パラメータを母集団薬物動態モデルを用いて推定した4)。
| 投与量 | Cmax,ss(μg/mL) | Ctrough,ss(μg/mL) | AUCτ,ss(h*μg/mL) | t1/2(h) |
| 400mg BID | 29.1(40.6) | 9.89(97.8) | 221(57.1) | 8.72(55.4) |
16.2 吸収
16.2.1 食事の影響
健康成人(30例)にマリバビル400mgを単回経口投与したとき、高脂肪食後投与の空腹時投与に対するCmax、AUC∞及びAUClastの最小二乗幾何平均値の比は、それぞれ0.716、0.878及び0.874であった。また、低脂肪/低カロリー食後投与の空腹時投与に対するCmax、AUC∞及びAUClastの最小二乗幾何平均値の比は、それぞれ0.766、0.847及び0.841であった5)(外国人データ)。
16.3 分布
16.4 代謝
16.4.1 薬物代謝
16.5 排泄
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
マリバビル400mgを単回投与したとき、腎機能正常者(12例)、軽度/中等度腎機能障害者(軽度:クレアチニンクリアランス50mL/min以上80mL/min以下/中等度:クレアチニンクリアランス30mL/min以上50mL/min未満)(10例)及び高度腎機能障害者(高度:クレアチニンクリアランス30mL/min未満)(8例)において、薬物動態パラメータの比較では、軽度/中等度腎機能障害者の腎機能正常群に対するAUC及びCmaxの最小二乗幾何平均値の比は、それぞれ1.084、及び0.959であった。また、高度腎機能障害者の腎機能正常群に対するAUC及びCmaxの最小二乗幾何平均値の比は、それぞれ0.961及び0.930であった8)(外国人データ)。
16.6.2 肝機能障害患者
16.7 薬物相互作用
16.7.1 In vitro試験
(1)トランスポーター
マリバビルはP-gp及びBCRPの基質であり、P-gp(IC50=33.8μM)、BCRP(IC50=7.05μM)及びMATE1(IC50=20.4μM)に対して阻害作用を示した9)。
(2)CYP及びUGT阻害作用
マリバビルは、CYP1A2(IC50=40μM)、CYP2C9(IC50=18μM)、CYP2C19(IC50=35μM)及びUGT1A1(IC50=32.3μM)の阻害作用を示し、CYP3A4に対して時間依存的阻害作用を示した。代謝物VP44469はCYP3A4に対して阻害作用を示した(IC50=30μM)9)。
(3)CYP誘導作用
マリバビルはCYP1A2及びCYP3A4に対して誘導作用を示した9)。
16.7.2 臨床薬物相互作用試験
臨床薬物相互作用試験により、併用薬投与時のマリバビルの薬物動態に及ぼす影響及びマリバビル投与による併用薬の薬物動態に及ぼす影響を示した(外国人データ)。[2.3、10.1、10.2参照]
| 併用薬 | 併用薬 投与方法 | マリバビル 投与方法注1) | 例数 | マリバビルの薬物動態パラメータの最小二乗幾何平均値の比(併用時/非併用時) (90%信頼区間) | |
| AUC | Cmax | ||||
| 抗真菌薬(CYP3A4/5/P-gp阻害剤)10) | |||||
| ケトコナゾール | 400mg SD | 400mg SD | 19 | 1.533 (1.444,1.628) | 1.097 (1.013,1.188) |
| 抗酸菌症薬(CYP誘導剤)11) | |||||
| リファンピシン | 600mg QD | 400mg BID | 14 | 0.398 (0.361,0.440) | 0.612 (0.523,0.717) |
| 制酸剤12) | |||||
| 水酸化アルミニウム/水酸化マグネシウム | 20mL SD | 100mg SD | 15 | 0.891 (0.828,0.958) | 0.837 (0.747,0.939) |
| 併用薬 | 併用薬 投与方法 | 例数 | 併用薬の薬物動態パラメータの最小二乗幾何平均値の比(マリバビル併用時/非併用時) (90%信頼区間) | |
| AUC | Cmax | |||
| 抗真菌薬(CYP2C19基質)13) | ||||
| ボリコナゾール | 200mg BID | 19 | ボリコナゾール 0.93 (0.83,1.05) | ボリコナゾール 1.00 (0.87,1.15) |
| ボリコナゾール-N-オキシド 1.04 (0.99,1.10) | ボリコナゾール-N-オキシド 1.01 (0.93,1.08) | |||
| 感冒薬(CYP2D6基質)14) | ||||
| デキストロメトルファン注2,3) | 30mg SD | 18 | デキストロルファン 0.97 (0.95,1.00) | デキストロルファン 0.94 (0.88,1.01) |
| デキストロメトルファン 0.88 (0.70,1.12) | デキストロメトルファン 0.94 (0.78,1.14) | |||
| ジギタリス配糖体製剤(P-gp基質)14) | ||||
| ジゴキシン注3) | 0.5mg SD | 18 | 1.21 (1.10,1.32) | 1.25 (1.13,1.38) |
| 免疫抑制薬(CYP3A4/P-gp基質)15) | ||||
| タクロリムス | 安定用量 | 20 | 1.51 (1.39,1.65) | 1.38 (1.20,1.57) |
| 併用薬 | 併用薬 投与方法 | 例数 | 薬物動態パラメータの最小二乗幾何平均値の比(マリバビル併用時/非併用時) (90%信頼区間) |
| CYP2C9基質16) | |||
| ワルファリン注4) | 10mg SD | 16 | S-ワルファリン AUC∞比1.01(0.95,1.07) Cmax比1.04(0.96,1.12) |
| CYP3A4基質16) | |||
| ミダゾラム注4) | 0.075mg/kg SD | 16 | ミダゾラム AUC∞比0.89(0.79,1.00) Cmax比0.82(0.70,0.96) |
| 1-ヒドロキシミダゾラム AUC∞比1.06(0.91,1.21) Cmax比0.98(0.71,1.26) | |||
| CYP1A2基質16) | |||
| カフェイン注4) | 2mg/kg SD | 15 | 尿中カフェイン代謝物注5) (投与後12時間までの尿中濃度の比) 0.86(0.80,0.92) |
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験
日本人の造血幹細胞移植又は固形臓器移植におけるサイトメガロウイルス(CMV)感染又は感染症の患者(本剤が投与された被験者41例、このうち直近に投与された抗CMV薬に難治性注1)を示すCMV感染又は感染症3例)を対象注2)に有効性及び安全性を評価する多施設共同、非盲検、単群試験を実施した。定量的ポリメラーゼ連鎖反応(qPCR)又は同等の定量的CMV DNA検査結果によりCMV感染が確認された被験者にマリバビル400mg1日2回を8週間経口投与した。
難治性のCMV感染又は感染症の被験者において、主要評価項目である投与開始後8週時点(8週間の投与完了の有無を問わない)のCMV血症消失の割合は33.3%(1/3例)であった。
本剤が投与された被験者41例において、副作用発現頻度は36.6%(15/41例)であった。主な副作用は、悪心14.6%(6例)、味覚不全4.9%(2例)及び頭痛4.9%(2例)であった17)。[5.1参照]
難治性のCMV感染又は感染症の被験者において、主要評価項目である投与開始後8週時点(8週間の投与完了の有無を問わない)のCMV血症消失の割合は33.3%(1/3例)であった。
本剤が投与された被験者41例において、副作用発現頻度は36.6%(15/41例)であった。主な副作用は、悪心14.6%(6例)、味覚不全4.9%(2例)及び頭痛4.9%(2例)であった17)。[5.1参照]
注1)静注ガンシクロビル、経口バルガンシクロビル、又は静注ホスカルネットによる14日間以上の治療後に、血漿中CMV DNA量の1 log10を超える減少が未達成であると確認された状態。
注2)本剤の承認された効能又は効果は「臓器移植(造血幹細胞移植も含む)における既存の抗サイトメガロウイルス療法に難治性のサイトメガロウイルス感染症」である。
17.1.2 海外第III相試験
造血幹細胞移植又は固形臓器移植における既存の抗CMV薬に難治性注3)のCMV感染又は感染症の患者(無作為化された被験者352例)を対象に有効性及び安全性を評価する多施設共同、無作為化、非盲検、実薬対照試験を実施した。qPCR又は同等の定量的CMV DNA検査結果によりCMV感染が確認された被験者にマリバビル400mg1日2回経口投与又は治験担当医師が選択するIAT(静注ガンシクロビル、経口バルガンシクロビル、静注ホスカルネット及び静注cidofovir(国内未承認)のうち1又は2種類)を8週間投与した。
主要評価項目である投与開始後8週時点(8週間の投与完了の有無を問わない)のCMV血症消失の割合は表のとおりであり、マリバビル群とIAT群との対比較において統計学的に有意な差が検証された。
主要評価項目である投与開始後8週時点(8週間の投与完了の有無を問わない)のCMV血症消失の割合は表のとおりであり、マリバビル群とIAT群との対比較において統計学的に有意な差が検証された。
| マリバビル | IAT | |
| 235例 | 117例 | |
| CMV血症の消失例数(割合) | 131例(55.7%) | 28例(23.9%) |
| 投与群間の割合の差(95%信頼区間)a) | 32.8(22.80,42.74) | |
| 未調整の投与群間の割合の差(95%信頼区間) | 31.8(21.81,41.82) | |
| P値:調整済みa) | p<0.001 | |
副作用発現頻度は60.3%(141/234例)であった。主な副作用は、味覚不全35.9%(84例)、味覚障害8.5%(20例)、悪心8.5%(20例)、嘔吐7.7%(18例)及び免疫抑制剤濃度増加6.0%(14例)であった18)。[5.1参照]
注3)静注ガンシクロビル、経口バルガンシクロビル、静注ホスカルネット、又は静注cidofovir(国内未承認)による14日間以上の治療後に、全血又は血漿中CMV DNA量の1 log10を超える減少が未達成であると確認された状態。
18. 薬効薬理
18.1 作用機序
マリバビルはCMVの増殖に必須であるウイルス由来のUL97遺伝子によりコードされるプロテインキナーゼを阻害することでウイルス増殖を阻害する19)。
18.2 抗ウイルス作用
マリバビルは細胞傷害性を示さない濃度ではCMVの増殖を選択的に阻害し、EC50は0.03〜2.2μMの範囲であった(in vitro)19)。
マリバビルの抗ウイルス活性は、10種類のCMVの臨床分離株に対しても評価されており、DNAハイブリダイゼーション法を用いて測定したEC50(中央値)は0.1μM(範囲:0.03〜0.13μM)であった。4つのヒトCMV糖蛋白質B遺伝子型(gB1、gB2、gB3及びgB4)の臨床分離株の間で、EC50に大きな差は認められなかった(in vitro)19)。
マリバビルの抗ウイルス活性は、10種類のCMVの臨床分離株に対しても評価されており、DNAハイブリダイゼーション法を用いて測定したEC50(中央値)は0.1μM(範囲:0.03〜0.13μM)であった。4つのヒトCMV糖蛋白質B遺伝子型(gB1、gB2、gB3及びgB4)の臨床分離株の間で、EC50に大きな差は認められなかった(in vitro)19)。
18.2.1 併用時の抗ウイルス活性
18.2.2 耐性ウイルス
既存の抗サイトメガロウイルス薬の標的であるUL54変異はガンシクロビル/バルガンシクロビル、ホスカルネット及びcidofovirに対する耐性を付与する可能性があるが、マリバビルはUL54遺伝子にコードされるウイルスポリメラーゼ活性に影響を及ぼさなかった。
UL97変異(L337M、F342Y、V353A、L397R、T409M、H411L/N/Y及びC480F)により、EC50値が約3〜200倍超に上昇し、マリバビルに対する耐性を付与した。
UL27変異(R233S、W362R、W153R、L193F、A269T、V353E、L426F、E22stop、W362stop、218delC、301-311del)により、軽度のマリバビルに対する耐性を付与した(EC50値の5倍未満)(in vitro)19)。
海外第III相試験においては、マリバビルに対する耐性を付与するUL97遺伝子変異が234例中60例(25.6%)に認められた。そのうち18例では試験期間を通してCMV血症消失が認められず、試験期間中にCMV血症消失が認められた42例中39例ではCMV血症が再発した20)。
UL97変異(L337M、F342Y、V353A、L397R、T409M、H411L/N/Y及びC480F)により、EC50値が約3〜200倍超に上昇し、マリバビルに対する耐性を付与した。
UL27変異(R233S、W362R、W153R、L193F、A269T、V353E、L426F、E22stop、W362stop、218delC、301-311del)により、軽度のマリバビルに対する耐性を付与した(EC50値の5倍未満)(in vitro)19)。
海外第III相試験においては、マリバビルに対する耐性を付与するUL97遺伝子変異が234例中60例(25.6%)に認められた。そのうち18例では試験期間を通してCMV血症消失が認められず、試験期間中にCMV血症消失が認められた42例中39例ではCMV血症が再発した20)。
18.2.3 交差耐性
マリバビル及びガンシクロビルのEC50は、F342Yによりそれぞれ4.5及び6.0倍増加し、C480Fによりそれぞれ224倍及び2.3倍増加した(in vitro)20)。[8.参照]
19. 有効成分に関する理化学的知見
19.1. マリバビル
20. 取扱い上の注意
20.1 ボトルキャップの開け方
キャップをボトル本体に強く押しつけたまま(カチカチ音がしない状態まで)左に回して開けること。
21. 承認条件
21.1 医薬品リスク管理計画を策定の上、適切に実施すること。
21.2 国内での治験症例が極めて限られていることから、製造販売後、一定数の症例に係るデータが集積されるまでの間は、全症例を対象に使用成績調査を実施することにより、本剤の使用患者の背景情報を把握するとともに、本剤の安全性及び有効性に関するデータを早期に収集し、本剤の適正使用に必要な措置を講じること。
22. 包装
ボトル
28錠(バラ)
23. 主要文献
- マリバビルの非臨床薬物動態試験成績(2024年6月24日承認、CTD2.6.4.8)
- マリバビルの非臨床毒性試験成績(2024年6月24日承認、CTD2.6.6.9)
- マリバビルの第I相単回投与試験成績(2024年6月24日承認、CTD2.7.6.10)(社内資料)
- マリバビルの薬物動態特性(PBPKモデル解析)(2024年6月24日承認、CTD2.7.2.3)(社内資料)
- マリバビルの食事の影響試験成績(2024年6月24日承認、CTD2.7.6.1)(社内資料)
- マリバビルの薬物動態特性(2024年6月24日承認、CTD2.7.2.3)(社内資料)
- マリバビルのマスバランス試験成績(2024年6月24日承認、CTD2.7.6.6)(社内資料)
- マリバビルの薬物動態特性(内因性要因)(2024年6月24日承認、CTD2.7.2.3)(社内資料)
- マリバビルの非臨床薬物動態試験成績(2024年6月24日承認、CTD2.6.4.7)
- マリバビルの薬物相互作用検討[1](2024年6月24日承認、CTD2.7.6.14)(社内資料)
- マリバビルの薬物相互作用検討[2](2024年6月24日承認、CTD2.7.6.17)(社内資料)
- マリバビルの薬物相互作用検討[3](2024年6月24日承認、CTD2.7.6.3)(社内資料)
- マリバビルの薬物相互作用検討[4](2024年6月24日承認、CTD2.7.6.16)(社内資料)
- マリバビルの薬物相互作用検討[5](2024年6月24日承認、CTD2.7.6.18)(社内資料)
- マリバビルの薬物相互作用検討[6](2024年6月24日承認、CTD2.7.6.15)(社内資料)
- マリバビルの薬物相互作用検討[7](2024年6月24日承認、CTD2.7.6.13)(社内資料)
- マリバビルの国内第III相試験(2024年6月24日承認、CTD2.7.6.24)(社内資料)
- マリバビルの海外第III相試験(2024年6月24日承認、CTD2.7.6.21)(社内資料)
- マリバビルの薬効薬理試験(2024年6月24日承認、CTD2.6.2)(社内資料)
- マリバビルの特別な試験(2024年6月24日承認、CTD2.7.2.4)(社内資料)
24. 文献請求先及び問い合わせ先
文献請求先
武田薬品工業株式会社
くすり相談室
〒103-8668
東京都中央区日本橋本町二丁目1番1号
電話:フリーダイヤル 0120-566-587 受付時間 9:00〜17:30(土日祝日・弊社休業日を除く)
製品情報問い合わせ先
武田薬品工業株式会社
くすり相談室
〒103-8668
東京都中央区日本橋本町二丁目1番1号
電話:フリーダイヤル 0120-566-587 受付時間 9:00〜17:30(土日祝日・弊社休業日を除く)
26. 製造販売業者等
26.1 製造販売元
武田薬品工業株式会社
〒540-8645
大阪市中央区道修町四丁目1番1号