医薬品情報
| 総称名 | アウィクリ |
|---|---|
| 一般名 | インスリン イコデク(遺伝子組換え) |
| 欧文一般名 | Insulin Icodec(Genetical Recombination) |
| 製剤名 | インスリン イコデク(遺伝子組換え) |
| 薬効分類名 | 週1回持効型溶解インスリンアナログ注射液 |
| 薬効分類番号 | 2492 |
| ATCコード | A10AE07 |
| KEGG DRUG |
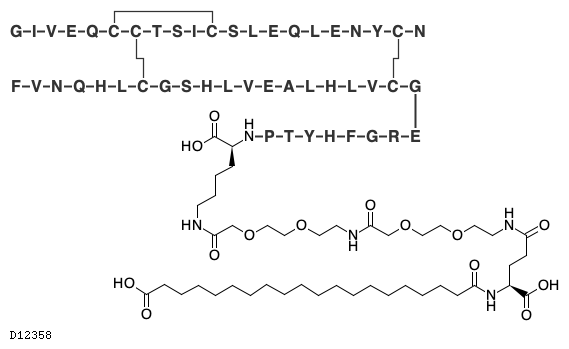
D12358
インスリンイコデク
|
| KEGG DGROUP |
DG01636
インスリン製剤
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年4月 改訂(第5版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| アウィクリ注フレックスタッチ総量300単位 | Awiqli injection FlexTouch | ノボノルディスクファーマ | 2492424G1022 | 2081円/キット | 劇薬, 処方箋医薬品注) |
| アウィクリ注フレックスタッチ総量700単位 | Awiqli injection FlexTouch | ノボノルディスクファーマ | 2492424G2029 | 3809円/キット | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 低血糖症状を呈している患者[11.1.1参照]
2.2 本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
インスリン療法が適応となる糖尿病
5. 効能または効果に関連する注意
5.1 1型糖尿病患者を対象とした臨床試験において、連日投与のBasalインスリンと比較して本剤で低血糖の発現が多く、また、同一患者において複数回発現した場合も多かった。1型糖尿病患者においては、本剤の有効性及び安全性を十分に理解し、連日投与のBasalインスリン等を用いたインスリン治療を選択することも検討したうえで、本剤の適用を慎重に考慮すること。また、2型糖尿病患者を対象とした臨床試験においても、1型糖尿病患者と比較すると低血糖が発現した患者の割合は低いものの、対照群との比較においては同様の傾向が認められていることを考慮したうえで、本剤の適用の可否を判断すること。[17.1.1-4参照]
5.2 2型糖尿病患者においては、急を要する場合以外は、あらかじめ糖尿病治療の基本である食事療法、運動療法を十分行ったうえで適用を考慮すること。
6. 用法及び用量
通常、成人では、1週間に1回皮下注射する。初期は通常1回30〜140単位とし、患者の状態に応じて適宜増減する。他のインスリン製剤を併用することがあるが、他のインスリン製剤の投与量を含めた維持量は、通常1週間あたり30〜560単位である。但し、必要により上記用量を超えて使用することがある。
7. 用法及び用量に関連する注意
7.2 特に1型糖尿病患者においては、生活様式の変化により血糖値が変動しやすいことから、慎重な血糖モニタリングを行いながら患者の状態を注意深く観察し、投与量を調整すること。低血糖を繰り返し発現する場合も含め、適切な血糖コントロールが得られない場合には、連日投与のBasalインスリン製剤等を用いたインスリン治療に変更すること。
7.3 Basalインスリンの投与を受けていない患者に本剤を投与する際には、本剤開始時の投与量は70単位以下を目安とし、低用量からの投与を考慮するなど慎重に投与を開始すること。
7.4 連日投与のBasalインスリン製剤から本剤に変更する場合は、以下を参考に本剤の投与を開始し、その後の患者の状態に応じて用量を増減するなど、本剤の作用特性を考慮の上で慎重に行うこと。
7.4.1 本剤を1週間に1回投与する投与量は、それまで連日投与していたBasalインスリンの1日総投与量の7倍に相当する単位数を目安とすること。
7.4.2 連日投与のBasalインスリン製剤から本剤への切り替え時に血糖値が上昇するおそれがある。血糖値の上昇を防ぐため、2型糖尿病患者においては、初回投与時のみ、本剤の投与量を7.4.1項で示した単位数を1.5倍に増量して投与することが推奨されるが、患者の血糖コントロールと低血糖のリスクのバランスを考慮して増量の必要性を慎重に判断すること。
1型糖尿病患者においては、初回投与時のみ、原則として本剤の投与量を7.4.1項で示した単位数を1.5倍に増量して投与すること。ただし、患者の血糖コントロール及び低血糖の発現リスクを踏まえ、初回投与量の増量の必要性を慎重に判断すること。
1型糖尿病患者においては、初回投与時のみ、原則として本剤の投与量を7.4.1項で示した単位数を1.5倍に増量して投与すること。ただし、患者の血糖コントロール及び低血糖の発現リスクを踏まえ、初回投与量の増量の必要性を慎重に判断すること。
7.4.3 初回投与量を増量した場合、2回目の投与の際は、7.4.1項で示した単位数を投与すること。3回目以降の投与量は、血糖コントロール、低血糖の発現状況等の患者の状態に加えて、本剤の作用特性を考慮して調整すること。
7.5 インスリン以外の他の糖尿病用薬との併用は、本剤の作用特性を考慮の上で、慎重に行うこと。
7.6 本剤の投与開始時及びその後血糖コントロールが安定するまでの間は血糖モニタリングを十分に行うこと。連日投与のBasalインスリン製剤から本剤に変更する場合、本剤の作用特性により、適切な血糖コントロールが得られるまでに時間を要することがある。また、併用する超速効型、速効型インスリン又は他の糖尿病用薬の用量や投与スケジュールの調整が必要となることがある。[16.1.1、16.1.2、16.8.1、16.8.2参照]
7.7 本剤は週1回投与する薬剤であり、同一曜日に投与させること。やむを得ず週1回投与の曜日を変更する必要がある場合は、投与間隔を4日間以上とし、血糖モニタリングを十分に行うこと。
7.8 投与を忘れた場合は、気づいた時点で直ちに投与し、次の投与は4日間以上の間隔をあけて開始すること。その後は、新たな開始日と同一曜日に週1回投与し、血糖モニタリングを十分に行うこと。
7.9 糖尿病性昏睡、急性感染症、手術等緊急の場合は、本剤のみで処置することは適当でなく、速効型又は超速効型インスリン製剤を使用すること。
8. 重要な基本的注意
8.2 低血糖症状を起こすことがあるので、高所作業、自動車の運転等に従事している患者に投与するときには注意すること。[11.1.1参照]
8.3 本剤はインスリン イコデク700単位/mL製剤専用のペン型注入器を使用しているため、単位数を再計算せず、指示された単位数をそのまま設定して投与するよう、患者に十分指導すること。
8.4 他のインスリン製剤やGLP-1受容体作動薬等から本剤に変更する場合や、これらの薬剤と本剤を併用する場合において、本剤を連日投与する、又は指示された単位数より多く設定して投与する等の投薬過誤が生じ、その結果、重大な低血糖を起こすおそれがある。本剤の投与方法に過誤が生じないよう、本剤が週1回投与する薬剤であること及び本剤の単位数の設定方法について、患者に十分指導すること。[8.6、11.1.1、14.1.1参照]
8.5 急激な血糖コントロールに伴い、糖尿病網膜症の顕在化又は増悪、眼の屈折異常、治療後神経障害(主として有痛性)があらわれることがあるので注意すること。
8.6 本剤の自己注射にあたっては以下の点に留意すること。[8.4参照]
・投与法について十分な教育訓練を実施したのち、患者自ら確実に投与できることを確認した上で、医師の管理指導の下で実施すること。
・全ての器具の安全な廃棄方法について指導を徹底すること。
・添付されている取扱説明書を必ず読むよう指導すること。
8.7 本剤と他のインスリン製剤を取り違えないよう、毎回注射する前に本剤のラベル等を確認するよう患者に十分指導すること。
8.8 同一箇所への繰り返し投与により、注射箇所に皮膚アミロイドーシス又はリポジストロフィーがあらわれることがあるので、定期的に注射箇所を観察するとともに、以下の点を患者に指導すること。
・本剤の注射箇所は、少なくとも前回の注射箇所から2〜3cm離すこと。[14.1.2参照]
・注射箇所の腫瘤や硬結が認められた場合には、当該箇所への投与を避けること。
8.9 皮膚アミロイドーシス又はリポジストロフィーがあらわれた箇所に本剤を投与した場合、本剤の吸収が妨げられ十分な血糖コントロールが得られなくなることがある。血糖コントロールの不良が認められた場合には、注射箇所の腫瘤や硬結の有無を確認し、注射箇所の変更とともに投与量の調整を行うなどの適切な処置を行うこと。血糖コントロールの不良に伴い、過度に増量されたインスリン製剤が正常な箇所に投与されたことにより、低血糖に至った例が報告されている。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 手術、外傷、感染症等の患者
インスリン需要の変動が激しい。
9.1.2 低血糖を起こすおそれがある以下の患者又は状態
9.2 腎機能障害患者
9.2.1 重度の腎機能障害のある患者
低血糖を起こすおそれがある。[11.1.1参照]
9.3 肝機能障害患者
9.3.1 重度の肝機能障害のある患者
低血糖を起こすおそれがある。[11.1.1参照]
9.5 妊婦
治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。本剤を妊婦に投与した臨床試験成績は得られていない。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。本剤のヒト乳汁中への移行は不明である。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。生理機能が低下していることが多く、低血糖が発現しやすい。[11.1.1参照]
10. 相互作用
10.2 併用注意
| 糖尿病用薬 ビグアナイド薬 スルホニルウレア薬 速効型インスリン分泌促進薬 α-グルコシダーゼ阻害薬 チアゾリジン薬 DPP-4阻害薬 GLP-1受容体作動薬 SGLT2阻害薬 等 | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | 血糖降下作用が増強される。 |
| モノアミン酸化酵素(MAO)阻害剤 | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | インスリン分泌促進、糖新生抑制作用による血糖降下作用を有する。 |
| 三環系抗うつ剤 ノルトリプチリン塩酸塩 等 | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | 機序は不明であるが、インスリン感受性を増強するなどの報告がある。 |
| サリチル酸誘導体 アスピリン エテンザミド | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | 糖に対するβ細胞の感受性の亢進やインスリン利用率の増加等による血糖降下作用を有する。また、末梢で弱いインスリン様作用を有する。 |
| 抗腫瘍剤 シクロホスファミド水和物 | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | インスリンが結合する抗体の生成を抑制し、その結合部位からインスリンを遊離させる可能性がある。 |
| β-遮断剤 プロプラノロール塩酸塩 アテノロール ピンドロール | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | アドレナリンによる低血糖からの回復反応を抑制する。また、低血糖に対する交感神経系の症状(振戦、動悸等)をマスクし、低血糖を遷延させる可能性がある。 |
| クマリン系薬剤 ワルファリンカリウム | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | 機序不明 |
| クロラムフェニコール | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | 機序不明 |
| ベザフィブラート | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | インスリン感受性増強等の作用により、本剤の作用を増強する。 |
| サルファ剤 | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | 膵臓でのインスリン分泌を増加させることにより、低血糖を起こすと考えられている。腎機能低下、空腹状態の遷延、栄養不良、過量投与が危険因子となる。 |
| シベンゾリンコハク酸塩 ジソピラミド ピルメノール塩酸塩水和物 | 血糖降下作用の増強による低血糖症状があらわれることがある。併用する場合は血糖値その他患者の状態を十分観察しながら投与すること[11.1.1参照]。 | インスリン分泌作用を認めたとの報告がある。 |
| チアジド系利尿剤 トリクロルメチアジド | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | カリウム喪失が関与すると考えられている。カリウム欠乏時には、血糖上昇反応に対するβ細胞のインスリン分泌能が低下する可能性がある。 |
| 副腎皮質ステロイド プレドニゾロン トリアムシノロン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 糖新生亢進、筋肉組織・脂肪組織からのアミノ酸や脂肪酸の遊離促進、末梢組織でのインスリン感受性低下等による血糖上昇作用を有する。 |
| ACTH テトラコサクチド酢酸塩 | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 副腎皮質刺激作用により糖質コルチコイドの分泌が増加する。糖質コルチコイドは、糖新生亢進、筋肉組織・脂肪組織からのアミノ酸や脂肪酸の遊離促進、末梢組織でのインスリン感受性低下等による血糖上昇作用を有する。 |
| アドレナリン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 糖新生亢進、末梢での糖利用抑制、インスリン分泌抑制による血糖上昇作用を有する。 |
| グルカゴン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 糖新生亢進、肝グリコーゲン分解促進による血糖上昇作用を有する。 |
| 甲状腺ホルモン レボチロキシンナトリウム水和物 | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 糖新生亢進、肝グリコーゲン分解促進による血糖上昇作用を有する。 |
| 成長ホルモン ソマトロピン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 抗インスリン様作用による血糖上昇作用を有する。 |
| 卵胞ホルモン エチニルエストラジオール 結合型エストロゲン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 末梢組織でインスリンの作用に拮抗する。 |
| 経口避妊薬 | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 末梢組織でインスリンの作用に拮抗する。 |
| ニコチン酸 | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 末梢組織でのインスリン感受性を低下させるため耐糖能障害を起こす。 |
| 濃グリセリン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 代謝されて糖になるため、血糖値が上昇する。 |
| イソニアジド | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 炭水化物代謝を阻害することによる血糖上昇作用を有する。 |
| ダナゾール | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | インスリン抵抗性を増強するおそれがある。 |
| フェニトイン | 血糖降下作用の減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | インスリン分泌抑制作用を有する。 |
| 蛋白同化ステロイド メテノロン | 血糖降下作用の増強による低血糖症状[11.1.1参照]、又は減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | 機序不明 |
| ソマトスタチンアナログ製剤 オクトレオチド酢酸塩 ランレオチド酢酸塩 | 血糖降下作用の増強による低血糖症状[11.1.1参照]、又は減弱による高血糖症状があらわれることがある。 併用する場合は血糖値その他患者の状態を十分観察しながら投与すること。 | インスリン、グルカゴン及び成長ホルモン等互いに拮抗的に調節作用をもつホルモン間のバランスが変化することがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 低血糖(頻度不明)
脱力感、倦怠感、高度の空腹感、冷汗、顔面蒼白、動悸、振戦、頭痛、めまい、嘔気、視覚異常、不安、興奮、神経過敏、集中力低下、精神障害、痙攣、意識障害(意識混濁、昏睡)等があらわれることがある。無処置の状態が続くと低血糖昏睡等を起こし、重篤な転帰(中枢神経系の不可逆的障害、死亡等)をとるおそれがある。
長期にわたる糖尿病、糖尿病性神経障害、β-遮断剤投与あるいは強化インスリン療法が行われている場合では、低血糖の初期の自覚症状(冷汗、振戦等)が通常と異なる場合や、自覚症状があらわれないまま、低血糖あるいは低血糖性昏睡に陥ることがある。症状が認められた場合には糖質を含む食品を摂取する等、適切な処置を行うこと。α-グルコシダーゼ阻害薬との併用時にはブドウ糖を投与すること。経口摂取が不可能な場合は、ブドウ糖の静脈内投与やグルカゴンの筋肉内投与等、適切な処置を行うこと。
低血糖は臨床的に回復した場合にも、再発することがあるので継続的に観察すること。本剤は週1回投与する薬剤であり、その作用は持続的であるため、回復が遅延するおそれがある。
なお、本剤の臨床試験では、低血糖は各投与後の2〜4日に最も多く認められている。
[2.1、8.1、8.2、8.4、8.10、9.1.2、9.2.1、9.3.1、9.8、10.2、16.8.1、16.8.2参照]
長期にわたる糖尿病、糖尿病性神経障害、β-遮断剤投与あるいは強化インスリン療法が行われている場合では、低血糖の初期の自覚症状(冷汗、振戦等)が通常と異なる場合や、自覚症状があらわれないまま、低血糖あるいは低血糖性昏睡に陥ることがある。症状が認められた場合には糖質を含む食品を摂取する等、適切な処置を行うこと。α-グルコシダーゼ阻害薬との併用時にはブドウ糖を投与すること。経口摂取が不可能な場合は、ブドウ糖の静脈内投与やグルカゴンの筋肉内投与等、適切な処置を行うこと。
低血糖は臨床的に回復した場合にも、再発することがあるので継続的に観察すること。本剤は週1回投与する薬剤であり、その作用は持続的であるため、回復が遅延するおそれがある。
なお、本剤の臨床試験では、低血糖は各投与後の2〜4日に最も多く認められている。
[2.1、8.1、8.2、8.4、8.10、9.1.2、9.2.1、9.3.1、9.8、10.2、16.8.1、16.8.2参照]
11.1.2 アナフィラキシーショック(頻度不明)
呼吸困難、血圧低下、頻脈、発汗、全身の発疹、血管神経性浮腫等の症状が認められた場合は投与を中止すること。
11.2 その他の副作用
| 1〜5%未満 | 0.2〜1%未満 | 頻度不明 | |
| 免疫系障害 | 過敏症(蕁麻疹、口唇腫脹、顔面腫脹等) | ||
| 代謝および栄養障害 | 抗インスリン抗体産生に伴う血糖コントロール不良 | ||
| 神経系障害 | 浮動性めまい、頭痛、振戦 | ||
| 眼障害 | 糖尿病網膜症 | 黄斑浮腫 | |
| 胃腸障害 | 下痢、悪心、消化不良、嘔吐 | ||
| 皮膚および皮下組織障害 | 多汗症、冷汗 | ||
| 筋骨格系および結合組織障害 | 筋痙縮 | ||
| 全身障害および投与部位の状態 | 空腹、注射部位反応(注射部位紅斑、注射部位内出血、注射部位過敏反応、注射部位腫脹、注射部位蕁麻疹等)、倦怠感、無力症、異常感 | リポジストロフィー(皮下脂肪の萎縮・肥厚等)、浮腫 | |
| 臨床検査 | 体重増加 |
14. 適用上の注意
14.1 薬剤投与時の注意
14.1.1 投与時
(1)本剤はJIS T 3226-2に準拠したA型専用注射針を用いて使用すること。本剤はA型専用注射針との適合性の確認をペンニードルプラスで行っている。
(2)本剤とA型専用注射針との装着時に液漏れ等の不具合が認められた場合には、新しい注射針に取り替える等の処置方法を患者に十分指導すること。
(3)1本の本剤を複数の患者に使用しないこと。
(4)本剤の単位合わせダイアルの1クリック(1目盛り)は10単位に相当し、本剤の投与単位数は10単位刻みで設定可能である。[8.4参照]
14.1.2 投与部位
皮下注射は、大腿、上腕、腹部に行う。同じ部位に注射を行う場合は、その中で注射箇所を毎回変えること。前回の注射箇所より2〜3cm離して注射すること。
[8.8参照]
[8.8参照]
14.1.3 投与経路
静脈内及び筋肉内に投与しないこと。皮下注射したとき、まれに注射針が血管内に入り、注射後直ちに低血糖があらわれることがあるので注意すること。
14.1.4 その他
(1)本剤と他の薬剤を混合しないこと。本剤は他の薬剤との混合により、成分が分解するおそれがある。
(2)注射後は必ず注射針を外すこと。注射針は毎回新しいものを、必ず注射直前に取り付けること。針を付けたままにすると、液漏れや針詰まりにより正常に注射できないおそれがある。また、薬剤の濃度変化や感染症の原因となることがある。
(3)インスリンカートリッジにインスリン製剤を補充してはならない。
(4)インスリンカートリッジにひびが入っている場合は使用しないこと。
(5)液に濁りが生じていたり、変色している場合は、使用しないこと。
(6)本剤のカートリッジを取り外して使用しないこと。また、シリンジを用いてカートリッジから薬液を抜き取らないこと。過少投与や過量投与となるおそれがある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 インスリン又は経口糖尿病薬の投与中にアンジオテンシン変換酵素阻害剤を投与することにより、低血糖が起こりやすいとの報告がある1)。
15.1.2 ピオグリタゾンと併用した場合、浮腫が多く報告されている。併用する場合には、浮腫及び心不全の徴候を十分観察しながら投与すること。
16. 薬物動態
16.1 血中濃度
16.1.1 1型糖尿病
日本人1型糖尿病患者24例に本剤を被験者ごとに設定した用量で8週間週1回皮下投与したときの薬物動態パラメータ及び血清中濃度推移を以下に示す。
| パラメータ | 1週目投与後 (24例) | 8週目投与後 (24例) |
| 1回投与量(単位/kg) | 1.71[1.2,3.1] | 1.69[1.2,3.1] |
| 投与量で補正したCmax(nmol/L/(単位/kg)) | 52.2(19.0) | 91.2(14.7) |
| 投与量で補正したAUC0-168(nmol・h/L/(単位/kg)) | 6108.5(12.8) | 10849.0(10.6) |
| tmax(h) | 12.0[12.0,36.0] | 16.0[12.0,18.0] |
| t1/2(h) | − | 164(11.4) |
実線:初回投与後のインスリン イコデク濃度
点線:最終投与後のインスリン イコデク濃度
16.1.2 2型糖尿病
2型糖尿病患者46例に本剤を被験者ごとに設定した用量で8週間週1回皮下投与したときの薬物動態パラメータを以下に示す。
| パラメータ | 1週目投与後 (46例) | 8週目投与後 (42例) |
| 1回投与量(単位/kg) | 2.56[1.21,5.27] | 2.91[1.53,5.64] |
| 投与量で補正したCmax(nmol/L/(単位/kg)) | 50.8(22.5) | 105.8(21.0)a) |
| 投与量で補正したAUC0-168(nmol・h/L/(単位/kg)) | 6064.5(15.8) | 12748.4(20.0)a) |
| tmax(h) | 21.2[11.6,59.9] | 15.1[12.0,42.0]a) |
| t1/2(h) | − | 155(15.3) |
16.2 吸収
2型糖尿病患者25例に本剤5.6単位/kgを大腿部、腹部、上腕部に単回皮下投与し、薬物動態特性及び投与後36〜60時間のグルコースクランプ下における血糖降下作用を検討した。大腿部への投与に対する腹部又は上腕部への投与での最高血中濃度(Cmax)及び総曝露量(AUC0-inf,SD)の幾何平均値の比とその95%信頼区間は、腹部投与時では1.17[1.07,1.29]及び1.02[0.96,1.09]、上腕部投与時では1.24[1.14,1.35]及び1.04[0.98,1.10]であった。また、本剤の血糖降下作用は、大腿部、腹部又は上腕部に投与した場合のいずれの場合でも同程度であった5)(外国人データ)。
16.3 分布
16.4 代謝
本剤の代謝はヒトインスリンと同様であり、認められたすべての代謝物は不活性であった8)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者における薬物動態
腎機能障害の程度の異なる被験者(実測糸球体濾過量:mGFR(mL/min)による分類)に本剤1.5単位/kgを単回皮下投与し、腎機能が正常な被験者(mGFR 90以上)と薬物動態特性を比較検討した結果を以下に示す9)(外国人データ)。
| 腎機能 | AUC0-840,SD比の推定値 [95%信頼区間] | Cmax,SD比の推定値 [95%信頼区間] |
| 軽度/正常 (軽度:mGFR 60以上90未満) | 1.12 [0.96;1.31] | 1.05 [0.85;1.30] |
| 中等度/正常 (中等度:mGFR 30以上60未満) | 1.21 [1.04;1.41] | 1.05 [0.85;1.30] |
| 重度/正常 (重度:mGFR 30未満) | 1.16 [0.99;1.36] | 0.91 [0.74;1.13] |
| 末期/正常 (末期:血液透析を必要とする被験者) | 1.13 [0.95;1.33] | 1.02 [0.81;1.29] |
16.6.2 肝機能障害患者における薬物動態
肝機能障害の程度の異なる被験者(Child-Pugh scoresに基づく分類)に本剤1.5単位/kgを単回皮下投与し、肝機能が正常な被験者と薬物動態特性を比較検討した結果を以下に示す10)(外国人データ)。
| 肝機能 | AUC0-inf,SD比の推定値 [95%信頼区間] | Cmax,SD比の推定値 [95%信頼区間] |
| 軽度/正常 (軽度:Child-Pugh分類A) | 1.13 [1.00;1.28] | 1.13 [0.90;1.42] |
| 中等度/正常 (中等度:Child-Pugh分類B) | 1.15 [1.02;1.29] | 1.05 [0.83;1.31] |
| 重度/正常 (重度:Child-Pugh分類C) | 0.97 [0.86;1.09] | 0.97 [0.77;1.21] |
16.6.3 高齢者における薬物動態
1型糖尿病患者及び2型糖尿病患者1244例(日本人127例)を対象とした母集団薬物動態解析の結果、18歳以上65歳未満の被験者に対する65歳以上75歳未満及び75歳以上の被験者の、定常状態での本剤の投与量補正した平均血清中濃度の比の推定値及びその90%信頼区間は、1.05[1.02;1.07]及び1.11[1.07;1.14]であった。
16.8 その他
16.8.1 1型糖尿病患者における薬力学的作用
16.8.2 2型糖尿病患者における薬力学的作用
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 インスリン治療歴のない2型糖尿病患者における試験:本剤の週1回投与とインスリンを除く糖尿病治療薬の併用療法(第III相国際共同試験)
インスリン治療歴のない2型糖尿病患者984例を対象に無作為割り付けを行い、非盲検下で本剤を週1回又はインスリン グラルギン100単位/mLを1日1回、52週間皮下投与した(本剤:492例(日本人:78例)、インスリン グラルギン100単位/mL:492例(日本人:86例))。本剤又はインスリン グラルギン100単位/mLは、糖尿病治療薬(メトホルミン、DPP-4阻害薬、SGLT2阻害薬、チアゾリジン薬、α-グルコシダーゼ阻害薬、GLP-1受容体作動薬)併用下で投与した。本剤群の開始用量は70単位、インスリン グラルギン100単位/mL群の開始用量は10単位とし、試験実施中、本剤及びインスリン グラルギン100単位/mLの投与量は、平均朝食前血糖値(血糖自己測定)に基づいて継続的に調節した。
主要評価項目であるHbA1cのベースラインから投与後52週までの変化量は下表のとおりであり、本剤のインスリン グラルギン100単位/mLに対する非劣性が検証された(非劣性マージン:0.3%)。
主要評価項目であるHbA1cのベースラインから投与後52週までの変化量は下表のとおりであり、本剤のインスリン グラルギン100単位/mLに対する非劣性が検証された(非劣性マージン:0.3%)。
| 本剤群 (492例) | インスリン グラルギン100単位/mL群 (492例) | ||
| HbA1c(%) | |||
| ベースラインa) | 8.50±0.99(492例) | 8.44±1.02(492例) | |
| 投与52週時b) | 6.93±0.06(492例) | 7.12±0.05(492例) | |
| 変化量b) | −1.55±0.06(492例) | −1.35±0.05(492例) | |
| インスリン グラルギンとの群間差 [95%信頼区間]c) | −0.19 [−0.36;−0.03] | ||
主な副次評価項目の結果を下表に示す。
| 本剤群 (492例) | インスリン グラルギン100単位/mL群 (492例) | ||
| HbA1c 7%未満の達成 | |||
| 投与52週時の達成割合(%)a) | 57.57(492例) | 45.44(492例) | |
| レベル2又はレベル3の低血糖を発現せずにHbA1c 7%未満の達成 | |||
| 投与52週時の達成割合(%)a) | 52.56(492例) | 42.58(492例) | |
| 空腹時血糖値(mg/dL) | |||
| ベースラインb) | 185.31±48.96(480例) | 185.71±51.66(474例) | |
| 投与52週時c) | 125.19±1.67(480例) | 125.43±1.68(474例) | |
| 変化量c) | −60.32±1.67(480例) | −60.08±1.68(474例) | |
| 血糖値の目標範囲内(70-180mg/dL)時間(time in range)(%) | |||
| 48週〜52週b) | 71.94±18.23(439例) | 66.90±18.19(440例) | |
| 1週間あたりのBasalインスリン投与量(単位) | |||
| 50週〜52週d) | 230.0(10.0,980.0)(472例) | 221.5(14.0,1022.7)(477例) | |
重大な低血糖(レベル3)、重大な低血糖又は臨床的に問題となる低血糖(レベル2)、及びレベル3又はレベル2の夜間低血糖の患者あたりの年間発現件数及び発現割合を下表に示す11)。
| 本剤群 (492例) | インスリン グラルギン100単位/mL群 (492例) | |
| 患者あたりの年間発現件数(発現割合(%)) | ||
| レベル3の低血糖 | <0.01(0.2) | <0.01(0.6) |
| レベル3又はレベル2の低血糖 | 0.30(9.8) | 0.16(10.6) |
| レベル3又はレベル2の夜間低血糖 | 0.04(1.8) | 0.03(2.2) |
17.1.2 Basalインスリンで治療中の2型糖尿病患者における試験:本剤の週1回投与とインスリンを除く糖尿病治療薬の併用療法(第III相国際共同試験)
Basalインスリンで治療中の2型糖尿病患者526例を対象に無作為割り付けを行い、非盲検下で本剤を週1回又はインスリン デグルデクを1日1回、26週間皮下投与した(本剤:262例(日本人:51例)、インスリン デグルデク:263例(日本人:49例))。本剤又はインスリン デグルデクは、糖尿病治療薬(メトホルミン、DPP-4阻害薬、SGLT2阻害薬、チアゾリジン薬、α-グルコシダーゼ阻害薬、GLP-1受容体作動薬)併用下で投与した。試験実施中、本剤及びインスリン デグルデクの投与量は、平均朝食前血糖値(血糖自己測定)に基づいて継続的に調節したが、本剤群では、初回投与時には、割り付け前のBasalインスリン1日投与量の7倍量をさらに1.5倍に増量した用量を投与し、その後はBasalインスリン1日投与量の7倍量を投与し、以降は適宜用量調節することとした。
主要評価項目であるHbA1cのベースラインから投与後26週までの変化量は下表のとおりであり、本剤のインスリン デグルデクに対する非劣性が検証された(非劣性マージン:0.3%)。
主要評価項目であるHbA1cのベースラインから投与後26週までの変化量は下表のとおりであり、本剤のインスリン デグルデクに対する非劣性が検証された(非劣性マージン:0.3%)。
| 本剤群 (263例) | インスリン デグルデク群 (263例) | ||
| HbA1c(%) | |||
| ベースラインa) | 8.17±0.77(263例) | 8.10±0.77(263例) | |
| 投与26週時b) | 7.20±0.05(263例) | 7.42±0.06(263例) | |
| 変化量b) | −0.93±0.05(263例) | −0.71±0.06(263例) | |
| インスリン デグルデクとの群間差 [95%信頼区間]c) | −0.22 [−0.37;−0.08] | ||
主な副次評価項目の結果を下表に示す。
| 本剤群 (263例) | インスリン デグルデク群 (263例) | ||
| HbA1c 7%未満の達成 | |||
| 投与26週時の達成割合(%)a) | 40.32(263例) | 26.49(263例) | |
| レベル2又はレベル3の低血糖を発現せずにHbA1c 7%未満の達成 | |||
| 投与26週時の達成割合(%)a) | 36.73(263例) | 26.79(263例) | |
| 空腹時血糖値(mg/dL) | |||
| ベースラインb) | 152.24±47.47(260例) | 150.70±40.92(257例) | |
| 投与26週時c) | 123.01±2.08(260例) | 122.30±2.10(257例) | |
| 変化量c) | −28.47±2.08(260例) | −29.18±2.10(257例) | |
| 血糖値の目標範囲内(70-180mg/dL)時間(time in range)(%) | |||
| 22週〜26週b) | 63.13±17.40(238例) | 59.50±18.92(239例) | |
| 1週間あたりのBasalインスリン投与量(単位) | |||
| 24週〜26週d) | 280.0(10.0,980.0)(249例) | 253.97(49.0,1364.0)(252例) | |
17.1.3 Basal-Bolus療法で治療中の2型糖尿病患者における試験:糖尿病治療薬の併用/非併用下でのBasal-Bolus療法(第III相国際共同試験)
Basal-Bolus療法で治療中の2型糖尿病患者582例を対象に無作為割り付けを行い、非盲検下で本剤を週1回又はインスリン グラルギン100単位/mLを1日1回、26週間皮下投与した(本剤:291例(日本人:44例)、インスリン グラルギン100単位/mL:291例(日本人:41例))。本剤又はインスリン グラルギン100単位/mLは、糖尿病治療薬(メトホルミン、DPP-4阻害薬、SGLT2阻害薬、チアゾリジン薬、α-グルコシダーゼ阻害薬、GLP-1受容体作動薬)併用又は非併用下かつBolusインスリンとしてインスリン アスパルト1日2〜4回皮下投与の併用下で投与した。試験実施中、本剤及びインスリン グラルギン100単位/mLの投与量は、平均朝食前血糖値(血糖自己測定)に基づいて継続的に調節したが、本剤群では、初回投与時には、割り付け前のBasalインスリン1日投与量の7倍量をさらに1.5倍に増量した用量を投与し、その後はBasalインスリン1日投与量の7倍量を投与し、以降は適宜用量調節することとした。
主要評価項目であるHbA1cのベースラインから投与後26週までの変化量は下表のとおりであり、本剤のインスリン グラルギン100単位/mLに対する非劣性が検証された(非劣性マージン:0.3%)。
主要評価項目であるHbA1cのベースラインから投与後26週までの変化量は下表のとおりであり、本剤のインスリン グラルギン100単位/mLに対する非劣性が検証された(非劣性マージン:0.3%)。
| 本剤群 (291例) | インスリン グラルギン100単位/mL群 (291例) | ||
| HbA1c(%) | |||
| ベースラインa) | 8.29±0.86(291例) | 8.31±0.90(291例) | |
| 投与26週時b) | 7.14±0.05(291例) | 7.12±0.05(291例) | |
| 変化量b) | −1.16±0.05(291例) | −1.18±0.05(291例) | |
| インスリン グラルギンとの群間差 [95%信頼区間]c) | 0.02 [−0.11;0.15] | ||
主な副次評価項目の結果を下表に示す。
| 本剤群 (291例) | インスリン グラルギン100単位/mL群 (291例) | ||
| HbA1c 7%未満の達成 | |||
| 投与26週時の達成割合(%)a) | 40.69(291例) | 45.48(291例) | |
| レベル2又はレベル3の低血糖を発現せずにHbA1c 7%未満の達成 | |||
| 投与26週時の達成割合(%)a) | 26.48(291例) | 25.24(291例) | |
| 空腹時血糖値(mg/dL) | |||
| ベースラインb) | 166.59±54.10(283例) | 173.05±63.46(284例) | |
| 投与26週時c) | 138.28±2.90(283例) | 140.76±2.93(284例) | |
| 変化量c) | −31.54±2.90(283例) | −29.06±2.93(284例) | |
| 血糖値の目標範囲内(70-180mg/dL)時間(time in range)(%) | |||
| 22週〜26週b) | 66.88±15.62(244例) | 66.44±16.17(237例) | |
| 1週間あたりのBasalインスリン投与量(単位) | |||
| 24週〜26週d) | 360.0(45.0,1450.0)(261例) | 294.0(52.0,1116.5)(264例) | |
17.1.4 1型糖尿病患者における試験:Basal-Bolus療法(第III相国際共同試験)
Basal-Bolus療法で治療中の1型糖尿病患者582例を対象に無作為割り付けを行い、非盲検下で本剤を週1回又はインスリン デグルデクを1日1回、26週間皮下投与した(本剤:290例(日本人:32例)、インスリン デグルデク:292例(日本人:48例))。Bolusインスリンとしてインスリン アスパルトを1日2〜4回皮下投与した。試験実施中、本剤及びインスリン デグルデクの投与量は、平均朝食前血糖値(血糖自己測定)に基づいて継続的に調節したが、本剤群では、試験参加前のBasalインスリン製剤の種類及び投与方法並びにスクリーニング時のHbA1c値に基づき、初回投与時には、割り付け前のBasalインスリン1日投与量の7倍量をさらに1.5倍又は2倍に増量した用量を投与し、その後はBasalインスリン1日投与量の7倍量を投与し、以降は適宜用量調節することとした。
主要評価項目であるHbA1cのベースラインから投与後26週までの変化量は下表のとおりであり、本剤のインスリン デグルデクに対する非劣性が検証された(非劣性マージン:0.3%)。
主要評価項目であるHbA1cのベースラインから投与後26週までの変化量は下表のとおりであり、本剤のインスリン デグルデクに対する非劣性が検証された(非劣性マージン:0.3%)。
| 本剤群 (290例) | インスリン デグルデク群 (292例) | ||
| HbA1c(%) | |||
| ベースラインa) | 7.59±0.96(290例) | 7.63±0.93(292例) | |
| 投与26週時b) | 7.15±0.07(290例) | 7.10±0.06(292例) | |
| 変化量b) | −0.47±0.07(290例) | −0.51±0.06(292例) | |
| インスリン デグルデクとの群間差 [95%信頼区間]c) | 0.05 [−0.13;0.23] | ||
主な副次評価項目の結果を下表に示す。
| 本剤群 (290例) | インスリン デグルデク群 (292例) | ||
| HbA1c 7%未満の達成 | |||
| 投与26週時の達成割合(%)a) | 40.20(290例) | 45.72(292例) | |
| レベル2又はレベル3の低血糖を発現せずにHbA1c 7%未満の達成 | |||
| 投与26週時の達成割合(%)a) | 9.55(290例) | 16.74(292例) | |
| 空腹時血糖値(mg/dL) | |||
| ベースラインb) | 179.17±73.86(276例) | 172.31±72.30(287例) | |
| 投与26週時c) | 160.60±3.65(276例) | 142.02±3.55(287例) | |
| 変化量c) | −15.08±3.65(276例) | −33.66±3.55(287例) | |
| 血糖値の目標範囲内(70-180mg/dL)時間(time in range)(%) | |||
| 22週〜26週b) | 59.10±15.66(261例) | 60.85±15.03(272例) | |
| 1週間あたりのBasalインスリン投与量(単位) | |||
| 24週〜26週d) | 170.0(50.0,720.0)(263例) | 147.0(14.4,686.0)(282例) | |
重大な低血糖(レベル3)、重大な低血糖又は臨床的に問題となる低血糖(レベル2)、及びレベル3又はレベル2の夜間低血糖の患者あたりの年間発現件数及び発現割合を下表に示す15)。
| 本剤群 (290例) | インスリン デグルデク群 (292例) | |
| 患者あたりの年間発現件数(発現割合(%)) | ||
| レベル3の低血糖 | 0.33(3.1) | 0.12(3.1) |
| レベル3又はレベル2の低血糖 | 19.93(85.2) | 10.37(76.4) |
| レベル3又はレベル2の夜間低血糖 | 3.38(46.6) | 1.58(33.6) |
18. 薬効薬理
18.1 作用機序
本剤の主な薬理作用は、グルコース代謝の調節である。本剤は、他のインスリン製剤と同様にインスリンレセプターに結合し、骨格筋及び脂肪細胞における糖の取り込みを促進し、また肝臓におけるグルコース産生を阻害することによって血糖値を降下させる。さらに、脂肪細胞における脂肪分解及び蛋白質分解を阻害し、蛋白質合成を促進する。
本剤の半減期延長作用は、主に本剤がアルブミンと可逆的に結合することによる。本剤は投与後に血漿中に移行した後、血中のアルブミンに結合することで活性を示さない状態となり、その後、緩徐にアルブミンと解離し、インスリンレセプターと結合することで、血糖降下作用が持続する17)。
本剤の半減期延長作用は、主に本剤がアルブミンと可逆的に結合することによる。本剤は投与後に血漿中に移行した後、血中のアルブミンに結合することで活性を示さない状態となり、その後、緩徐にアルブミンと解離し、インスリンレセプターと結合することで、血糖降下作用が持続する17)。
19. 有効成分に関する理化学的知見
19.1. インスリン イコデク(遺伝子組換え)
20. 取扱い上の注意
使用中は室温にキャップ等により遮光して保管し、アウィクリ注フレックスタッチ総量300単位は6週間以内、アウィクリ注フレックスタッチ総量700単位は12週間以内に使用すること。冷蔵庫保管(2〜8℃)も可能であるが、凍結を避けること。残った場合は廃棄すること。
21. 承認条件
医薬品リスク管理計画を策定の上、適切に実施すること。
22. 包装
<総量300単位>
0.43mL×2本
<総量700単位>
1.0mL×2本
23. 主要文献
- Herings RMC,et al., Lancet., 345, 1195-8, (1995)
- 社内資料:第1相臨床試験(NN1436-4422)(2024年6月24日承認,CTD2.7.2.3)
- 社内資料:第1相臨床試験(NN1436-4569)(2024年6月24日承認,CTD2.7.2.3)
- 社内資料:第1相臨床試験(NN1436-4314)(2024年6月24日承認,CTD2.7.6)
- 社内資料:第1相臨床試験(NN1436-4572)(2024年6月24日承認,CTD2.7.2.3)
- 社内資料:マウス、ラット、ウサギ、イヌ及びヒト血漿を用いたin vitroタンパク質結合(2024年6月24日承認,CTD2.6.4.4)
- 社内資料:血清アルブミン結合の置換(2024年6月24日承認,CTD2.6.4.7)
- 社内資料:In vitro代謝(2024年6月24日承認,CTD2.6.4.5)
- 社内資料:第1相臨床試験(NN1436-4226)(2024年6月24日承認,CTD2.7.2.3)
- 社内資料:第1相臨床試験(NN1436-4570)(2024年6月24日承認,CTD2.7.2.3)
- 社内資料:第3相臨床試験(NN1436-4477主要パート)(2024年6月24日承認,CTD2.7.3及びCTD2.7.4)
- 社内資料:第3相臨床試験(NN1436-4477)(2024年6月24日承認,CTD2.7.3及びCTD2.7.4)
- 社内資料:第3相臨床試験(NN1436-4478)(2024年6月24日承認,CTD2.7.3及びCTD2.7.4)
- 社内資料:第3相臨床試験(NN1436-4480)(2024年6月24日承認,CTD2.7.3及びCTD2.7.4)
- 社内資料:第3相臨床試験(NN1436-4625主要パート)(2024年6月24日承認,CTD2.7.3及びCTD2.7.4)
- 社内資料:第3相臨床試験(NN1436-4625)(2024年6月24日承認,CTD2.7.3及びCTD2.7.4)
- Nishimura E,et al., BMJ Open Diabetes Res Care., 9, e002301, (2021) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
ノボノルディスクファーマ株式会社
カスタマーセンター
〒100-0005
東京都千代田区丸の内2-1-1
電話:0120-180363(フリーダイアル)
製品情報問い合わせ先
ノボノルディスクファーマ株式会社
カスタマーセンター
〒100-0005
東京都千代田区丸の内2-1-1
電話:0120-180363(フリーダイアル)