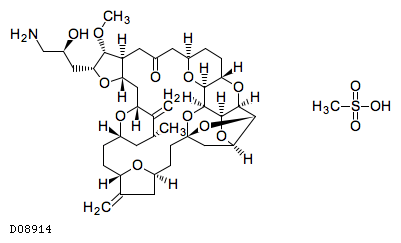
医薬品情報
| 総称名 | エリブリンメシル酸塩 |
|---|---|
| 一般名 | エリブリンメシル酸塩 |
| 欧文一般名 | Eribulin Mesilate |
| 製剤名 | エリブリンメシル酸塩静注液 |
| 薬効分類名 | 抗悪性腫瘍剤 |
| 薬効分類番号 | 4291 |
| ATCコード | L01XX41 |
| KEGG DRUG |
D08914
エリブリンメシル酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年8月 作成(第1版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| エリブリンメシル酸塩静注液1mg「ニプロ」 (後発品) | Eribulin Mesilate Intravenous | ニプロ | 4291420A1049 | 22997円/瓶 | 毒薬, 処方箋医薬品注) |
1. 警告
1.1 本剤を含むがん化学療法は、緊急時に十分な対応ができる医療施設において、がん化学療法に十分な知識・経験を持つ医師のもとで、本療法が適切と判断される症例についてのみ実施すること。また、本剤による治療開始に先立ち、患者又はその家族に有効性及び危険性を十分に説明し、同意を得てから投与すること。
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
手術不能又は再発乳癌
5. 効能または効果に関連する注意
5.1 本剤の術前・術後補助化学療法における有効性及び安全性は確立していない。
5.2 本剤の投与を行う場合には、アントラサイクリン系抗悪性腫瘍剤及びタキサン系抗悪性腫瘍剤を含む化学療法を施行後の増悪若しくは再発例を対象とすること。
6. 用法及び用量
通常、成人には、エリブリンメシル酸塩として、1日1回1.4mg/m2(体表面積)を2〜5分間かけて、週1回、静脈内投与する。これを2週連続で行い、3週目は休薬する。これを1サイクルとして、投与を繰り返す。なお、患者の状態により適宜減量する。
7. 用法及び用量に関連する注意
7.1 他の抗悪性腫瘍剤との併用について、有効性及び安全性は確立していない。
7.2 本剤の投与にあたっては、以下の基準を参考に必要に応じて、投与を延期、減量又は休薬すること。
| 投与開始基準 | 下記の基準を満たさない場合、投与を延期する。 ・好中球数:1,000/mm3以上 ・血小板数:75,000/mm3以上 ・非血液毒性:Grade2注1)以下 |
| 減量基準 | 前サイクルにおいて以下の副作用等が発現した場合、減量した上で投与する注2)。 ・7日間を超えて継続する好中球数減少(500/mm3未満) ・発熱又は感染を伴う好中球数減少(1,000/mm3未満) ・血小板数減少(25,000/mm3未満) ・輸血を要する血小板数減少(50,000/mm3未満) ・Grade3注1)以上の非血液毒性 ・副作用等により、2週目に休薬した場合 |
| 投与開始基準 | 下記の基準を満たさない場合、投与を延期する。 ・好中球数:1,000/mm3以上 ・血小板数:75,000/mm3以上 ・非血液毒性:Grade2注1)以下 |
| 投与再開基準 | 投与延期後1週間以内に上記の投与開始基準を満たした場合、減量して投与する注2)。 |
| 休薬基準 | 投与延期後1週間以内に上記の投与開始基準を満たさない場合は、休薬する。 |
注1)Common Terminology Criteria for Adverse Events(CTCAE)に基づく。
注2)減量を行う際、次の用量を参考にすること。
| 減量前の投与量→減量後の投与量 |
| 1.4mg/m2→1.1mg/m2 |
| 1.1mg/m2→0.7mg/m2 |
| 0.7mg/m2→投与中止を考慮 |
8. 重要な基本的注意
8.2 QT間隔延長があらわれたとの報告があるので、投与開始前は心電図検査及び電解質検査を行うこと。本剤投与中は適宜心電図検査を行うなど患者の状態を十分に観察すること。
8.3 肝機能障害があらわれることがあるので、本剤投与中は定期的に肝機能検査を行い、患者の状態を十分に観察すること。[11.1.4参照]
8.4 間質性肺炎があらわれることがあるので、胸部X線検査を行うなどして、患者の状態を十分に観察すること。[11.1.5参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.2 腎機能障害患者
9.3 肝機能障害患者
9.4 生殖能を有する者
生殖可能な年齢の患者に投与する必要がある場合には、性腺に対する影響を考慮すること。動物実験(ラット、イヌ)において精巣毒性が認められている。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。動物実験(ラット)で胚致死作用及び催奇形作用が報告されている。[2.3参照]
9.6 授乳婦
授乳しないことが望ましい。本剤が乳汁に移行する可能性があり、乳児が乳汁を介して摂取した場合、乳児に重篤な副作用が発現するおそれがある。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を十分に観察し、慎重に投与すること。一般に生理機能が低下していることが多く、骨髄抑制や消化器症状等の副作用があらわれやすい。[1.2参照]
10. 相互作用
10.2 併用注意
| 抗悪性腫瘍剤 放射線照射 | 併用により、骨髄抑制が増強するおそれがある。併用する場合には、患者の状態を十分に観察し、必要に応じて減量又は休薬期間の延長を行うこと。 | ともに骨髄抑制作用を有し、骨髄抑制が増強するおそれがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 骨髄抑制
11.1.2 感染症(頻度不明)
敗血症、肺炎等があらわれることがある。
11.1.3 末梢神経障害(末梢性ニューロパチー)(28.0%)
観察を十分に行い、しびれ等の症状が認められた場合には、減量や休薬等の適切な処置を行うこと。
11.1.4 肝機能障害(8.3%)[8.3参照]
11.1.5 間質性肺炎(1.5%)[8.4参照]
11.1.6 皮膚粘膜眼症候群(Stevens-Johnson症候群)、多形紅斑(いずれも頻度不明)
11.2 その他の副作用
| 30%以上 | 5〜30%未満 | 5%未満 | 頻度不明 | |
| 血液 | 血小板増加 | |||
| 消化器 | 悪心(40.2%)、口内炎(34.1%) | 嘔吐、便秘、下痢、腹痛 | 口唇炎、口内乾燥、口の感覚鈍麻、流涎過多、歯痛、歯肉痛、歯周炎、舌炎、舌苔、嚥下障害、腹部不快感、消化不良、胃腸粘膜障害、胃炎、裂肛、肛門周囲痛 | 膵炎、粘膜の炎症 |
| 全身症状 | 疲労(34.1%)、発熱(31.1%) | 倦怠感、浮腫 | 無力症、疼痛、インフルエンザ様疾患 | |
| 精神神経系 | 味覚異常、頭痛、めまい | 同名性半盲、傾眠、不眠症、不安、感覚鈍麻、感覚障害 | ||
| 代謝 | 食欲減退(34.8%) | 血中アルブミン、カリウム、リンの低下、総コレステロールの上昇、耐糖能障害 | 血中ナトリウム、クロール、カルシウム、総蛋白、血糖の低下、血中リン、トリグリセリドの上昇 | |
| 筋骨格系 | 筋肉痛、関節痛 | 頸部痛、背部痛、鼡径部痛、四肢痛、筋固縮、筋痙縮、関節炎、変形性関節症 | 骨痛 | |
| 呼吸器 | 咳嗽、口腔咽頭痛 | 呼吸困難、鼻出血、鼻漏、口腔咽頭不快感、上気道炎、胸膜炎、放射線性肺臓炎、発声障害、肺塞栓症、喀血、胸水 | ||
| 皮膚 | 脱毛症(46.2%) | 発疹 | 湿疹、蕁麻疹、そう痒症、光線過敏性反応、皮膚乾燥、皮膚筋炎 | |
| 肝臓 | AST、ALT、Al-P、γ-GTP、LDHの上昇 | 総ビリルビンの上昇、脂肪肝 | ||
| 循環器 | 動悸、血圧上昇、頻脈、心電図QT延長、心室性期外収縮 | |||
| 泌尿器 | 蛋白尿、尿潜血 | 尿意切迫、BUN、血中クレアチニンの上昇、尿路感染、排尿障害、腎不全 | ||
| 感覚器 | 結膜炎、眼の異常感、複視、眼脂、眼痛、眼乾燥、流涙増加、耳漏、耳鳴、白内障 | |||
| その他 | CK、CRPの上昇、体重減少 | 注射部位反応(そう痒感等)、注射部位漏出、胸痛、口渇、過敏症、膣分泌物、血管炎、出血、ほてり、体重増加、不規則月経 |
14. 適用上の注意
14.1 薬剤調製時の注意
14.1.1 本剤を他の医薬品と混注しないこと。
14.1.2 本剤を5%ブドウ糖注射液で希釈した場合、反応生成物が検出されるため、希釈する場合は日本薬局方生理食塩液を使用すること。また、0.01mg/mL未満の濃度に希釈しないこと。
14.1.3 調製時には手袋、ゴーグル及び保護衣の着用が望ましい。本剤が皮膚に付着した場合には、直ちに石鹸及び多量の流水で洗い流すこと。また、粘膜に付着した場合には、直ちに多量の流水で洗い流すこと。
14.2 薬剤投与時の注意
14.2.1 本剤をシリンジに入れ、室温で保存した場合は6時間以内、冷蔵で保存した場合は24時間以内に投与すること。
15. その他の注意
15.1 臨床使用に基づく情報
前治療歴を有する患者において、本剤の投与後に骨髄異形成症候群(MDS)が発生したとの報告がある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
日本人固形がん患者15例にエリブリンメシル酸塩0.7注)、1.0注)、1.4又は2.0注)mg/m2を2〜10分間かけて静脈内投与したとき、エリブリンは3相性の消失推移を示した1)。
| Cmax(ng/mL) | AUC0-inf(ng・hr/mL) | t1/2(hr) | CL(L/hr/m2) | Vss(L/m2) | |
| 第1日目 | 519.4±107.2 | 672.7±113.7 | 39.4±8.3 | 1.89±0.33 | 76.3±19.2 |
| 第8日目 | 544.4±52.5 | 698.5±128.8 | 38.6±5.2 | 1.82±0.34 | 67.8±12.4 |
注)本剤の承認された用量は、成人1日1回1.4mg/m2(体表面積)である。
16.3 分布
In vitro試験におけるエリブリン(100〜1,000ng/mL)のヒト血漿蛋白結合率は48.92〜65.07%であった2)。
ラットに14C標識エリブリン酢酸塩0.75mg/kgを単回静脈内投与したとき、投与後7日目までに多くの組織に放射能が分布していた。特に、肺、膀胱、腎皮質、腎髄質、肝臓、脾臓、甲状腺、胃、唾液腺で高い放射能が認められ、中枢神経系では低かった3)。
イヌに14C標識エリブリン酢酸塩0.08mg/kgを単回静脈内投与したとき、血液中放射能/血漿中放射能の比は0.94〜1.25であった4)。
16.4 代謝
固形がん患者6例に14C標識体を単回静脈内投与したとき、血漿中の放射能の大部分が未変化体であった。また、投与後168時間までに尿糞中に排泄された放射能の78.6%が未変化体であった5)(外国人データ)。
In vitro試験の結果から、CYP3A4が主にエリブリンの代謝に寄与すると考えられた6)。
16.5 排泄
固形がん患者6例に14C標識体を単回投与したとき、投与後168時間までに、投与した放射能の8.9%が尿中に、77.6%が糞中に排泄された。尿糞中の放射能のうち、78.6%が未変化体として排泄された5)(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
固形がん患者19例の腎機能をクレアチニンクリアランスによって、正常(≧80mL/min)、中等度腎機能障害(30-50mL/min)及び重度腎機能障害(15-29mL/min)に分類し、それぞれエリブリンメシル酸塩を1.4mg/m2、1.4mg/m2及び0.7mg/m2投与した際の薬物動態パラメータにおいて、腎機能の低下に伴い半減期は変化しないものの、クリアランスの低下、AUC(投与量補正時)の増加及びCmax(投与量補正時)の増加が認められた7)(外国人データ)。[9.2参照]
| 正常 (N=6) | 中等度 (N=7) | 重度 (N=6) | |
| 用量(mg/m2) | 1.4 | 1.4 | 0.7 |
| Cmax(ng/mL/mg)注) | 109±50.4 | 140±51.6 | 236±176 |
| AUC0-inf(ng・hr/mL/mg)注) | 408±224 | 595±299a) | 575±232 |
| t1/2(hr) | 43.4±15.3 | 43.9±10.9a) | 38.7±12.5 |
| CL(L/hr) | 3.13±1.65 | 2.07±1.03a) | 2.01±0.875 |
| Vss(L) | 144±73.7 | 86.5±32.7a) | 66.6±26.8 |
16.6.2 肝機能障害患者
固形がん患者18例の肝機能をChild-Pugh分類によって、正常、軽度肝機能障害(Child-Pugh A)及び中等度肝機能障害(Child-Pugh B)に分類し、それぞれエリブリンメシル酸塩を1.4mg/m2、1.1mg/m2及び0.7mg/m2投与した際の薬物動態パラメータにおいて、肝機能の低下に伴いクリアランスの低下、半減期の延長、AUC(投与量補正時)の増加及びCmax(投与量補正時)の増加が認められた8)(外国人データ)。[9.3参照]
| 正常 (N=6) | Child-Pugh A (N=7) | Child-Pugh B (N=5) | |
| 用量(mg/m2) | 1.4 | 1.1 | 0.7 |
| Cmax(ng/mL/mg)注) | 72.0±20.2 | 83.9±28.5 | 100±46.2 |
| AUC0-inf(ng・hr/mL/mg)注) | 229±58.3 | 420±175.4 | 646±412.6 |
| t1/2(hr) | 36.1±8.65 | 41.1±12.73 | 65.9±18.50 |
| CL(L/hr) | 4.57±0.959 | 2.75±1.094 | 2.06±1.028 |
| Vss(L) | 166±50.1 | 113±29.1 | 149±81.5 |
16.6.3 高齢者
母集団薬物動態解析より、エリブリンのクリアランスは、65歳以上の患者と65歳未満の患者において有意な差は認められなかった9)。
16.7 薬物相互作用
16.7.1 その他
In vitro試験においてエリブリンはCYP3A4に対して可逆的な競合阻害作用(Ki:3〜17μmol/L)を示したが、CYP1A2、CYP2C9、CYP2C19、CYP2D6及びCYP2E1に対してはほとんど阻害作用を示さなかった。また、ヒト肝細胞においてCYP1A、CYP2C9、CYP2C19及びCYP3Aの酵素活性及び蛋白発現量に影響を及ぼさなかった6)。
外国人固形がん患者10例にエリブリンメシル酸塩とケトコナゾールを併用投与した際に、エリブリンの薬物動態パラメータはケトコナゾールの影響を受けなかった10)。
外国人固形がん患者11例にリファンピシンを反復投与した後にエリブリンメシル酸塩と併用投与した際に、エリブリンの薬物動態パラメータはリファンピシンの影響を受けなかった11)。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 進行又は再発乳癌を対象とした国内臨床第II相試験
アントラサイクリン系薬剤及びタキサン系薬剤を含む前治療を有する進行又は再発乳癌患者に対し、奏効率は21.3%(17/80例)であった12)。
安全性解析対象症例81例中全例に副作用が認められた。主な副作用は、好中球減少(98.8%)、白血球減少(98.8%)、脱毛症(58.0%)、リンパ球減少(54.3%)、疲労(44.4%)、食欲減退(43.2%)、悪心(42.0%)、口内炎(38.3%)、味覚異常(33.3%)、ヘモグロビン減少(32.1%)、ASTの上昇(29.6%)、ALTの上昇(27.2%)、CKの上昇(25.9%)、発熱(24.7%)、末梢神経障害(24.7%)、γ-GTPの上昇(19.8%)、耐糖能障害(16.0%)、嘔吐(14.8%)、頭痛(14.8%)、発熱性好中球減少(13.6%)、下痢(13.6%)、Al-Pの上昇(12.3%)、LDHの上昇(12.3%)、筋肉痛(12.3%)、発疹(11.1%)、便秘(11.1%)、血小板減少(11.1%)、倦怠感(11.1%)であった13)。
安全性解析対象症例81例中全例に副作用が認められた。主な副作用は、好中球減少(98.8%)、白血球減少(98.8%)、脱毛症(58.0%)、リンパ球減少(54.3%)、疲労(44.4%)、食欲減退(43.2%)、悪心(42.0%)、口内炎(38.3%)、味覚異常(33.3%)、ヘモグロビン減少(32.1%)、ASTの上昇(29.6%)、ALTの上昇(27.2%)、CKの上昇(25.9%)、発熱(24.7%)、末梢神経障害(24.7%)、γ-GTPの上昇(19.8%)、耐糖能障害(16.0%)、嘔吐(14.8%)、頭痛(14.8%)、発熱性好中球減少(13.6%)、下痢(13.6%)、Al-Pの上昇(12.3%)、LDHの上昇(12.3%)、筋肉痛(12.3%)、発疹(11.1%)、便秘(11.1%)、血小板減少(11.1%)、倦怠感(11.1%)であった13)。
17.1.2 進行又は再発乳癌を対象とした外国臨床第III相試験
アントラサイクリン系薬剤及びタキサン系薬剤を含む前治療2〜5レジメンの進行又は再発乳癌患者(762例)において、主治医選択治療注)を比較対照とし、全生存期間を主要評価項目としてエリブリンメシル酸塩の主治医選択治療に対する優越性の検証を目的とした第III相比較試験が実施された。
その結果、全生存期間において、エリブリンメシル酸塩の主治医選択治療に対する優越性が確認された。
エリブリンメシル酸塩投与群における全生存期間の中央値は399日であった14)。
安全性解析対象症例のうちエリブリンメシル酸塩が投与された503例中474例(94.2%)に副作用が認められた。主な副作用は、好中球減少(52.7%)、脱毛症(44.3%)、末梢神経障害(31.9%)、悪心(29.8%)、疲労(25.6%)、白血球減少(24.1%)、無力症(21.7%)、貧血(16.7%)、食欲減退(16.1%)、便秘(15.1%)、発熱(13.3%)、嘔吐(12.7%)、下痢(12.5%)、体重減少(11.7%)、頭痛(10.3%)であった15)。
その結果、全生存期間において、エリブリンメシル酸塩の主治医選択治療に対する優越性が確認された。
エリブリンメシル酸塩投与群における全生存期間の中央値は399日であった14)。
安全性解析対象症例のうちエリブリンメシル酸塩が投与された503例中474例(94.2%)に副作用が認められた。主な副作用は、好中球減少(52.7%)、脱毛症(44.3%)、末梢神経障害(31.9%)、悪心(29.8%)、疲労(25.6%)、白血球減少(24.1%)、無力症(21.7%)、貧血(16.7%)、食欲減退(16.1%)、便秘(15.1%)、発熱(13.3%)、嘔吐(12.7%)、下痢(12.5%)、体重減少(11.7%)、頭痛(10.3%)であった15)。
注)主治医選択治療のうち、10例以上で使用された薬剤は以下の通り。
| 薬剤名:例数(%) | |
| ビノレルビン:61(24.0) | パクリタキセル:26(10.2) |
| ゲムシタビン:46(18.1) | ドキソルビシン:23(9.1) |
| カペシタビン:44(17.3) | ドセタキセル:10(3.9) |
18. 薬効薬理
18.1 作用機序
18.2 抗腫瘍効果
18.2.1 in vitro試験
(2)β-チューブリン変異を有するパクリタキセル耐性ヒト卵巣癌由来細胞株(1A9PTX10及び1A9PTX22)に対して、エリブリンメシル酸塩の細胞増殖抑制作用は減弱しなかった20)。
18.2.2 in vivo試験
19. 有効成分に関する理化学的知見
19.1. エリブリンメシル酸塩
22. 包装
2mL×1バイアル
23. 主要文献
- 日本人固形がん患者を対象とした臨床第I相試験(国内試験)(ハラヴェン静注:2011年4月22日承認、CTD 2.7.6.3)
- エリブリンメシル酸塩の血漿たん白結合(ハラヴェン静注:2011年4月22日承認、CTD 2.6.4.4.3)
- 14C-エリブリン酢酸塩由来放射能の分布(ラット)(ハラヴェン静注:2011年4月22日承認、CTD 2.6.4.4.2.2)
- 14C-エリブリン酢酸塩由来放射能の分布(イヌ)(ハラヴェン静注:2011年4月22日承認、審査報告書)
- 固形がん患者を対象としたマスバランス試験(外国試験)(ハラヴェン静注:2011年4月22日承認、CTD 2.7.6.4)
- エリブリンメシル酸塩のin vitro代謝(ハラヴェン静注:2011年4月22日承認、CTD 2.6.4.5)
- Tan A.R.et al., Cancer Chemother.Pharmacol., 76 (5), 1051-1061, (2015)
- Devriese L.A.et al., Cancer Chemother.Pharmacol., 70 (6), 823-832, (2012)
- エリブリンメシル酸塩の母集団薬物動態解析(ハラヴェン静注:2011年4月22日承認、CTD 2.7.2.3.2.3)
- Devriese L.A.et al., Invest.New Drugs, 31 (2), 381-389, (2013)
- Devriese L.A.et al., Br.J.Clin.Pharmacol., 75 (2), 507-515, (2013)
- 進行又は再発乳癌を対象とした臨床第II相試験(国内試験)(ハラヴェン静注:2011年4月22日承認、CTD 2.7.6.11)
- 進行又は再発乳癌を対象とした臨床第II相試験(国内試験)の臨床的安全性(ハラヴェン静注:2011年4月22日承認、CTD 2.7.4.7)
- 進行又は再発乳癌を対象とした臨床第III相試験(外国試験)(ハラヴェン静注:2011年4月22日承認、CTD 2.7.6.12)
- 進行又は再発乳癌を対象とした臨床第III相試験(外国試験)の臨床的安全性(ハラヴェン静注:2011年4月22日承認、CTD 2.7.4.7)
- Towle M.J.et al., Cancer Res., 61 (3), 1013-1021, (2001)
- Kuznetsov G.et al., Cancer Res., 64 (16), 5760-5766, (2004)
- Jordan M.A.et al., Mol.Cancer Ther., 4 (7), 1086-1095, (2005)
- エリブリンメシル酸塩の作用機序に関する検討(ハラヴェン静注:2011年4月22日承認、CTD 2.6.2.2.1.2)
- エリブリンメシル酸塩のがん細胞増殖抑制作用(in vitro)(ハラヴェン静注:2011年4月22日承認、CTD 2.6.2.2.1)
- エリブリンメシル酸塩の抗腫瘍効果(in vivo)(ハラヴェン静注:2011年4月22日承認、CTD 2.6.2.2.2.1)
- エリブリンメシル酸塩と他の抗がん剤の併用効果(in vivo)(ハラヴェン静注:2011年4月22日承認、CTD 2.6.2.2.2.4)
24. 文献請求先及び問い合わせ先
文献請求先
ニプロ株式会社
医薬品情報室
〒566-8510
大阪府摂津市千里丘新町3番26号
電話:0120-226-898
FAX:050-3535-8939
製品情報問い合わせ先
ニプロ株式会社
医薬品情報室
〒566-8510
大阪府摂津市千里丘新町3番26号
電話:0120-226-898
FAX:050-3535-8939
26. 製造販売業者等
26.1 製造販売元
ニプロ株式会社
大阪府摂津市千里丘新町3番26号