医薬品情報
| 総称名 | クービビック |
|---|---|
| 一般名 | ダリドレキサント塩酸塩 |
| 欧文一般名 | Daridorexant Hydrochloride |
| 製剤名 | ダリドレキサント塩酸塩製剤 |
| 薬効分類名 | オレキシン受容体拮抗薬 不眠症治療薬 |
| 薬効分類番号 | 1190 |
| ATCコード | N05CJ03 |
| KEGG DRUG |
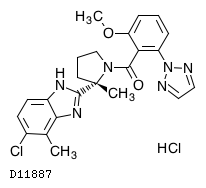
D11887
ダリドレキサント塩酸塩
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年12月 改訂(第4版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| クービビック錠25mg | QUVIVIQ Tablets | ネクセラファーマジャパン | 1190033F1028 | 56.9円/錠 | 習慣性医薬品注1), 処方箋医薬品注2) |
| クービビック錠50mg | QUVIVIQ Tablets | ネクセラファーマジャパン | 1190033F2024 | 90.2円/錠 | 習慣性医薬品注1), 処方箋医薬品注2) |
2. 禁忌
次の患者には投与しないこと
4. 効能または効果
6. 用法及び用量
通常、成人にはダリドレキサントとして1日1回50mgを就寝直前に経口投与する。なお、患者の状態に応じて1日1回25mgを投与することができる。
7. 用法及び用量に関連する注意
7.1 本剤は就寝の直前に服用させること。また、服用して就寝した後、睡眠途中で一時的に起床して仕事等で活動する可能性があるときは服用させないこと。
7.2 入眠効果の発現が遅れるおそれがあるため、本剤の食事と同時又は食直後の服用は避けること。
食後投与では、空腹時投与に比べ、投与直後の本剤の血漿中濃度が低下することがある。[16.2.1参照]
食後投与では、空腹時投与に比べ、投与直後の本剤の血漿中濃度が低下することがある。[16.2.1参照]
7.4 中程度のCYP3A阻害剤と併用する場合は、本剤の血漿中濃度が上昇し、傾眠等の副作用が増強するおそれがあるため、患者の状態を慎重に観察した上で、本剤投与の可否を判断すること。なお、投与する場合は、1日1回25mgとし、慎重に投与すること。[10.2、16.7.2参照]
7.5 他の不眠症治療薬と併用したときの有効性及び安全性は確立されていない。
8. 重要な基本的注意
8.1 本剤の影響が服用の翌朝以後に及び、眠気、注意力・集中力・反射運動能力等の低下が起こることがあるので、自動車の運転など危険を伴う機械の操作に従事させないよう注意すること。[17.3.1参照]
8.2 症状が改善した場合は、本剤の投与継続の要否について検討し、本剤を漫然と投与しないよう注意すること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 ナルコレプシー又はカタプレキシーのある患者
症状を悪化させるおそれがある。
9.1.2 中等度及び重度の呼吸機能障害(閉塞性睡眠時無呼吸及び中等度以下の慢性閉塞性肺疾患患者を除く)を有する患者
これらの患者を対象とした臨床試験は実施していない。[17.3.2参照]
9.1.3 閉塞性睡眠時無呼吸及び慢性閉塞性肺疾患患者
長期投与におけるこれらの患者に対する使用経験はない。
9.1.4 脳に器質的障害のある患者
作用が強くあらわれるおそれがある。
9.3 肝機能障害患者
9.3.1 重度の肝機能障害(Child-Pugh分類C)を有する患者
9.3.2 中等度の肝機能障害(Child-Pugh分類B)を有する患者
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること1)。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ヒト母乳中に本剤が移行することが確認されている2)。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら投与すること。一般に高齢者では生理機能が低下している。
10. 相互作用
相互作用序文
ダリドレキサントは主に薬物代謝酵素CYP3Aによって代謝される。[16.4参照]
薬物代謝酵素用語
CYP3A
10.1 併用禁忌
10.2 併用注意
| 中枢神経抑制剤 フェノチアジン誘導体、 バルビツール酸誘導体 等 | 中枢神経系に対する抑制作用を増強させるおそれがあるため、本剤又は併用薬の投与量の減量の必要性を検討したうえで慎重に投与すること。 | 本剤及びこれらの薬剤は中枢神経系に対する抑制作用を有するため、相互に作用を増強させるおそれがある。 |
| アルコール(飲酒) [16.7.10参照] | 本剤投与中の患者の飲酒に注意する必要がある。 | 本剤及びアルコールは中枢神経抑制作用を有するため、相互に作用を増強させる。 |
| 中程度のCYP3A阻害剤 ジルチアゼム、 ベラパミル、 エリスロマイシン、 フルコナゾール 等 [7.4、16.7.2参照] | 本剤の血漿中濃度が上昇し、本剤の副作用が増強するおそれがある。 | 本剤の代謝酵素であるCYP3Aを中程度に阻害し、本剤の血漿中濃度を上昇させる。 |
| 強い又は中程度のCYP3A誘導剤 リファンピシン、 フェニトイン、 エファビレンツ、 カルバマゼピン 等 [16.7.3参照] | 本剤の効果が減弱するおそれがあるため、CYP3A誘導作用のない又は弱い薬剤への代替を考慮すること。 | 本剤の代謝酵素であるCYP3Aを誘導し、本剤の血漿中濃度を減少させる。 |
| CYP3A基質 ミダゾラム、 シンバスタチン、 タクロリムス 等 [16.7.4参照] | これらの薬剤の血中濃度が上昇するおそれがあるため、患者の状態を慎重に観察し、副作用の発現に十分注意すること。 | 本剤がCYP3Aを阻害し、これらの薬剤の血中濃度を上昇させる可能性がある。 |
| 治療域の狭いP-gp基質 ジゴキシン 等 [16.7.7参照] | これらの薬剤の血中濃度が上昇するおそれがあるため、患者の状態を慎重に観察し、副作用の発現に十分注意すること。 | 本剤がP-gpを阻害し、これらの薬剤の血中濃度を上昇させる可能性がある。 |
11. 副作用
11.2 その他の副作用
| 3%以上 | 1〜3%未満 | 1%未満 | 頻度不明 | |
| 神経系障害 | 傾眠 | 頭痛・頭部不快感 | 浮動性めまい、睡眠時麻痺 | |
| 一般・全身障害 | 倦怠感・疲労 | |||
| 精神障害 | 悪夢 | 幻覚、異常な夢、睡眠時随伴症(夢遊症、ねごと等) | ||
| 胃腸障害 | 悪心 | |||
| 免疫系障害 | 過敏症(発疹、蕁麻疹等) |
13. 過量投与
13.1 症状
本剤の過量投与に関する情報は少ない。臨床薬理試験において健康被験者に最大で本剤200mgを単回投与した。
50mgを超える用量では、傾眠、筋力低下、睡眠時麻痺、注意力障害、疲労、頭痛及び便秘の副作用が観察された(外国人データ)。
50mgを超える用量では、傾眠、筋力低下、睡眠時麻痺、注意力障害、疲労、頭痛及び便秘の副作用が観察された(外国人データ)。
13.2 処置
本剤に特異的な解毒剤はない。ダリドレキサントの血漿タンパク結合率は高いため、血液透析では除去できない。
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
16. 薬物動態
16.1 血中濃度
16.1.1 健康成人
日本人健康非高齢者及び高齢者男女にダリドレキサント25mg及び50mgを1日1回4日間投与したときの血漿中濃度推移及び薬物動態パラメータは下記のとおりであった3)。
1日1回投与時の1日目及び4日目の血漿中ダリドレキサント濃度推移(平均値±標準偏差)
(25mg)
(50mg)
投与2日目及び3日目は投与直前(トラフ)の血漿中濃度のみ測定した。
| 25mg | 50mg | |||
| 投与1日目 (N=6) | 投与4日目 (N=6) | 投与1日目 (N=6) | 投与4日目 (N=6) | |
| Cmax(ng/mL) | 735(567,904) | 868(597,1138) | 944(532,1354) | 1262(675,1849) |
| Tmax(h) | 1.00(−0.05,2.05) | 0.75(0.11,1.39) | 1.42(0.11,2.72) | 1.00(−0.05,2.05) |
| AUC0-24(ng・h/mL) | 3927(2804,5050) | 4114(3185,5043) | 7185(4446,9924) | 6804(4606,9003) |
| t1/2(h) | 6.16(4.24,8.08) | 6.42(5.18,7.65) | 6.92(5.30,8.53) | 6.60(4.48,8.71) |
| 25mg | 50mg | |||
| 投与1日目 (N=6) | 投与4日目 (N=5) | 投与1日目 (N=6) | 投与4日目 (N=6) | |
| Cmax(ng/mL) | 824(636,1013) | 692(384,1001) | 1059(871,1247) | 1034(849,1219) |
| Tmax(h) | 0.58(0.37,0.80) | 1.10(0.29,1.91) | 1.00(0.34,1.66) | 1.25(0.61,1.89) |
| AUC0-24(ng・h/mL) | 3819(3020,4617) | 4677(3441,5914) | 6357(4367,8348) | 6860(5141,8579) |
| t1/2(h) | 11.66(8.47,14.85) | 9.80(7.06,12.55) | 9.73(7.60,11.86) | 8.87(7.05,10.69) |
16.2 吸収
16.2.1 食事の影響
健康成人20名にダリドレキサント50mgを単回投与(20名の被験者を2つのグループに分け、2期のクロスオーバー試験)した際の中止例を除いた19名のTmax、Cmax及びAUC0-24及びこれらの摂食時/絶食時の幾何平均比は以下のとおりである。Tmaxが1.28時間延長し、Cmaxは15.6%減少した4)(外国人データ)。[7.2参照]
| 摂食時 (N=19) | 絶食時 (N=19) | 幾何平均比 摂食時/絶食時 (N=19) | |
| Cmax(ng/mL) | 800(673,951) | 947(806,1112) | 0.84(0.73,0.98) |
| Tmax(h) | 4.0(1.0,8.0) | 2.0(0.5,5.0) | 1.28(0.50,2.31) |
| AUC0-24(ng・h/mL) | 6858(5649,8327) | 7556(6358,8981) | 0.91(0.83,1.00) |
16.3 分布
ダリドレキサントの血漿タンパク結合率は99.7〜99.9%であり、アルブミン及びα1-酸性糖蛋白のいずれにも結合した5)。
16.4 代謝
16.5 排泄
健康成人男性6名に14C-ダリドレキサント50mgを単回投与したとき、投与終了後168時間までの放射能の尿中及び糞便中の累積回収率の算術平均(95%信頼区間)はそれぞれ27.9%(23.4〜32.4)及び56.6%(49.6〜63.5)であり、糞便中が主な排泄経路であった。尿中及び糞便中から回収された未変化体は微量であった(投与量の0.3%)7)(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 高齢者
日本人健康高齢者(65〜74歳)にダリドレキサント25mg及び50mg(各6名)を1日1回4日間反復投与したときの4日目のダリドレキサントのCmaxの幾何平均比(健康高齢者/健康非高齢者)及びその90%信頼区間はそれぞれ0.79(0.53〜1.15)及び0.88(0.62〜1.25)であった。一方AUC0-24では1.14(0.90〜1.45)及び1.03(0.77〜1.38)であった。t1/2は1.52(1.21〜1.90)及び1.38(1.03〜1.83)であった3)。
16.6.2 腎機能障害患者
重度の腎機能障害患者(Cockcroft-Gault式によるCCrで重度の腎機能障害[30mL/分未満])8名にダリドレキサント25mgを単回投与したとき、ダリドレキサントのCmax及びAUC0-∞の幾何平均比(腎機能障害患者/健康成人)及びその90%信頼区間は、0.94(0.60〜1.46)及び1.16(0.63〜2.12)であり、健康成人と重度の腎機能障害患者の違いはなかった。一方t1/2でも幾何平均比は0.99(0.66〜1.48)であり両者に違いはなかった8)(外国人データ)。
16.6.3 肝機能障害患者
軽度及び中等度の肝機能障害患者(Child-Pugh分類A及びB)それぞれ8名にダリドレキサント25mgを単回投与したとき、血漿タンパク非結合型ダリドレキサントのCmax及びAUC0-∞の幾何平均比(肝機能障害患者/健康成人)及びその90%信頼区間は、Cmaxが軽度及び中等度でそれぞれ0.92(0.72〜1.18)及び0.94(0.74〜1.20)、AUC0-∞がそれぞれ0.94(0.57〜1.54)及び1.60(0.93〜2.73)であり、健康成人と比較して軽度肝機能障害患者では違いはなかったものの、中等度肝機能障害患者ではAUC0-∞が60%増加した。一方、t1/2の幾何平均比及びその90%信頼区間は軽度及び中等度の肝機能障害患者でそれぞれ0.97(0.62〜1.53)及び2.09(0.32〜3.30)であり、中等度肝機能障害患者では延長した9)(外国人データ)。
重度肝機能障害患者(Child-Pugh分類C)での薬物動態は検討していない。[2.2、7.3、9.3.1、9.3.2参照]
重度肝機能障害患者(Child-Pugh分類C)での薬物動態は検討していない。[2.2、7.3、9.3.1、9.3.2参照]
16.7 薬物相互作用
16.7.1 In vitro試験
In vitroにおいて、ダリドレキサントはCYP3A4を最も強く阻害し、その阻害定数は約5μMであった10)。
16.7.2 ジルチアゼム(中程度のCYP3A4阻害剤)
16.7.3 エファビレンツ(中程度のCYP3A4誘導剤)
16.7.4 ミダゾラム(CYP3A4の基質)
健康成人男性20名にダリドレキサント25mgを1日1回5日間投与の5日目にミダゾラム2mgを単回投与した際のミダゾラムのCmax、AUC0-24及びt1/2の幾何平均比(併用/非併用)及びその90%信頼区間はそれぞれ0.94(0.83〜1.05)、0.98(0.91〜1.05)及び0.88(0.78〜0.98)であった13)(外国人データ)。
健康成人男性18名にダリドレキサント50mgを8日間反復投与後の定常状態においてミダゾラム2mgを併用したときのミダゾラムのCmax、AUC0-24及びt1/2の幾何平均比(併用/非併用)及びその90%信頼区間はそれぞれ1.12(0.96〜1.29)、1.35(1.23〜1.47)及び1.14(1.05〜1.23)であった14)(外国人データ)。[10.2参照]
健康成人男性18名にダリドレキサント50mgを8日間反復投与後の定常状態においてミダゾラム2mgを併用したときのミダゾラムのCmax、AUC0-24及びt1/2の幾何平均比(併用/非併用)及びその90%信頼区間はそれぞれ1.12(0.96〜1.29)、1.35(1.23〜1.47)及び1.14(1.05〜1.23)であった14)(外国人データ)。[10.2参照]
16.7.5 生理学的薬物速度論モデルによるシミュレーション(イトラコナゾール(強いCYP3A4阻害剤))
16.7.6 ワルファリン(CYP2C9の基質)
健康成人男性18名にダリドレキサント50mgを単回投与し1時間後にワルファリン25mgを単回投与した際のワルファリンのCmax、AUC0-24及びt1/2の幾何平均比(併用/非併用)及びその90%信頼区間はそれぞれ0.97(0.91〜1.04)、1.00(0.96〜1.04)及び1.15(1.09〜1.22)であった14)(外国人データ)。
16.7.7 ダビガトランエテキシラート(P-gpの基質)
16.7.8 ロスバスタチン(BCRPの基質)
健康成人男性20名にダリドレキサント25mgを1日1回8日間反復投与中の4日目にロスバスタチン10mgを単回投与した際のロスバスタチンのCmax、AUC0-t及びt1/2の幾何平均比(併用/非併用)及びその90%信頼区間はそれぞれ0.93(0.82〜1.04)、0.94(0.85〜1.04)及び1.09(0.92〜1.29)であり、健康成人男性24名にダリドレキサント50mgを1日1回8日間反復投与中の5日目の定常状態においてロスバスタチン10mgを単回投与した際のロスバスタチンのCmax、AUC0-t及びt1/2の幾何平均比(併用/非併用)及びその90%信頼区間はそれぞれ1.06(0.93〜1.21)、1.00(0.92〜1.10)及び1.13(0.97〜1.32)であった16)17)(外国人データ)。
16.7.9 ファモチジン(胃内pH調節剤)
健康成人男性24名にファモチジン40mgを単回投与し3時間後にダリドレキサント50mgを単回投与した際のダリドレキサントのCmax及びAUC0-∞の幾何平均比(併用/非併用)及びその90%信頼区間はそれぞれ0.61(0.50〜0.73)及び1.03(0.92〜1.16)であり、ファモチジンとの併用によりCmaxは39%減少したが、AUC0-∞に変化はなかった。また、t1/2の幾何平均比及びその90%信頼区間は1.27(1.13〜1.42)でありファモチジンとの併用において大きな変化はなかった18)(外国人データ)。
16.7.10 アルコール
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験
精神疾患の診断・統計マニュアル第5版(DSM-5)の基準により不眠症患者と診断された成人患者(20〜83歳)489名(うち65歳以上の高齢者を30.1%[147/489名]含む)を対象にダリドレキサント又はプラセボを1日1回就寝前に4週間投与した。
主要評価項目は二つ設定した。一つ目の主要評価項目は睡眠日誌を用いて調査したダリドレキサント50mg群の主観的総睡眠時間(sTST)のベースラインから4週間後への変化であった。sTST(平均値±標準偏差)はプラセボ群では19.69±36.99分延長したのに対し、ダリドレキサント50mg群では41.01±49.19分延長し、ダリドレキサント50mg群において統計学的に有意な延長を認めた(プラセボ群vs.ダリドレキサント50mg群の差(最小二乗平均値、95%信頼区間)は20.30(11.39〜29.20):p<0.001)。
主要評価項目は二つ設定した。一つ目の主要評価項目は睡眠日誌を用いて調査したダリドレキサント50mg群の主観的総睡眠時間(sTST)のベースラインから4週間後への変化であった。sTST(平均値±標準偏差)はプラセボ群では19.69±36.99分延長したのに対し、ダリドレキサント50mg群では41.01±49.19分延長し、ダリドレキサント50mg群において統計学的に有意な延長を認めた(プラセボ群vs.ダリドレキサント50mg群の差(最小二乗平均値、95%信頼区間)は20.30(11.39〜29.20):p<0.001)。
| 評価時期 | 項目 | プラセボ群 (N=163)** | 25mg群 (N=163)** | 50mg群 (N=162)** |
| ベースライン | 平均値(分) | 317.82 | 314.37 | 314.86 |
| 4週 | 平均値(分) | 337.31 | 344.32 | 355.07 |
| ベースラインからの変化(分) | 19.69 | 29.27 | 41.01 | |
| プラセボとの差(分)* | − | 9.23 | 20.30 |
もう一つの主要評価項目は、睡眠日誌を用いて調査したダリドレキサント50mg群の主観的睡眠潜時(sLSO)のベースラインから4週間後への変化であり、sLSO(平均値±標準偏差)はプラセボ群では5.56±26.22分短縮したのに対し、ダリドレキサント50mg群では16.81±28.38分短縮し、ダリドレキサント50mg群において統計学的に有意な短縮を認めた(プラセボ群vs.ダリドレキサント50mg群の差(最小二乗平均値、95%信頼区間)は−10.66(−15.78〜−5.54):p<0.001)。
| 評価時期 | 項目 | プラセボ群 (N=163)** | 25mg群 (N=163)** | 50mg群 (N=162)** |
| ベースライン | 平均値(分) | 53.35 | 53.05 | 54.03 |
| 4週 | 平均値(分) | 47.59 | 40.83 | 37.89 |
| ベースラインからの変化(分) | −5.56 | −12.95 | −16.81 | |
| プラセボとの差(分)* | − | −7.16 | −10.66 |
副作用の発現頻度は、プラセボ群が8.5%(14/164名)及びダリドレキサント25mg群が7.4%(12/163名)、ダリドレキサント50mg群が11.1%(18/162名)であった。ダリドレキサント投与群の1%以上の患者で発現した副作用は、傾眠がプラセボ群で1.8%(3/164名)、ダリドレキサント25mg群で3.7%(6/163名)及びダリドレキサント50mg群で6.8%(11/162名)、浮動性めまいがプラセボ群で0.6%(1/164名)、ダリドレキサント25mg群で0%(0/163名)及びダリドレキサント50mg群で1.9%(3/162名)であった20)。
17.3 その他
17.3.1 自動車運転能力に対する影響
高齢者を含む健康成人男女60名にダリドレキサント50mg又は100mg注)を1日1回4日間就寝前に投与し、1日目及び4日目の投与9時間後(それぞれ2日目及び5日目の朝)に、自動車運転シミュレーターを用いて自動車の横方向位置の中心からのずれを連続測定し、その標準偏差(SDLP)を算出した。SDLPのプラセボ群との差の平均値(97.5%信頼区間)は2日目において50mg群が2.19(0.46〜3.93)cm及び100mg群が4.43(2.72〜6.15)cmであり、両群とも信頼区間の上限は閾値†として設定した2.6cmを超えた。一方、5日目において50mg群が0.26(−1.08〜1.59)cm及び100mg群が0.94(−0.40〜2.27)cmであり、いずれも信頼区間の上限は閾値†を下回った21)(外国人データ)。[8.1参照]
注)本剤の承認用量は50mgまでである。
†:閾値:血中アルコール濃度が0.05%の際に得られるSDLPの値
17.3.2 呼吸機能への影響
中等度の慢性閉塞性肺疾患(COPD)患者男女28名にダリドレキサント50mg又はプラセボを1日1回夜間に5日間反復投与中の5日目の就寝中に測定した酸素飽和度(SpO2)の平均値(95%信頼区間)はプラセボ群が91.55(90.86〜92.25)に対しダリドレキサント50mg群が91.77(91.03〜92.51)であり、ダリドレキサントによる影響はなかった22)(外国人データ)。
軽度から中等度の閉塞性睡眠時無呼吸(OSA)患者28名にダリドレキサント50mgを1日1回5日間夜間に投与した際の5日目の就寝中に測定した無呼吸/低呼吸指数(AHI)†の平均値(95%信頼区間)はプラセボ群が14.23(11.06〜17.40)回/時間に対しダリドレキサント50mg群が15.11(11.97〜18.24)回/時間であり、ダリドレキサントによる影響はなかった23)(外国人データ)。
重度の閉塞性睡眠時無呼吸(OSA)患者男女16名にダリドレキサント50mg又はプラセボを1日1回夜間に5日間反復投与中の5日目の就寝中の無呼吸/低呼吸指数(AHI)†の平均値(95%信頼区間)はプラセボ群が47.90(40.92〜54.89)回/時間に対しダリドレキサント50mg群が44.16(37.41〜50.92)回/時間であり、ダリドレキサントによる影響はなかった24)(外国人データ)。[9.1.2参照]
軽度から中等度の閉塞性睡眠時無呼吸(OSA)患者28名にダリドレキサント50mgを1日1回5日間夜間に投与した際の5日目の就寝中に測定した無呼吸/低呼吸指数(AHI)†の平均値(95%信頼区間)はプラセボ群が14.23(11.06〜17.40)回/時間に対しダリドレキサント50mg群が15.11(11.97〜18.24)回/時間であり、ダリドレキサントによる影響はなかった23)(外国人データ)。
重度の閉塞性睡眠時無呼吸(OSA)患者男女16名にダリドレキサント50mg又はプラセボを1日1回夜間に5日間反復投与中の5日目の就寝中の無呼吸/低呼吸指数(AHI)†の平均値(95%信頼区間)はプラセボ群が47.90(40.92〜54.89)回/時間に対しダリドレキサント50mg群が44.16(37.41〜50.92)回/時間であり、ダリドレキサントによる影響はなかった24)(外国人データ)。[9.1.2参照]
†:無呼吸/低呼吸指数:就寝中の無呼吸又は低呼吸の回数を総睡眠時間(分)で除して60を乗じた値
17.3.3 薬物乱用の可能性
レクリエーションドラッグを使用している健康成人男女71名にダリドレキサント50mg、100mg及び150mg注)を単回投与した際の薬物嗜好度の視覚的アナログスケールを用いた評価では、陽性対照のスボレキサント150mg及びゾルピデム30mgでのスコア±標準誤差がそれぞれ80.7±1.88及び79.9±1.81であったのに対し、ダリドレキサントの50mg、100mg及び150mgではそれぞれ73.2±2.11、79.1±2.07及び81.3±1.79であり、50mgでは陽性対照に比べ有意に低かった25)(外国人データ)。
注)本剤の承認用量は50mgまでである。
17.3.4 夜間の安全性
健康成人36名にそれぞれプラセボ、ダリドレキサント25mg及び50mgを就寝前に単回投与し、投与4時間後の夜中に姿勢安定性†を評価した(クロスオーバー試験)。重心動揺はダリドレキサント25mg及び50mg群ではプラセボ群に比べて用量依存的な増加が見られた26)(外国人データ)。
†:姿勢安定性:重心動揺計を用いて被験者の重心の揺れを2分間測定し、積分した値(mm)
18. 薬効薬理
18.1 作用機序
ダリドレキサントは、オレキシン神経ペプチドによるオレキシン受容体タイプ1(OX1R)及びオレキシン受容体タイプ2(OX2R)の両方の活性を抑制する、デュアルオレキシン受容体拮抗薬である。In vitroにおけるダリドレキサントのヒトOX1R及びヒトOX2Rに対する見かけの平衡解離定数は、それぞれ0.47nM及び0.93nMであった27)。
18.2 睡眠障害に対する作用
ダリドレキサントは、ラット及びイヌにおいてノンレム睡眠及びレム睡眠時間をともに増加することで、全体の睡眠時間を増加させた。
また、ダリドレキサントは、ラットにおいて睡眠構造を変えることなく、用量依存的に持続入眠潜時を短縮した28)。
また、ダリドレキサントは、ラットにおいて睡眠構造を変えることなく、用量依存的に持続入眠潜時を短縮した28)。
19. 有効成分に関する理化学的知見
19.1. ダリドレキサント塩酸塩
20. 取扱い上の注意
アルミピロー包装開封後は湿気を避けて保存すること。
21. 承認条件
医薬品リスク管理計画を策定の上、適切に実施すること。
22. 包装
<クービビック錠25mg>100錠(10錠PTP×10)
<クービビック錠50mg>100錠(10錠PTP×10)
23. 主要文献
- 社内資料:胚・胎児発生に関する試験(2024年9月24日承認、CTD 2.6.6.6.2)
- 社内資料:授乳中健康女性を対象とした乳汁移行を検討した試験(2024年9月24日承認、CTD 2.7.6.1.25)
- 社内資料:日本人健康成人を対象とした第I相試験(2024年9月24日承認、CTD 2.7.6.1.16)
- 社内資料:健康成人を対象とした食事の影響試験(2024年9月24日承認、CTD 2.7.6.1.13)
- 社内資料:血漿タンパク結合及び血球移行(2024年9月24日承認、CTD 2.6.4.4.2)
- 社内資料:代謝酵素(2024年9月24日承認20、CTD 2.6.4.5.5)
- 社内資料:健康成人を対象とした絶対的バイオアベイラビリティ、マスバランス及び代謝を検討した試験(2024年9月24日承認、CTD 2.7.6.1.1)
- 社内資料:腎機能障害患者を対象とした臨床薬理試験(2024年9月24日承認、CTD 2.7.6.1.15)
- 社内資料:肝機能障害患者を対象とした臨床薬理試験(2024年9月24日承認、CTD 2.7.6.1.12)
- 社内資料:ダリドレキサントの相互作用薬としての可能性(2024年9月24日承認、CTD 2.6.4.7.2)
- 社内資料:ジルチアゼムとの相互作用試験(2024年9月24日承認、CTD 2.7.6.1.3)
- 社内資料:エファビレンツとの相互作用試験(2024年9月24日承認、CTD 2.7.6.1.18)
- 社内資料:ミダゾラムとの相互作用試験(2024年9月24日承認、CTD 2.7.6.1.4)
- 社内資料:ミダゾラム及びワルファリンとの相互作用試験(2024年9月24日承認、CTD 2.7.6.1.21)
- 社内資料:生理学的薬物速度論モデルを用いた薬物相互作用の予測(2024年9月24日承認、CTD 2.6.4.7.3)
- 社内資料:ダビガトラン及びロスバスタチンとの相互作用試験(2024年9月24日承認、CTD 2.7.6.1.20)
- 社内資料:ロスバスタチンとの相互作用試験(2024年9月24日承認、CTD 2.7.6.1.6)
- 社内資料:ファモチジンとの相互作用試験(2024年9月24日承認、CTD 2.7.6.1.18)
- 社内資料:アルコールとの相互作用試験(2024年9月24日承認、CTD 2.7.6.1.11)
- 社内資料:日本人不眠症患者を対象とした第3相試験(2024年9月24日承認、CTD 2.7.6.2.7)
- 社内資料:健康成人を対象とした自動車運転影響試験(2024年9月24日承認、CTD 2.7.6.1.8)
- 社内資料:慢性閉塞性肺疾患患者を対象とした呼吸器への影響を検討した臨床薬理試験(2024年9月24日承認、CTD 2.7.6.1.9)
- 社内資料:閉塞性睡眠時無呼吸患者を対象とした呼吸器への影響を検討した臨床薬理試験(2024年9月24日承認、CTD 2.7.6.1.10)
- 社内資料:閉塞性睡眠時無呼吸患者を対象とした呼吸器への影響を検討した臨床薬理試験(2024年9月24日承認、CTD 2.7.6.1.24)
- 社内資料:レクリエーションドラッグ使用経験者を対象とした薬物乱用への影響を検討した臨床薬理試験(2024年9月24日承認、CTD 2.7.6.1.7)
- 社内資料:夜間の安全性試験(2024年9月24日承認、CTD 2.7.6.1.23)
- 社内資料:オレキシン受容体におけるダリドレキサントの阻害の効力、持続性及び滞留時間(2024年9月24日承認、CTD 2.6.2.2.1.1)
- 社内資料:In vivo薬理試験(2024年9月24日承認、CTD 2.6.2.2.2)
24. 文献請求先及び問い合わせ先
文献請求先
製品情報問い合わせ先
26. 製造販売業者等
26.1 製造販売元
ネクセラファーマジャパン株式会社
東京都港区赤坂9丁目7番2号
26.2 販売元
塩野義製薬株式会社
大阪市中央区道修町3丁目1番8号