医薬品情報
| 総称名 | ユバンシ |
|---|---|
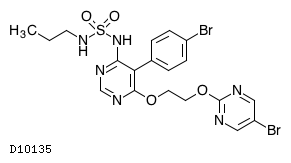
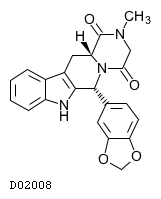
| 一般名 | マシテンタン タダラフィル |
| 欧文一般名 | Macitentan Tadalafil |
| 製剤名 | マシテンタン・タダラフィル配合錠 |
| 薬効分類名 | エンドセリン受容体拮抗薬 ホスホジエステラーゼ5阻害剤 |
| 薬効分類番号 | 2190 |
| ATCコード | C02KX54 |
| KEGG DRUG |
D12963
マシテンタン・タダラフィル
|
| JAPIC | 添付文書(PDF) |
添付文書情報2026年3月 改訂(第3版)
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ユバンシ配合錠 | Yuvanci Combination Tablets | ヤンセンファーマ | 2190105F1029 | 13272.5円/錠 | 劇薬, 処方箋医薬品※ |
1. 警告
タダラフィルと硝酸剤又は一酸化窒素(NO)供与剤(ニトログリセリン、亜硝酸アミル、硝酸イソソルビド、ニコランジル等)との併用により降圧作用が増強し、過度に血圧を下降させることがあるので、本剤投与の前に、硝酸剤又は一酸化窒素(NO)供与剤が投与されていないことを十分確認し、本剤投与中及び投与後においても硝酸剤又は一酸化窒素(NO)供与剤が投与されないよう十分注意すること。[2.3、10.1参照]
ただし、肺動脈性肺高血圧症の治療において一酸化窒素吸入療法と本剤の併用が治療上必要と判断される場合は、緊急時に十分対応できる医療施設において、肺動脈性肺高血圧症の治療に十分な知識と経験を持つ医師のもとで、慎重に投与すること。
ただし、肺動脈性肺高血圧症の治療において一酸化窒素吸入療法と本剤の併用が治療上必要と判断される場合は、緊急時に十分対応できる医療施設において、肺動脈性肺高血圧症の治療に十分な知識と経験を持つ医師のもとで、慎重に投与すること。
2. 禁忌
次の患者には投与しないこと
2.2 重度の低血圧(血圧<90/50mmHg)の患者[8.4参照]
2.3 硝酸剤又は一酸化窒素(NO)供与剤(ニトログリセリン、亜硝酸アミル、硝酸イソソルビド、ニコランジル等)を投与中の患者[1.、10.1参照]
2.4 可溶性グアニル酸シクラーゼ(sGC)刺激剤(リオシグアト)を投与中の患者[10.1参照]
2.5 強いCYP3A4阻害剤(イトラコナゾール、リトナビル含有製剤、アタザナビル、ダルナビル含有製剤、クラリスロマイシン、コビシスタット含有製剤、エンシトレルビル、セリチニブ)を投与中の患者[10.1、16.7.2(2)参照]
2.7 重度の腎障害患者[9.2.1参照]
2.8 重度の肝障害患者[9.3.1参照]
2.9 本剤及び本剤の成分に過敏症の既往歴のある患者
4. 効能または効果
5. 効能または効果に関連する注意
5.1 本剤を肺動脈性肺高血圧症の第一選択薬としないこと。
5.2 本剤の使用にあたっては、最新の治療ガイドラインを参考に投与の要否を検討すること。
5.3 原則として、マシテンタン10mg1日1回及びタダラフィル40mg1日1回による併用治療を受けている場合に、本剤の使用を検討すること。
5.4 WHO機能分類クラスIにおける有効性及び安全性は確立していない。
6. 用法及び用量
通常、成人には1日1回1錠(マシテンタンとして10mg及びタダラフィルとして40mg)を経口投与する。
8. 重要な基本的注意
8.1 他のエンドセリン受容体拮抗薬(ERA)において肝酵素値上昇が認められているため、肝機能検査を必ず投与開始前に行い、投与中は、必要に応じて肝機能検査を定期的に実施すること。本剤投与中に臨床的に顕著にAST、ALT値が上昇した場合、これら肝酵素値上昇に伴いビリルビン値が基準値上限の2倍を超える場合、又はこれら肝酵素値上昇に伴い黄疸などの肝障害の徴候を伴う場合には、本剤の投与を中止すること。[9.3.2参照]
8.3 本剤の投与により肺水腫の徴候がみられた場合は肺静脈閉塞性疾患の可能性を考慮すること。肺静脈閉塞性疾患が疑われた場合には、本剤の投与を中止すること。[9.1.3参照]
8.4 本剤は血管拡張作用を有するため、本剤の投与に際しては、血管拡張作用により患者が有害な影響を受ける可能性がある状態(降圧剤投与中、安静時低血圧、血液量減少、重度の左室流出路閉塞、自律神経機能障害等)にあるのかを十分検討すること。[2.2参照]
8.5 4時間以上の勃起の延長又は持続勃起(6時間以上持続する痛みを伴う勃起)が外国にてごくまれに報告されている。持続勃起に対する処置を速やかに行わないと陰茎組織の損傷又は勃起機能を永続的に損なうことがあるので、勃起が4時間以上持続する症状がみられた場合、直ちに医師の診断を受けるよう指導すること。
8.6 タダラフィルの臨床試験において、めまいや視覚障害が認められているので、高所作業、自動車の運転等危険を伴う機械を操作する際には注意させること。
8.7 本剤投与後に急激な視力低下又は急激な視力喪失があらわれた場合には、速やかに眼科専門医の診察を受けるよう、患者に指導すること。[15.1.2(2)参照]
8.8 本剤投与後に急激な聴力低下又は突発性難聴(耳鳴り、めまいを伴うことがある)があらわれた場合には、速やかに耳鼻科専門医の診察を受けるよう、患者に指導すること。[15.1.2(4)参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.2 コントロール不良の不整脈又はコントロール不良の高血圧(安静時血圧>160/100mmHg)のある患者
これらの患者における安全性及び有効性は確立していない。
9.1.3 肺静脈閉塞性疾患患者
本剤を投与しないことが望ましい。血管拡張薬を使用した場合に肺水腫の発現が報告されている。[8.3参照]
9.1.4 脳梗塞・脳出血の既往歴が最近6カ月以内にある患者
これらの患者における安全性及び有効性は確立していない。
9.1.5 網膜色素変性症患者
ホスホジエステラーゼ(PDE)の遺伝的障害を持つ症例が少数認められる。
9.1.6 陰茎の構造上欠陥(屈曲、陰茎の線維化、Peyronie病等)のある患者
タダラフィルの薬理作用により勃起が起こり、その結果陰茎に痛みを引き起こす可能性がある。
9.1.7 持続勃起症の素因となり得る疾患(鎌状赤血球性貧血、多発性骨髄腫、白血病等)のある患者
9.1.8 出血性疾患又は消化性潰瘍のある患者
タダラフィルのin vitro試験でニトロプルシドナトリウム(NO供与剤)の血小板凝集抑制作用を増強することが認められている。出血性疾患又は消化性潰瘍のある患者に対する安全性は確立していない。
9.1.9 重症の左室流出路閉塞、体液減少、自律神経障害に伴う低血圧や安静時低血圧等を有する患者
本剤は血管拡張作用を有するため一過性の軽度の血圧低下があらわれる場合がある。
9.1.10 出血の危険因子(ビタミンK拮抗薬等の抗凝固療法、抗血小板療法、結合組織疾患に伴う血小板機能異常、経鼻酸素療法)を有する患者
出血の危険性が高まるおそれがある。[10.2参照]
9.2 腎機能障害患者
9.2.1 重度の腎障害患者
9.2.2 軽度又は中等度の腎障害患者
クレアチニンクリアランスが60mL/分未満又は慢性腎障害の徴候が見られる日本人患者は本剤の臨床試験では除外されている。[16.6.2参照]
9.3 肝機能障害患者
9.3.1 重度の肝障害患者
9.3.2 軽度又は中等度の肝障害患者
9.4 生殖能を有する者
9.5 妊婦
9.5.1 マシテンタン
動物実験(ラット及びウサギ)で下顎弓癒合異常及び心血管系異常などが報告されており、最小毒性量に基づく安全域はラットで約3倍未満、ウサギで約30倍未満であった。また、胚吸収増加などが報告されている。
9.6 授乳婦
本剤投与中は授乳しないことが望ましい。
9.6.1 マシテンタン
動物実験(ラット)では、マシテンタンは乳汁中に移行することが確認されている。また、母動物(ラット)に妊娠17日から分娩後20日まで経口投与した結果、出生児の体重の低値及び死亡の増加が認められている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
一般に生理機能が低下していることが多い。[16.6.3参照]
10. 相互作用
相互作用序文
マシテンタンは主にCYP3A4及びCYP2C9により代謝される。タダラフィルは主にCYP3A4により代謝される。[16.4.1参照]
薬物代謝酵素用語
CYP3A4
薬物代謝酵素用語
CYP2C9
10.1 併用禁忌
| 硝酸剤及びNO供与剤 ニトログリセリン 亜硝酸アミル 硝酸イソソルビド ニコランジル等 [1.、2.3参照] | これらの薬剤とタダラフィルの併用により、降圧作用を増強するとの報告がある。1)2)3) | NOはcGMPの産生を刺激し、一方、タダラフィルはcGMPの分解を抑制することから、これらの薬剤との併用によりcGMPの増大を介するNOの降圧作用が増強する。 |
| sGC刺激剤 リオシグアト(アデムパス) [2.4参照] | 併用により、血圧低下を起こすおそれがある。 | リオシグアトとタダラフィルの併用により、細胞内cGMP濃度が増加し、全身血圧に相加的な影響を及ぼすおそれがある。 |
| 強いCYP3A4阻害剤 イトラコナゾール(イトリゾール) リトナビル含有製剤(ノービア、カレトラ、パキロビッド) アタザナビル(レイアタッツ) ダルナビル含有製剤(プリジスタ、プレジコビックス、シムツーザ) クラリスロマイシン(クラリス、クラリシッド) コビシスタット含有製剤(スタリビルド、ゲンボイヤ、プレジコビックス、シムツーザ) エンシトレルビル(ゾコーバ) セリチニブ(ジカディア) [2.5、16.7.2(2)参照] | マシテンタン及びタダラフィルの血中濃度が上昇し、本剤の副作用が発現しやすくなるおそれがある。 | 強いCYP3A4阻害作用により、マシテンタン及びタダラフィルの曝露量を増加させる。 |
| 強いCYP3A4誘導剤 リファンピシン(リファジン) セイヨウオトギリソウ(セント・ジョーンズ・ワート)含有食品 カルバマゼピン(テグレトール) フェニトイン(アレビアチン、ヒダントール) フェノバルビタール(フェノバール等) リファブチン(ミコブティン) [2.6、16.7.1(5)参照] | マシテンタン及びタダラフィルの血中濃度が低下し、本剤の効果が減弱するおそれがある。 リファンピシン(600mg/日)との併用により、タダラフィル(10mg)のAUC及びCmaxがそれぞれ88%及び46%低下するとの報告がある。 | 強いCYP3A4誘導作用により、マシテンタン及びタダラフィルの曝露量を減少させる。 |
10.2 併用注意
| 中程度のCYP3A4阻害作用かつ中程度のCYP2C9阻害作用を有する薬剤 フルコナゾール [16.7.1(6)参照] | マシテンタンの血中濃度が上昇し、マシテンタンの副作用が発現しやすくなるおそれがある。 | CYP3A4阻害作用及びCYP2C9阻害作用により、マシテンタンの曝露量を増加させる可能性がある。 |
| CYP3A4誘導剤 エファビレンツ モダフィニル ルフィナミド等 | マシテンタン及びタダラフィルの血中濃度が低下し、本剤の効果が減弱するおそれがある。 | CYP3A4誘導作用により、マシテンタン及びタダラフィルの曝露量を減少させる。 |
| CYP3A4阻害剤 ホスアンプレナビル ジルチアゼム エリスロマイシン ベラパミル グレープフルーツジュース等 | タダラフィルの血中濃度が上昇し、タダラフィルの副作用が発現しやすくなるおそれがある。 | CYP3A4阻害作用により、タダラフィルの曝露量を増加させる。 |
| ボセンタン [16.7.2(3)参照] | ボセンタン(125mg/1日2回投与)との10日間併用により、タダラフィル(40mg)の10日目におけるAUC及びCmaxが初日と比べてそれぞれ41.5%及び26.6%低下するとの報告がある。タダラフィルによるボセンタンのAUC及びCmaxに対する影響はみられなかった。 | CYP3A4誘導によるクリアランスの増加によりタダラフィルの血漿中濃度が低下する。 |
| α遮断剤 ドキサゾシン テラゾシン等 [16.7.2(5)参照] | ドキサゾシン(8mg)とタダラフィル(20mg)の併用により、立位収縮期血圧及び拡張期血圧は最大それぞれ9.81mmHg及び5.33mmHg下降するとの報告がある。4)また、α遮断剤とタダラフィルの併用で失神等の症状を伴う血圧低下を来したとの報告がある。 | タダラフィルは血管拡張作用による降圧作用を有するため、併用により降圧作用を増強するおそれがある。 |
| 降圧剤 アムロジピン メトプロロール エナラプリル カンデサルタン等 | アンジオテンシンII受容体拮抗剤(単剤又は多剤)とタダラフィル(20mg)の併用により、自由行動下収縮期血圧及び拡張期血圧は最大それぞれ8mmHg及び4mmHg下降するとの報告がある。5) | タダラフィルは血管拡張作用による降圧作用を有するため、併用により降圧作用を増強するおそれがある。 |
| カルペリチド | タダラフィルとの併用により降圧作用が増強するおそれがある。 | タダラフィルは血管拡張作用による降圧作用を有するため、併用により降圧作用を増強するおそれがある。 |
| ビタミンK拮抗薬 ワルファリン [9.1.10参照] | タダラフィル(10及び20mg/日)との併用において、ワルファリン(25mg)の薬物動態及び抗凝固作用に対する影響は認められなかったが、併用により出血の危険性が高まるおそれがある。 | ビタミンK拮抗薬等の抗凝固療法を施行している患者では出血の危険性が高まるおそれがある。 |
| ベルイシグアト | 症候性低血圧を起こすおそれがある。治療上の有益性と危険性を十分に考慮し、治療上やむを得ないと判断された場合にのみ併用すること。 | 細胞内cGMP濃度が増加し、降圧作用を増強するおそれがある。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 貧血(6.5%)
11.1.2 過敏症
発疹(1.1%)、蕁麻疹(頻度不明)、顔面浮腫(0.5%)、剥脱性皮膚炎(頻度不明)、Stevens-Johnson症候群(頻度不明)等があらわれることがある。
11.2 その他の副作用
| 5%以上 | 5%未満 | 頻度不明 | |
| 感染症及び寄生虫症 | 上気道感染 | 上咽頭炎、インフルエンザ、尿路感染 | |
| 血液及びリンパ系障害 | 血小板減少、INR増加 | ||
| 免疫系障害 | 血管浮腫 | 皮疹、蕁麻疹、貪食細胞性組織球症 | |
| 代謝および栄養障害 | 食欲不振 | ||
| 精神障害 | 睡眠障害、うつ病 | ||
| 神経系障害 | 頭痛 | 片頭痛、失神、浮動性めまい、下肢静止不能症候群、感覚鈍麻、錯感覚、脳卒中注1) | |
| 眼障害 | 霧視、網膜静脈閉塞 | 眼充血、眼痛、結膜出血、視力低下、眼の異常感、眼乾燥、非動脈炎性前部虚血性視神経症注2)、視野欠損、視覚障害、中心性漿液性脈絡網膜症 | |
| 耳および迷路障害 | 回転性めまい | ||
| 心臓障害 | 動悸、心不全、頻脈 | ||
| 血管障害 | 低血圧、潮紅 | ほてり、心筋梗塞注1)、心突然死注1)、高血圧、レイノー現象、血腫 | |
| 呼吸器、胸郭及び縦隔障害 | 鼻閉、呼吸困難、鼻出血 | 副鼻腔うっ血 | |
| 胃腸障害 | 悪心、下痢、嘔吐、消化不良、腹部不快感、腹部膨満、口内乾燥、胃食道逆流性疾患 | 上腹部痛、胃炎、鼓腸、腹痛、胃不快感 | |
| 皮膚及び皮下組織障害 | そう痒症、多汗症 | ||
| 筋骨格系及び結合組織障害 | 筋肉痛、四肢痛 | 背部痛、筋痙縮、関節痛、筋骨格硬直、関節炎、四肢不快感 | |
| 生殖系及び乳房障害 | 子宮出血増加(月経中間期出血、重度月経出血、不規則月経等)、月経過多、持続勃起症、勃起延長 | ||
| 一般・全身障害及び投与部位の状態 | 浮腫/体液貯留 | 疼痛、顔面腫脹、疲労 | 腫脹、胸痛 |
| 臨床検査 | トランスアミナーゼ上昇、ALT増加、AST増加、体重増加 | 肝機能検査異常、ヘマトクリット減少、白血球数減少 | |
| 傷害、中毒および処置合併症 | 挫傷 |
13. 過量投与
13.1 症状
外国において、健康男性にマシテンタン600mgを単回経口投与した時、主な有害事象は、頭痛、悪心、嘔吐であった。
13.2 処置
個々の成分データに基づくと、透析による除去は期待できない。
14. 適用上の注意
14.1 薬剤交付時の注意
ブリスターシートから取り出して服用するよう指導すること。シートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 マシテンタン
(1)海外臨床試験において、月経障害、卵巣嚢胞、白血球減少症及び白血球減少に関する有害事象がプラセボ群では1.1%(2/184例)、0.0%(0/184例)、1.6%(4/249例)及び0.0%(0/249例)であったのに対し、マシテンタン10mg投与では5.1%(10/194例)、1.5%(3/194例)、2.5%(6/242例)及び0.8%(2/242例)であり、プラセボに比べ、マシテンタンで多く報告された。
(2)関連性は明確ではないがマシテンタン投与後に精子数減少をみとめた症例が報告されており、マシテンタンはヒトの精子形成に影響を及ぼすおそれがある。なお、他のERAを服用した患者においても精子数減少が報告されている。
15.1.2 タダラフィル
(1)勃起不全治療剤として使用されたタダラフィルの市販後の自発報告において、心筋梗塞、心突然死、心室性不整脈、脳出血、一過性脳虚血発作等の重篤な心血管系障害がタダラフィル投与後に発現している。これらの多くが心血管系のリスクファクターを有している患者であった。多くの事象が、性行為中又は性行為後に認められ、少数例ではあるが、性行為なしにタダラフィル投与後に認められたものもあった。その他は、タダラフィルを投与し性行為後の数時間から数日後に報告されている。これらの症例について、タダラフィル、性行為、本来患者が有していた心血管系障害、これらの要因の組合せ又は他の要因に直接関連するかどうかを確定することはできない。
(2)薬剤との因果関係は明らかではないが、外国において男性勃起不全治療剤として使用されたタダラフィルを含むPDE5阻害剤投与後に、まれに視力低下や視力喪失の原因となりうる非動脈炎性前部虚血性視神経症(NAION)の発現が報告されている。6)これらの患者の多くは、NAIONの危険因子[年齢(50歳以上)、糖尿病、高血圧、冠動脈障害、高脂血症、喫煙等]を有していた。7)
外国において、NAIONを発現した45歳以上の男性(肺動脈性肺高血圧症に使用された症例は除く)を対象として実施された自己対照研究では、PDE5阻害剤の投与から消失半減期(T1/2)の5倍の期間内(タダラフィルの場合約4日以内に相当)は、NAION発現リスクが約2倍になることが報告されている。8)[8.7、11.2参照]
外国において、NAIONを発現した45歳以上の男性(肺動脈性肺高血圧症に使用された症例は除く)を対象として実施された自己対照研究では、PDE5阻害剤の投与から消失半減期(T1/2)の5倍の期間内(タダラフィルの場合約4日以内に相当)は、NAION発現リスクが約2倍になることが報告されている。8)[8.7、11.2参照]
(4)薬剤との因果関係は明らかではないが、外国においてタダラフィルを含むPDE5阻害剤投与後に、まれに、急激な聴力低下又は突発性難聴が報告されている。これらの患者では、耳鳴りやめまいを伴うことがある。[8.8参照]
(5)アルコール飲用時にタダラフィルを投与した外国の臨床薬理試験(タダラフィル10mg、20mg)において、アルコール血中濃度、タダラフィルの血漿中濃度のいずれも相互に影響を受けなかったが、アルコールを高用量(0.7g/kg)飲用した被験者において、めまいや起立性低血圧が報告された。
15.1.3 マシテンタン・タダラフィル配合錠
肺動脈性肺高血圧症患者を対象とした国際共同第III相試験において、肺動脈性肺高血圧症治療薬による治療歴のない65歳超の患者に本剤の投与開始から1カ月以内に心不全事象(4例)が発現した。4例のうち2例は本剤投与中に回復し、残りの2例は他の有害事象[肺静脈閉塞性疾患の新規診断(治験実施計画書の規定による投与中止)及び貧血]により本剤の投与を中止した。
15.2 非臨床試験に基づく情報
15.2.1 マシテンタン
ラット及びイヌの反復投与毒性試験において、精細管萎縮又は拡張が認められた。ラットの反復投与毒性試験において、可逆的な異常精子の割合の増加が認められた。イヌの反復投与毒性試験において、精子形成の低下が認められた。
15.2.2 タダラフィル
25mg/kg/day以上の用量でタダラフィルをイヌに3〜12カ月間連日経口投与した毒性試験において、精巣重量の低下、精細管上皮の変性、精巣上体の精子数の減少が認められた。ヒトにおける精子形成能に対する影響を検討した外国臨床試験の一部では平均精子濃度の減少が認められたが、精子運動率、精子形態及び生殖ホルモン値はいずれの試験においても変化が認められなかった。11)
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
(1)マシテンタン
健康成人に、本剤(マシテンタン/タダラフィルとして10mg/40mg)又はオプスミット錠10mg及びタダラフィル40mg(単剤併用)を空腹時に単回投与したときのマシテンタン及びマシテンタンの活性代謝物の血漿中濃度推移及び薬物動態パラメータは以下のとおりであった。本剤投与時の血漿中濃度推移及び薬物動態パラメータは単剤併用時と類似しており、生物学的同等性の基準を満たす製剤である。12)(外国人データ)
健康成人に本剤(配合錠)又はオプスミット錠10mg及びタダラフィル40mg(単剤併用)を空腹時に単回投与したときのマシテンタン及びマシテンタンの活性代謝物の血漿中濃度推移
| 薬物動態パラメータ | 平均値(標準偏差)、tmax:中央値(範囲) | |||
| マシテンタン | 活性代謝物 | |||
| 配合錠 (34例) | 単剤併用 (34例) | 配合錠 (34例) | 単剤併用 (34例) | |
| tmax(h) | 10.0(2.48-10.2) | 10.0(3.55-12.0) | 48.0(24.0-72.0) | 48.0(24.0-72.0) |
| Cmax(ng/mL) | 210(39.7) | 206(32.6) | 187(36.4) | 191(51.2) |
| AUC∞(ng・h/mL) | 5934(1384) (33例) | 5903(1490) (33例) | 22638(5688) (33例) | 22500(5222) (33例) |
| t1/2(h) | 13.9(2.87) (33例) | 14.6(2.67) (33例) | 50.7(9.99) (33例) | 49.4(6.92) (33例) |
(2)タダラフィル
健康成人に、本剤(マシテンタン/タダラフィルとして10mg/40mg)又はオプスミット錠10mg及びタダラフィル40mg(単剤併用)を空腹時に単回投与したときのタダラフィルの血漿中濃度推移及び薬物動態パラメータは以下のとおりであった。本剤投与時の血漿中濃度推移及び薬物動態パラメータは単剤併用時と類似しており、生物学的同等性の基準を満たす製剤である。12)(外国人データ)
健康成人に本剤(配合錠)又はオプスミット錠10mg及びタダラフィル40mg(単剤併用)を空腹時に単回投与したときのタダラフィルの血漿中濃度推移
| 薬物動態パラメータ | 平均値(標準偏差)、tmax:中央値(範囲) | |
| 配合剤(34例) | 単剤併用(34例) | |
| tmax(h) | 3.00(1.00-24.0) | 2.50(1.00-7.00) |
| Cmax(ng/mL) | 545(143) | 610(120) |
| AUC∞(ng・h/mL) | 20733(7511) (33例) | 20913(7174) (33例) |
| t1/2(h) | 22.8(7.76) (33例) | 22.7(7.26) (33例) |
16.2 吸収
16.2.1 食事の影響
16.3 分布
16.3.1 血漿蛋白結合率
(1)マシテンタン
血漿蛋白結合率は、マシテンタンは99%以上、マシテンタンの活性代謝物は99.5%であり、主にアルブミン及びα1-酸性糖蛋白と結合する。13)
(2)タダラフィル
タダラフィルの血漿蛋白結合率は94%(in vitro、平衡透析法)であり、主にアルブミン及びα1-酸性糖蛋白と結合する。
16.4 代謝
16.4.1 マシテンタン
健康成人6例に14C-マシテンタン10mgを単回経口投与した時、血漿中にはマシテンタン未変化体、活性代謝物、カルボン酸体が認められた。血漿中の活性代謝物及びカルボン酸体とマシテンタン未変化体の放射能比はそれぞれ約190%及び約20%であった。14)(外国人データ)
マシテンタンの主要な代謝はCYP酵素、主にCYP3A4及びCYP2Cファミリー(CYP2C8、CYP2C9及びCYP2C19)による。活性代謝物の生成は主にCYP3A4によるものであり、CYP2C8、CYP2C9及びCYP2C19の関与はわずかであった。薬理活性を有さない代謝物の生成は主にCYP2C9によるものであり、CYP2C8、CYP2C19及びCYP3A4の関与はわずかであった。[10.参照]
マシテンタンの主要な代謝はCYP酵素、主にCYP3A4及びCYP2Cファミリー(CYP2C8、CYP2C9及びCYP2C19)による。活性代謝物の生成は主にCYP3A4によるものであり、CYP2C8、CYP2C9及びCYP2C19の関与はわずかであった。薬理活性を有さない代謝物の生成は主にCYP2C9によるものであり、CYP2C8、CYP2C19及びCYP3A4の関与はわずかであった。[10.参照]
16.4.2 タダラフィル
健康成人6例に14C-タダラフィル100mgを単回経口投与したとき、血漿中には主にタダラフィル未変化体及びメチルカテコールグルクロン酸抱合体が認められた。血漿中のメチルカテコール体はメチルカテコールグルクロン酸抱合体の10%未満であった。(外国人データ)
16.5 排泄
16.5.1 マシテンタン
健康成人6例に14C-マシテンタン10mgを単回経口投与した時、投与後14日間までの放射能回収率は、尿中49.7%、糞中23.9%であった。尿中にマシテンタン及びマシテンタンの活性代謝物は排泄されなかった。14)(外国人データ)
16.5.2 タダラフィル
健康成人6例に14C-タダラフィル100mgを単回経口投与したときの、投与後312時間までの放射能回収率は糞便中60.5%、尿中36.1%であった。糞便中には主にメチルカテコール体、カテコール体、尿中には主にメチルカテコールグルクロン酸抱合体及びカテコールグルクロン酸抱合体が認められた。(外国人データ)
16.6 特定の背景を有する患者
16.6.1 肝機能障害患者
(1)マシテンタン
(2)タダラフィル
健康成人8例及び肝障害患者25例注2)にタダラフィル10mg注1)を単回経口投与したとき、軽度肝障害患者(Child-Pugh class A)と中等度肝障害患者(Child-Pugh class B)のAUC0-∞は健康成人とほぼ同様であった。16)(外国人データ)[9.3参照]
注1)本剤の承認用量は1日1回1錠(マシテンタンとして10mg及びタダラフィルとして40mg)である。
注2)軽微肝障害(脂肪肝が認められた患者)、n=8:軽度肝障害(Child-Pugh class A)、n=8:中等度肝障害(Child-Pugh class B)、n=8:重度肝障害(Child-Pugh class C)、n=1。
16.6.2 腎機能障害患者
(1)マシテンタン
(2)タダラフィル
16.6.3 高齢者
16.7 薬物相互作用
16.7.1 マシテンタン
(1)ワルファリン
健康成人14例に、マシテンタン10mgとワルファリン25mgを併用投与した時、マシテンタンの薬物動態にワルファリンは影響を与えなかった。また、マシテンタンはワルファリンの薬物動態に影響を与えなかった。18)(外国人データ)
(2)シルデナフィル
健康成人12例に、マシテンタン10mgとシルデナフィル20mgを併用投与した時、マシテンタンの薬物動態にシルデナフィルは影響を与えなかった。また、マシテンタンはシルデナフィルの薬物動態に影響を与えなかった。19)(外国人データ)
(3)ケトコナゾール
健康成人12例に、ケトコナゾール400mg反復投与時にマシテンタン10mgを併用した結果、マシテンタンのCmax、tmax及びt1/2が増加し、AUC0-∞は約2倍に増加した。活性代謝物のCmaxは51%、AUC0-∞は26%減少し、tmaxは48時間から72時間に延長した。20)(外国人データ)
(4)シクロスポリン
健康成人10例に、マシテンタン10mg反復投与時にシクロスポリン100mgを併用した結果、マシテンタンのAUCτ及びCtroughはそれぞれ10%及び38%増加したが、活性代謝物のAUCτ及びCtroughに対する影響は認められなかった。21)(外国人データ)
(5)リファンピシン
(6)フルコナゾール
生理学的薬物動態モデルによる解析の結果、マシテンタン10mg単剤投与時に比べてフルコナゾール400mg/日の併用時では、マシテンタンのAUC及びCmaxがそれぞれ約3.8倍及び約1.3倍になることが推定された。活性代謝物のAUC及びCmaxはそれぞれ約1.0倍及び約0.6倍になることが推定された。[10.2参照]
16.7.2 タダラフィル
(1)経口ケトコナゾール
健康成人12例にケトコナゾール400mg(1日1回経口投与、国内未発売)とタダラフィル20mg注1)を併用投与したとき、タダラフィルのAUC0-∞及びCmaxは、それぞれ312%及び22%増加した。(外国人データ)
健康成人11例にケトコナゾール200mg(1日1回経口投与)とタダラフィル10mg注1)を併用投与したとき、タダラフィルのAUC0-∞及びCmaxはそれぞれ107%及び15%増加した。(外国人データ)
(2)リトナビル
(3)ボセンタン
健康成人15例にタダラフィル40mg(1日1回)及びボセンタン125mg(1日2回)を10日間併用投与した。投与1日目におけるタダラフィルのAUC及びCmaxは本剤を単独投与時の値と同程度であったが、投与10日目におけるタダラフィルのAUC及びCmaxは本剤を単独投与時の値と比べてそれぞれ41.5%及び26.6%低下した。一方、本剤によるボセンタンのAUC及びCmaxに対する影響は認められなかった。(外国人データ)[10.2参照]
(4)ジゴキシン
健康成人20例にジゴキシン0.25mgを1日1回反復経口投与時の定常状態で、タダラフィル40mgを1日1回10日間反復経口投与した結果、本剤によるジゴキシンのAUC、Cmax及びCminに対する明らかな影響は認められなかった。(外国人データ)
(5)α遮断剤
健康成人18例にドキサゾシン8mgを反復経口投与時の定常状態で、タダラフィル20mg注1)を単回経口投与したとき、立位の収縮期及び拡張期血圧の最大下降量はそれぞれ9.81mmHg及び5.33mmHg、臥位の収縮期及び拡張期血圧の最大下降量はそれぞれ3.64mmHg及び2.78mmHgであった。(外国人データ)
健康成人45例にドキサゾシン(4mgまで漸増)とタダラフィル5mg注1)を1日1回反復経口投与したとき、ドキサゾシンの血圧降下作用に増強がみられた。この試験において、失神等の症状を伴う血圧変化に関する有害事象がみられた。(外国人データ)[10.2参照]
健康成人18例にタムスロシン0.4mgを反復経口投与時の定常状態で、タダラフィル10mg又は20mg注1)を単回投与したとき、立位の収縮期及び拡張期血圧の最大下降量はそれぞれ2.3mmHg及び2.2mmHg、臥位の収縮期及び拡張期血圧の最大下降量はそれぞれ3.2mmHg及び3.0mmHgであり、明らかな血圧への影響は認められなかった。(外国人データ)
健康成人39例にタムスロシン0.4mgとタダラフィル5mg注1)を1日1回反復経口投与したとき、明らかな血圧への影響は認められなかった。(外国人データ)
健康成人45例にドキサゾシン(4mgまで漸増)とタダラフィル5mg注1)を1日1回反復経口投与したとき、ドキサゾシンの血圧降下作用に増強がみられた。この試験において、失神等の症状を伴う血圧変化に関する有害事象がみられた。(外国人データ)[10.2参照]
健康成人18例にタムスロシン0.4mgを反復経口投与時の定常状態で、タダラフィル10mg又は20mg注1)を単回投与したとき、立位の収縮期及び拡張期血圧の最大下降量はそれぞれ2.3mmHg及び2.2mmHg、臥位の収縮期及び拡張期血圧の最大下降量はそれぞれ3.2mmHg及び3.0mmHgであり、明らかな血圧への影響は認められなかった。(外国人データ)
健康成人39例にタムスロシン0.4mgとタダラフィル5mg注1)を1日1回反復経口投与したとき、明らかな血圧への影響は認められなかった。(外国人データ)
(6)経口避妊薬
健康成人26例に経口避妊薬(エチニルエストラジオール0.03mg及びレボノルゲストレル0.15mg含有製剤)とタダラフィル40mgを21日間併用投与した結果、エチニルエストラジオールのAUC及びCmaxは、経口避妊薬とプラセボを併用投与したときの値と比べてそれぞれ26%及び70%増加した。タダラフィル併用投与時とプラセボ併用投与時でレボノルゲストレルの血漿中濃度に統計学的に有意な差は認められなかった。(外国人データ)
(7)その他の薬剤
他剤(ニザチジン、制酸配合剤)又はアルコールがタダラフィル(10又は20mg注1))に及ぼす影響について検討した結果、ニザチジン、制酸配合剤又はアルコールによるタダラフィルの薬物動態に対する明らかな影響は認められなかった。また、タダラフィル(10又は20mg注1))が他剤(ミダゾラム、テオフィリン、ワルファリン及びアムロジピン)又はアルコールに及ぼす影響について検討した結果、タダラフィルによるミダゾラム、テオフィリン、ワルファリン、アムロジピン又はアルコールの薬物動態に対する明らかな影響は認められなかった。(外国人データ)
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 AC-077A301試験(A DUE試験)(国際共同第III相試験)
肺動脈性肺高血圧症患者186例(日本人患者8例を含む)を対象に、マシテンタン10mg単剤及びタダラフィル40mg単剤それぞれに対する本剤の有効性及び安全性を比較した、多施設共同、ランダム化、二重盲検実薬対照、並行群間試験を実施した。ベースライン時に服用しているERA及びPDE5阻害剤の1日総投与量は下表のとおりであった。
| 薬剤名 | 1日総投与量 | |
| ERA | マシテンタン | 10mg |
| ボセンタン | 250mg | |
| アンブリセンタン | 10mg | |
| PDE5阻害剤 | タダラフィル | 40mg |
| シルデナフィル | 60〜120mg注1) | |
| バルデナフィル注2) | 10mg |
主要評価項目である、16週間の二重盲検投与期間終了(End of Double-Blind Treatment:EDBT)時の肺血管抵抗(PVR)のベースラインからの変化比は、未治療及びERA既治療層ではマシテンタン単剤投与群と比較して本剤群で相対的に29%減少した。また、未治療及びPDE5阻害剤既治療層ではタダラフィル単剤投与群と比較して本剤群で相対的に28%減少した。
| 未治療又はERA既治療層 | 未治療又はPDE5阻害剤既治療層 | |||
| マシテンタン単剤投与群(35例) | 本剤群(70例) | タダラフィル単剤投与群(44例) | 本剤群(86例) | |
| ベースラインのPVR(dyn.sec/cm5)の平均値(標準偏差) | 815.9(401.22) | 834.3(630.93) | 802.1(551.98) | 884.7(640.34) |
| EDBT時のベースラインからの変化量(dyn.sec/cm5)の平均値(標準偏差) | −162.0(240.33) | −370.5(428.79) | −180.8(237.46) | −384.5(396.24) |
| EDBT時のベースラインからの変化比(幾何平均値) | 0.77 | 0.55 | 0.78 | 0.56 |
| 治療効果(調整95%信頼区間)注3) | 0.71(0.61,0.82) | 0.72(0.64,0.80) | ||
| 調整両側p値注4) | <0.0001 | <0.0001 | ||
主な副次評価項目であるEDBT時の6分間歩行距離(6MWD)のベースラインからの変化量は、各単剤投与群と比較して本剤群で改善傾向が認められた。22)
| 未治療又はERA既治療層 | 未治療又はPDE5阻害剤既治療層 | |||
| マシテンタン単剤投与群(35例) | 本剤群(70例) | タダラフィル単剤投与群(44例) | 本剤群(86例) | |
| ベースラインの6MWD(m)の平均値(標準偏差) | 347.2(88.82) | 354.3(103.49) | 361.8(70.44) | 351.0(98.85) |
| EDBT時のベースラインからの変化量(m)の平均値(標準偏差) | 38.5(70.42) | 52.9(88.23) | 15.9(45.04) | 43.4(78.03) |
| 治療効果(調整95%信頼区間)注5) | 16.04(−17.0,49.08) | 25.37(−0.93,51.59) | ||
本剤を投与された185例中69例(37.3%)に副作用(臨床検査値異常を含む)が認められた。主な副作用は、頭痛19例(10.3%)、浮腫/体液貯留17例(9.2%)、貧血12例(6.5%)、悪心7例(3.8%)、鼻閉7例(3.8%)、筋肉痛6例(3.2%)、呼吸困難5例(2.7%)、低血圧5例(2.7%)等であった。
18. 薬効薬理
18.1 作用機序
マシテンタンはエンドセリン(ET)A及びETB受容体に対して拮抗作用を示し、125I-ET-1結合に対するIC50値(平均値±標準誤差)はそれぞれ0.49±0.07nM及び391±49nMであった。活性代謝物もマシテンタンと同様の拮抗作用を示し、そのIC50値はそれぞれ3.4±0.20nM及び987±92nMであった。23)24)
タダラフィルは、肺血管系における主要なcGMP分解酵素であるPDE5を選択的に阻害し、cGMP濃度を増加させることで、肺血管平滑筋の弛緩及び肺血管の拡張を誘導する。
18.2 血管に対する作用
マシテンタンはラットから摘出した内皮剥離大動脈のET-1刺激誘発収縮(ETA受容体媒介性)及び上皮剥離気管のサラフォトキシンS6c刺激誘発収縮(ETB受容体媒介性)を阻害し、そのpA2値はそれぞれ7.6±0.2(ETA受容体)及び5.9±0.2(ETB受容体)であった。24)
18.3 PDE5阻害作用
タダラフィルは、ヒト遺伝子組み換えPDE5を約1nMのIC50値で阻害し、PDE6、PDE11及びその他のPDEサブタイプと比較して、それぞれ780、14及び9000倍以上の選択性を示した。25)
18.4 肺高血圧症モデルに対する作用
低酸素/Sugen-5416誘発性肺高血圧症モデルラットにマシテンタン及びタダラフィルを併用投与すると、それぞれを単独で投与した場合と比較し、平均肺動脈圧の低下の増強が認められた。26)
19. 有効成分に関する理化学的知見
19.1. マシテンタン
19.2. タダラフィル
20. 取扱い上の注意
吸湿性を有するためブリスター包装のまま保存すること。
21. 承認条件
医薬品リスク管理計画を策定の上、適切に実施すること。
22. 包装
30錠[10錠(ブリスター)×3]
23. 主要文献
- Kloner RA,et al., Am J Cardiol., 92 (Suppl), 37M-46M, (2003)
- Patterson D,et al., Br J Clin Pharmacol., 60 (5), 459-468, (2005) »PubMed
- Kloner RA,et al., J Am Coll Cardiol., 42 (10), 1855-1860, (2003) »PubMed
- Kloner RA,et al., J Urol., 172 (5 Pt 1), 1935-1940, (2004) »PubMed
- Kloner RA,et al., Am J Cardiol., 92 (suppl), 47M-57M, (2003)
- Pomeranz HD,et al., J Neuroophthalmol., 25 (1), 9-13, (2005) »PubMed
- Lee AG,et al., Am J Ophthalmol., 140 (4), 707-708, (2005) »PubMed
- Campbell UB,et al., J Sex Med., 12 (1), 139-151, (2015) »PubMed
- Gilad R,et al., BMJ., 325 (7369), 869, (2002) »PubMed
- Striano P,et al., BMJ., 333 (7572), 785, (2006) »PubMed
- Hellstrom WJG,et al., J Urol., 170 (3), 887-891, (2003) »PubMed
- 社内資料:健康成人を対象とした生物学的同等性及び食事の影響の検討(67896062PAH1006)(2024年9月24日承認、CTD2.7.1.2.1)
- 社内資料:血漿タンパク結合及び赤血球中への移行の検討(オプスミット錠:2015年3月26日承認、CTD2.7.2.3)
- Bruderer S,et al., Xenobiotica., 42, 901-910, (2012) »PubMed
- Sidharta PN,et al., J Clin Pharmacol., 54 (3), 291-300, (2014) »PubMed
- Forgue ST,et al., Br J Clin Pharmacol., 63 (1), 24-35, (2007) »PubMed
- 社内資料:血漿中濃度に及ぼす年齢の影響(オプスミット錠:2015年3月26日承認、CTD2.7.2.3)
- 社内資料:健康成人男性を対象としたワルファリンとの薬物相互作用の検討(オプスミット錠:2015年3月26日承認、CTD2.7.6.2)
- 社内資料:健康成人男性を対象としたシルデナフィルとの薬物相互作用の検討(オプスミット錠:2015年3月26日承認、CTD2.7.6.2)
- Atsmon J,et al., Clin Pharmacokinet., 52 (8), 685-692, (2013) »PubMed
- Bruderer S,et al., AAPS J., 14, 68-78, (2012) »PubMed
- 社内資料:肺動脈性肺高血圧症患者を対象とした第III相試験(AC-077A301試験)(2024年9月24日承認、CTD2.7.3.2.2)
- 社内資料:ET受容体へのET-1結合阻害試験(オプスミット錠:2015年3月26日承認、CTD2.6.2.2.1)
- Iglarz M,et al., J Pharmacol Exp Ther., 327, 736-745, (2008) »PubMed
- 山口高史,他, 日薬理誌, 131, 469-477, (2008) »PubMed
- 社内資料:ラット肺高血圧症モデルにおける肺動脈圧及び全身動脈圧に及ぼす影響(2024年9月24日承認、CTD2.6.2.2.1)
24. 文献請求先及び問い合わせ先
文献請求先
ヤンセンファーマ株式会社
メディカルインフォメーションセンター
〒101-0065
東京都千代田区西神田3-5-2
電話:フリーダイヤル 0120-183-275
製品情報問い合わせ先
ヤンセンファーマ株式会社
メディカルインフォメーションセンター
〒101-0065
東京都千代田区西神田3-5-2
電話:フリーダイヤル 0120-183-275
26. 製造販売業者等
26.1 製造販売元(輸入)
ヤンセンファーマ株式会社
〒101-0065
東京都千代田区西神田3-5-2
26.2 販売提携先
日本新薬株式会社
京都市南区吉祥院西ノ庄門口町14