医薬品情報
| 総称名 | ナウゼリン |
|---|---|
| 一般名 | ドンペリドン |
| 欧文一般名 | Domperidone |
| 製剤名 | ドンペリドン口腔内崩壊錠 |
| 薬効分類名 | 消化管運動改善剤 |
| 薬効分類番号 | 2399 |
| ATCコード | A03FA03 |
| KEGG DRUG |
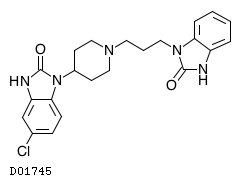
D01745
ドンペリドン
|
| JAPIC | 添付文書(PDF) |
添付文書情報2025年5月 改訂(第2版)

|
2.禁忌 4.効能または効果 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 20.取扱い上の注意 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ナウゼリンOD錠5 | Nauzelin OD Tablets | 協和キリン | 2399005F3020 | 6.3円/錠 | |
| ナウゼリンOD錠10 | Nauzelin OD Tablets | 協和キリン | 2399005F4026 | 7.8円/錠 |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 消化管出血、機械的イレウス、消化管穿孔の患者[症状が悪化するおそれがある。]
2.3 プロラクチン分泌性の下垂体腫瘍(プロラクチノーマ)の患者[抗ドパミン作用によりプロラクチン分泌を促す。]
4. 効能または効果
下記疾患および薬剤投与時の消化器症状(悪心、嘔吐、食欲不振、腹部膨満、上腹部不快感、腹痛、胸やけ、あい気)
成人
○慢性胃炎、胃下垂症、胃切除後症候群
○抗悪性腫瘍剤またはレボドパ製剤投与時
小児
○周期性嘔吐症、上気道感染症
○抗悪性腫瘍剤投与時
6. 用法及び用量
成人
通常、ドンペリドンとして1回10mgを1日3回食前に経口投与する。ただし、レボドパ製剤投与時にはドンペリドンとして1回5〜10mgを1日3回食前に経口投与する。
なお、年令、症状により適宜増減する。
なお、年令、症状により適宜増減する。
小児
通常、ドンペリドンとして1日1.0〜2.0mg/kgを1日3回食前に分けて経口投与する。
なお、年令、体重、症状により適宜増減する。
ただし、1日投与量はドンペリドンとして30mgを超えないこと。
また、6才以上の場合はドンペリドンとして1日最高用量は1.0mg/kgを限度とすること。
なお、年令、体重、症状により適宜増減する。
ただし、1日投与量はドンペリドンとして30mgを超えないこと。
また、6才以上の場合はドンペリドンとして1日最高用量は1.0mg/kgを限度とすること。
8. 重要な基本的注意
8.2 眠気、めまい・ふらつきがあらわれることがあるので、本剤投与中の患者には自動車の運転等危険を伴う機械操作に注意させること。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 心疾患のある患者
QT延長があらわれるおそれがある。
9.2 腎機能障害患者
副作用が強くあらわれるおそれがある。
9.3 肝機能障害患者
副作用が強くあらわれるおそれがある。
9.5 妊婦
妊婦又は妊娠している可能性のある女性、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。動物実験(ラット)で臨床用量の約65倍の投与量(体表面積換算)で骨格、内臓異常等の催奇形作用が報告されている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。投与する場合は大量投与を避けること。動物実験(ラット)で乳汁中へ移行することが報告されている。[16.3.4参照]
9.7 小児等
9.8 高齢者
減量するなど注意すること。一般的に高齢者では生理機能が低下している。[15.1参照]
10. 相互作用
相互作用序文
本剤は主にCYP3A4で代謝される。[16.4.1参照]
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| フェノチアジン系精神神経用剤 プロクロルペラジン クロルプロマジン チエチルペラジン等 ブチロフェノン系製剤 ハロペリドール等 ラウオルフィアアルカロイド製剤 レセルピン等 | 内分泌機能調節異常又は錐体外路症状が発現しやすくなる。 | フェノチアジン系精神神経用剤、ブチロフェノン系製剤は中枢性の抗ドパミン作用を有し、ラウオルフィアアルカロイド製剤は中枢でカテコールアミンを枯渇させる。一方、本剤は血液−脳関門を通過しにくいが強い抗ドパミン作用を有する。 |
| ジギタリス製剤 ジゴキシン等 | ジギタリス製剤飽和時の指標となる悪心、嘔吐、食欲不振症状を不顕化することがある。ジギタリス製剤の血中濃度のモニターを行う。 | 本剤は制吐作用を有する。 |
| 抗コリン剤 ブチルスコポラミン臭化物 チキジウム臭化物 チメピジウム臭化物水和物等 | 本剤の胃排出作用が減弱することがある。症状により一方を減量、中止する。又は必要に応じて間隔をあけて投与する。 | 抗コリン剤の消化管運動抑制作用が本剤の消化管運動亢進作用と拮抗する。 |
| 制酸剤 H2受容体拮抗剤 シメチジン ラニチジン等 プロトンポンプ阻害剤 オメプラゾール等 | 本剤の効果が減弱するおそれがあるので、両剤の投与時間を考慮する。 | 胃内pHの上昇により、本剤の消化管吸収が阻害される。 |
| CYP3A4阻害剤 イトラコナゾール エリスロマイシン等 [16.7.1、16.7.2参照] | 本剤の血中濃度が上昇する。また、エリスロマイシンとの併用においては、QT延長が報告されている。 | 強力又は中程度のCYP3A4阻害作用により本剤の代謝が阻害される。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック、アナフィラキシー(いずれも頻度不明)
ショック、アナフィラキシー(発疹、発赤、呼吸困難、顔面浮腫、口唇浮腫等)を起こすことがある。
11.1.2 錐体外路症状(0.1%未満)
11.1.3 意識障害、痙攣(いずれも頻度不明)[9.7参照]
11.1.4 肝機能障害、黄疸(いずれも頻度不明)
AST、ALT、γ-GTPの上昇等を伴う肝機能障害、黄疸があらわれることがある。
注)発現頻度はナウゼリン錠、細粒及びドライシロップの使用成績調査を含む。
11.2 その他の副作用
| 0.1〜5%未満 | 0.1%未満 | 頻度不明 | |
| 肝臓 | 肝機能異常(AST,ALT,γ-GTP,ビリルビン,Al-P,LDH上昇等) | ||
| 内分泌 | 女性化乳房、プロラクチン上昇、乳汁分泌、乳房膨満感、月経異常 | ||
| 消化器 | 下痢 | 便秘、腹痛、腹部圧迫感、口渇、胸やけ、悪心、嘔吐、腹部膨満感 | 腹部不快感、腹鳴、腸痙攣 |
| 循環器 | 心悸亢進 | QT延長 | |
| 皮膚 | じん麻疹、発疹、そう痒 | ||
| その他 | 口内のあれ、発汗、眠気、動揺感、めまい・ふらつき |
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
14.1.2 本剤は舌の上にのせて唾液を浸潤させると崩壊するため、水なしで服用可能である。また、水で服用することもできる。
15. その他の注意
15.1 臨床使用に基づく情報
外国において本剤による重篤な心室性不整脈及び突然死が報告されている。特に高用量を投与している患者又は高齢の患者で、これらのリスクが増加したとの報告がある。[9.8参照]
16. 薬物動態
16.1 血中濃度
健康成人にナウゼリンOD錠10(水なしで服用、水で服用)又はナウゼリン錠10(水で服用)を絶食下単回経口投与したときの血漿中ドンペリドン濃度は以下のとおりであった。ナウゼリンOD錠10は水なしで服用又は水で服用した場合のいずれにおいても、ナウゼリン錠10(水で服用)と生物学的に同等であった。
ナウゼリンOD錠10(水なしで服用)とナウゼリン錠10(水で服用)を単回経口投与したときの血漿中濃度推移
ナウゼリンOD錠10(水で服用)とナウゼリン錠10(水で服用)を単回経口投与したときの血漿中濃度推移
| 用量 | 投与製剤 | tmax(h) | Cmax(ng/mL) | AUC0-t(ng・h/mL) | t1/2(h) | |
| 水なし投与(n=20) | 10mg | ナウゼリンOD錠10 | 1.40±1.67 | 10.7±4.6 | 42.0±12.7 | 11.3±1.6 |
| ナウゼリン錠10a) | 0.738±0.250 | 11.5±4.6 | 40.6±12.0 | 10.9±1.9 | ||
| 水あり投与(n=24) | 10mg | ナウゼリンOD錠10 | 0.854±0.521 | 12.1±5.1 | 44.3±13.3 | 12.1±1.8 |
| ナウゼリン錠10 | 0.948±0.500 | 12.6±5.5 | 43.2±10.4 | 11.8±1.6 |
16.2 吸収
16.2.1 バイオアベイラビリティ
外国人健康成人7例にドンペリドン60mgを絶食下単回経口投与したときのバイオアベイラビリティは12.7%であった1)。
16.3 分布
16.3.1 体組織への分布
ラットに14C-ドンペリドン2.5mg/kgを経口及び静脈内投与したとき、いずれも腸管組織、肝臓、膵臓等に高濃度に分布したが、脳への分布は極めて低かった。また、蓄積性も認められなかった2)。
16.3.2 血液−脳関門通過性
ラットに14C-ドンペリドン2.5mg/kgを経口投与したとき、脳内放射能濃度は投与後0.25〜1時間で最高となり、その後定常状態に達した時点では血漿中放射能濃度の約1/5であった2)。
16.3.3 血液−胎盤関門通過性
妊娠ラットに14C-ドンペリドン2.5mg/kgを静脈内又は経口投与したとき、胎盤内放射能濃度は投与1時間後に最高となり、母体血漿中放射能濃度に比べ静脈内投与では2.7倍、経口投与では2倍であった2)。
16.3.4 母乳中への移行性
16.3.5 血漿蛋白結合率
ヒト血漿蛋白結合率は以下のとおりであった1)(in vitro、外国人データ)。
| 添加濃度(ng/mL) | 10 | 100 |
| 血漿蛋白結合率(%) | 91.8 | 93.0 |
16.4 代謝
16.4.2 外国人健康成人3例に14C-ドンペリドン40mgを経口投与したとき、尿中の主代謝物はN-脱アルキル体とその抱合体、糞中の主代謝物は水酸化体であった4)。
16.5 排泄
外国人健康成人3例に14C-ドンペリドン40mgを経口投与したとき、4日以内に総放射能の約95%が排泄された。なお、尿中と糞中への排泄の割合は約3:7であった。尿中には投与後24時間以内に大部分が排泄され、24時間後の尿中排泄率は投与量の29.5%であった。一方、糞中には投与量の約66%が投与後4日以内に排泄された。未変化体の尿中排泄率及び糞中排泄率は、それぞれ投与量の0.39%及び約10%であった1)。
16.7 薬物相互作用
16.7.1 イトラコナゾール
16.7.2 エリスロマイシン
外国人健康成人32例に本剤(経口剤、10mg/回、1日4回注)、5日間反復投与)とエリスロマイシン(500mg/日、1日3回、5日間反復投与)を併用投与したとき、本剤のCmax及びAUC(AUCτ及びAUC12h,ss)はそれぞれ約142%及び約167%増加した。
同試験において、QT延長が認められ、その最大値(95%信頼区間)は本剤単独投与では7.52ms(0.602-14.435)、エリスロマイシン単独投与では9.19ms(1.678-16.706)、併用投与では14.26ms(8.014-20.505)であった。[10.2参照]
同試験において、QT延長が認められ、その最大値(95%信頼区間)は本剤単独投与では7.52ms(0.602-14.435)、エリスロマイシン単独投与では9.19ms(1.678-16.706)、併用投与では14.26ms(8.014-20.505)であった。[10.2参照]
注)本剤の成人における承認された用法・用量は1回10mg、1日3回である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床試験(成人)
<慢性胃炎、胃下垂症、胃切除後症候群>
消化器系疾患に伴う不定愁訴をもつ患者695例を対象に、普通錠1日15、30及び60mgを7〜154日間経口投与したとき、有効率は慢性胃炎67.4%(277/411例)、胃下垂症74.2%(23/31例)及び胃切除後症候群85.7%(6/7例)であった6)。
副作用発現頻度は1.1%(8/744例)であった。認められた副作用は、腹部膨満感、下腹部圧迫感、下痢・腹痛、下痢、口渇、胸やけ、心悸亢進、乳汁分泌 各0.1%(1/744例)であった。
副作用発現頻度は1.1%(8/744例)であった。認められた副作用は、腹部膨満感、下腹部圧迫感、下痢・腹痛、下痢、口渇、胸やけ、心悸亢進、乳汁分泌 各0.1%(1/744例)であった。
<抗悪性腫瘍剤投与時>
抗悪性腫瘍剤投与に伴う消化器系不定愁訴をもつ患者390例を対象に、普通錠1日10〜60mgを2〜263日間経口投与したとき、有効率は55.4%(216/390例)であった7)。
副作用発現頻度は1.1%(5/438例)であった。認められた副作用は、発疹、便秘、眠気、圧迫感、嘔吐 各0.2%(1/438例)であった。
副作用発現頻度は1.1%(5/438例)であった。認められた副作用は、発疹、便秘、眠気、圧迫感、嘔吐 各0.2%(1/438例)であった。
<レボドパ製剤投与時>
レボドパ製剤投与に伴う消化器系不定愁訴をもつ患者238例を対象に、普通錠1日5〜60mgを1日〜19ヵ月間経口投与したとき、有効率は89.1%(212/238例)であった8)。
副作用発現頻度は3.7%(9/241例)であった。主な副作用は、口内のあれ0.8%(2/241例)であった。
副作用発現頻度は3.7%(9/241例)であった。主な副作用は、口内のあれ0.8%(2/241例)であった。
17.1.2 国内臨床試験(小児)
各種疾患及び抗悪性腫瘍剤投与に伴う消化器系不定愁訴をもつ患児236例を対象に、経口剤(普通錠、ドライシロップ)を投与した国内臨床試験の結果は以下の通りであった9)10)。
・患児59例を対象に、普通錠1日1〜4回(ドンペリドンとして0.1〜0.9mg/kg)注)を1〜35日間経口投与したとき、有効率は周期性嘔吐症91.7%(11/12例)、上気道感染症81.8%(9/11例)及び抗悪性腫瘍剤投与時60.0%(3/5例)であった。
副作用発現頻度は1.7%(1/59例)であった。認められた副作用は、眠気1.7%(1/59例)であった。
副作用発現頻度は1.7%(1/59例)であった。認められた副作用は、眠気1.7%(1/59例)であった。
・患児177例を対象に、ドライシロップ剤1日1〜7回(ドンペリドンとして0.1〜1.1mg/kg)注)を1〜33日間経口投与したとき、有効率は周期性嘔吐症80.9%(38/47例)、上気道感染症91.5%(43/47例)及び抗悪性腫瘍剤投与時62.5%(5/8例)であった。
副作用発現頻度は1.1%(2/177例)であった。認められた副作用は、下痢、眠気 各0.6%(1/177例)であった。
副作用発現頻度は1.1%(2/177例)であった。認められた副作用は、下痢、眠気 各0.6%(1/177例)であった。
注)本剤の小児における承認用量は1日1.0〜2.0mg/kg(3回/日)である。
18. 薬効薬理
18.1 作用機序
上部消化管並びにCTZ(化学受容器引き金帯)に作用し、抗ドパミン作用により薬効を発現する。
18.2 消化管運動に及ぼす作用
18.2.1 胃運動促進作用
収縮頻度やトーヌスに影響を及ぼさず、胃の律動的な収縮力を長時間(約2時間)増大した(イヌ)11)。
18.2.2 胃・十二指腸協調運動促進作用
胃の自動運動を増大させると同時に、胃前庭部−十二指腸協調運動を著明に促進した(モルモット摘出胃)12)。
18.2.3 胃排出能の正常化作用
18.2.4 下部食道括約部圧(LESP)の上昇作用
18.3 選択的な制吐作用
19. 有効成分に関する理化学的知見
19.1. ドンペリドン
20. 取扱い上の注意
本剤の錠剤表面に斑点が認められることがあるが、これは使用色素によるものであり、品質に影響はない。
22. 包装
<ナウゼリンOD錠5>
[PTP]100錠(10錠×10)
<ナウゼリンOD錠10>
[PTP]100錠(10錠×10)、1000錠(10錠×100)
23. 主要文献
- Heykants J,et al., Eur J Drug Metab Pharmacokinet., 6, 61-70, (1981) »PubMed »DOI
- Michiels M,et al., Eur J Drug Metab Pharmacokinet., 6, 37-48, (1981) »PubMed »DOI
- 社内資料:ドンペリドンの代謝について
- Meuldermans W,et al., Eur J Drug Metab Pharmacokinet., 6, 49-60, (1981) »PubMed »DOI
- Yoshizato T,et al., Eur J Clin Pharmacol., 68, 1287-1294, (2012) »PubMed »DOI
- 三好秋馬ほか, 診療と新薬, 17, 2923-2933, (1980)
- 棟久龍夫ほか, 医学と薬学, 3, 867-875, (1980)
- 長岡正範ほか, 新薬と臨床, 29, 1818-1843, (1980)
- 岩波文門ほか, 小児科臨床, 34, 931-938, (1981)
- 前田和一ほか, 新薬と臨床, 29, 1845-1849, (1980)
- 藤井一元ほか, 日平滑筋誌, 16, 37-46, (1980) »DOI
- Schuurkes JAJ,et al., Scand J Gastroenterol., 16, 33-36, (1981)
- Harasawa S,et al., 内科宝函, 28, 67-75, (1981)
- 原沢茂ほか, 臨床成人病, 13, 2313-2317, (1983)
- 本郷道夫ほか, 医学と薬学, 4, 665-668, (1980)
- 白羽誠ほか, 医学と薬学, 4, 533-537, (1980)
- 周藤勝一ほか, 応用薬理, 21, 179-189, (1981)
- Shuto K,et al., J Pharm Dyn., 3, 709-714, (1980)
- Niemegeers CJE,et al., Arch Int Pharmacodyn Ther., 244, 130-140, (1980) »PubMed
24. 文献請求先及び問い合わせ先
文献請求先
協和キリン株式会社
くすり相談窓口
〒100-0004
東京都千代田区大手町1-9-2
電話:0120-850-150
製品情報問い合わせ先
協和キリン株式会社
くすり相談窓口
〒100-0004
東京都千代田区大手町1-9-2
電話:0120-850-150
26. 製造販売業者等
26.1 製造販売元
協和キリン株式会社
東京都千代田区大手町1-9-2