医薬品情報
| 総称名 | ビカルタミド |
|---|---|
| 一般名 | ビカルタミド |
| 欧文一般名 | Bicalutamide |
| 製剤名 | ビカルタミド錠・ビカルタミド口腔内崩壊錠 |
| 薬効分類名 | 前立腺癌治療剤 |
| 薬効分類番号 | 4291 |
| ATCコード | L02BB03 |
| KEGG DRUG |
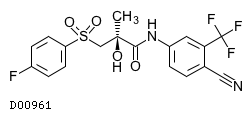
D00961
ビカルタミド
|
| KEGG DGROUP |
DG01591
アンドロゲン受容体拮抗薬
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年4月 改訂(第2版)

|
2.禁忌 4.効能または効果 5.効能又は効果に関連する注意 6.用法及び用量 8.重要な基本的注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 17.臨床成績 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| ビカルタミド錠80mg「日医工」 (後発品) | Bicalutamide Tablets | 日医工 | 4291009F1160 | 97.1円/錠 | 劇薬, 処方箋医薬品注) |
| ビカルタミドOD錠80mg「日医工」 (後発品) | Bicalutamide OD Tablets | 日医工 | 4291009F2086 | 97.1円/錠 | 劇薬, 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 小児[本薬の薬理作用に基づき、男子小児の生殖器官の正常発育に影響を及ぼす恐れがある。また、本薬の毒性試験(ラット)において、雌性ラットで子宮の腫瘍性変化が認められている。]
2.3 女性[本薬の毒性試験(ラット)において、子宮の腫瘍性変化及び雄児の雌性化が報告されている。]
4. 効能または効果
5. 効能または効果に関連する注意
5.1 本剤による治療は、根治療法ではないことに留意し、本剤投与12週後を抗腫瘍効果観察のめどとして、本剤投与により期待する効果が得られない場合、あるいは病勢の進行が認められた場合には、手術療法等他の適切な処置を考慮すること。
5.2 本剤投与により、安全性の面から容認し難いと考えられる副作用が発現した場合は、治療上の有益性を考慮の上、必要に応じ、休薬又は集学的治療法などの治療法に変更すること。
6. 用法及び用量
通常、成人にはビカルタミドとして80mgを1日1回、経口投与する。
8. 重要な基本的注意
8.1 外国の臨床試験において、本剤投与例で本剤との関連性が否定できなかった前立腺癌以外の死亡例が報告されている。そのうち心・循環器系疾患による死亡は9%未満であり、その主な死因は心不全、心筋梗塞、脳血管障害等であった。これら外国の臨床試験で報告された心・循環器系疾患による死亡率は、対照の去勢術群(16%未満)より低く、高齢者で一般に予期される死亡率の範囲内であったが、本剤を投与する場合は十分に観察を行い、慎重に投与すること。
8.2 本剤は内分泌療法剤であり、がんに対する薬物療法について十分な知識・経験を持つ医師のもとで、本剤による治療が適切と判断される患者についてのみ使用すること。
8.3 劇症肝炎、肝機能障害、黄疸があらわれることがあるので、本剤投与中は定期的に肝機能検査を行うなど、患者の状態を十分に観察すること。[11.1.1参照]
9. 特定の背景を有する患者に関する注意
9.3 肝機能障害患者
本剤は肝臓でほぼ完全に代謝を受けるため、定常状態時の血中濃度が高くなる可能性がある。[16.6.2参照]
9.8 高齢者
高齢者への投与の際には患者の状態を観察しながら慎重に投与すること。本剤の臨床試験成績から、高齢者と非高齢者において血漿中濃度及び副作用の発現に差はみられていないが、一般に高齢者では、心・循環器系の機能が低下していることが多く、心・循環器系の有害事象の発現頻度が若年層より高い。
10. 相互作用
相互作用序文
本剤は、主として肝代謝酵素CYP3A4を阻害する。[16.7参照]
薬物代謝酵素用語
CYP3A4
10.2 併用注意
| クマリン系抗凝血薬 ワルファリン等 | クマリン系抗凝血薬の作用を増強するおそれがある。 プロトロンビン時間を測定する、又は、トロンボテストを実施するなど、血液凝固能検査等出血管理を十分に行いつつ、凝固能の変動に注意し、患者の状態を観察しながら慎重に投与すること。 | in vitro試験で蛋白結合部位においてワルファリンと置換するとの報告がある。 |
| トルブタミド | トルブタミドの作用を増強するおそれがある。 但し、相互作用に関する報告症例はない。 | 本剤は、in vitro試験でトルブタミドの代謝を阻害した。 |
| デキストロメトルファン | デキストロメトルファンの作用を増強するおそれがある。 但し、相互作用に関する報告症例はない。 | 本剤は、in vitro試験でデキストロメトルファンの代謝を阻害した。 |
| 主にCYP3A4によって代謝される薬物 カルバマゼピン、シクロスポリン、トリアゾラム等 | 主にCYP3A4によって代謝される薬物の作用を増強するおそれがある。 但し、相互作用に関する報告症例はない。 | 本剤は、in vitro試験でCYP3A4によるテストステロン6β-水酸化酵素活性を阻害した。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 劇症肝炎、肝機能障害、黄疸(いずれも頻度不明)
劇症肝炎、AST、ALT、Al-P、γ-GTP、LDHの上昇等を伴う肝機能障害、黄疸があらわれることがある。[8.3参照]
11.1.2 白血球減少(1.0%)、血小板減少(1.9%)
11.1.3 間質性肺炎(頻度不明)
11.1.4 心不全、心筋梗塞(いずれも頻度不明)
注)副作用頻度は承認時までの国内臨床試験を基に集計した。
11.2 その他の副作用
| 5%以上 | 1〜5%未満 | 1%未満 | 頻度不明 | |
| 内分泌 | 乳房腫脹(44.7%)、乳房圧痛(46.6%)、ほてり | |||
| 生殖器 | 勃起力低下 | |||
| 肝臓 | AST上昇、ALT上昇、Al-P上昇 | γ-GTP上昇、LDH上昇 | ||
| 泌尿器 | 腎機能障害(クレアチニン上昇、BUN上昇) | 血尿、夜間頻尿 | ||
| 皮膚 | そう痒、発疹 | 発汗、皮膚乾燥、脱毛、多毛、光線過敏症 | ||
| 精神神経系 | 性欲減退 | 傾眠 | 頭痛、めまい、不眠、抑うつ状態 | |
| 循環器 | 心電図異常 | |||
| 消化器 | 便秘 | 口渇 | 食欲不振、下痢、悪心、嘔吐、消化不良、鼓腸放屁、腹痛 | |
| 筋・骨格系 | 胸痛 | 骨盤痛 | ||
| 過敏症 | 血管浮腫、蕁麻疹 | |||
| その他 | 総コレステロール上昇、中性脂肪上昇 | さむけ | 貧血、浮腫、倦怠感、無力症、疲労、高血糖、体重増加・減少 |
14. 適用上の注意
14.1 薬剤交付時の注意
<製剤共通>
14.1.1 PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することがある。
<OD錠>
14.1.2 本剤は舌の上にのせて唾液を浸潤させ舌で軽くつぶすことにより崩壊するため、水なしで服用可能である。また、水で服用することもできる。
14.1.3 本剤は寝たままの状態では、水なしで服用させないこと。
15. その他の注意
15.1 臨床使用に基づく情報
外国において、呼吸困難が発現したとの報告がある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
(1)健康成人
健康成人男子にビカルタミド錠80mg又はビカルタミドOD錠80mg(水なし)をクロスオーバー法にて空腹時に単回経口投与した。R-ビカルタミド(活性体)の血漿中濃度は投与後36時間に最高値を示し、消失半減期は4.9〜5.2日であった。また、ビカルタミド錠とOD錠は生物学的に同等であった1)。
| n | Cmax (μg/mL) | tmax (h) | AUC∞ (μg・h/mL) | t1/2 (日) | |
| ビカルタミド錠80mg | 23 | 1.21±0.23 | 36.0(24.0〜72.0) | 280±80 | 5.2±1.5 |
| ビカルタミドOD錠80mg | 21 | 1.26±0.21 | 36.0(15.0〜72.0) | 286±69 | 4.9±1.1 |
健康成人男子にビカルタミドOD錠80mgを水とともに空腹時単回経口投与し、クロスオーバー法にてビカルタミド錠80mgと比較したところ、両製剤は生物学的に同等であった1)。
| n | Cmax (μg/mL) | tmax (h) | AUC∞ (μg・h/mL) | t1/2 (日) | |
| ビカルタミド錠80mg | 22 | 1.25±0.27 | 36.0(9.0〜72.0) | 262±78 | 4.6±0.7 |
| ビカルタミドOD錠80mg | 22 | 1.29±0.25 | 36.0(5.0〜72.0) | 277±86 | 4.8±1.2 |
(2)前立腺癌患者
前立腺癌患者にビカルタミド80mgを単回経口投与したとき、投与後6、12及び24時間の血漿中R-ビカルタミド(活性体)濃度はほぼ一定(1.5〜1.7μg/mL,n=3)であった2)。
16.1.2 反復投与
16.1.3 生物学的同等性試験
(1)ビカルタミド錠80mg「日医工」
ビカルタミド錠80mg「日医工」及びカソデックス錠80mgを、クロスオーバー法によりそれぞれ1錠(ビカルタミドとして80mg)健康成人男子に絶食単回経口投与して活性体であるR-ビカルタミドの血漿中濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.8)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された4)。
| 判定パラメータ | 参考パラメータ | |||
| AUC0→336 (μg・hr/mL) | Cmax (μg/mL) | Tmax (hr) | t1/2 (hr) | |
| ビカルタミド錠80mg「日医工」 | 210.5±33.8 | 1.27±0.18 | 29.3±19.6 | 100.2±16.0 |
| カソデックス錠80mg | 211.2±59.7 | 1.19±0.24 | 31.7±19.3 | 111.6±23.3 |
図1 血漿中薬物濃度推移
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
(2)ビカルタミドOD錠80mg「日医工」
ビカルタミドOD錠80mg「日医工」及びカソデックスOD錠80mgを、クロスオーバー法によりそれぞれ1錠(ビカルタミドとして80mg)健康成人男子に絶食単回経口投与(水で服用及び水なしで服用)して活性体であるR-ビカルタミドの血漿中濃度を測定し,得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された5)。
| 判定パラメータ | 参考パラメータ | |||
| AUC0→504 (μg・hr/mL) | Cmax (μg/mL) | Tmax (hr) | t1/2 (hr) | |
| ビカルタミドOD錠80mg「日医工」 | 237.54±65.16 | 1.1746±0.2271 | 27.8±13.1 | 118.67±30.45 |
| カソデックスOD錠80mg | 227.64±55.20 | 1.1333±0.2010 | 28.5±15.7 | 117.64±34.57 |
図2 血漿中薬物濃度推移(水あり)
| 判定パラメータ | 参考パラメータ | |||
| AUC0→504 (μg・hr/mL) | Cmax (μg/mL) | Tmax (hr) | t1/2 (hr) | |
| ビカルタミドOD錠80mg「日医工」 | 246.38±60.56 | 1.2106±0.2130 | 27.2±12.2 | 123.63±46.11 |
| カソデックスOD錠80mg | 240.84±61.83 | 1.2051±0.1901 | 28.1±12.4 | 118.28±42.60 |
図3 血漿中薬物濃度推移(水なし)
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.3 分布
In vitroにおけるヒト血漿蛋白結合率(ラセミ体)は96%であった6)。
16.4 代謝
ヒトにおけるビカルタミドの代謝は、水酸化及びグルクロン酸抱合であった。血漿中には未変化体が、尿中には未変化体のグルクロン酸抱合体及び水酸化体のグルクロン酸抱合体が、糞中には未変化体及び水酸化体が認められた7)(外国人データ)。
16.5 排泄
健康成人男子にビカルタミド50mgを経口投与後9日目までの累積尿中及び糞中排泄率は、それぞれ36%及び43%であった7)(外国人データ)。
16.6 特定の背景を有する患者
16.7 薬物相互作用
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内臨床試験
承認時までに前立腺癌患者(病期C/D)を対象として国内で総計197例について実施された二重盲検比較試験を含む臨床試験2)3)12)13)の概要は次のとおりである。
| 試験名 | 投与量 | 投与期間 | 症例数 | 有効率 (部分奏効以上) |
| 第I相試験 | 80mg/日 | 12週間 | 3 | 66.7%(2/3) |
| 前期第II相試験 | 80mg/日 | 12週間 | 41 | 61.0%(25/41) |
| 後期第II相試験 | 80mg/日 | 12週間 | 59 | 64.4%(38/59) |
| 長期投与試験 | 80mg/日 | 48週間 | 26 | 76.9%(20/26) |
副作用は、ビカルタミド錠の承認用量(80mg/日)において、第I相試験で3例中3例(100.0%)に認められ、主な副作用は、乳房圧痛(66.7%)、乳房腫脹(33.3%)、ほてり(33.3%)であった。前期第II相試験では41例中25例(61.0%)に認められ、主な副作用は、乳房圧痛(41.5%)、乳房腫脹(36.6%)、ほてり(12.2%)等であった。後期第II相試験では59例中38例(64.4%)に認められ、主な副作用は、乳房圧痛(33.9%)、乳房腫脹(33.9%)、性欲減退(11.9%)等であった。(承認時)
また、未治療進行前立腺癌患者(病期C/D)を対象としたビカルタミド錠とLH-RHアゴニストとの併用療法とLH-RHアゴニスト単独療法を比較した国内第III相二重盲験比較試験14)15)の成績は次のとおりである。
| ビカルタミド錠及びLH-RHアゴニスト併用 | LH-RHアゴニスト単独 | P値(95%信頼区間) | ハザード比 | |
| PSA正常化注1)率 (投与12週時) | 79.4% (81/102例) | 38.6% (39/101例) | <0.001 (27.6-52.0) | − |
| PSA正常化注1)までの期間 (中央値) | 8.1週 | 24.1週 | <0.001 (2.77-5.66) | 3.96 |
| 奏効率 (投与12週時) | 77.5% (79/102例) | 65.3% (66/101例) | 0.063 (-0.3-24.1) | − |
| TTTF注2) (中央値) | 117.7週 | 60.3週 | <0.001 (0.38-0.77) | 0.54 |
| TTP注3) (中央値) | 未到達 | 96.9週 | <0.001 (0.26-0.63) | 0.40 |
本試験において、副作用はビカルタミド錠及びLH-RHアゴニスト併用療法群で66.7%に認められ、主な副作用は、ほてり(16.7%)、血中アルカリフォスファターゼ増加(10.8%)、貧血(8.8%)等であった。
17.1.2 海外臨床試験
海外において、標準治療として経過観察又は根治的治療(放射線療法、前立腺全摘除術)を施行した早期前立腺癌患者8,113例を対象としたビカルタミド錠150mg/日注4)による無作為化プラセボ対照二重盲検比較臨床試験16)が実施されている。ビカルタミド錠投与群全体で無増悪生存率は有意に改善した(HR=0.79、95%信頼区間0.73-0.85、P<0.001)が、全生存率についてはプラセボ群との差は認めなかった(HR=0.99、95%信頼区間0.91-1.09、P=0.89)。病期別解析において、限局性前立腺癌の経過観察を行った患者におけるビカルタミド錠投与群では、統計学的な有意差はないもののプラセボ群と比較して全生存率の減少傾向が認められた(HR=1.16、95%信頼区間0.99-1.37)(追跡期間中央値7.4年時点)。ビカルタミド錠投与群で認められた主な有害事象は、乳房痛(73.6%、2962/4022例)及び女性化乳房(68.8%、2766/4022例)等であった。
注4)本邦における承認用法用量は80mg/日である。
18. 薬効薬理
18.1 作用機序
ビカルタミドは、前立腺腫瘍組織のアンドロゲン受容体に対するアンドロゲンの結合を阻害し、抗腫瘍効果を発揮する。なお、ビカルタミドの抗アンドロゲン活性は実質的にR体によるものであった17)。
なお、臨床上、ビカルタミドの投与の中止により一部の患者でAWS(antiandrogen withdrawal syndrome)をみることがある18)。
18.2 抗腫瘍効果
18.3 アンドロゲン受容体との結合能
ラット及びヒト前立腺アンドロゲン受容体に対する結合能は、ジヒドロテストステロンの約2%であった22)。
19. 有効成分に関する理化学的知見
19.1. ビカルタミド
22. 包装
<ビカルタミド錠80mg「日医工」>
30錠[10錠×3;PTP]
100錠[10錠×10;PTP]
<ビカルタミドOD錠80mg「日医工」>
30錠[10錠×3;PTP]
100錠[10錠×10;PTP]
23. 主要文献
- 鷲尾兼寿 他, 医学と薬学, 70 (2), 277-284, (2013)
- 古武敏彦 他, 泌尿器科紀要, 42 (2), 143-153, (1996)
- 古武敏彦 他, 泌尿器科紀要, 42 (2), 155-168, (1996)
- 中道昇 他, 診療と新薬, 46 (4), 400-406, (2009)
- 社内資料:生物学的同等性試験(OD錠80mg)
- Cockshott I.D.,et al., Xenobiotica., 21 (10), 1347-1355, (1991) »PubMed
- McKillop D.,et al., Xenobiotica., 23 (11), 1241-1253, (1993) »PubMed
- Cockshott I.D.,et al., Eur.Urol., 18 (Suppl 3), 10-17, (1990)
- Furr B.J.A.,et al., Hormone Dependent Cancer.Pasqualini,JR,Katzenellenbogen BS,(Eds)., 397-424, (1996), (Marcel Dekker,New York.)
- Cockshott I.D., Clin Pharmacokinet., 43 (13), 855-878, (2004) »PubMed
- Kaisary A.,et al., Anti-Cancer Drugs., 7, 54-59, (1996) »PubMed
- 古武敏彦 他, 泌尿器外科, 9 (3), 243-256, (1996)
- 古武敏彦 他, 泌尿器外科, 9 (4), 343-355, (1996)
- Usami M.,et al., Prostate Cancer Prostatic Dis., 10 (2), 194-201, (2007) »PubMed
- Akaza H.,et al., Jpn.J.Clin.Oncol., 34 (1), 20-28, (2004) »PubMed
- McLeod D.G.,et al., BJU Int., 97 (2), 247-254, (2006) »PubMed
- 第十八改正日本薬局方解説書, C4254-C4262, (2021), (廣川書店)
- 赤倉功一郎, 排尿障害プラクティス, 19 (2), 173-177, (2011)
- Veldscholte J.,et al., Biochemistry., 31, 2393-2399, (1992) »PubMed
- Darbre P.D.,et al., J.Steroid Biochem., 36 (5), 385-389, (1990) »PubMed
- Furr B.J.A.,et al., Excerpta Med.Int.Cong.Series., 1064, 157-175, (1994)
- Furr B.J.A., Eur.Urol., 29 (Suppl 2), 83-95, (1996)
24. 文献請求先及び問い合わせ先
文献請求先
日医工株式会社
お客様サポートセンター
〒930-8583
富山市総曲輪1丁目6番21
電話:0120-517-215
FAX:076-442-8948
製品情報問い合わせ先
日医工株式会社
お客様サポートセンター
〒930-8583
富山市総曲輪1丁目6番21
電話:0120-517-215
FAX:076-442-8948
26. 製造販売業者等
26.1 製造販売元
日医工株式会社
富山市総曲輪1丁目6番21