医薬品情報
| 総称名 | トラネキサム酸 |
|---|---|
| 一般名 | トラネキサム酸 |
| 欧文一般名 | Tranexamic Acid |
| 薬効分類名 | 抗プラスミン剤 |
| 薬効分類番号 | 3327 4490 |
| ATCコード | B02AA02 |
| KEGG DRUG |
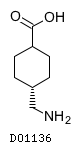
D01136
トラネキサム酸
|
| JAPIC | 添付文書(PDF) |
添付文書情報2024年1月 改訂(第1版)

|
2.禁忌 4.効能または効果 6.用法及び用量 7.用法及び用量に関連する注意 9.特定の背景を有する患者に関する注意 10.相互作用 11.副作用 14.適用上の注意 15.その他の注意 16.薬物動態 18.薬効薬理 19.有効成分に関する理化学的知見 22.包装 23.主要文献 24.文献請求先及び問い合わせ先 26.製造販売業者等 |
商品情報 3.組成・性状
| 販売名 | 欧文商標名 | 製造会社 | YJコード | 薬価 | 規制区分 |
|---|---|---|---|---|---|
| トラネキサム酸注250mg/5mL「日新」 (後発品) | Tranexamic Acid Inj.250mg/5mL"NISSIN″ | 日新製薬-山形 | 3327401A1160 | 104円/管 | 処方箋医薬品注) |
| トラネキサム酸注1000mg/10mL「日新」 (後発品) | Tranexamic Acid Inj.1000mg/10mL"NISSIN" | 日新製薬-山形 | 3327401A4274 | 104円/管 | 処方箋医薬品注) |
2. 禁忌
次の患者には投与しないこと
2.1 トロンビンを投与中の患者[10.1参照]
2.2 本剤の成分に対し過敏症の既往歴のある患者
4. 効能または効果
○全身性線溶亢進が関与すると考えられる出血傾向(白血病、再生不良性貧血、紫斑病等、及び手術中・術後の異常出血)
○局所線溶亢進が関与すると考えられる異常出血(肺出血、鼻出血、性器出血、腎出血、前立腺手術中・術後の異常出血)
○下記疾患における紅斑・腫脹・そう痒などの症状
湿疹及びその類症、蕁麻疹、薬疹・中毒疹
○下記疾患における咽頭痛・発赤・充血・腫脹などの症状
扁桃炎、咽喉頭炎
○口内炎における口内痛及び口内粘膜アフター
6. 用法及び用量
トラネキサム酸として通常成人1日250〜500mgを1〜2回に分けて静脈内又は筋肉内注射する。術中、術後等には必要に応じ1回500〜1000mgを静脈内注射するか、又は500〜2500mgを点滴静注する。なお、年令、症状により適宜増減する。
7. 用法及び用量に関連する注意
<注250mg/5mL>
通常成人1日5〜10mL(1〜2アンプル)を1〜2回に分けて静注又は筋注する。術中・術後など、必要に応じ1回10〜50mL(2〜10アンプル)を点滴静注する。
<注1000mg/10mL>
通常成人1日2.5〜5mLを1〜2回に分けて静注又は筋注する。術中・術後など、必要に応じ1回5〜10mLを静注するか、又は5〜25mLを点滴静注する。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 血栓のある患者(脳血栓、心筋梗塞、血栓性静脈炎等)及び血栓症があらわれるおそれのある患者
血栓を安定化するおそれがある。
9.1.2 消費性凝固障害のある患者
ヘパリン等と併用すること。血栓を安定化するおそれがある。
9.1.3 術後の臥床状態にある患者及び圧迫止血の処置を受けている患者
静脈血栓を生じやすい状態であり、本剤投与により血栓を安定化するおそれがある。離床、圧迫解除に伴い肺塞栓症を発症した例が報告されている。
9.2 腎機能障害患者
9.5 妊婦
治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
9.8 高齢者
減量するなど注意すること。一般に生理機能が低下していることが多い。
10. 相互作用
10.1 併用禁忌
| トロンビン [2.1参照] | 血栓形成傾向があらわれるおそれがある。 | 血栓形成を促進する作用があり、併用により血栓形成傾向が増大する。 |
10.2 併用注意
| ヘモコアグラーゼ | 大量併用により血栓形成傾向があらわれるおそれがある。 | ヘモコアグラーゼによって形成されたフィブリン塊は、本剤の抗プラスミン作用によって比較的長く残存し閉塞状態を持続させるおそれがあると考えられている。 |
| バトロキソビン | 血栓・塞栓症を起こすおそれがある。 | バトロキソビンによって生成するdesAフィブリンポリマーの分解を阻害する。 |
| 凝固因子製剤 エプタコグアルファ等 | 口腔等、線溶系活性が強い部位では凝固系がより亢進するおそれがある。 | 凝固因子製剤は凝固系を活性化させることにより止血作用を発現する。一方、本剤は線溶系を阻害することにより止血作用を発現する。 |
11. 副作用
11.1 重大な副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1.1 ショック(頻度不明)
11.1.2 痙攣(頻度不明)
人工心肺を用いた心臓大血管手術の周術期に本剤を投与した患者において、術後に痙攣があらわれることがある。また、人工透析患者において痙攣があらわれたとの報告がある。[9.2.2参照]
11.2 その他の副作用
| 0.1〜1%未満 | 0.1%未満 | 頻度不明 | |
| 過敏症 | そう痒感、発疹等 | ||
| 消化器 | 悪心、嘔吐 | 食欲不振、下痢 | |
| 眼 | 一過性の色覚異常(静脈内注射時) | ||
| その他 | 眠気、頭痛 |
14. 適用上の注意
14.1 薬剤投与時の注意
14.1.1 静脈内注射時
ゆっくり静脈内に投与すること。急速に投与すると、まれに悪心、胸内不快感、心悸亢進、血圧低下等があらわれることがある。
14.1.2 筋肉内注射時
組織・神経等への影響を避けるため、次の点に注意すること。
・注射部位については、神経走行部位を避けて慎重に投与すること。
・繰り返し注射する場合には、左右交互に注射するなど、同一部位を避けること。なお、小児等には特に注意すること。
・注射針を刺入したとき、激痛を訴えたり、血液の逆流をみた場合は、直ちに針を抜き、部位をかえて注射すること。
15. その他の注意
15.2 非臨床試験に基づく情報
イヌに長期・大量投与したところ網膜変性があらわれたとの報告がある。
16. 薬物動態
16.8 その他
<トラネキサム酸注250mg/5mL「日新」>
トラネキサム酸注250mg/5mL「日新」の生物学的同等性に関しては、ヘムロン注(昭和54年承認、販売名変更前製剤)の承認申請時添付資料により評価された。
<トラネキサム酸注1000mg/10mL「日新」>
トラネキサム酸注1000mg/10mL「日新」の生物学的同等性に関しては、ヘムロン注S(昭和54年承認、販売名変更前製剤)の承認申請時添付資料により評価された。
18. 薬効薬理
18.1 作用機序
トラネキサム酸は抗線溶薬である。凝固した血液(フィブリン塊)は繊維素溶解(線溶)系により徐々に溶解されるが、フィブリンを分解するのはプラスミンである。トラネキサム酸はプラスミンの前駆物質であるプラスミノーゲンからプラスミンへの変換を阻害すると共に、プラスミンのフィブリンへの結合を阻害してフィブリンの溶解を防ぐ1)。
19. 有効成分に関する理化学的知見
19.1. トラネキサム酸
22. 包装
<トラネキサム酸注250mg/5mL「日新」>
5mL×50管(ルアーフィットポリエチレンボトル)
<トラネキサム酸注1000mg/10mL「日新」>
10mL×50管(ルアーフィットポリエチレンボトル)
23. 主要文献
- 第十七改正日本薬局方解説書, C-3457, (2016), (廣川書店)
24. 文献請求先及び問い合わせ先
文献請求先
日新製薬株式会社
安全管理部
〒994-0069
山形県天童市清池東二丁目3番1号
電話:023-655-2131
FAX:023-655-3419
Email:d-info@yg-nissin.co.jp
製品情報問い合わせ先
日新製薬株式会社
安全管理部
〒994-0069
山形県天童市清池東二丁目3番1号
電話:023-655-2131
FAX:023-655-3419
Email:d-info@yg-nissin.co.jp
26. 製造販売業者等
26.1 製造販売元
日新製薬株式会社
山形県天童市清池東二丁目3番1号